文章信息
- 曾楚楚, 娄钧翼, 郭明, 王冰璇, 卢闻君
- Zeng Chuchu, Lou Junyi, Guo Ming, Wang Bingxuan, Lu Wenjun
- 防治核桃干腐病的新型纳米生物基农药缓释胶囊制备及缓释性能
- Preparation and Sustained Release Properties of A New Nano-Bio-Based Pesticide Sustained-Release Capsule against Carya cathayensis Canker Disease
- 林业科学, 2018, 54(5): 87-100.
- Scientia Silvae Sinicae, 2018, 54(5): 87-100.
- DOI: 10.11707/j.1001-7488.20180510
-
文章历史
- 收稿日期:2017-03-08
- 修回日期:2018-01-10
-
作者相关文章
2. 浙江农林大学化学系 临安 311300;
3. 浙江农林大学林业与生物技术学院 临安 311300
2. Department of Chemistry, Zhejiang Agriculture and Forestry University Lin'an 311300;
3. School of Forestry Science and Biotechnology, Zhejiang Agriculture and Forestry University Lin'an 311300
病虫害严重影响林木生长,农药防治是控制病虫害的有效手段之一。但农药使用中的流失率可达到50%~60%,降低了农药杀灭病虫害的作用效率,同时,易对环境造成严重污染(Yang et al., 2011)。为了减少农药的流失率,提高农药使用效率,包载农药形成农药缓释胶囊是一种有效方法(Aouada et al., 2010; Zhao et al., 2016)。
农药缓释胶囊制备方法有化学法、物理法、物理化学法等(冯建国等, 2014)。目前,农药缓释胶囊多采用物理化学法中的相分离法与界面聚合法制备。Suttia等(2016)以两亲性聚(乙二醇)-嵌段-聚(双酚A碳酸酯)共聚物作为囊壁材料,采用相分离法制备纳米胶囊,粒径达到85 nm±30 nm。李北兴等(2013)以4, 4-二苯基甲烷二异氰酸酯(MDI)与乙二胺作为壁材单体,采用界面聚合技术制备二甲戊灵微囊,粒径4~15.5 μm,等等。文献报道的缓释胶囊粒径范围为0.085 ~15.5 μm,表明胶囊尺度的大小对缓释效果的影响至关重要,普遍规律是纳米尺度的农药缓释胶囊明显优于常规尺度的缓释胶囊。故开展纳米农药缓释胶囊的研究十分有意义。当前,新型纳米缓释胶囊既是材料学的研究热点又是纳米科学的前沿,同时也是林业等植保领域有望获得突破的领域(Bakshi, 2016; Sosnik et al., 2016)。
农药缓释胶囊的缓释效果与壁材密切相关,近年来,选用的壁材主要以高分子聚合物材料为主(Ramadossa et al., 2017; 席丽霞等, 2013),虽然获得的胶囊具有韧性好,缓释时效长等优点,但同时存在难降解、污染环境等不足(李继昭等, 2016)。因此探寻环境友好型生物质材料作为胶囊壁材极其必要。生物质材料是指由动物、植物、微生物等生命体中的一些天然成分作为基质或对其进行结构衍生、加工等方法得到的材料,主要由有机高分子物质组成,具有可再生性和生物可降解性(Zhang et al., 2012; 俞娟等, 2016; Casettari et al., 2012),如纤维素、壳聚糖、淀粉等典型的生物质材料。基于此,将其作为胶囊基材应用于农药缓释胶囊中,可克服传统材料的缺点,且具有来源广、降解性好等优点,故开展新型纳米生物基缓释胶囊制备极具应用前景。
本研究选用海藻酸钠、羧甲基纤维素钠和羧甲基壳聚糖(郭明等, 2014; Jiang et al., 2015)作为生物基材料,设计绿色反应路线合成制备新型纳米生物基农药缓释胶囊,并探讨其对林业病虫害防治的防治治效果。山核桃(Carya cathayensis)是临安地区主要经济林树种,核桃干腐病是影响山核桃产量的主要因素之一,其病原菌主要为葡萄座腔菌(Botryosphaeria dothidea)(田甜等, 2012),该菌以菌丝体的形态感染树皮细胞,并通过孢子大量繁殖,产生对寄主细胞有毒害作用的代谢物,可改变寄主细胞膜透性,细胞壁破裂,细胞死亡,出现病斑,引起树木溃疡病。目前,生产上广泛防治干腐病的戊唑醇药剂存在流失严重、药效短等问题,如果采用新型生物基农药缓释胶囊包载干腐病抑菌剂戊唑醇,就可能克服单施戊唑醇防治干腐病的不足,大幅提高防效。因此,开展新型纳米农药缓释胶囊制备及应用研究可为核桃干腐病提供新的技术方法,具有重要意义。
1 材料与方法 1.1 材料与仪器 1.1.1 材料海藻酸钠(sodium alginate, SA) (黏度200±20 mPa·s,上海景颜化工科技有限公司);羧甲基纤维素钠(carboxymethyl cellulose, CMC) (CP,西陇化工股份有限公司);羧甲基壳聚糖(carboxymethyl chitosan, CMCS) (取代度≥80%,上海麦克林生化科技有限公司);胆固醇(AR,安耐吉);N, N′-二环己基碳二亚胺(dicyclohexylcarbodiimide, DCC)(安耐吉);4-二甲氨基吡啶(4-dimethylaminopyridine, DMAP)(阿拉丁);二甲亚砜(dimethyl sulfoxide, DMSO) (AR,>99%,国药集团化学试剂有限公司);戊唑醇(98%,上海三鹰化学试剂有限公司);其他试剂均为分析纯,试验用水为双蒸蒸馏水(ddH2O)。
1.1.2 仪器DF-101S型加热磁力搅拌器(巩义市予华仪器有限责任公司);DZG-6050型真空恒温干燥箱(上海森信实验仪器有限公司);Mettler Toledo AB104-14型电子天平(瑞士梅特勒-托利多公司);IR Prestige-21型傅里叶红外光谱仪(Shimadzu,日本);AVANCE Ⅲ /500 MHz和AVANCE Ⅱ/400 MHz核磁共振波谱仪(Bruker,瑞士);X-射线衍射仪(Shimadzu,日本);Zeta PALS型高灵敏度Zeta电位及粒度分析仪(Brookhave,美国);JEM2100型高分辨透射电子显微镜(TEM,日本Joel公司);紫外分光光度计(Shimadzu,日本)。
1.2 新型生物基材料制备参考文献方法(Yang et al., 2007),利用绿色缩水反应制备新型生物基材料。25 mL DMSO置于圆底烧瓶中,分别加入1 g SA、1 g CMC、1 g CMCS。1.5 g胆固醇、1.03 g DMAP和0.24 g DCC (胆固醇:DMAP:DCC=2:2.5:1)依次加入上述混合液中,室温反应24 h,透析3天,无水乙醇醇沉,过滤,真空干燥,获得海藻酸钠衍生物(SA derivatives, SAD)、羧甲基纤维素钠衍生物(CMC derivatives, CMCD)及羧甲基壳聚糖衍生物(CMCS derivatives, CMCSD)。
1.3 原料及新型生物基材料的表征红外光谱仪分别测定SA、CMC、CMCS、胆固醇、SAD、CMCD和CMCSD的IR谱,KBr压片法制样,波数范围500~4 000 cm-1。AVANCE Ⅲ /500 MHz核磁共振仪测定SA、CMC、CMCS、胆固醇、SAD、CMCD和CMCSD的1H NMR谱,CDCl3为溶剂。AVANCE Ⅱ /400 MHz核磁共振仪测定SA、CMC、CMCS、胆固醇、SAD、CMCD和CMCSD的13C NMR谱,魔角自旋速度3.8 MHz;观测频率13C 75 MHz;采集数据点8 192,扫描累计696次;内参考物:氨基乙酸;分辨率4.88 Hz。X射线衍射仪测定SA、CMC、CMCS、SAD、CMCD和CMCSD的XRD谱,扫描范围2θ(5°~50°)。
1.4 戊唑醇微纳米胶囊的制备参考文献方法(Fallaha et al., 2016),采用相分离法将320 mg SAD、CMCD和CMCSD分别溶于120 mL蒸馏水。800 mg戊唑醇溶于6 mL甲苯,加入上述混合液中。0.10 mol·L-1 HCl和0.10 mol·L-1 NaOH调pH=5.5,高速搅拌24 h,得到SAD纳米胶囊、CMCD纳米胶囊和CMCSD纳米胶囊。
1.5 戊唑醇微纳米胶囊的粒径分布和形貌粒度分析仪测试3种载药纳米胶囊及3种空白纳米胶囊的粒径大小及粒径分布。取3种载药纳米胶囊及3种空白纳米胶囊分别滴至铜网支持膜上,自然晾干,通过透射电镜进行测试观察其形态特征。
1.6 戊唑醇微纳米胶囊的包封率5 mL载药纳米胶囊离心10 min,取3 mL上清液加3 mL无水乙醇,UV-Vis法测量戊唑醇浓度。采用(1)式计算载药纳米胶囊的包封率。
| $ \begin{array}{l} \;\;\;\;\;{\rm{包封率}}\left(\% \right) = {\rm{ }}\\ \frac{{{\rm{总农药量}} - {\rm{蒸馏水中游离的农药量}}}}{{{\rm{总农药量}}}} \times 100\% 。\end{array} $ | (1) |
分别移取3种载药纳米胶囊溶液和相同质量浓度戊唑醇乙酸乙酯溶液5 mL,装入透析袋中,置于1 000 mL 50%乙醇溶液中,室温下分别在10、20、30、50、70、90、120、150、180、240、300、360、450、570、720、900、1 110及1 440 min取样5 mL,补充相同体积的50%乙醇,保持体积恒定。UV-Vis法测量戊唑醇的浓度。根据试验数据绘制累积释药率随时间变化的释药动力学曲线,由动力学曲线解析戊唑醇缓释规律。
1.8 戊唑醇微纳米胶囊抑菌试验相同质量浓度(12.05 mg·L-1)的3种载药纳米胶囊溶液和戊唑醇乙酸乙酯溶液作为处理组,3种空白纳米胶囊和乙酸乙酯作为对照组。处理组和对照组向马铃薯葡萄糖琼脂培养基中接种直径为6 mm山核桃干腐病菌菌饼,25 ℃生化培养箱内培养,分别在培养后第1、2、3、4、6、8、11和14天用十字交叉法测定培养皿中的菌落直径。采用(2)式计算菌丝生长抑制率。
| $ \begin{array}{l} {\rm{抑菌率}}\left(\% \right)=\frac{{{\rm{对照组菌落直径 }} - {\rm{处理组菌落直径}}}}{{{\rm{对照组菌落直径}} - {\rm{菌饼直径}}}}{\rm{ }}\\ \;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\; \times 100\% 。\end{array} $ | (2) |
田间试验在浙江省山核桃主产区的临安市乡登村进行。取山核桃树势、土壤类型、施肥和种植体系具有典型性的丘陵地块为试验点,设5个处理,分别为SAD载药纳米胶囊(K1组)、CMCD载药纳米胶囊(K2组)、CMCSD载药纳米胶囊(K3组)、98%戊唑醇(B1组)、清水空白对照(CK组)。各处理小区随机排列,每处理小区为3株山核桃树,3次重复,周围设保护行。山核桃干腐病初期施药(2017年4月),采用干腐病病患树干喷雾施药法(药液质量浓度为12.05 mg·L-1)。调查方法:施药当天调查初始病情(干腐病由浙江农林大学森林保护实验室鉴定),之后第4、7天调查病情,记录树干2 m以下溃疡斑数目和级别,采用(3)、(4)式计算病情指数和防治效果。山核桃干腐病病斑严重程度分级标准参照文献方法(杨淑贞等, 2009)。
| $ {\rm{病情指数}} = \frac{{\sum \left({{\rm{各级树干发病数目}} \times {\rm{该病级数}}} \right)}}{{{\rm{调查总数}} \times {\rm{最高级数}}}}\;\;\;\;\;\;\;\;\;\; \times 100, $ | (3) |
| $ \begin{array}{l} \;\;\;\;\;\;\;\;{\rm{防治效果}}\left( \% \right) = {\rm{ }}\\ \left( 1 -{\frac{{ {\rm{对照区药前病情指数}} \times {\rm{处理区药后病情指数}}}}{{{\rm{对照区药后病情指数}} \times {\rm{处理区药前病情指数}}}}} \right)\\ \times 100\% 。\end{array} $ | (4) |
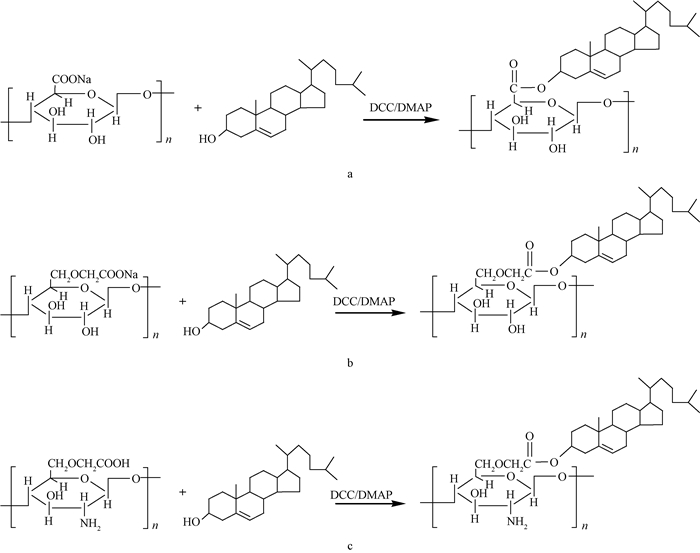
SAD、CMCD及CMCSD合成路线如图 1所示。
|
图 1 SAD(a)、CMCD(b)及CMCSD(c)合成路线 Figure 1 Synthesis route of SAD(a), CMCD(b) and CMCSD(c) |
在N, N′-DCC和4-DMAP作为活化剂的条件下,SA、CMC及CMCS分子链上的羧基可与胆固醇的羟基发生酯化反应,胆固醇基接枝于SA、CMC及CMCS的分子主链上,合成获得SAD、CMCD及CMCSD。
2.2 新型生物基材料的表征 2.2.1 红外光谱分析SA、CMC、CMCS、SAD、CMCD和CMCSD的红外光谱如图 2所示。

|
图 2 7种生物基材料的红外光谱 Figure 2 FT-IR spectra for 7 kinds of bio-based materials a.CMCS; b.CMC; c.SA; d.胆固醇Cholesterol; a1.CMCSD; b1.CMCD; c1.SAD. |
由图 2分析SA、CMC、SA、胆固醇、SAD、CMCD及CMCSD的IR谱峰归属,如表 1所示。
|
|
由图 2结合表 1可知,7条IR曲线在3 200~ 3 600 cm-1出现强而宽的吸收峰,为—OH伸缩振动产生;2 800~3 000 cm-1存在—CH3、—CH2—和C—H的伸缩峰,在1 300~1 450 cm-1存在—CH3、—CH2—和C—H的变形峰,可知存在—CH3、—CH2—和C—H基团。与IR曲线a、b、c相比,曲线a1、b1以及c1在1 700~1 750 cm-1出现新的吸收峰,此是由酯键中C=O的伸缩振动所致,在900~1 150 cm-1出现C—O—C的伸缩振动峰,可知存在酯键。故可以推断胆固醇分子很可能接枝到SA、CMC、CMCS分子链上,初步说明SAD、CMCD、CMCSD合成成功。
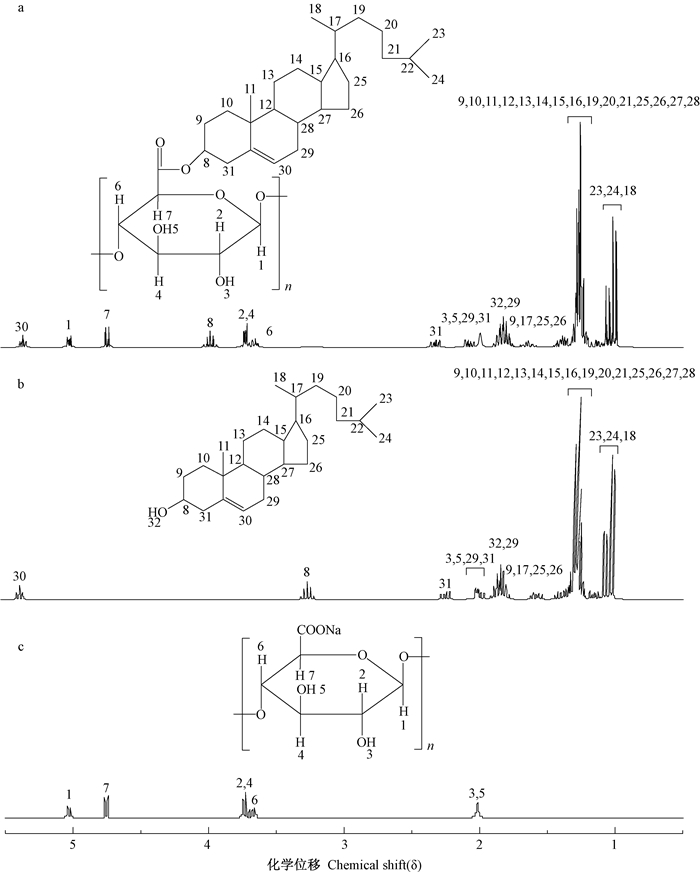
2.2.2 核磁共振波谱(1H NMR,13C NMR)分析SA、胆固醇及SAD的核磁氢谱如图 3所示。
|
图 3 SA(a)、胆固醇(b)及SAD(c)的氢谱 Figure 3 1H-NMR of SA(a), cholesterol(b) and SAD(c) |
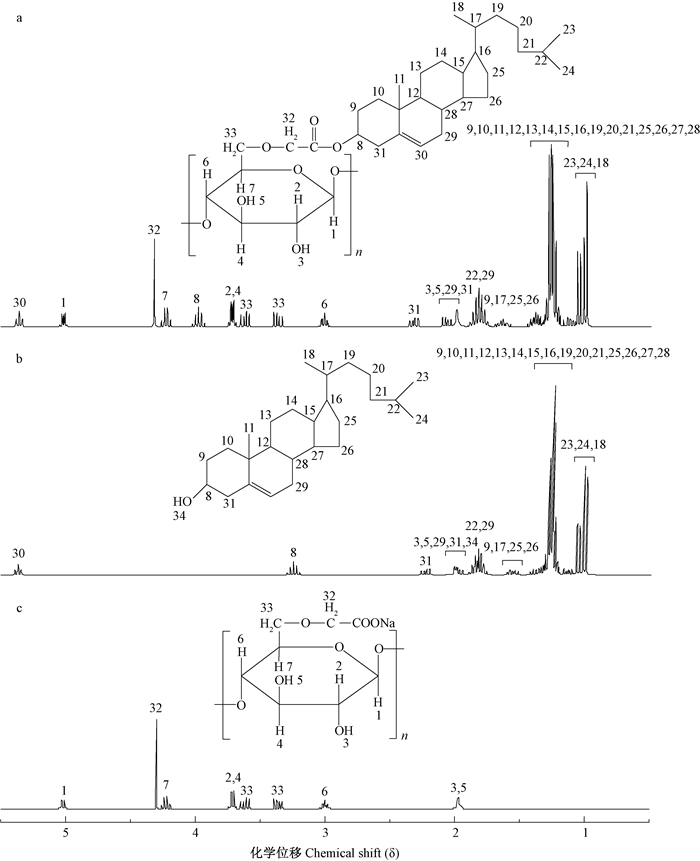
CMC、胆固醇及CMCD的核磁氢谱如图 4所示。
|
图 4 CMC(a)、胆固醇(b)及CMCD(c)的核磁氢谱 Figure 4 1H-NMR of CMC(a), cholesterol(b) and CMCD(c) |
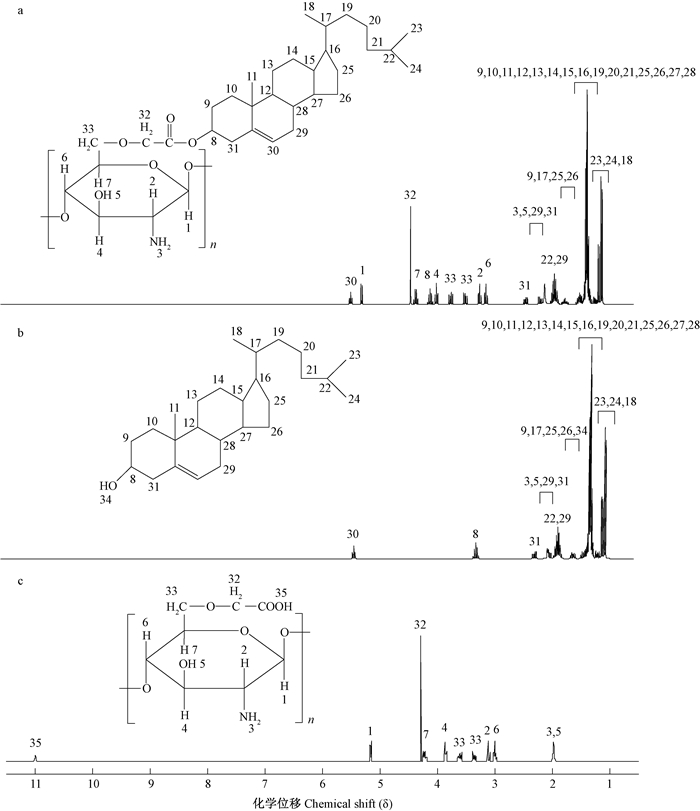
CMCS、胆固醇及CMCSD的核磁氢谱如图 5所示。
|
图 5 CMCS(a)、胆固醇(b)及CMCSD(c)的核磁氢谱 Figure 5 1H-NMR of CMCS(a), cholesterol(b) and CMCSD(c) |
由图 3、图 4及图 5中产物与原料的氢谱对比可知,SAD、CMCD及CMCSD的氢谱中δ=3.5~5.5的信号峰为SA、CMC及CMCS主链上的质子核磁波谱峰。δ=0.5~2.5的信号峰为胆固醇上的质子核磁波谱峰。同时H8的δ由3.25移至4.0,是由于新形成的酯基具有负诱导效应,使得与之相连C上的质子周围电子云密度降低,屏蔽效应减少,δ增加。该结果表明SA、CMC及CMCS分子主链上接枝了胆固醇分子。
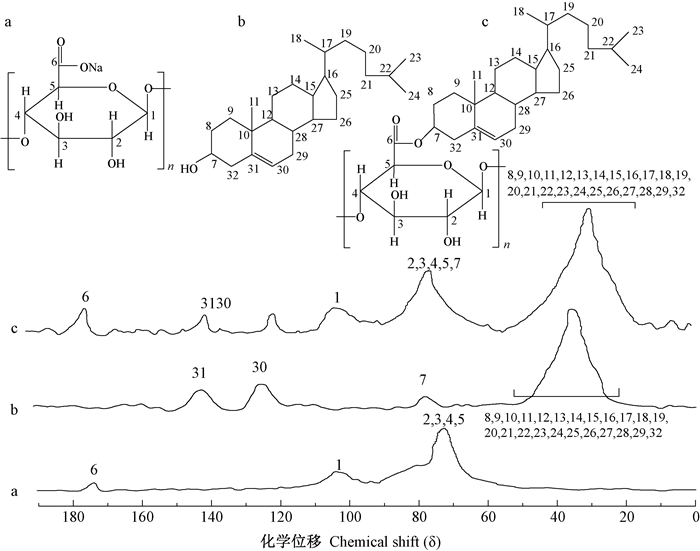
SA、胆固醇及SAD的核磁碳谱如图 6所示。
|
图 6 SA(a)、胆固醇(b)及SAD(c)的核磁碳谱 Figure 6 13C-NMR of SA(a), cholesterol(b) and SAD(c) |
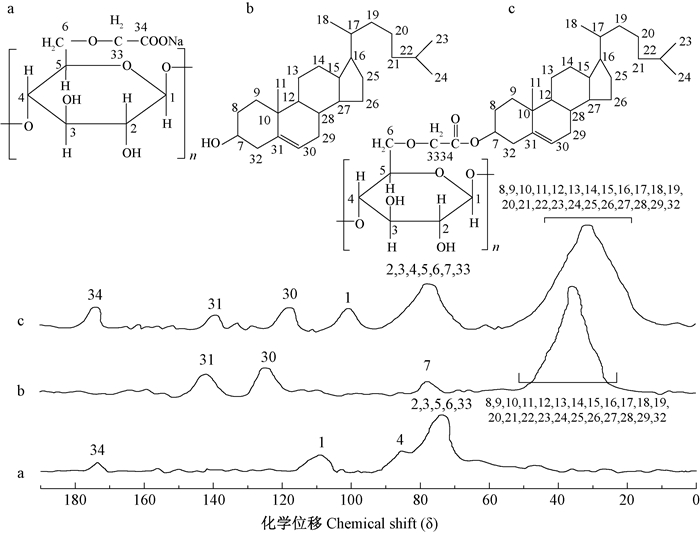
CMC、胆固醇及CMCD的核磁碳谱如图 7所示。
|
图 7 CMC(a)、胆固醇(b)及CMCD(c)的核磁碳谱 Figure 7 13C-NMR of CMC(a), cholesterol(b) and CMCD(c) |
CMCS、胆固醇及CMCSD的核磁碳谱如图 8所示。

|
图 8 CMCS、胆固醇及CMCSD的核磁碳谱 Figure 8 13C-NMR of CMCS, cholesterol and CMCSD |
由图 6、图 7及图 8中产物与原料碳谱对比可知,SAD、CMCD及CMCSD在δ=175出现了羰基碳原子的核磁波谱峰,在δ=108出现了C1的核磁波谱峰,δ=60~95出现了SA、CMC及CMCS基本碳骨架核磁波谱峰。在δ=140及δ=120分别出现了胆固醇中C31及C30的核磁波谱峰,δ=20~50出现了胆固醇基本碳骨架的核磁波谱峰。结果表明SA、CMC及CMCS分子主链上接枝了胆固醇分子。
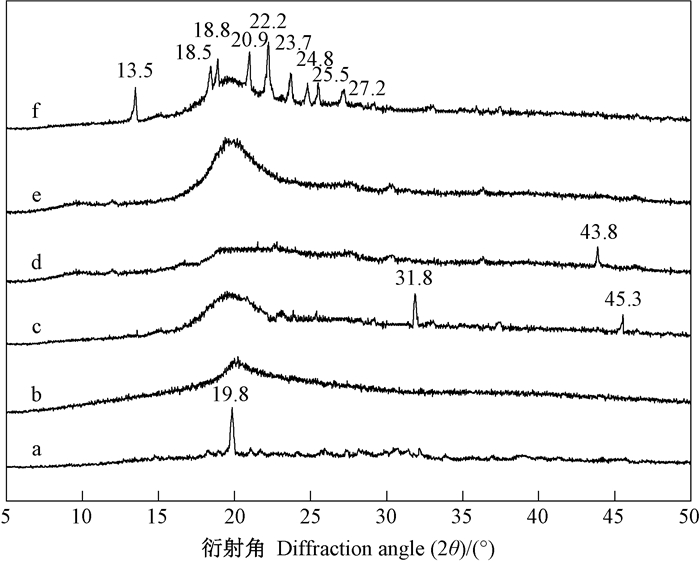
2.2.3 X射线衍射谱图分析SA、CMC、CMCS、SAD、CMCD和CMCSD X射线衍射谱如图 9所示。
|
图 9 6种生物基材料的X射线衍射图谱 Figure 9 X-ray diffraction patterns for 6 kinds of boi-based materials a.SA; b.SAD; c.CMC; d.CMCD; e.CMCS; f.CMCSD. |
上述6种物质的结晶度按公式(3)计算得出,相应数据如表 2所示。
| $ {X_{\rm{c}}} = {S_{\rm{c}}}/\left({K \times {S_{\rm{c}}} + {S_{\rm{a}}}} \right)。$ | (3) |
|
|
式中:Xc为结晶度,Sc为X射线衍射图谱中晶区部分面积,K为校正因子,Sa为X射线衍射图谱中非晶区部分面积。
根据曲线a及b分析,SA衍射曲线在19.8°有一个很强的特征峰,是典型的多晶体系。而在SAD图谱中,19.8°衍射峰峰型减弱、变宽,说明SA结晶结构遭到破坏。
根据曲线c及d分析,CMC衍射曲线由尖峰衍射特征和弥散衍射特征组成,是典型的多晶体系。而在CMCD图谱中,CMC特征峰31.8°和45.3°消失,多晶体系受到破坏。但在43.8°出现新的特征峰,出现新的结晶区,说明胆固醇分子的引入改变其结晶结构。
根据曲线e及曲线f分析,CMCS衍射曲线在20°存在一个很宽的峰,说明CMCS形成无定型结构。而CMCSD谱中,13.5°、18.5°、18.8°、20.9°、22.2°、23.7°、24.8°、25.5°及27.2°处存在9个强峰,说明胆固醇分子的引入增加了其结晶结构。
由图 9结合表 2可知,原料与产物的结晶情况不一致,说明胆固醇分子接枝到SA、CMC及CMCS的分子链上。NMR分析进一步证实了FTIR的结果。
2.3 戊唑醇微纳米胶囊制备新型生物基材料因含有大量亲水基团而具有亲水性,而接枝胆固醇使其分子具有疏水性,即为双亲性分子。该双亲性分子在水中能自发形成一种疏水性内核与亲水性外壳的典型结构,即“核-壳”组装体(Gevorkyen, 2006; Liu et al., 2015)。采用相分离法,在弱酸条件下由新型生物基材制备的纳米胶囊外部具有亲水性,囊壁内侧为疏水区域,从而可将疏水性农药包载于胶囊内部。载药缓释胶囊制备过程如图 10所示。

|
图 10 载药缓释胶囊制备示意 Figure 10 Sketches of drug-loaded sustained-release capsules preparation |
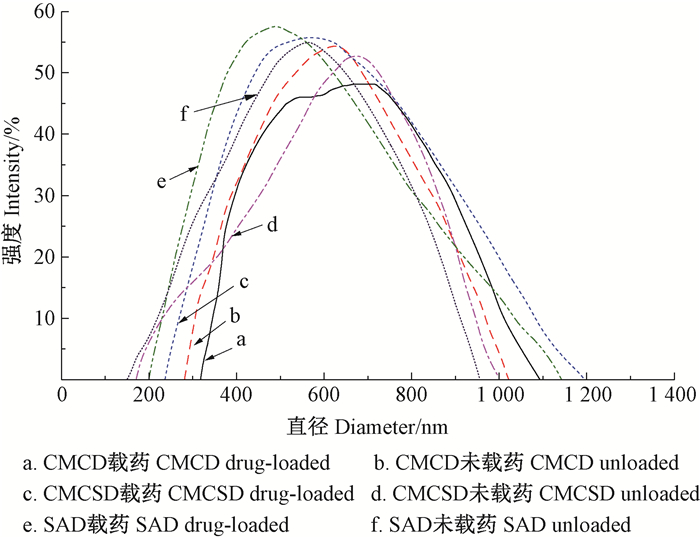
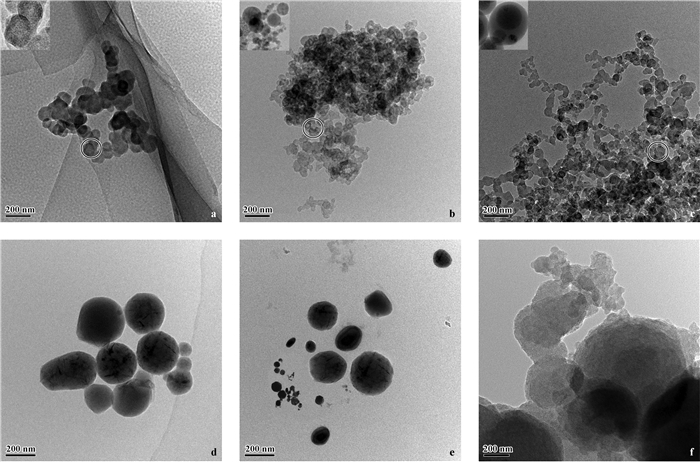
纳米胶囊的粒径分布、平均粒径、TEM分别如图 11、表 3及图 12所示。由图 11结合表 3可知,由动态光散射(dynamic light scattering, DLS)测得未载药纳米胶囊和载药纳米胶囊的平均粒径分别约为549.4~ 638.1 nm和615.9~661.9 nm。图 12中照片a-f均为球形颗粒,其中未载药纳米胶囊的粒径约为50~100 nm,而载药的粒径约为200~300 nm,说明包载农药者大于未包载农药者,初步获得预期目标的载药纳米胶囊。由表 3结合图 12可知,DLS测得的粒径大于透射电镜测得的粒径,主要是因为纳米胶囊在溶液中发生部分聚集,故所测的粒径偏大。
|
图 11 载药与未载药纳米胶囊的粒径分布 Figure 11 Size distribution of blank micelle and tebuconazole- loaded micelle |
|
|
|
图 12 未载药和载药纳米胶囊的透射电镜照片 Figure 12 TEM images of blank micelle and tebuconazole-loaded micelle |
根据(1)式计算SAD纳米胶囊的包封率为72.5%,CMCD纳米胶囊的包封率为69.7%,CMCSD纳米胶囊的包封率为71.1%。说明纳米胶囊具有良好的载药性能。
2.5.2 戊唑醇纳米胶囊的释放动力学3种新型载戊唑醇纳米胶囊及戊唑醇乙酸乙酯溶液的戊唑醇累积释药率如图 13所示。

|
图 13 3种纳米胶囊以及戊唑醇乙酸乙酯溶液的累积释放 Figure 13 Release profiles for 3 kinds of nanocapsules and tebuconazole ethyl acetate solution |
由图 13可知,3种载药纳米胶囊在不同时间的累积释药率与戊唑醇乙酸乙酯溶液相比均达到差异显著水平(P < 0.01)。180 min前,与戊唑醇乙酸乙酯溶液相比,3种载药纳米胶囊累积释药率明显略低,此时戊唑醇乙酸乙酯溶液的累积释药率达到91%,说明戊唑醇绝大部分已从乙酸乙酯溶液中渗出。180 min后,3种载药纳米胶囊累积释药率快速增加,300 min后累积释药率缓慢增加,在1 440 min累积释药率高低顺序为CMCSD > CMCD > SAD, 分别为85.5%、75.2%和51.8%,说明此时戊唑醇还未完全释放,表明3种载药纳米胶囊具有良好的缓释特性。
Peppas方程是根据可降解体系的药物释放动力学研究成果提出的,其描述药物释放规律的表达式为(Ritger et al., 1987):
| $ {\rm{ln}}\frac{{{M_{\rm{t}}}}}{{{M_\infty }}} = {\rm{ln}}k + n{\rm{ln}}t。$ | (5) |
式中:Mt为t时间的累积释放量,M∞为∞时累积释放量;k、n为模型参数;t为释放时间。可利用该公式描述戊唑醇纳米胶囊释药过程。
采用公式(5)对CMCSD、CMCD和SAD纳米胶囊在300 min前累积释药率进行拟合,得到各模型参数,结果见表 4。
|
|
该模型适用于t≤300 min时的数据分析。对于Peppas方程释药特征指数n值:当n≤0.45,药物的释放机制为Fick扩散;当0.45 < n < 0.89,药物释放机制为non-Fick扩散;当n≥0.89,药物释放机制为骨架溶蚀。如表 4所示,相关系数r≥0.99,以上3种戊唑醇纳米胶囊的释药过程符合该模型方程。其中CMCSD纳米胶囊0.45 < n < 0.89,所以该药物释放属于non-Fick扩散,是药物扩散和骨架溶蚀共同作用。而CMCD纳米胶囊和SAD纳米胶囊n < 0.45,故该药物释放属于Fick扩散,主要是药物扩散。
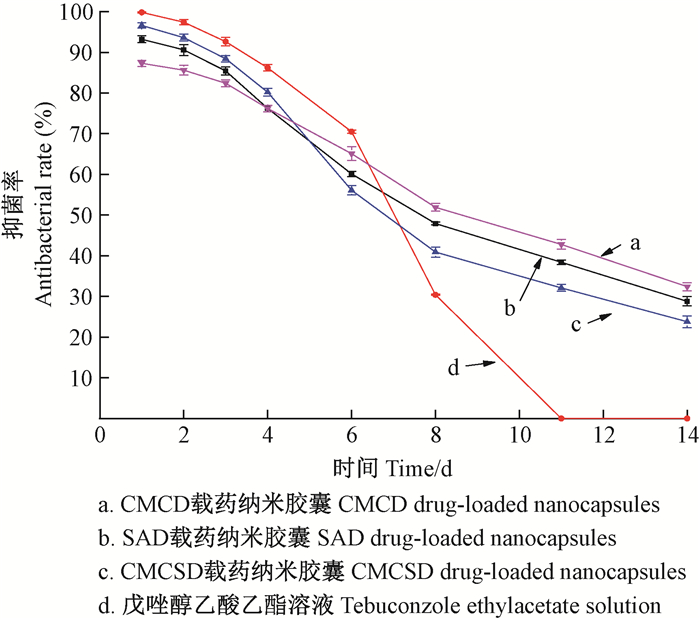
2.5.3 戊唑醇微纳米胶囊抑菌效果3种戊唑醇纳米胶囊及戊唑醇乙酸乙酯溶液对山核桃干腐病菌的抑制效果见图 14。不同处理组对干腐病病菌的抑菌率随时间逐渐降低,与戊唑醇乙酸乙酯溶液的抑菌率相比,前6天3种载药纳米胶囊的抑菌效果略低,但第8天后3种载药纳米胶囊的抑菌效果明显高于戊唑醇乙酸乙酯溶液,同时在第11天戊唑醇乙酸乙酯溶液的抑菌率为0。3种载药纳米胶囊在不同时间的抑菌率与戊唑醇乙酸乙酯溶液相比均达到差异显著水平(P < 0.01)。3种载药纳米胶囊在14天的抑菌效果的强弱顺序为:SAD > CMCD > CMCSD,分别达到32.4%、28.8%和23.8%。说明载药微纳米胶囊具有缓释、长效抑菌性能。
|
图 14 3种载药纳米胶囊及戊唑醇乙酸乙酯溶液对山核桃干腐病菌的抑菌效果 Figure 14 Bacteriostatic effects of three kinds of tebuconazole nanocapsules and tebuconazole ethyl acetate solution on Carya cathayensis canker disease |
田间防效试验结果如表 5所示。施药前山核桃干腐病的病情指数为28.20~30.95;施药后第4天,98%戊唑醇的防效明显优于3种载药纳米胶囊的防效,达到46.8%,主要是由于98%戊唑醇直接作用于患处,具有很好的抑菌效果,而3种载药纳米胶囊中的戊唑醇还未从包载材料中大量释放,只有少量戊唑醇作用于患处,因此抑菌效果较差。施药后第7天,3种载药纳米胶囊的防效超过98%戊唑醇,主要是由于胶囊中的戊唑醇已从包载材料中大量释放,达到很好抑菌效果,而98%戊唑醇已经流失,逐渐失去防效。表明3种载药纳米胶囊具有持久缓释的性能,能够较长时间释放药物,达到抑制山核桃干腐病菌的效果。
|
|
本研究制备的新型SAD、CMCD和CMCSD载药纳米胶囊具有良好的缓释性能,可能是由于纳米胶囊颗粒尺度小、比表面积大,在发挥药效的过程中,农药渗出速度慢所致(Chen et al., 2011),因此3种载药纳米胶囊缓释时间长,抑菌效果较好。同时本研究制备的3种纳米壁材具有两亲性,在水溶液中形成胶束结构,该胶束具有疏水内核与亲水外壳结构,其与水相相互作用,提供了一个相对稳定的相界面(Kato et al., 2006),使疏水性农药稳定分散于水溶液中,但其稳定性受到外界条件的影响,如光、温度、环境的酸碱性等(Langer, 1990)。一般情况下,壁材疏水相的疏水性高,缓释慢,反之疏水性低,亲水相的亲水性高,缓释快(Michael et al., 2006)。同时由于缓释胶囊应用地区不同,其缓释效果也有差别,比如南方酸性环境条件和北方碱性环境条件等,都会影响缓释胶囊壁材的稳定性,从而引起缓释效果的差别。3种载药纳米胶囊具有包载稳定性,降低农药的毒性,减少对环境的污染等优点。但包载过程中由于壁材与药物之间存在分配、吸附等作用,存在部分农药残留,该残留也与环境影响有关,这将是后续探究的重要内容。
在田间防效试验中,3种新型纳米缓释胶囊对山核桃干腐病表现出一定的防效,具有长期防治效果,主要是由于纳米胶囊缓慢释放的戊唑醇对山核桃干腐病病原菌具有抑菌的效果,对干腐病表现出防效,同时由于纳米胶囊中的药物缓慢释放,可增加药物的持效性。但受室外环境影响,对干腐病菌抑菌效果不如室内实验防效有规律性,主要由于试验期间雨水多,有利于干腐病病原菌生长,防治效果不佳。因此室外抑菌试验可作为进一步开展工作的方向。
4 结论本研究以SA、CMC和CMCS为原材料,制备新型生物基材料,利用FT-IR、1H NMR、13C NMR和XRD结构表征谱从结构层次验证设计的目标物;通过包载山核桃干腐病抑菌剂,利用DLS及TEM表观形貌分析结果从定性层次说明形成载药纳米胶囊粒径,利用紫外光谱从定量层次考证载药纳米胶囊的载药性和缓释性,通过抑菌试验从功能层次检验制备载药纳米胶囊抑菌性。依据结构、定性、定量、性能综合试验结果,证明新型纳米生物基农药缓释胶囊制备取得成功。本试验制得粒径为615.9~661.9 nm的3种新型纳米生物基农药缓释胶囊,包封率分别为72.5%、69.7%和71.1%,具有良好的缓释性能;试验第14天时,戊唑醇乙酸乙酯溶液的抑菌率为0%,而3种胶囊对干腐菌的抑菌率分别为32.4%、28.9%和23.8%,具有较好的长期抑菌效果。本研究还进行了田间防治试验,通过试验证实,与施用98%戊唑醇的防治效果相比,3种载药纳米胶囊对山核桃干腐菌具有良好的长期防治效果。该研究结果可以为山核桃干腐病提供新的绿色防治方法,具有广阔的应用前景。
冯建国, 徐妍, 罗湘仁, 等. 2014. 浅谈溶剂蒸发法制备微胶囊与农药微胶囊的开发[J]. 农药学报, 13(6): 568-575. (Feng J G, Xu Y, Luo X R, et al. 2014. Discussion on the solvent evaporation method for preparation of microcapsule and the development of the pesticide microcapsules[J]. Chinese Journal of Pesticide Science, 13(6): 568-575. [in Chinese]) |
郭明, 褚旭东, 王春歌, 等. 2014. 纤维素基生物活性分子生物质材料的制备与表征[J]. 高分子材料科学与工程, 30(4): 148-153. (Guo M, Chu X D, Wang C G, et al. 2014. Preparation and characterization of cellulose-based materials containing single-stranded DNA[J]. Polymer Materials Science and Engineering, 30(4): 148-153. [in Chinese]) |
李北兴, 王凯, 张大侠, 等. 2013. 高含量二甲戊灵微囊悬浮剂物理稳定性的影响因素及优化[J]. 农药学报, 15(6): 692-698. (Li B X, Wang K, Zhang D X, et al. 2013. Factors that affecting physical stability of high content pendimethalin capsule suspension and its optimization[J]. Chinese Journal of Pesticide Science, 15(6): 692-698. [in Chinese]) |
李继昭, 袁志强, 闫萌, 等. 2016. cRGD介导的pH敏感性紫杉醇羧甲基壳聚糖-软脂酸胶束[J]. 药学学报, 51(4): 642-649. (Li J Z, Yuan Z Q, Yan M, et al. 2016. pH-sensitive micelles loaded paclitaxel using carboxymethyl chitosan-palmitic acid mediated by cRGD[J]. Chinese Journal of Pesticide Science, 51(4): 642-649. [in Chinese]) |
田甜, 沈振明, 徐秋芳, 等. 2012. 土壤中山核桃干腐病抑制菌的筛选和鉴定[J]. 浙江农林大学学报, 29(1): 58-64. (Tian T, Shen Z M, Xu Q F, et al. 2012. Screening and identification of inhibiting strains for carya cathayensis canker disease[J]. Journal of Zhejiang A & F University, 29(1): 58-64. [in Chinese]) |
席丽霞, 马星霞, 蒋明亮. 2013. 三唑制剂的防腐及防白蚁性能[J]. 林业科学, 49(7): 123-128. (Xi L X, Ma X X, Jiang M L, et al. 2013. Decay and termite resistant performance of triazole preservatives[J]. Scientia Silvae Sinicae, 49(7): 123-128. DOI:10.11707/j.1001-7488.20130718 [in Chinese]) |
俞娟, 刘少峰, 刘玉鹏, 等. 2016. 两亲性纤维素接枝聚脱氢枞酸共聚物的制备及性能研究[J]. 高分子学报, 16(5): 591-598. (Yu J, Liu S F, Liu Y P, et al. 2016. Preparation and properties of amphiphilic cellulose grafted dehydroabietic acid copolymer[J]. Macromolecular Material, 16(5): 591-598. [in Chinese]) |
杨淑贞, 丁立忠, 楼君芳, 等. 2009. 山核桃干腐病发生发展规律及防治技术[J]. 浙江林学院学报, 26(2): 228-232. (Yang S Z, Ding L Z, Lou J F, et al. 2009. Occurrence regularity of Carya cathayensis canker disease and its control[J]. Journal of Zhejiang Forestry College, 26(2): 228-232. [in Chinese]) |
Aouada F A, Moura M A, Orts W J. 2010. Polyacrylamide and methylcellulose hydrogel as delivery vehicle for the controlled release of paraquat pesticide[J]. Journal of Materials Science, 45(18): 4977-4985. DOI:10.1007/s10853-009-4180-6 |
Bakshi M S. 2016. How surfactants control crystal growth of nanomaterials[J]. Crystal Growth & Design, 16(2): 1104-1133. |
Casettari L, Vllasaliu D, Castagnina E, et al. 2012. PEGylated chitosan detivatives: Synthesis, characterizations and pharmaceutical applications[J]. Progress in Polymer Science, 37(5): 659-685. DOI:10.1016/j.progpolymsci.2011.10.001 |
Chen H D, Yada R. 2011. Nanotechnologies in agriculture: New tools for sustainable development[J]. Trends in Food Science & Technology, 22(11): 585-594. |
Fallaha F, Khorasanib M, Ebrahimic M. 2016. Comparative study of gel emulsification and direct mechanical emulsification methods[J]. Physicochemical and Engineering Aspects, 492(5): 207-212. |
Gevorkyen M G. 2006. Influence of micelles of different types of surfactant on the mechanism of diphenylamine oxidation with potassium persulfate[J]. Kinetics and Catalysis, 37(17): 364-367. |
Jiang Z W, Han B Q, Li H, et al. 2015. Preparation and anti-tumor metastasis of carboxymethl chitosan[J]. Carbohydrate Polymers, 125(2): 53-60. |
Kato M, Toyoda H, Namikawa T, et al. 2006. Optimized use of a biodegradable polymer as a carrier material for the local delivery of recombinant human bone morphogenetic protein-2(rhBMP-2)[J]. Biomaterials, 27(9): 2035-2041. DOI:10.1016/j.biomaterials.2005.10.007 |
Liu N J, He Q, Bu W F. 2015. Self-assembly of star micelle into vedicle in solvents of variable quality:the star micelle retains its core-shell nanostructure in the vesicle[J]. Langmuir: the Acs Journal of Surfaces and Colloids, 31(8): 2262-2268. DOI:10.1021/la504817q |
Langer R. 1990. New methods of drug delivery[J]. Science, 249(4976): 1527-1533. DOI:10.1126/science.2218494 |
Michael C B, Lei Z, Robert E C, et al. 2006. Controlled drug release from porous polyelectrolyte multilayers[J]. Biomacromolecules, 7(1): 357-364. DOI:10.1021/bm050174e |
Ramadossa P, Arulab K, Ramyaa J, et al. 2017. Enhanced mechanical strength and sustained drug release of gelatin/keratin scaffolds[J]. Materials Letters, 186(1): 109-112. |
Ritger P L, Peppas N A. 1987. A simple equation for description of solute release Ⅰ. Fickian and anomalous release from nonswellable devices in the form of slabs, spheres, cylinders or discs[J]. Journal of Controlled Release, 5(1): 23-36. DOI:10.1016/0168-3659(87)90034-4 |
Sosnik A. 2016. Drug self-assembly: A phenomenon at the nanometer scale with major impact in the structure biological properties relationship and the treatment of disease[J]. Progress in Materials Science, 82(9): 39-82. |
Suttia A, Chaffraixa T, Vodaa A S, et al. 2016. Nano-capsules of amphiphilic poly(ethylene glycol)-block-poly(bisphenol A carbonate) copolymers via thermodynamic entrapment[J]. Rsc Advances, 6(8): 6065-6071. DOI:10.1039/C5RA23555C |
Yang J S, Ren H B, Xie Y J. 2011. Synthesis of amidic alginate derivatives and their application in microencapsulation of λ-cyhalothrin[J]. Biomacromolecules, 12(8): 2982-2987. DOI:10.1021/bm200571k |
Yang L Q, Zhang B F, Wen L Q, et al. 2007. Amphiphilic cholesteryl grafted sodium alginate derivative: Synthesis and self-assembly in aqueous solution[J]. Carbohydrate Polymers, 68(2): 218-225. DOI:10.1016/j.carbpol.2006.12.020 |
Zhang Z Y, Zhai S H, Wang J H. 2012. Preparation of cyhalothrin micro-emulsion formulation and its micro-droplet size[J]. Agrochemicals, 51(5): 351-355. |
Zhao S F, Zhang X, Zhang X J, et al. 2016. Preparation and release characteristics study on the novel minocycline hydroch-loride sustained-release capsule[J]. Bangladesh Journal of Pharmacology, 11(S1): S36-S43. DOI:10.3329/bjp.v11iS1.26415 |
 2018, Vol. 54
2018, Vol. 54

