文章信息
- 刘生冬, 孟昕, 孟庆繁, 李燕, 赵红蕊, 高文韬
- Liu Shengdong, Meng Xin, Meng Qingfan, Li Yan, Zhao Hongrui, Gao Wentao
- 阔叶红松林不同林分对地表甲虫群落的影响
- Influence of Different Stands on Ground-Dwelling Beetle Community in Broad-Leaved Korean Pine Forests
- 林业科学, 2018, 54(2): 110-118.
- Scientia Silvae Sinicae, 2018, 54(2): 110-118.
- DOI: 10.11707/j.1001-7488.20180212
-
文章历史
- 收稿日期:2017-05-04
- 修回日期:2017-06-27
-
作者相关文章
阔叶红松(Pinus koraiensis)林是我国东北东部林区地带性顶级植物群落, 林内动植物种类丰富, 林分结构稳定, 在生物多样性保护中起着重要作用。多年来, 阔叶红松林经过采伐等人为干扰, 形成了大面积次生阔叶混交林, 仅在局部地区存在小面积的原始阔叶红松林(胡艳波等, 2003;魏丽萍, 2014;傅俊卿, 2009)。
在森林地表生活的甲虫(简称地表甲虫)是森林昆虫的重要组成部分, 其结构特殊、食性复杂, 对环境具有较强的适应能力, 在维持森林生态系统平衡过程中起着重要作用, 引起了研究者的广泛关注(任国栋等, 2005;于晓东等, 2004;贺春霞等, 2009;Irmler, 2003;Butterfield et al., 1995;Noss, 1990;Hanavan et al., 2008;Jung et al., 2014)。天然林在保护地表甲虫物种多样性方面作用不可替代(于晓东等, 2002;2006a;Whitter, 1977), 同时, 天然林中的枯腐木和碎木屑对地表甲虫的影响可能超过其他环境因子, 枯木和碎屑能够增加地表甲虫的丰富度(Topp et al., 2006)。短期采伐的森林中地表甲虫丰富度较高(于晓东等, 2006b), 森林的边缘有助于提高地表甲虫的数量(Avgin, 2006;Francese et al., 2008;Diamond, 1975;Saunders et al., 1991)。植被组成也影响着地表甲虫的多样性, 不同功能的地表甲虫对环境变化的反应各不相同(Schaffers et al., 2008;Aldhafer et al., 2016)。森林中地表甲虫多以捕食性和腐食性种类占优势, 不同类群的地表甲虫对林冠层的覆盖度和枯落物厚度反应各不相同(于晓东等, 2006a;2006c)。森林的郁闭度、枯落物和土壤含水量影响着地表甲虫多度的分布格局(于晓东等, 2006a;Sroka et al., 2006;杭佳等, 2014), 有研究显示, 枯落物对地表甲虫的影响可能是间接的, 枯落物能够增加地表的湿度和温度进而影响地表甲虫分布, 湿度和温度可能超过了枯落物自身对地表甲虫具有更大的影响(Magura et al., 2004)。
现有研究中, 林分因子对地表甲虫的影响报道较少。鉴于此, 本研究通过2年时间, 在地表甲虫活跃期内连续诱集甲虫标本, 全面调查阔叶红松林中地表甲虫的物种组成和多样性, 揭示林分类型和主要林分因子对地表甲虫多样性的影响, 以及地表甲虫优势类群对不同林分的适应能力, 为评价天然林在保护地表甲虫中的作用及为制定基于地表甲虫保护与利用的森林经营方案提供科学依据。
1 研究区概况与研究方法 1.1 研究区概况研究区位于吉林省蛟河林业实验区内, 属于长白山林区, 地理位置127°35′—127°51′E, 43°51′—44°05′N。海拔最高为1 176 m, 海拔最低约330 m, 平均海拔800 m。研究区植物资源丰富, 人为干扰较少, 保留了长白山林区少有的原始阔叶红松林, 以及杨桦林[山杨(Populus davidiana)白桦(Betula platyphylla)]、水胡林[水曲柳(Fraxinus mandshurica)胡桃楸(Juglans mandschurica)]和阔叶混交林等(王辉等, 2012;李良等, 2014)。主要乔木树种有红松、沙冷杉(Abies holophylla)、鱼鳞云杉(Picea jezoensis var.microsperma)、水曲柳、胡桃楸、紫椴(Tilia amurensis)、糠椴(Tilia mandschurica)、花曲柳(Fraxinus rhynchophylla)、蒙古栎(Quercus mongolica)、色木槭(Acer mono)、假色槭(Acer pseudo-sieboldianum)、白牛槭(Acer mandshuricum)、春榆(Ulmus japonica)、白桦、枫桦(Betula costata)和山杨等, 常见的灌木有珍珠梅(Sorbaria kirilowii)、暴马丁香(Syringa reticulata var. mandshurica)、长白忍冬(Lonicera ruprechtiana)和胡枝子(Lespedeza bicolor)等。
1.2 研究方法 1.2.1 样地设置根据研究区林分分布特点, 选择有代表性的杨桦林(YHL)、水胡林(SHL)、阔叶红松林A(KHA)和阔叶红松林B(KHB)4种林分, 每个林分面积为300 m×400 m。各林分概况如下:1)杨桦林—中心坐标127°42′53″E, 43°57′59″N, 海拔430 m, 平均林龄约50年, 属中龄林, 主要乔木树种有白桦、山杨、胡桃楸、水曲柳、春榆和假色槭等, 郁闭度0.6;2)水胡林—中心坐标127°43′12″E, 43°57′52″N, 海拔430 m, 平均年龄约70年, 属近熟林, 主要乔木树种有胡桃楸、水曲柳、白桦、山杨、红松、鱼鳞云杉、春榆和色木槭等, 郁闭度0.7;3)阔叶红松林A—中心坐标127°45′26″E, 43°59′33″N, 海拔550 m, 平均年龄约80年, 属成熟林, 主要乔木树种有红松、鱼鳞云杉、胡桃楸、水曲柳、春榆、紫椴、山杨、色木槭和白牛槭等, 郁闭度0.8; 4)阔叶红松林B—中心坐为127°45′22″E, 43°58′2″N, 海拔660 m, 平均年龄约90年, 属成熟林, 主要乔木树种有红松、鱼鳞云杉、水曲柳、胡桃楸、紫椴、枫桦、春榆、色木槭和白牛槭等, 郁闭度0.8。
1.2.2 调查方法采用陷阱法诱捕地表甲虫, 在每种林分的中心点和4个顶点分别设置1个样地。每个样地按2 m边长的正方形布置诱杯, 诱杯间距1 m, 每个样地共9个诱杯。诱杯使用高约9 cm的一次性塑料水杯, 诱杯中放入约100 mL诱剂, 诱剂由醋、白糖、酒精和水配制, 比例约为2:1:1:20;同时在诱杯中放入少量无味的食盐, 防止标本腐烂。以每个样地的全部诱杯为记录单位, 分别记录各样地诱杯所捕获的地表甲虫, 并分类标号保存。
1.2.3 调查时间2012—2013年每年5月中旬布置诱捕器, 8月下旬取回诱捕器, 布设时间涵盖整个地表甲虫活跃期, 每月上旬和下旬各回收1次地表甲虫标本。
1.2.4 地表甲虫鉴定在实验室分类统计采集到的全部地表甲虫标本, 并编号、制成针插标本保存。所有标本收藏在北华大学林学院昆虫标本室, 参考现已出版的各类甲虫相关分类资料进行标本鉴定。步甲科(Carabidae)部分种类由中国科学院动物研究所梁红斌副研究员鉴定, 隐翅虫科(Staphylinidae)部分种类由上海师范大学汤亮老师鉴定。
1.2.5 数据分析以下参数用于数据多样性分析(庞雄飞等, 1996;马克平等, 1994;戈峰, 2008): 1)物种丰富度指数采用Margalef指数(D):D=(S-1)/lnN, 式中:S为物种数, N为个体总数。2)物种多样性采用Shannon-Wiener指数(H′):
采集地表甲虫9 849头, 隶属于22科79种, 其物种组成见表 1。
|
|
本研究调查时间涵盖地表甲虫整个活跃期, 采集到地表甲虫的物种数和个体数都较多, 其中, 步甲科共21种5 252个个体, 分别占总物种数的26.58%和总个体数的53.34%, 在整个地表甲虫中占绝对优势, 尖齿通缘步甲(Pterostichus acutidens)为优势种, 数量占总个体数的27.36%。步甲科、埋葬甲科和隐翅虫科为优势类群, 金龟科和阎甲科为常见类群, 其余17个科为稀有类群。
杨桦林中采集地表甲虫1 415头, 占总个体数的13.37%, 优势种为尖齿通缘步甲、粒步甲(Carabus granulatus)和赤条棘步甲(Leptocarabus kurilensis); 水胡林中采集地表甲虫717头, 占总个体数的7.28%, 优势种为尖齿通缘步甲、赤条棘步甲和四星覆葬甲(Nicrophorus quadripunctatus); 阔叶红松林A中采集地表甲虫3 530头, 占总个体数的35.84%, 优势种为尖齿通缘步甲、比氏步甲(Carabus billbergi)和四星覆葬甲; 阔叶红松林B中采集表甲虫4 187头, 占总个体数的42.51%, 优势种为尖齿通缘步甲、细腿黑覆葬甲(Nicrophorus tenuipes)和日真葬甲(Necrophila japonica)。杨桦林和水胡林中的地表甲虫个体数小于阔叶红松林A和阔叶红松林B。各类群中, 步甲科在4种林分中都为优势类群, 并且数量所占比重很大, 埋葬甲科在水胡林、阔叶红松林(A和B)中为优势类群, 隐翅虫科在杨桦林、阔叶红松林A中为优势类群。
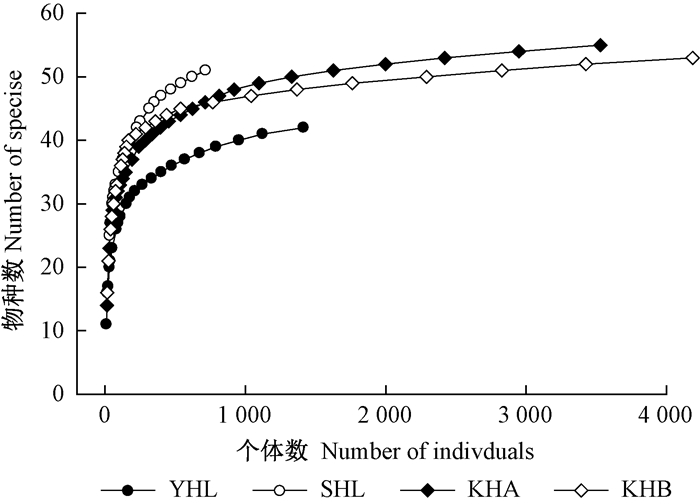
2.1.2 地表甲虫种-多度曲线不同林分地表甲虫种-多度曲线见图 1。
|
图 1 不同林分地表甲虫种-多度曲线 Figure 1 Rarefaction curve based on species-individuals of ground-dwelling beetles in different stands |
由图 1可知, 在阔叶红松林(A和B)中地表甲虫的个体数量远高于杨桦林和水胡林, 其中, 水胡林和阔叶红松林(A和B)中的物种数量相差较少, 当抽取个体数少于2 000时, 水胡林中地表甲虫的多样性较高, 当抽取个体超过2 000时, 阔叶红松林A中地表甲虫的多样性最高, 杨桦林最低。
2.1.3 不同林分地表甲虫多样性不同林分地表甲虫多样性各指数见表 2。
|
|
由表 2可知, 阔叶红松林A中地表甲虫物种数最多, 显著高于杨桦林和水胡林, 阔叶红松林B显著高于杨桦林(F=6.026;df=3, 16;P < 0.01)。阔叶红松林A和阔叶红松林B中个体数显著高于杨桦林和水胡林, 杨桦林显著高于水胡林(F=51.938;df=3, 16;P < 0.001)。丰富度在阔叶红松林A中最高, 杨桦林最低, 林分对丰富度指数无显著影响(F=3.507;df=3, 16;P>0.05)。多样性指数在水胡林中最高, 杨桦林最低, 林分对多样性指数无显著影响(F=3.271; df=3, 16;P>0.05)。均匀度指数在水胡林中最高, 显著高于其他3种林分, 阔叶红松林B最低, 林分对均匀度指数影响显著(F=8.114;df=3, 16;P < 0.01)。经相关分析, 不同林分中地表甲虫的个体数量与均匀度指数呈负相关(R=-0.975;P < 0.05)。
2.1.4 不同林分地表甲虫相似性不同林分间地表甲虫相似性见表 3。
|
|
阔叶红松林(A和B)中环境条件相似, 相同种类较多, 使其林分间地表甲虫的相似性最高, 相似性系数为0.60, 达到了中等相似水平。阔叶红松林B和杨桦林、水胡林间植被条件差异较大, 使阔叶红松林B与杨桦林、水胡林间的相似性都较低, 相似性系数为0.44, 为中等不相似。
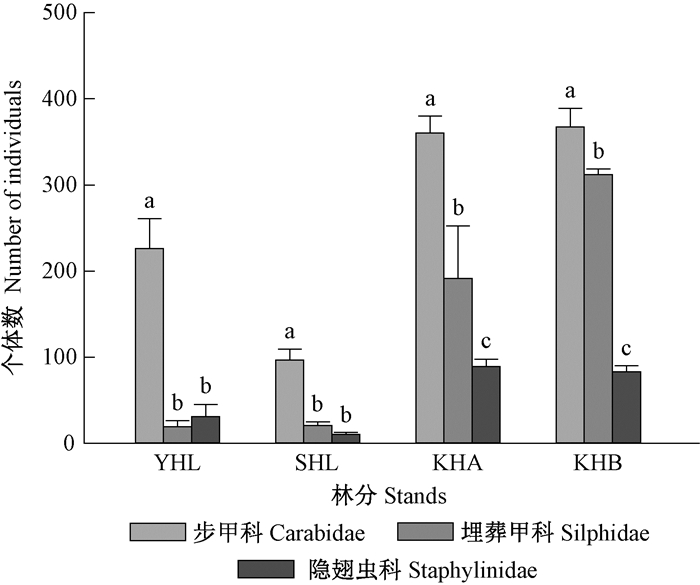
2.1.5 不同林分地表甲虫优势类群个体数步甲科、埋葬甲科和隐翅虫科是本研究中地表甲虫的优势类群, 分别占总个体数的53.34%、27.57%和10.83%, 3个类群合计占总个体数的91.74%。4种林分中, 步甲科、埋葬甲科和隐翅虫科个体数见图 2、3。
|
图 2 不同林分步甲科、埋葬甲科和隐翅虫科个体数 Figure 2 The number of individuals of Carabidae, Silphidae and Staphylinidae in different stands |
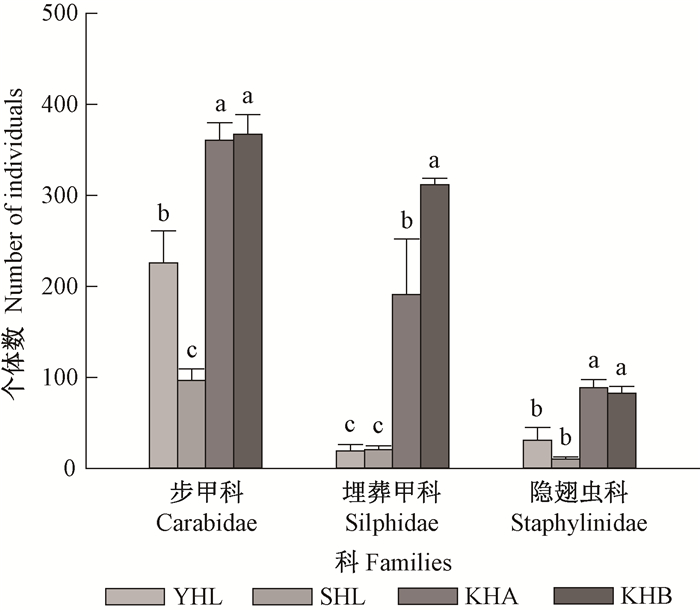
|
图 3 步甲科、埋葬甲科和隐翅虫科在不同林分中的个体数 Figure 3 The number of individuals of different stands of Carabidae, Silphidae and Staphylinidae |
在4种林分中, 林分类型对步甲科、埋葬甲科和隐翅虫科的个体数都有显著影响(F>14.44;df=2, 12; P < 0.001), 步甲科的个体数显著高于埋葬甲科和隐翅虫科, 在阔叶红松林A和B中埋葬甲科显著高于隐翅虫科。在杨桦林和水胡林中埋葬甲科和隐翅虫科的个体数无显著差异。林分对步甲科的数量影响显著(F=29.529;df=3, 16;P < 0.001), 在阔叶红松林A和B中步甲科个体数显著高于杨桦林和水胡林, 杨桦林中的数量显著高于水胡林。林分对埋葬甲科的个体数影响显著(F=21.096;df=3, 16;P < 0.001), 阔叶红松林A和B中的数量显著高于其他2种林分, 阔叶红松林A中数量显著高于阔叶红松林B。林分对隐翅虫科的数量影响显著(F=17.879;df=3, 16;P < 0.001), 隐翅虫科在阔叶红松林A和B中的数量显著高于其他2种林分。不同林分中步甲科的个体数与隐翅虫的个体数具有较强的相关性, 符合线性模型Y=89.68+ 3.241x(R2=0.951)。
2.2 主要林分因子对地表甲虫个体数的影响通过对地表甲虫各类群的个体数与杨桦林、水胡林、阔叶红松林A、阔叶红松林B的典范对应分析(CCA), 能够比较直观的反映出甲虫各类群对不同林分的选择倾向性, 以及主要林分因子对地表甲虫各类群的影响。本研究选择与地表甲虫群落关系比较密切的郁闭度、林龄、枯落物厚度、草本盖度、每公顷株数、灌木盖度6个因子, 不同林分各主要因子见表 4。
|
|
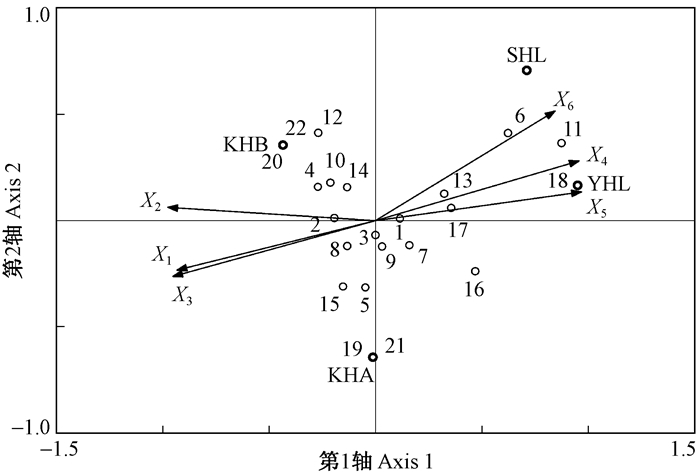
图 4中以步甲科和象甲科为界限, 阔叶红松林2种林分中的地表甲虫个体数多于杨桦林和水胡林, 表明地表甲虫对阔叶红松林的选择倾向性高于其他2种林分。步甲科对杨桦林的选择倾向性高于埋葬甲科、隐翅虫科, 埋葬甲科、隐翅虫科对阔叶红松林的选择倾向性高于步甲科。其他类群中, 阎甲科、吉丁虫科对阔叶红松林A的倾向性较高; 金龟科、拟步甲科、锹甲科和花金龟科对阔叶红松林B具有较强的倾向性。在杨桦林和水胡林个体数相对较多的地表甲虫类群中, 叩甲科、水龟虫科、卷象科、露尾甲科和虎甲科对杨桦林和水胡林的选择倾向性高于其他类群。卷象科、皮金龟科、丸甲科、叶甲科和蚁形甲科只在1个林分中采集到。
|
图 4 22个甲虫类群与4种林分和林分因子典范对应分析 Figure 4 Canonical correspondence analysis of 22 groups, 4 stands and stand factors 1.步甲科 Carabidae; 2.埋葬甲科 Silphidae; 3.隐翅虫科 Staphylinidae; 4.金龟科 Scarabaeidae; 5.阎甲科 Histeridae; 6.叩甲科 Elateridae; 7.象甲科 Curculionidae; 8.芫菁科 Meloidae; 9.鳃金龟科 Melolonthidae; 10.拟步甲科 Tenebrionidae; 11.水龟虫科 Hydrophilidae; 12.锹甲科 Lucanidae; 13.虎甲科 Cicindelidae; 14.花金龟科 Cetoniidae; 15.吉丁虫科 Buprestidae; 16.粪金龟科 Geotrupidae; 17.露尾甲科 Nitidulidae; 18.卷象科 Attelabidae; 19.皮金龟科 Troaidae; 20.丸甲科 Byrrhidae; 21.叶甲科 Chrysomelidae; 22.蚁形甲科 Anthicidae. |
由图 4可知, 郁闭度X1、林龄X2与枯落物厚度X3相关性较强, 可划分为一类, 而郁闭度X1、林龄X2在本研究中位置几乎重叠, 显示出极强的相关性。草本盖度X4、每公顷株数X5和灌木盖度X6都分布在第一象限, 相关性较强。叩甲科、水龟虫科、卷象科、虎甲科、粪金龟科、露尾甲科与草本盖度、每公顷株数、灌木盖度有较高的相关性。丸甲科、蚁形甲科、锹甲科、金龟科、拟步甲科、埋葬甲科、花金龟科与林龄关系比较密切。皮金龟科、叶甲科、吉丁虫科、阎甲科、芫菁科与郁闭度和枯落物厚度比较密切。从各林分因子上看, 郁闭度和枯落物厚度对皮金龟科、叶甲科、丸甲科、蚁形甲科、吉丁虫科影响较大, 影响程度依次降低。林龄对丸甲科、蚁形甲科、吉丁虫科、锹甲科、金龟科、拟步甲科的影响依次降低。灌木盖度对水龟虫科、叩甲科、水龟虫科影响较大, 草本盖度和每公顷株数对卷象科、水龟虫科、叩甲科影响较大。在3个优势类群中, 埋葬甲科对郁闭度、林龄、枯落物厚度的选择倾向性高于其他2个类群, 步甲科较倾向于草本盖度、每公顷株数、灌木盖度高的环境, 而隐翅虫科对环境因子没有表现出明显的选择倾向性。
3 讨论地表甲虫是森林昆虫的重要组成部分, 其食性复杂、数量巨大, 多为捕食性和腐食性种类。不同林分中地表甲虫多样性的差异化, 显示出地表甲虫对森林环境的不同适应能力。林分因子影响森林内的枯落物厚度、湿度和郁闭度等微环境, 进而影响地表甲虫的组成和结构, 已有研究显示枯落物厚度、郁闭度、土壤含水量和地表温度等是影响地表甲虫多样性的主要因素(于晓东等, 2006a; 2006b; 2006c;Magura et al., 2004)。在人为干扰较小的情况下, 林分各主要因子存在一定的相关性, 本研究的6个林分因子中, 郁闭度、林龄和枯落物厚度对大多数地表甲虫有较高的正向影响, 不同林分中, 地表甲虫的个体数在阔叶红松林中最高, 这主要是由于阔叶红松林的树种组成结构复杂, 林内植物丰富, 随着林龄增加能够使林木的蓄积、郁闭度和林内的枯落物厚度都有所增加, 土壤的含水能力得到增强, 含水量有所提升。森林郁闭度的增高能降低林中的光照, 有利于保持地表枯落物的湿度, 这些都会使林内地表甲虫的数量有所增加(Sroka et al., 2006;杭佳等, 2014)。
在各主要林分因子中, 步甲科倾向于选择每公顷株数、草本盖度和灌木盖度较高的环境, 这与一些研究结果(Eyre et al., 2004;Tyler, 2008)比较相似。步甲科是甲虫中古老和较大的类群, 对环境适应能力较强, 步甲科多为一些地表甲虫研究中的优势类群(于晓东等, 2003;Renkema et al., 2012;冀卫荣等, 2008), 由于步甲的取食特征, 林内食物资源的数量将会影响步甲科的物种组成和多样性变化(Khobrakova et al., 2005), 潮湿的环境能够增加步甲科的多度(李景科, 1992)。埋葬甲科对林龄、郁闭度较高和枯落物厚的环境具有倾向性, 这可能是由于在高郁闭度的老龄林中, 枯落物较厚, 可取食的腐烂食物较多。各林分因子对隐翅虫科的影响相对较小, 这与隐翅虫的取食方式和生活习性有关, 使其对森林的变化反应不敏感。在不同林分中, 只有步甲科与隐翅虫科的个体数具有一定的相关性, 符合线性模型分布, 而其他类群间没有表现出相关性, 2个类群的个体数在其他生境中是否也存在这种相互关系需要进一步验证。
4 结论本研究在阔叶红松林4种林分中共采集到地表甲虫9 849头, 隶属于22科79种, 稀有类群较多。在步甲科、埋葬甲科和隐翅虫科3个优势类群中, 步甲科和隐翅虫科的个体数在阔叶红松林中最多, 这与阔叶红松林中生物多样性较高、能为步甲科和隐翅虫科昆虫提供充足的食物资源有关, 步甲科对杨桦林的适应能力略高于埋葬甲科和隐翅虫科。埋葬甲科的个体数在阔叶红松林中远高于其他林分, 表现出其对环境变化较高的敏感性, 这与研究凉水自然保护区和长白山保护区地表甲虫物种多样性的结果(顾伟等, 2014;贾玉珍等, 2011)较为相似。
林分类型对地表甲虫的物种数和个体数均有显著影响, 阔叶红松林中地表甲虫的数量显著高于杨桦林和水胡林。地表甲虫的个体数与均匀度具有较高水平的负相关, 尖齿通缘步甲等个别优势种得到了很好的发展, 使阔叶红松林中地表甲虫的多样性指数和均匀度较低。相似的环境条件使得阔叶红松林2种林分间相似性最高, 达到中等相似水平。阔叶红松林相对于其他林分在保护地表甲虫多样性方面具有更加重要的作用。
傅俊卿. 2009. 东北天然红松林资源现状与保护经营对策[J]. 东北林业大学学报, 37(2): 75-78. (Fu J Q. 2009. Current situation of natural Korean pine forests in northeast china and their management counter measures[J]. Journal of Northeast Forestry University, 37(2): 75-78. [in Chinese]) |
戈峰. 2008. 昆虫生态学原理与方法[M]. 北京: 高等教育出版社. (Ge F. 2008. Principle and method of insect ecology[M]. Beijing: Higher Education Press. [in Chinese]) |
顾伟, 马玲, 刘哲强, 等. 2014. 凉水自然保护区不同林型地表甲虫物种多样性[J]. 东北林业大学学报, 42(1): 131-135. (Gu W, Ma L, Liu Z Q, et al. 2014. Diversity of ground-dwelling beetle with different forest type in Liangshui Nature Reserve[J]. Journal of Northeast Forestry University, 42(1): 131-135. [in Chinese]) |
杭佳, 石云, 刘文惠, 等. 2014. 宁夏黄土丘陵区不同生态恢复生境地表甲虫多样性[J]. 生物多样性, 22(4): 516-524. (Hang J, Shi Y, Liu W H, et al. 2014. Diversity of ground-dwelling beetles (Coleoptera) in restored habitats in the hill and gully area of Loess Plateau, Ningxia Hui Autonomous Region[J]. Biodiversity Science, 22(4): 516-524. [in Chinese]) |
贺春霞, 杜沛宜, 于晓东, 等. 2009. 大巴山北坡地表甲虫的物种多样性[J]. 应用生态学报, 20(6): 1459-1464. (He C X, Du P Y, Yu X D, et al. 2009. Species diversity of ground-dwelling beetles on northern slope of Daba Mountain, China[J]. Chinese Journal of Applied Ecology, 20(6): 1459-1464. [in Chinese]) |
胡艳波, 惠刚盈, 戚继忠, 等. 2003. 吉林蛟河天然红松阔叶林的空间结构分析[J]. 林业科学研究, 16(5): 523-530. (Hu Y B, Hui G Y, Qi J Z, et al. 2003. Analysis of the spatial structure of natural korean pine broad leaved forest[J]. Forest Research, 16(5): 523-530. [in Chinese]) |
冀卫荣, 胡俊杰, 孟翔, 等. 2008. 庞泉沟国家级自然保护区落叶松林地表甲虫的多样性[J]. 林业科学, 44(9): 95-99. (Ji W R, Hu J J, Meng X, et al. 2008. Diversity of ground-dwelling beetles (Coleoptera) in Larix principis-rupprechtii forest with different stages of reforestation in Pangquangou National Nature Reserve[J]. Scientia Silvae Sinicae, 44(9): 95-99. DOI:10.11707/j.1001-7488.20080917 [in Chinese]) |
贾玉珍, 赵秀海, 孟庆繁. 2011. 长白山阔叶红松林不同演替阶段地表甲虫组成和多样性[J]. 应用与环境生物学报, 17(6): 797-802. (Jia Y Z, Zhao X H, Meng Q F. 2011. Composition and diversity of ground-dwelling beetle (coleoptera) along a succession gradient in broad-leaved and korean pine mixed forest in the Changbai Mountains[J]. China.Chin J Appl Environ Biol, 17(6): 797-802. [in Chinese]) |
李景科. 1992. 锥须步甲的分布密度与土壤含水量的关系[J]. 生物防治通报, 8(3): 140. (Li J K. 1992. The relationship between distribution density of Bembidinae sp.and soil moisture content[J]. Chinese Journal of Biological Control, 8(3): 140. [in Chinese]) |
李良, 夏富才, 杨晓燕, 等. 2014. 张广才岭阔叶红松林林分结构研究[J]. 林业资源管理, (1): 56-61. (Li L, Xia F C, Yang X Y, et al. 2014. A study on stand spatial structure of broad-leaved korean pine forest in Zhangguangcai Mountains[J]. Forest Resources Management, (1): 56-61. [in Chinese]) |
马克平, 刘玉明. 1994. 生物群落多样性的测量方法Ⅰ:α多样性的测量方法(下)[J]. 生物多样性, 2(4): 231-239. (Ma K P, Liu Y M. 1994. Measurement of biotic community diversity methods Ⅰ:α measurement of diversity methods(next)[J]. Chinese Biodiversity, 2(4): 231-239. DOI:10.17520/biods.1994038 [in Chinese]) |
庞雄飞, 尤民生. 1996. 昆虫群落生态学[M]. 北京: 中国农业出版社. (Pang X F, You M S. 1996. Entomological coenoecology[M]. Beijing: China Agriculture Press. [in Chinese]) |
任国栋, 张润志, 石福明. 2005. 昆虫分类与多样性[M]. 北京: 中国农业科学技术出版社. (Ren G D, Zhang R Z, Shi F M. 2005. Insect classification and diversity[M]. Beijing: China Agriculture Scientech Press. [in Chinese]) |
王辉, 秦树林. 2012. 吉林省蛟河林业实验区管理局森林资源现状及可持续经营对策[J]. 林业勘查设计, (2): 2-5. (Wang H, Qing S L. 2012. Forest resource status and sustainable management countermeasures of jiaohe forestry experimental region Administration of Jilin Province[J]. Forest Investigation Design, (2): 2-5. [in Chinese]) |
魏丽萍. 2014. 吉林蛟河阔叶红松林主要树种功能性状随树冠高度的变化. 北京: 北京林业大学硕士论文. (Wei L P. 2014. Variations in functional traits of main tree species along tree-crown in broad-leaved korean pine forest in Jiaohe, Jilin Province. Beijing: MS thesis of Beijing Forestry University. [in Chinese]) |
于晓东, 罗天宏, 周红章. 2002. 东灵山地区地表甲虫群落组成及季节变化[J]. 昆虫学报, 45(6): 785-793. (Yu X D, Luo T H, Zhou H Z. 2002. Composition and seasonal dynamics of litter-layer beetle community in the Dongling Mountain region[J]. Acta Entomologica Sinica, 45(6): 785-793. [in Chinese]) |
于晓东, 罗天宏, 周红章. 2003. 四川蜂桶寨国家自然保护区地表甲虫物种多样性[J]. 昆虫学报, 46(5): 609-616. (Yu X D, Luo T H, Zhou H Z. 2003. Species diversity of litter-layer beetles in the Fengtongzhai National Nature Reserve, Sichuan Province[J]. Acta Entomologica Sinica, 46(5): 609-616. [in Chinese]) |
于晓东, 罗天宏, 周红章. 2004. 横断山区东部四种林型地表甲虫的物种多样性[J]. 动物学研究, 25(1): 7-14. (Yu X D, Luo T H, Zhou H Z. 2004. Species diversity of litter-layer beetles in four forest types in eastern Hengduan Mountain Region[J]. Zoological Research, 25(1): 7-14. [in Chinese]) |
于晓东, 罗天宏, 周红章. 2006a. 林业活动和森林片断化对甲虫多样性的影响及保护对策[J]. 昆虫学报, 49(1): 126-136. (Yu X D, Luo T H, Zhou H Z. 2006a. Effects of forestry practices and forest fragmentation on beetle diversity and conservation strategies[J]. Acta Entomologica Sinica, 49(1): 126-136. [in Chinese]) |
于晓东, 罗天宏, 杨建. 2006b. 卧龙自然保护区落叶松林不同恢复阶段地表甲虫的多样性[J]. 动物学研究, 27(1): 1-11. (Yu X D, Luo T H, Yang J. 2006b. Diversity of ground-dwelling beetles (coleoptera) in larch plantation with different stages of reforestation in Wolong Natural Reserve[J]. Zoological Research, 27(1): 1-11. [in Chinese]) |
于晓东, 罗天宏, 周红章, 等. 2006c. 边缘效应对卧龙自然保护区森林-草地群落交错带地表甲虫多样性的影响[J]. 昆虫学报, 49(2): 277-286. (Yu X D, Luo T H, Zhou H Z, et al. 2006c. Influence of edge effect on diversity of ground-dwelling beetles across a forest-grassland ecotone in Wolong Natural Reserve[J]. Acta Entomologica Sinica, 49(2): 277-286. [in Chinese]) |
Aldhafer H M, Abdel-Dayem M S, Aldryhim Y N, et al. 2016. Diversity and composition of ground-dwelling beetle assemblages (Insecta:Coleoptera) in Rawdhat Khorim National Park, Kingdom of Saudi Arabia[J]. Journal of Arid Environments, 127: 187-191. DOI:10.1016/j.jaridenv.2015.11.007 |
Avgin S S. 2006. Distribution and diversity of ground beetles in Baskonus Mountain National Park of Turkey[J]. Journal of Environmental Biology, 27(3): 515-521. |
Butterfield J, Luff M L, Babes M, et al. 1995. Carbide beetle communities as indicators of conservation potential in upland forests[J]. Forest Ecology and Management, 79(1/2): 63-77. |
Diamond J M. 1975. The island dilemma:lessons of modern biogeographic studies for the design of natural reserves[J]. Biological Conservation, 7(2): 129-146. DOI:10.1016/0006-3207(75)90052-X |
Eyre M D, Rushton S P, Luff M L, et al. 2004. Predicting the distribution of ground beetle species (Coleoptera, Carabidae) in Britain using land cover variables[J]. Journal of Environmental Management, 72(3): 163-174. DOI:10.1016/j.jenvman.2004.04.007 |
Francese J A, Oliver J B, Fraser I, et al. 2008. Influence of trap placement and design on capture of the emerald ash borer (Coleoptera:Buprestidae)[J]. Journal of Economic Entomology, 101(6): 1831-1837. DOI:10.1603/0022-0493-101.6.1831 |
Hanavan R P, Bosque-Perez N A. 2008. Early-season aerial adult colonization and ground activity of pea leaf weevil (Coleoptera:Cureulionidae)in pea as influenced by tillage system[J]. Journal of Economic Entomology, 101(5): 1606-1613. DOI:10.1093/jee/101.5.1606 |
Irmler U. 2003. The spatial and temporal pattern of carabid beetles on arable fields in northern Germany (Schleswig-Holstein) and their value as ecological indicators[J]. Agriculture.Ecosystems and Environment, 98(1): 141-151. |
Jung J K, Kim S T, Lee S Y, et al. 2014. A comparison of diversity and species composition of ground beetles (Coleoptera:Carabidae) between conifer plantations and regenerating forests in Korea[J]. Ecological Research, 29(5): 877-887. DOI:10.1007/s11284-014-1175-9 |
Khobrakova L T, Sharova I K. 2005. Life cycles of ground beetles (Coleoptera, Carabidae) from the mountain taiga and mountain forest-steppe in the Eastern Sayan[J]. Biology Bulletin, 32(6): 571-575. DOI:10.1007/s10525-005-0145-8 |
Magura T, Tóthmérész B, Molnár T. 2004. Changes in carabid beetle assemblages along an urbanisation gradient in the city of Debreeen, Hungary[J]. Landscape Ecology, 19(7): 747-759. DOI:10.1007/s10980-005-1128-4 |
Noss R F. 1990. Indicators for monitoring biodiversity:a hierarchical approach[J]. Conservation Biology, 4(4): 355-364. DOI:10.1111/cbi.1990.4.issue-4 |
Renkema J M, Lynch D H, Cutler G C, et al. 2012. Ground and rove beetles (Coleoptera:Carabidae and Staphylinidae) are affected by mulches and weeds in highbush blueberries[J]. Environmental Entomology, 41(5): 1097-1106. DOI:10.1603/EN12122 |
Saunders D A, Hobbs R J, Margules C R. 1991. Biological consequences of ecosystem fragmentation:a review[J]. Conservation Biology, 5(1): 18-32. DOI:10.1111/cbi.1991.5.issue-1 |
Schaffers A P, Raemakers I P. 2008. Arthropod assemblages are best predicted by plant species composition[J]. Ecology, 89(3): 782-794. DOI:10.1890/07-0361.1 |
Sroka K, Finch O D. 2006. Ground beetle diversity in ancient woodland remnants in north-western Germany (Coleoptera, Carabidae)[J]. Journal of Insect Conservation, 10(4): 335-350. DOI:10.1007/s10841-006-9008-y |
Topp W, Kappes H, Kulfan J, et al. 2006. Litter-dwelling beetles in primeval forests of Central Europe:does deadwood matter?[J]. Journal of Insect Conservation, 10(3): 229-239. DOI:10.1007/s10841-005-3814-5 |
Tyler G. 2008. The gound beetle fauna (Coleoptera:Carabidae) of abandoned fields, as related to plant cover, previous management and succession stage[J]. Biodiversity and Conservation, 17(1): 155-172. DOI:10.1007/s10531-007-9236-9 |
Whitter R H. 1977. Evolution of species diversity in land communities[J]. Evolutionary Biology, 10: 1-67. |
 2018, Vol. 54
2018, Vol. 54

