文章信息
- 李河, 李杨, 蒋仕强, 刘君昂, 周国英
- Li He, Li Yang, Jiang Shiqiang, Liu Jun'ang, Zhou Guoying
- 湖南省油茶炭疽病病原鉴定
- Pathogen of Oil-Tea Trees Anthracnose Caused by Colletotrichum spp. in Hunan Province
- 林业科学, 2017, 53(8): 43-53.
- Scientia Silvae Sinicae, 2017, 53(8): 43-53.
- DOI: 10.11707/j.1001-7488.20170806
-
文章历史
- 收稿日期:2016-11-17
- 修回日期:2017-01-11
-
作者相关文章
油茶(Camellia oleifera)是我国特有的木本食用油料树种,广泛分布于我国南方14个省(市、自治区)。炭疽属(Colletotrichum)真菌能够侵染油茶树造成落叶、落花、落果,经济损失巨大。油茶树的炭疽病病原菌——胶孢炭疽菌(C.gloeosporioides)(周仲铭,1990;袁嗣令等,1997;杨光道等,2004;段琳等,2005)是广义胶孢炭疽菌,即Arx(1957)和Sutton(1992)所定义的胶孢炭疽菌复合群(C. gloeosporioides complex)。形态学特征和寄主范围是区别炭疽菌种间关系的重要依据,但这些特征因寄主、培养条件的不同会在一定范围内变化。Weir等(2012)通过形态学结合多基因系统发育学方法确定了胶孢炭疽菌复合群中22个合格种和1个亚种,其中包括Cannon等(2008)所描述的狭义胶孢炭疽菌附加模式种。湖南省油茶栽培面积广,油茶炭疽病危害严重。本研究拟采用多基因位点系统发育学方法并结合形态学研究,明确湖南省油茶炭疽病原菌种类,以期为该病害的防治提供依据。
1 材料与方法 1.1 样品采集及病原菌的分离从湖南省长沙、株洲、浏阳、永州、怀化、常德、常宁等油茶主产区9个样地采集油茶树上的典型炭疽病叶450份。采用组织分离法和(或)单孢法分离菌株,在4 ℃和-80 ℃温度下各保存1份。
1.2 致病性测定油茶叶片和果实经酒精表面消毒后,将各菌株分生孢子配制成浓度为1×105个·mL-1,采用有伤和无伤2种方式接种油茶嫩叶锯齿状叶缘(油茶自然林中,叶缘炭疽病发生率较其他部位高;叶缘蜡质层和角质层较薄,接种后发病时间较短)和有伤接种油茶果实。对照采用无菌水处理,每个菌株设6个重复,培养箱中28 ℃、12 h光照/12 h黑暗保湿培养,统计是否发病以及显症时间。进一步对发病组织进行再分离,观察分离菌株是否与原接种菌株相同(黄俊斌等,1999)。
1.3 病菌形态学及产孢病菌在PDA平板上28 ℃培养5天后,用无菌打孔器在菌落边缘处打孔,取菌块至新的PDA平板上培养,每株3个重复,28 ℃、12 h光照/12 h黑暗培养5天后测量菌落直径并记录菌落形态特征。病菌在PD液体培养基中摇瓶培养3天后,统计每种菌的分生孢子产生率并测量50个分生孢子和附着胞的大小,描述其形态特征。
1.4 菌株DNA提取、基因选择、PCR扩增及测序用无菌牙签刮取约0.5 g菌丝,采用北京索莱宝科技有限公司生产的真菌基因组DNA提取试剂盒提取DNA,-20 ℃保存。对所有菌株的核糖体转录间隔区(ITS)、3-磷酸甘油醛脱氢酶基因(GAPDH)和钙调蛋白基因(CAL)3个基因进行扩增测序,具体操作方法参见Weir等(2012)。相应的PCR扩增引物和退火温度见表 1。PCR扩增产物测序由上海博尚生物技术有限公司完成(Cai et al., 2009)。
|
|
对测定的序列在GenBank中进行Blast比对,根据比对结果初步确定归属,选用Sharma等(2013)、Cannon等(2012)和Weir等(2012)等炭疽菌模式菌株的序列与本研究分离纯化获得的菌株序列共同构建系统发育树。利用ClustalX 1.83(Thompson et al., 1997)软件进行比对分析。利用BioEdit 7.0.5.3(Hall,1999)校正,采用PAUP*4.0 beta10(Swofford,2002)以最大简约法(maximum parsimony, MP)和MrBayes v.3.1.2(Ronquist et al., 2003)构建系统发育树,所有碱基赋予相同权重,自举检验(bootstraping)重复1 000次以获得各分支的支持率。
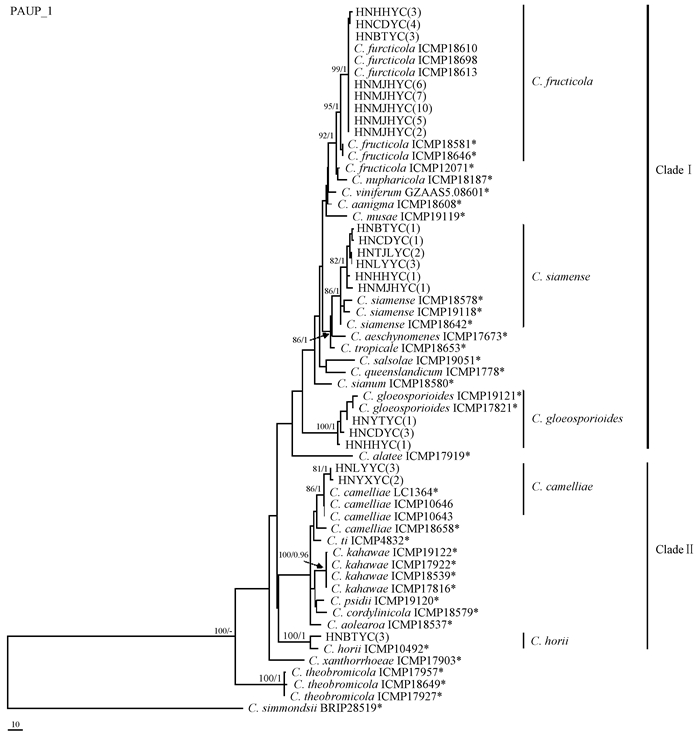
2 结果与分析 2.1 病原菌分离及系统发育学分析从湖南省9个采样地油茶炭疽病叶上共分离、纯化获得真菌156株,通过菌落、菌丝和分生孢子等形态特征,确定炭疽属真菌62株。在基于ITS-CAL-GPDH多基因序列构建的系统树(图 1)中,分离自湖南省9个不同采样地的62株油茶炭疽菌以非常高的支持率聚为5个进化分支,这些分支又分别位于2个Clade中。其中,40个菌株以高支持率(Bootstrap=95%、后验概率值为1.00) 与C. fructicola模式菌株和权威菌株构成的进化分支、9个菌株以高支持率(Bootstrap=86%、后验概率值1.00) 与C. siamense模式菌株构成的进化分支以及5个菌株以高支持率(Bootstrap=100%、后验概率值为1.00) 与C. gloeosporioides模式菌株构成的进化分支位于CladeⅠ中。3个进化分支中,C. fructicola与C. siamense亲缘关系较近,与之前报道的油茶炭疽病菌C. gloeosporioides的亲缘关系相对较远。另外,有5个菌株以86%的Bootstrap值和后验概率值为1.00与C. camelliae模式菌株构成进化分支以及3个菌株以100%的Bootstrap值和后验概率值为1.00与C. horii模式菌株构成进化分支,这2个分支位于Clade Ⅱ中。
|
图 1 炭疽病菌系统发育树 Fig.1 Phylogenetic tree of Colletotrichum species isolated from oil-tea tree *表示模式菌株;括号中的数字表示菌株数量。 *Type culture; Data in brackets is the quantity of strains. |
系统发育分析表明,湖南省9个不同采样地62个油茶炭疽病菌的2种建树方法均以非常高的支持率聚为5个进化分支,分别代表5个分类单元且可以归为2个Clade,这说明湖南省的油茶炭疽病菌主要有2个进化方向。另外,C. fructicola分布范围非常广,9个采样地中有8个样地都分离得到了该菌,分布地包括湖南怀化、常德、板塘、马家河、天际岭、浏阳、新宁和攸县,共分离获得40个菌株,占总分离菌株的64.5%,为优势菌;C. siamense则在6个样地中分离得到,包括湖南板塘、常德、天际岭、浏阳、怀化和马家河,共获得9个菌株,占总分离菌株的14.5%,为次要菌株;5株C. gloeosporioides,占总分离菌株的8.1%,分布在云田、常德和怀化3个采样地;5株C. camelliae,占总分离菌株的8.1%,分布在浏阳和攸县2个采样地;3株C. horii,占总分离菌株的4.8%,只在湖南板塘样地分离获得。
2.2 菌株致病性测定通过回接油茶嫩叶及果实进行致病性测定,结果表明这62个菌株均能引起油茶炭疽病症,但部分不同的菌株间显症时间有一定差异(表 2)。62个菌株回接油茶嫩叶和果实出现的症状与自然状态下的油茶炭疽病症状一致:病叶初期为褐色斑点,然后逐渐变成黑褐色病斑,有时可见橘黄色分生孢子堆,病斑有隆起的轮纹,边缘有1条暗褐色或暗红色的隆起线;植株活体接种的病叶后期病斑中心呈灰白色,密生许多分生孢子盘。通过柯赫氏法则验证这62株炭疽属真菌均是油茶炭疽病病原菌。
|
|
根据系统发育学分析,62个菌株共划分为果生炭疽菌(C. fructicola)、暹罗炭疽菌(C. siamense)、胶孢炭疽菌(C.gloeosporioides)、山茶炭疽菌(C. camelliae)和哈锐炭疽菌(C. horii)5种类型菌株。
2.3.1 果生炭疽菌菌落特征:在PDA培养基上,菌落厚重浓密,棉絮状,浅灰色至深灰色,圆形,规则完整,边缘颜色稍浅一些,气生菌丝绒毛状,菌落背面黑色素沉积,灰白色至黑褐色,分生孢子堆浅黄色;5天平均生长速率为10.68 mm ·d-1。
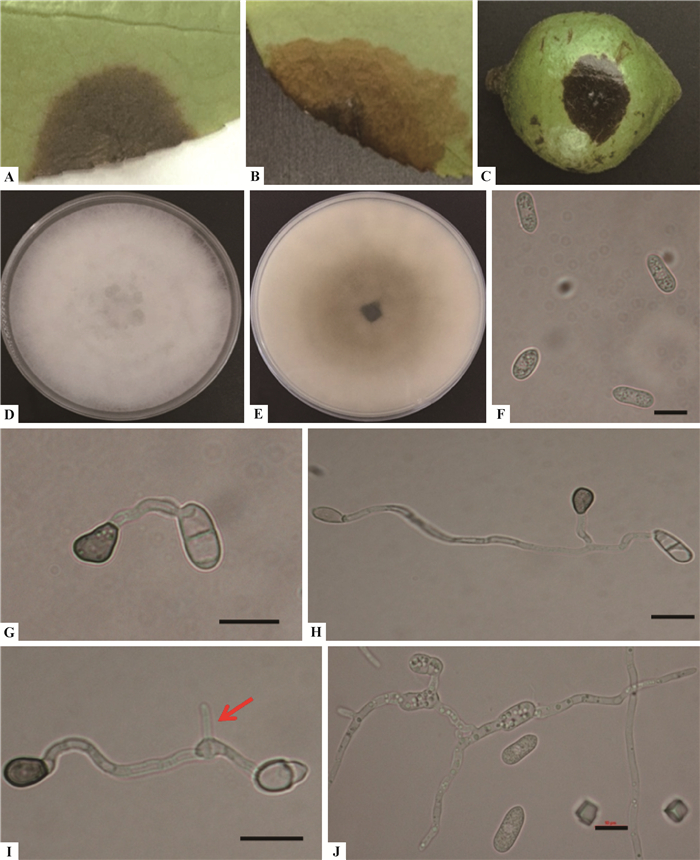
形态特征:营养菌丝透明,光滑,有隔膜,分枝;厚垣孢子未发现;分生孢子盘未见,刚毛未发现;分生孢子直,无隔膜,圆柱状或椭圆形,两端钝圆或一端略尖,光滑,无色,单孢,大小为(16.2±0.9) μm×(5.5±0.7) μm;分生孢子附着胞近圆形,褐色,边缘完整;附着胞通常单个或多个,浅棕色至深棕色,球状,圆柱状或纺锤状,极少数为不规则状,大小为(9.3 ± 1.67) μm× (5.8 ± 0.9) μm。在PDA平板培养后期可见有性态(图 2)。这些特征与果生炭疽菌特征一致(Prihastuti et al., 2009)。

|
图 2 果生炭疽菌 Fig.2 Colletotrichum fructicola A.油茶叶无伤接种症状;B.油茶叶有伤接种症状;C.油茶果有伤接种症状;D,E.PDA培养基上的菌落(正面,反面);F.分生孢子;G,H.附着胞; I.附着胞萌发形成侵染钉(丝);J.包囊被;K.子囊;L.子囊孢子。标尺=10 μm。 A. Symptom on no-wounded oil-tea leaf; B. Symptom on wounded oil-tea leaf; C. Symptom on wounded oil-tea fruit; D, E.Colony on PDA(upper, reverse); F. Conidia; G, H. Appressoria; I. Germinated appressoria developed infection peg(hypha); J. Peridium; K. Asci; L. Ascospores. Scale bar=10 μm. |
菌落特征:在PDA培养基上,菌丝呈辐射生长,菌落圆形,初期为白色,后逐渐变为浅灰色;气生菌丝由白色渐变为深灰色绒状;菌落背面浅灰色至浅黄色,中心颜色深,边缘颜色浅;5天平均生长速率为11.0 mm ·d-1。
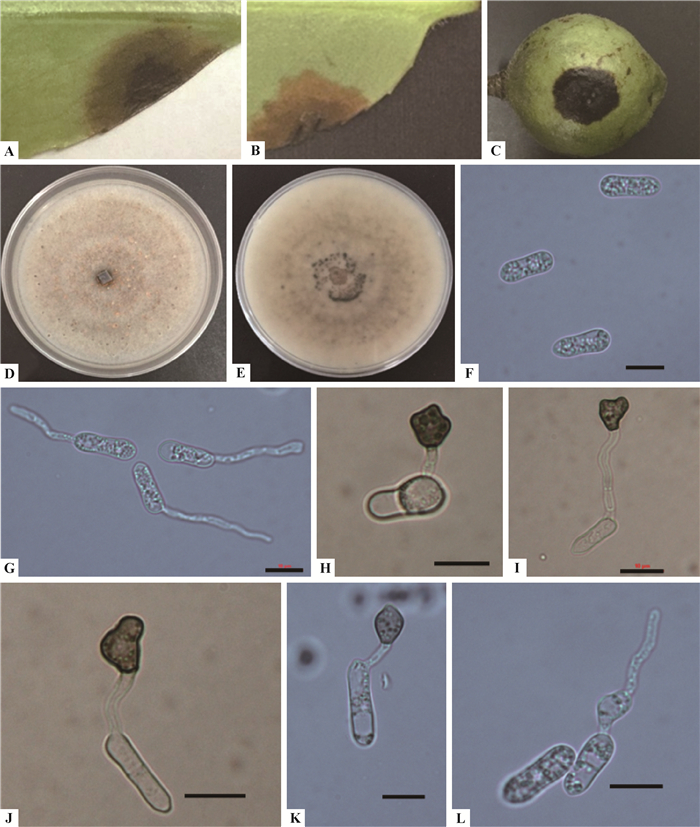
形态特征:分生孢子为单胞,直、圆柱状,无色,光滑,两端钝圆或一端钝圆,另一端稍尖,分生孢子大小为(15.6±1.12) μm×(4.93±0.53) μm;分生孢子附着胞单个或呈簇状分布,浅棕色到深棕色,卵圆形,近球形或短圆柱形,部分轻微不规则形,大小为(9.62±1.8) μm×(5.84±0.93)μm(图 3)。这些特征与果炭疽菌特征一致(Prihastuti et al., 2009)。
|
图 3 暹罗炭疽菌 Fig.3 Colletotrichum siamense A.油茶叶无伤接种症状;B.油茶叶有伤接种症状;C.油茶果有伤接种症状;D,E.PDA培养基上的菌落(正面,反面);F.分生孢子;G,H.附着胞; I.附着胞萌发形成侵染钉(丝);J.分生孢子萌发后芽管可继续形成新的分生孢子。标尺=10 μm。 A. Symptom on no-wounded oil-tea leaf; B. Symptom on wounded oil-tea leaf; C. Symptom on wounded oil-tea fruit; D, E.Colony on PDA(upper, reverse); F. Conidia; G, H. Appressoria; I. Germinated appressoria developed infection peg(hypha); J. Germinated conidia developed new conidia. Scale bar=10 μm. |
菌落特征:在PDA培养基平板上,菌落圆形,规则;菌落形态主要有2种:一种气生菌丝厚重浓密,浅灰色至深灰色,棉絮状;另一种菌丝稀疏,中心黄褐色而边缘白色。菌落背面橄榄灰;未见刚毛;5天平均生长速率为11.5 mm ·d-1。
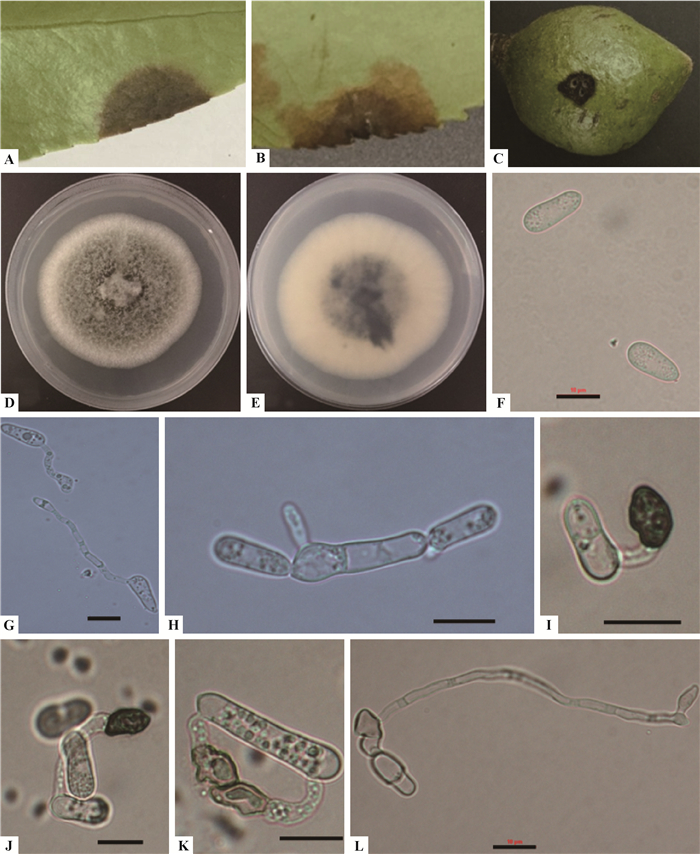
形态特征:营养菌丝透明,光滑,有隔膜,分枝;分生孢子堆橘红色,分生孢子直、圆柱状,两端钝圆或一端略尖,无色,光滑,有油球, 大小为(14.7±1.3) μm×(5.3±0.64) μm。分生孢子附着胞通常单个或散生,近椭圆形,浅褐色,边缘完整,大小为(8.47±1.41) μm×(5.95±0.86)μm(图 4)。这些特征与胶炭疽菌特征一致(Cannon et al., 2008)。
|
图 4 胶孢炭疽菌 Fig.4 Colletotrichum gloeosporioides A.油茶叶无伤接种症状;B.油茶叶有伤接种症状;C.油茶果有伤接种症状;D, E. PDA培养基上的菌落(正面,反面);F.分生孢子;G.萌发的分生孢子;H, K.附着胞; L.附着胞萌发形成侵染钉。标尺=10 μm。 A. Symptom on no-wounded oil-tea leaf; B. Symptom on wounded oil-tea leaf; C. Symptom on wounded oil-tea fruit; D, E.Colony on PDA(upper, reverse); F. Conidia; G. Germinated conidia; H, K. Appressoria; L. Germinated appressoria developed infection peg(hypha). Scale bar=10 μm. |
菌落特征:在PDA培养基上,菌落近似圆形,边缘平整,气生菌丝白色渐变为灰色,棉花状,稀疏;背面开始为白色,然后中心灰至黑;5天平均生长速率为7.06 mm ·d-1。
形态特征:分生孢子无色、光滑,单孢,长椭圆形或圆柱形,两端圆或一端略粗,另一端稍尖,大小为(16.2±2.4) μm×(5.4±0.78) μm;附着胞形状不规则,棍棒状,圆齿,浅裂,褐色至黑褐色,单个,支链,链状;大小为(9.82±2.1) μm×(7.1±1.94)μm(图 5)。这些特征与山茶炭疽菌特征一致(Weir et al., 2012)。
|
图 5 山茶炭疽菌 Fig.5 Colletotrichum camelliae A.油茶叶无伤接种症状;B.油茶叶有伤接种症状;C.油茶果有伤接种症状;D, E.PDA培养基上的菌落(正面,反面);F.分生孢子;G.萌发的分生孢子;H.分生孢子萌发后芽管可继续形成新的分生孢子;I, K.附着胞; L.附着胞萌发形成侵染钉。标尺=10 μm。 A. Symptom on no-wounded oil-tea leaf; B. Symptom on wounded oil-tea leaf; C. Symptom on wounded oil-tea fruit; D, E.Colony on PDA(upper, reverse); F. Conidia; G. Germinated conidia; H. Germinated conidia developed new conidia; I, K.Appressoria; L. Germinated appressoria developed infection peg(hypha). Scale bar=10 μm. |
菌落特征:在PDA培养基上,菌落边缘规则,形态均匀,气生菌丝较薄,棉花状,灰色到灰黑色;菌落背面中央呈褐色,边缘灰白色,随菌龄增长菌落颜色变深,可产生同心轮纹;5天平均生长速率为10.34 mm ·d-1。
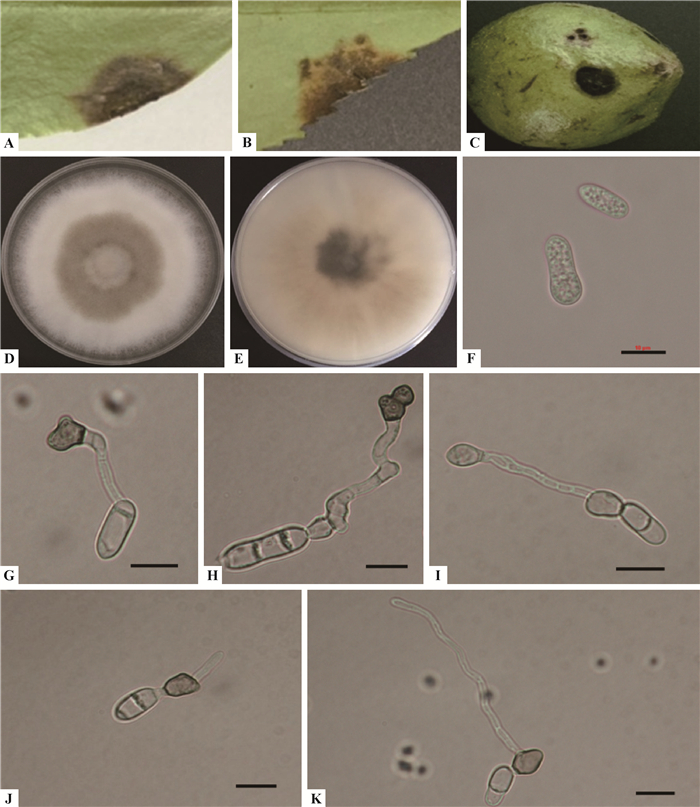
形态特征:分生孢子堆橙色;分生孢子直、柱形或长椭圆形,表面光滑,两端钝圆,无色,单孢,大小为(18.0±3.5) μm×(5.2±0.67) μm。附着胞短圆柱形,一般轮廓均匀或不规则裂,大小为(9.8±2.4) μm×(6.6±1.2) μm(图 6)。这些特征与哈锐炭疽特征一致(Weir et al., 2010)。
|
图 6 哈锐炭疽菌 Fig.6 Colletotrichum horii A.油茶叶无伤接种症状;B.油茶叶有伤接种症状;C.油茶果有伤接种症状;D,E.PDA培养基上的菌落(正面,反面);F.分生孢子;G,H.附着胞;H.附着胞萌发后可继续形成新的附着胞;J,K.附着胞萌发形成侵染钉(侵染丝)。标尺=10 μm。 A. Symptom on no-wounded oil-tea leaf; B. Symptom on wounded oil-tea leaf; C. Symptom on wounded oil-tea fruit; D, E.Colony on PDA(upper, reverse); F. Conidia; G, H. Appressoria; I. Germinated appressoria developed a new appressoria; J, K. Germinated appressoria developed infection peg(hypha). Scale bar=10 μm. |
通过形态学结合多基因序列特征,鉴定出引起湖南省油茶炭疽病5种病原菌,分别是果生炭疽菌、暹罗炭疽菌、胶孢炭疽菌、山茶炭疽菌和哈锐炭疽菌。系统发育分析表明,这5种病原菌可以归为2个Clade。CladeⅠ包括果生炭疽菌、暹罗炭疽菌和胶孢炭疽菌3个分类单元,CladeⅡ包括山茶炭疽菌和哈锐炭疽菌2个分类单元,说明湖南省油茶炭疽病菌主要有2个进化方向,且每个方向又存在遗传分化现象。
果生炭疽菌最初描述源自咖啡豆(coffee berries)上的分离物(Prihastuti et al., 2009),该菌在生物学和地理学上都差异较大。其模式种为MFLU090228,该菌株现保存为ICMP 18581。笔者于2014年报道了该菌是油茶的致病菌,并广泛分布在我国几乎所有油茶产区(李河等,2014)。本研究从湖南省油茶炭疽病叶上分离获得40株果生炭疽菌,形态特征与模式菌株相似(Prihastuti et al., 2009),菌株数量占总分离菌株的64.5%,包括8个样品采集地,说明该病菌分布范围非常广。
暹罗炭疽菌是由Prihastuti等(2009)定名的,其模式种为MFLU 09230,该菌株现保存为ICMP 18578。有研究者则认为暹罗炭疽菌是一个复合种(Sharma et al., 2015)。Weir等(2012)研究了30株暹罗炭疽菌的代表性菌株进行系统发育分析,发现它们形成了一个无法再区分的单系分离枝。Liu等(2016)也认为暹罗炭疽菌不存在生殖隔离、地理和寄主植物的基因流障碍,不是复合种。本研究中,笔者从湖南省6个样地中分离得到暹罗炭疽菌菌株,形态特征与模式菌株相似(Prihastuti et al., 2009)。6个样地包括湖南板塘、常德、天际岭、浏阳、怀化和马家河,共有9个菌株,占总分离菌株的14.5%,说明该菌分布范围较广。
在先前的研究中大多数植物炭疽病病原菌或寄生菌是胶孢炭疽菌,但自从该菌指代模式种的全基因测序公布后,发现其寄主范围较小,许多热带水果植物炭疽病均不是由胶孢炭疽菌引起的(Phoulivong et al., 2010)。目前报道的寄主主要包括柑橘(Citrus reticulata)、柠檬(Citrus limon)、榕树(Ficus microcarpa)、芒果(Mangifera indica)、葛根(Pueraria lobata)、葡萄(Vitis vinifera)等(符丹丹,2014)。本研究共分离获得5株胶孢炭疽菌,形态特征与模式菌株相似(Cannon et al., 2008),菌株数量占总分离菌株的8.1%,分布在云田、常德和怀化3个采样地,该病菌数量较少,分布范围有限。
山茶炭疽菌最早的记录是斯里兰卡的茶叶炭疽病菌(Massee,1899),目前将其作为茶树褐枯病的病原菌广泛使用(Weir et al., 2012)。我国科学家早期定名油茶炭疽病原菌就是山茶炭疽菌(袁嗣令等,1963;翁月霞等,1982;王敬文,1985;贺正兴等,1985),后来又改为胶孢炭疽菌(周仲铭,1990;袁嗣令等,1997)。本研究从湖南省共分离获得5株山茶炭疽菌,形态特征与模式菌株相似(Massee,1899),菌株数量占总分离菌株的8.1%,菌株数量较少且只分布在浏阳和攸县2个采样地,分布范围小。
哈锐炭疽菌是Weir等(2010)研究中国、日本和新西兰的柿树(Diospyros kaki)炭疽病病原菌后定名的,依据ITS,EFla和GPDH基因序列,可将其区分为一个明确的种,自此柿树炭疽病的病原菌被正式确定为柿树炭疽菌,并被广泛使用(Xie et al., 2010; Kwon et al., 2013;余贤美等,2015;郗慧,2015)。哈锐炭疽菌没有寄主专化性,谢柳(2010)研究发现其能够侵染香蕉(Musa nana)和西葫芦(Cucurbita pepo)产生典型症状。本研究中,共分离获得3株哈锐炭疽菌,形态特征与模式菌株相似(Weir et al., 2010),菌株数量占总分离菌株的4.8%,只在湖南板塘样地分离获得,数量和分布范围均最小,但这是哈锐炭疽菌能引起油茶炭疽病的首次报道。
目前我国已有1种植物上有多种炭疽菌种类作为病原菌同时被侵染的报道。符丹丹等(2013)报道中国苹果炭疽病的病原有7种,分别是C. alienum、C. fructicola、C. gloeosporioides、C. nymphaeae、C. siamense和C. orientalis。王玉春等(2015)报道的中国主要茶区茶树炭疽菌有3种,分别是C. camelliae、C. fructicola和C. siamense。湖南省油茶种植面积广泛,是我国油茶种植的核心地区,本研究鉴定出湖南省油茶5种炭疽病原菌,丰富了对油茶炭疽病原种类的认识。对全国范围内的油茶炭疽病仍需要进行深入研究,以期全面了解其病原种类、分布规律以及遗传变异机制,为我国制定有针对性的病害防治策略提供理论依据。
4 结论分别获得湖南省油茶炭疽病的病原菌5种,分别是果生炭疽菌、暹罗炭疽菌、胶孢炭疽菌、山茶炭疽菌和哈锐炭疽菌,其中果生炭疽菌分布范围最广,分离率最高,达到64.5%。
| [] |
段琳, 杨光道, 束庆龙, 等. 2005. 油茶果皮颜色对炭疽病的抗性的影响. 经济林研究, 23(2): 9–12.
( Duan L, Yang G D, Shu Q L, et al. 2005. Relationship of peel color with resistance to anthracnose in oil tea Camellia. Nonwood Forest Research, 23(2): 9–12. [in Chinese] ) |
| [] |
符丹丹, 庄杰丽, 张荣, 等. 2013. 苹果炭疽病病原菌ISSR-PCR反应体系的优化及遗传多样性分析. 植物保护学报, 40(3): 231–236.
( Fu D D, Zhuang J L, Zhang R, et al. 2013. Optimization of ISSR-PCR reaction system and genetic diversity analysis of Colletotrichum species causing bitter rot of apple. Acta Phytophylacica Sinica, 40(3): 231–236. [in Chinese] ) |
| [] |
符丹丹. 2014. 中国苹果炭疽病病原菌的遗传多样性. 西安: 西北农林科技大学博士学位论文. ( Fu D D.2014. Pathogenetic diversity of Colletotrichum spp. on apple in China. Xi'an:PhD thesis of Northwest Sci-Tech University of Agriculture and Forestry.[in Chinese]) http://cdmd.cnki.com.cn/Article/CDMD-10712-1014421136.htm |
| [] |
贺正兴, 何美云, 廖正乾, 等. 1985. 油茶炭疽病菌对油茶花果的侵染及早期防治研究. 湖南林业科技, 12(1): 20–27.
( He Z X, He M Y, Liao Z Q, et al. 1985. Camellia anthracnose of Camellia fruit and early prevention and treatment of infection. Hunan Forestry Science & Technology, 12(1): 20–27. [in Chinese] ) |
| [] |
黄俊斌, 赵纯森, 周茂繁. 1999. 三种药用植物根腐病的病原鉴定. 华中农业大学学报, 18(3): 212–213.
( Huang J B, Zhao C S, Zhou M F. 1999. Identification of root rot disease son three species of medicinal plant. Journal of Huazhong Agricultural University, 18(3): 212–213. [in Chinese] ) |
| [] |
李河, 周国英, 徐建平, 等. 2014. 一种油茶新炭疽病原的多基因系统发育分析鉴定. 植物保护学报, 41(5): 602–607.
( Li H, Zhou G Y, Xu J P, et al. 2014. Pathogen identification of a new anthracnose of Camellia oleifera in China based on multiple-gene phylogeny. Acta Phytophylacica Sinica, 41(5): 602–607. [in Chinese] ) |
| [] |
王玉春, 郝心愿, 黄玉婷, 等. 2015. 中国主要茶区茶树炭疽菌系统发育学. 中国农业科学, 48(24): 4924–4935.
( Wang Y C, Hao X Y, Huang Y T, et al. 2015. Phylogenetic Study of Colletotrichum species associated with Camellia sinensis from the major tea areas in China. Scientia Agricultura Sinica, 48(24): 4924–4935. DOI:10.3864/j.issn.0578-1752.2015.24.007 [in Chinese] ) |
| [] |
王敬文. 1985. 油茶炭疽病菌(Colltotrichum camelliae)分生孢子的自身抑制作用. 植物生理学通讯, 21(1): 25–27.
( Wang J W. 1985. Self inhibitory effect of the spores of Colltotrichum camelliae from Camellia oil. Plant Physiology Communication, 21(1): 25–27. [in Chinese] ) |
| [] |
翁月霞, 张常青, 赵汉明, 等. 1982. 油茶春梢炭疽病的研究. 林业科学, 18(3): 289–295.
( Weng Y X, Zhang C Q, Zhao H M, et al. 1982. The role of spring shoots lesions in anthracnose disease of Camellia oleifera. Scientia Silvae Sinicae, 18(3): 289–295. [in Chinese] ) |
| [] |
郗慧. 2015. 我国柿树炭疽病调查、鉴定及其防治研究. 洛阳: 河南科技大学硕士学位论文. ( Xi H. 2015. Investigation isolating identification and chemical control of anthracnose from persimmon in China. Luoyang:MS thesis of Henan University of Science and Technology.[in Chinese]) http://cdmd.cnki.com.cn/Article/CDMD-10464-1015902788.htm |
| [] |
谢柳. 2010. 哈锐炭疽菌的分类和侵染特征的研究. 杭州: 浙江大学硕士学位论文. ( Xie L.2010. Study on Infection characteristics and species identification of Colletotrichum horii. Hangzhou: MS thesis of Zhejiang University.[in Chinese]) http://d.wanfangdata.com.cn/Thesis/Y1653316 |
| [] |
杨光道, 束庆龙, 段琳, 等. 2004. 主要油茶品种对炭疽病的抗性研究. 安徽农业大学学报, 31(4): 480–483.
( Yang G D, Shu Q L, Duan L, et al. 2004. Resistance of main cultivars of oil tea to Colletotrichum gloeosporioides. Journal of Anhui Agricultural University, 31(4): 480–483. [in Chinese] ) |
| [] |
余贤美, 侯长明, 王洁, 等. 2015. 山东牛心柿炭疽病菌的分离鉴定及致病性. 林业科学, 51(4): 126–133.
( Yu X M, Hou C M, Wang J, et al. 2015. Identification of pathogen causing beef heart persimmon anthracnose in Shandong and its pathogenicity. Scientia Silvae Sinicae, 51(4): 126–133. [in Chinese] ) |
| [] |
袁嗣令, 张能唐, 翁月霞, 等. 1963. 油茶炭疽病的研究. 植物保护学报, 2(3): 253–262.
( Yuan S L, Zhang N T, Weng Y X, et al. 1963. The anthracnose disease of Camellia oleosa (Lour.) rehd. Acta Phytophylacica Sinica, 2(3): 253–262. [in Chinese] ) |
| [] |
袁嗣令, 邵力平, 李传道. 1997. 中国乔、灌木病害. 北京, 科学出版社.
( Yuan S L, Shao L P, Li C D. 1997. Chinese arbor and shrub diseases. Beijing, Science Press. [in Chinese] ) |
| [] |
周仲铭. 1990. 林木病理学. 北京, 中国林业出版社.
( Zhou Z M. 1990. Forest pathology. Beijing, China Forestry Publishing House. [in Chinese] ) |
| [] | Arx J A. 1957. Die arten der gattung Colletotrichum Cda. Phytopathologische Zeitschrift, 29(1): 413–468. |
| [] | Cai L, Hyde K D, Taylor P W J, et al. 2009. A polyphasic approach for studying Colletotrichum. Fungal Diversity, 39(2): 183–204. |
| [] | Cannon P F, Buddie A G, Bridge P D. 2008. The typification of Colletotrichum gloeosporioides. Mycotaxon, 104(2): 189–204. |
| [] | Cannon P F, Damm U, Johnston P R, et al. 2012. Colletotrichum-current status and future dirctions. Studies in Mycology, 73: 181–213. DOI:10.3114/sim0014 |
| [] | Hall T A. 1999. BioEdit:auser-friendly biological sequence alignment editor and analysis program for Windows 95/98/NT. Nucl Acids Symp Ser, 41: 95–98. |
| [] | Kwon J H, Kim J, Chio O, et al. 2013. Anthracnose caused by Colletotrichum horii on sweet persimmon in Korea:dissemination of conidia and disease development. Journal of Phytopathology, 161(7/8): 497–502. |
| [] | Liu F, Wang M, Damm U, et al. 2016. Species boundaries in plant pathogenic fungi:a Colletotrichum case study. BMC Evolutionary Biology, 16: 81. DOI:10.1186/s12862-016-0649-5 |
| [] | Massee G. 1899. Tea and coffee diseases. Bulletin of Miscellaneous Informations of the Royal Botanical Gardens Kew: 89–94. |
| [] | Phoulivong S, Cai L, Chen H, et al. 2010. Colletotrichum gloeosporioides is not a common pathogen on tropical fruits. Fungal Div, 44(1): 33–43. DOI:10.1007/s13225-010-0046-0 |
| [] | Prihastuti H, Cai L, Chen H, et al. 2009. Characterisation of Colletotrichum species associated with coffee berries in northern Thailand. Fungal Diversity, 39(2): 89–109. |
| [] | Ronquist F, Huelsenbeck J P. 2003. MrBayes 3:Bayesian phyloge netic inference under mixed models. Bioinformatics, 19(12): 1572–1574. DOI:10.1093/bioinformatics/btg180 |
| [] | Sharma G, Pinnaka A K, Shenoy B D. 2015. Resolving the Colletotrichum siamense species complex using ApMat marker. Fungal Diversity, 71(1): 247–264. DOI:10.1007/s13225-014-0312-7 |
| [] | Sharma G, Kumar N, Weir B S, et al. 2013. The ApMat marker can resolve Colletotrichum species:a case study with Mangifera indica. Fungal Diversity, 61(1): 117–138. DOI:10.1007/s13225-013-0247-4 |
| [] | Swofford D L.2002. PAUP*. Phylogenetic analysis using parsimony (*and other methods). Version 4. Sinauer Associates, Sunderland, Massachusetts, USA. |
| [] | Sutton B C. 1992. The genus Glomerella and its anamorph Colletotrichum//Bailey J A, Jeger M J.Colletotrichum biology, pathology and control. CAB International, Wallingford:1-26. |
| [] | Thompson J D, Gibson T J, Plewniak F, et al. 1997. The Clustal X windows interface:flexible strategies for multiple sequence alignment aided by quality analysis tools. Nucleic Acids Res, 25(24): 4876–4882. DOI:10.1093/nar/25.24.4876 |
| [] | Weir B S, Peter R, Johnston. 2010. Characterisation and neotypification of Gloeosporium kaki Hori as Colletotrichum horii nom. nov. Mycotaxon, 111(1): 209–219. DOI:10.5248/111.209 |
| [] | Weir B S, Johnston P R, Damm U. 2012. The Colletotrichum gloeosporioides species complex. Studies in Mycology, 73(1): 115–180. |
| [] | Xie L, Zhang J Z, Cai L, et al. 2010. Biology of Colletotrichum horii, the causal agent of persimmon anthracnose. Mycology, 1(4): 242–253. DOI:10.1080/21501203.2010.526644 |
 2017, Vol. 53
2017, Vol. 53

