文章信息
- 王凤娟, 李伟庆, 牟志美, 王彦文, 刘庆信, 高绘菊
- Wang Fengjuan, Li Weiqing, Mu Zhimei, Wang Yanwen, Liu Qingxin, Gao Huiju
- Paraconiothyium variable GHJ-4木质素降解酶的酶学性质
- Enzymological Characteristics of Ligninolytic Enzyme from Paraconiothyrium variabile GHJ-4
- 林业科学, 2017, 53(1): 94-100
- Scientia Silvae Sinicae, 2017, 53(1): 94-100.
- DOI: 10.11707/j.1001-7488.20170112
-
文章历史
- 收稿日期:2015-08-21
- 修回日期:2015-11-02
-
作者相关文章
木质素是一类以苯丙烷为基本单元的结构复杂且稳定的芳香族生物大分子物质(董旭杰等,2007;段传人等,2009),同时也是地球上仅次于纤维素、第二丰富的可再生资源,约占植物生物量的25%(Adler,1977)。在自然环境条件下,木质素的完全降解是真菌、细菌、放线菌及相应微生物群落共同作用的结果,其中真菌起主导作用(崔艳红等,2012)。木质素生物降解过程主要涉及3种细胞外酶:漆酶(laccase)、锰过氧化物酶(MnP) 和木质素过氧化物酶(LiP)(Abrahão et al., 2008;Leonowicz et al., 2001;苏小军等,2009;池玉杰等,2009)。laccase (EC1.10.3.2) 是一种含铜的多酚氧化酶,广泛存在于担子菌、子囊菌和植物中,其中真菌漆酶来源广泛,在合适的氧化还原辅基存在条件下,可参与木质素的降解过程(尤纪雪等,2008;金春德等,2009;王娟等,2010)。MnP (EC1.11.1.13) 是一种最常见依赖H2O2降解木质素的含亚铁血红素糖蛋白酶,在木腐菌和各种栖息土壤的枯落层降解担子菌中广泛存在(Orth et al., 1993;Hatakka,1994)。LiP (EC1.11.1.14) 与MnP同样也是一类含亚铁血红素辅基的过氧化物酶,最早由Glenn等(1983)从黄孢原毛平革菌(Phanerochaete chrysosporium) 中发现,并与其他木质素降解酶相互作用将木质素彻底氧化为CO2和H2O (喻云梅等,2005;王敏,2011;李阿敏等,2015)。
目前,国内外报道的产生木质素降解酶的菌株主要局限于白腐菌中的担子菌,如黄孢原毛平革菌、变色栓菌(Trametes versicolor)、糙皮侧耳(Pleurotusos treatus) 等菌种,而关于子囊菌产木质素降解酶的研究报道相对较少。Paraconiothyrium variabileGHJ-4是本实验室从泰山脚下一腐朽柳木中分离到的1株木质素降解子囊菌(GenBank注册号为GQ331986)(Gao et al., 2011),本研究对Paraconiothyrium variabile GHJ-4菌株产生laccase,MnP和LiP的情况进行检测,并研究其酶学性质,旨在查明GHJ-4降解木质素的主要酶系,为今后利用该菌株进行木质素降解酶的工业化生产和应用以及深入研究GHJ-4降解木质素的作用机制提供依据。
1 材料与方法 1.1 菌株和培养基 1.1.1 菌株子囊菌Paraconiothyrium variabile GHJ-4,由本实验室自行筛选并保存。
1.1.2 培养基PDA培养基:马铃薯200 g,葡萄糖20 g,琼脂15 g,KH2PO4 3 g,MgSO4·7H2O 1.5 g,加水定容至1 000 mL,用于GHJ-4菌株的活化。
产酶培养基:酒石酸铵10 mL (22 g·L-1),葡萄糖2.5 mL (200 g·L-1),大量元素15 mL,微量元素15 mL,VB1 3 mL (100 mg·L-1),加水至50 mL,pH 4.2。其中大量元素:KH2PO4 20 g·L-1,MgSO4·7H2O 13.8 g·L-1,CaCl2 1 g·L-1,NaCl 0.6 g·L-1;微量元素:MnSO4·H2O 0.35 g·L-1,FeSO4·7H2O 60 mg·L-1,CoCl·6H2O 110 mg·L-1,ZnSO4·7H2O 60 mg·L-1,CuSO4·5H2O 95 mg·L-1,AlK (SO4)2·12H2O 6 mg·L-1,H3BO3 6 mg·L-1,Na2MoO4·2H2O 6 mg·L-1(张文婷,2011)。
1.2 GHJ-4的培养方法和酶液制备在250 mL三角瓶中放入80 mL产酶培养基,接种直径为10 mm的GHJ-4菌饼3个,28 ℃、160 r·min-1条件下进行摇床培养,于特定时间取出,4 ℃、4 000 r·min-1离心20 min,吸取上清液为粗酶液,-80 ℃保存备用。
1.3 木质素降解酶酶活测定 1.3.1 漆酶活性的测定采用Gao等(2013)方法,在4.0 mL含1.0 mmol·L-1愈创木酚的50 mmol·L-1 pH 4.5的醋酸钠缓冲液中加入1.0 mL适当稀释的酶液,充分混匀后30 ℃反应30 min,冰浴中终止反应,测定465 nm处的吸光度(ε465=36 000 L·cm-1mol-1)。定义每分钟氧化1 μmol·L-1愈创木酚所需酶量为酶活单位U,其计算公式为:
| $ U = \frac{{{{10}^6} \times {V_{\rm{T}}} \times \Delta A}}{{{V_{\rm{E}}} \times \varepsilon \times \Delta t}} $ | (1) |
式中:VT,VE分别代表反应体系的总体积和反应酶液的体积;ε为吸光系数。
1.3.2 锰过氧化物酶活性的测定采用Wariishi等(1992)方法,向pH 4.5的3.36 mL 50 mmol·L-1的丙二酸钠缓冲液中依次加入0.2 mL 10 mmol·L-1的MnSO4、0.2 mL 10 mmol·L-1的2, 6-DMP、0.2 mL酶液样品和40 μL10 mmol·L-1的H2O2,25 ℃下保温5 min,于470 nm处测定吸光度(ε470=496 000 L·cm-1mol-1)。定义每分钟氧化1 μmol·L-1 2, 6-DMP所需酶量为酶活单位U,计算方法同1.3.1。
1.3.3 木质素过氧化物酶活性的测定采用Gao等(2011)方法,在4 mL体系中加入2.5 mL酒石酸缓冲液(100 mmol·L-1,pH 3.0)、1.0 mL 10 mmol·L-1藜芦醇、0.1 mL 10 mmol·L-1H2O2和0.4 mL酶液,于37 ℃测定酶反应前3 min内在310 nm处的吸光度(ε310=9 300 L·cm-1mol-1),酶促反应由加入H2O2后而启动。定义每分钟氧化1 μmol·L-1藜芦醇所需酶量为酶活单位U,计算方法同1.3.1。
1.4 木质素降解酶酶学性质测定 1.4.1 pH对木质素降解酶活性及稳定性的影响取适量酶液分别置于pH 2.0~9.0的缓冲体系中,测定3种酶的酶活,确定最适反应pH;将酶液置于pH 2.0~9.0的缓冲体系中25 ℃下保温1 h,测定剩余酶活,以酶活最高者为100%计算相对酶活。
1.4.2 温度对木质素降解酶活性及稳定性的影响将酶液分别在20~90 ℃下测定酶活,确定最适反应温度;将酶液分别在20~90 ℃保温1 h后测定剩余酶活,以酶活最高者为100%计算相对酶活。
1.4.3 金属离子对木质素降解酶活性的影响在酶液中分别加入KCl,NaCl,CaCl2,FeCl3,MgCl2,ZnCl2,MnCl2,CoCl2,AlCl3,CuCl2,(CH3COO)2Pb至终浓度为0.1,1.0,5.0 mmol·L-1,25 ℃保温1 h,测定剩余酶活,以未添加金属离子的酶活为100%计算相对酶活。
1.5 数据处理每个测试组样品平行测定3次,取平均值,所有试验数据运用Microsoft Excel数据处理系统进行统计分析。
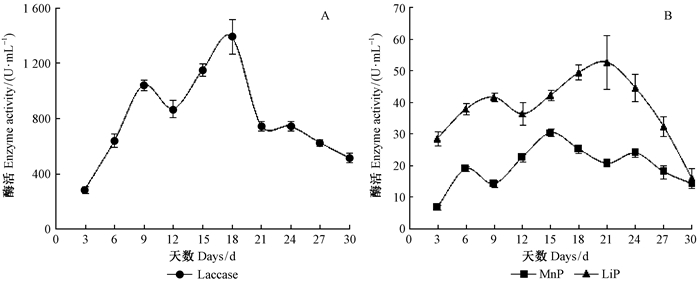
2 结果与分析 2.1 培养时间对GHJ-4产木质素降解酶的影响由图 1A和图 1B可知,GHJ-4菌株在接种后的第9天,laccase出现一分泌高峰,之后又经历下降、重新升高,到18天时达到最高值1 390.3 U·mL-1;MnP和LiP的分泌规律与laccase相类似,其中MnP在第15天达到最高酶活30.3 U·mL-1,LiP在第21天达到最高酶活52.5 U·mL-1。因此分别选取18,15和21天的发酵液进行laccase,MnP和LiP酶学特性的测定。
|
图 1 培养时间对GHJ-4产木质素降解酶的影响 Fig.1 Effect of incubation time on ligninolytic enzymes produced by GHJ-4 |
分别在不同pH反应体系下测定GHJ-4木质素降解酶的酶活,结果如图 2所示。由图 2可知,GHJ-4菌株laccase的最适反应pH为5.5左右,pH4.5~6.5时相对酶活在80%以上,pH>6.5时酶活迅速下降,pH 9.0时仅有少量酶活;MnP的最适反应pH为5.0左右,pH 4.5~7.0时相对酶活为在80%以上,pH>7.0时酶活呈现缓慢下降趋势,pH 9.0时相对酶活仍为63%;LiP的最适反应pH为3.0左右,pH 2.0~4.0时相对酶活在80%以上,pH>4.0时酶活迅速下降,pH 9.0时已经几乎检测不到酶活。

|
图 2 pH对GHJ-4木质素降解酶活性的影响 Fig.2 Effect of pH on enzyme activity of ligninolytic enzymes produced by GHJ-4 |
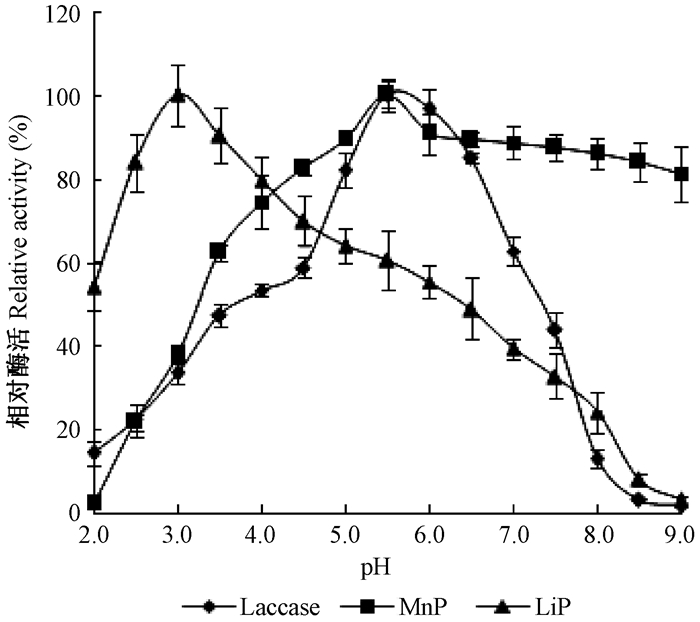
将酶液置于不同pH的缓冲液中保存1 h后测定木质素降解酶剩余酶活,结果如图 3所示。由图 3可知,laccase在pH 5.0~6.5时稳定性较好,酶活可保持在80%以上,pH>7.0时酶活损失较快;MnP有较宽的pH稳定性范围,pH 4.5~9.0时酶活均保持在80%以上,pH 9.0时仍能保持81%的酶活;LiP在酸性条件下较碱性条件下稳定,pH 3.0~3.5时酶活相对稳定,保持在80%以上,pH 3.5时,酶活迅速下降,pH 7.0时,相对剩余酶活仅为40%。
|
图 3 GHJ-4木质素降解酶的pH稳定性 Fig.3 Effect of pH on stability of ligninolytic enzymes produced by GHJ-4 |
分别在不同温度下测定GHJ-4木质素降解酶的酶活,结果如图 4所示。由图 4可知,GHJ-4木质素降解酶均在一定温度范围内随温度升高其酶活不断增强,laccase的最适反应温度为55 ℃左右,在45~60 ℃之间均有较高酶活,相对酶活在80%以上,之后酶活迅速下降;MnP的最适反应温度为60 ℃左右,55~70 ℃之间相对酶活在80%以上,超过70 ℃酶活迅速下降;LiP的最适反应温度为40 ℃左右,35~55 ℃之间相对酶活在80%以上,超过55 ℃酶活明显下降。当反应温度为90 ℃时,3种酶酶活均检测不到。

|
图 4 温度对GHJ-4木质素降解酶活性的影响 Fig.4 Effect of temperature on enzyme activity of ligninolytic enzymes produced by GHJ-4 |
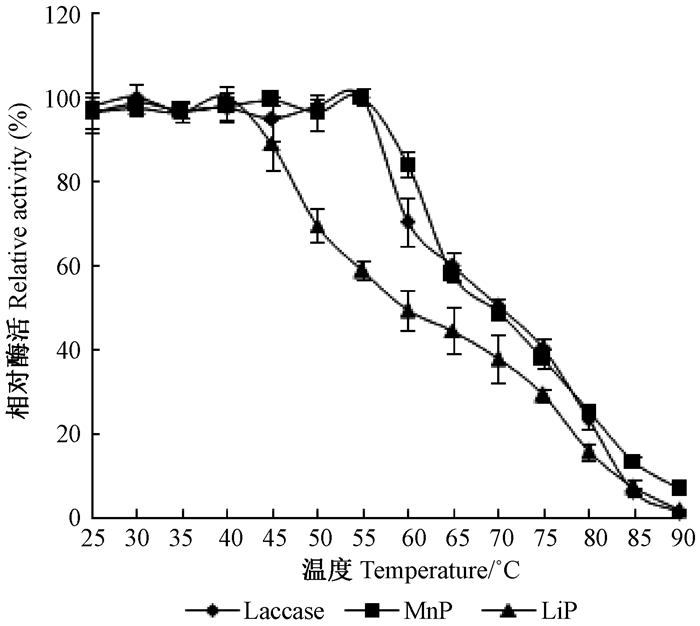
将酶液分别在不同温度下保温1 h后测定剩余酶活,结果如图 5所示。由图 5可知,laccase,MnP和LiP的相对酶活随着保存温度的升高迅速下降,laccase和MnP在55 ℃以下相对稳定,当温度超过55 ℃时,酶活迅速下降;而LiP在40 ℃以下相对稳定,当温度超过45 ℃时,酶活呈现迅速下降趋势。
|
图 5 GHJ-4木质素降解酶的热稳定性 Fig.5 Effect of temperature on stability of ligninolytic enzymes produced by GHJ-4 |
将酶液置于不同浓度的金属离子缓冲液中保存1 h后测定剩余酶活,结果如表 1所示。从表 1可看出,Mg2+,Zn2+,Cu2+和K+对laccase有促进作用,Mn2+,Fe3+,Ca2+,Pb2+,Co2+,Na+,Al3+对laccase都表现出一定程度的抑制作用,其中Fe3+,Ca2+,Pb2+和Co2+抑制作用较强;Mn2+对MnP有激活作用,其他金属离子在某种程度上都存在着对MnP的抑制作用,其中Fe3+和Pb2+抑制作用最为明显;Na+,Zn2+对LiP具有激活作用,而其他金属离子均存在不同程度的抑制作用,其中Mg2+,Fe3+,Ca2+,Pb2+,Co2+,Al3+的抑制作用较强。可见Fe3+和Al3+对3种酶都存在着一定程度的抑制作用,其中Fe3+为5 mmol·L-1时抑制作用最强。
|
|
关于木腐真菌培养条件的研究报道,不同菌株即使是同一菌株不同培养条件,其产酶的最佳时间也不相同。laccase的最佳产酶时间为36 h~32天(周菲,2011;宋安东等,2005),MnP的最佳产酶时间为7~24天(张连慧,2005;宋安东等,2005),LiP的最佳产酶时间为4~24天(杨暖,2009;宋安东等,2005)。本文通过研究GHJ-4所分泌的3种木质素降解酶随时间的变化规律,得到laccase,MnP和LiP的最佳产酶时间分别为18,15和21天,这与前人的研究结果基本一致。
关于木质素降解酶酶学性质的研究,大多认为laccase的最适反应温度为20~65 ℃,温度稳定性为25~60 ℃;最适反应pH为4.0~5.5,pH 3.5~8.0范围内均有较高酶活(董学卫等,2007;赵晓燕等,2012;肖楚等,2011;王维乐,2011)。MnP的最适反应温度为35~55 ℃,温度稳定性为20~50 ℃,最适反应pH为3.0~7.0,pH 2.5~9.0范围内均有较高酶活(程晓滨,2007;吴会广,2008;白娜,2010)。LiP的最适反应温度为35~50 ℃,温度稳定性为15~60 ℃,最适反应pH为2.5~7.0,pH 2.0~9.0范围内均有较高酶活(孔令营等,2010;杨暖,2009;金剑等,2010)。本研究中GHJ-4分泌的laccase最适反应温度55 ℃,55 ℃以下相对稳定,最适反应pH为5.5,pH 4.0~7.0稳定性较好;MnP最适反应温度60 ℃,55 ℃以下相对稳定,最适反应pH为5.0,pH 4.0~9.0较为稳定;LiP最适反应温度40 ℃,40 ℃以下稳定,最适反应pH为3.0,pH 2.0~4.0稳定。这表明LiP较laccase和MnP热稳定性差,laccase, LiP较MnP的pH稳定性范围窄,与其他白腐真菌木质素降解酶相比,除MnP最适反应温度略高外,其他酶学性质基本一致。
本研究中Mg2+,Zn2+,Cu2+,K+对laccase起激活作用,Na+和Zn2+对LiP起促进作用,Mn2+对MnP起促进作用,而Fe3+,Ca2+,Pb2+,Co2+,Al3+对3种酶都起抑制作用,其中以Fe3+的抑制作用最明显,浓度为5 mmol·L-1时,对3种酶活性的抑制率达到80%~100%,这与其他报道(肖楚等,2011;王维乐,2011;吴会广,2008;徐淑霞等,2007;金剑等,2010;张莉,2009) 有很大不同,说明同种金属离子对不同菌种木质素降解酶的影响不同,可能与其化学组成和分子结构不同有关。
为了更好地将GHJ-4进行工业应用,目前本实验室正通过对其降解酶进行分子改造和异源表达来进一步提高其反应温度和pH,相关研究正在进行中。
4 结论本研究通过对木质素降解子囊菌Paraconiothyrium variabile GHJ-4进行发酵培养,明确了GHJ-4所分泌的3种木质素降解酶随时间的变化规律;通过研究金属离子对GHJ-4产3种木质素降解酶活性的影响,证明即使是同种金属离子对不同菌种木质素降解酶的影响也不同,这可能与其化学组成和分子结构不同有关。研究结果为下一步进行该菌株木质素降解酶的分子改造以及木质素降解研究提供了重要的理论依据,对该菌株木质素降解酶的工业化生产、开发和利用具有重要的理论和实践意义。
| [] |
白娜. 2010.哈茨木霉WRF-2木质素降解酶系高产菌株培育及其对玉米秸秆生物降解研究.杨凌:西北农林科技大学硕士学位论文. ( Bai N. 2010. Cultivation of high ligninilytic enzyme of Trichoderma harzianumWRF-2 and study on biodergradation of corn straw. Yangling: MS thesis of Northwest A & F University. [in Chinese][in Chinese]) |
| [] |
程晓滨. 2007.裂褶菌F17锰过氧化物酶的分离纯化及其对偶氮染料脱色的研究.合肥:安徽大学硕士学位论文. ( Cheng X B. 2007. Purification of a new manganese peroxidase of the white-rot fungus Schizophyllumsp. F17, and decolorization of azo dyes by the enzyme. Hefei: MS thesis of Anhui University. [in Chinese][in Chinese]) |
| [] |
池玉杰, 闫洪波. 2009. 红平菇木质素降解酶系统漆酶、锰过氧化物酶及木质素过氧化物酶的检测. 林业科学, 45(12): 154–158.
( Chi Y J, Yan H B. 2009. Detection on laccase, manganese peroxidase and lignin peroxidase in ligninolytic enzymes of Pleurotus djamor. Scientia Silvae Sinicae, 45(12): 154–158. [in Chinese] ) |
| [] |
崔艳红, 韩庆功, 胡志明, 等. 2012. 木质层孔菌诱导漆酶及部分酶学性质研究. 广东农业科学(12): 114–116.
( Cui Y H, Han Q G, Hu Z M, et al. 2012. Research on laccase induced by Fomes ligmosus and its enzymatic properties. Guangdong Agricultural Sciences(12): 114–116. [in Chinese] ) |
| [] |
董旭杰, 曹福祥, 陈静, 等. 2007. 3种白腐菌木质素降解酶的比较. 中南林业科技大学学报, 27(3): 131–135.
( Dong X J, Cao F X, Chen J, et al. 2007. Comparison of lignin degradation enzymes produced by three white-rot fungi. Journal of Central South University of Forestry & Technology, 27(3): 131–135. [in Chinese] ) |
| [] |
董学卫, 朱启忠, 吕新萍, 等. 2007. 白毒鹅膏菌胞外漆酶的部分酶学性质研究. 石河子大学学报:自然科学版, 25(2): 132–136.
( Dong X W, Zhu Q Z, Lü X P, et al. 2007. Studies on partial character of extracellular laccase fromAmanita verna. Journal of Shihezi University: Natural Science, 25(2): 132–136. [in Chinese] ) |
| [] |
段传人, 朱丽平, 姚月良. 2009. 三种白腐菌及其组合菌种木质素降解酶比较研究. 菌物学报, 28(4): 577–583.
( Duan C R, Zhu L P, Yao Y L. 2009. Comparative studies on lignin degradation enzymes produced by three species of white-rot fungi and combination of the strains. Mycosystema, 28(4): 577–583. [in Chinese] ) |
| [] |
金春德, 王进, 毛胜凤, 等. 2009. 漆酶活化产生的活性氧类自由基与竹粉板性能的关系. 北京林业大学学报, 31(2): 119–121.
( Jin C D, Wang J, Mao S F, et al. 2009. Treatment of bamboo flour by reactive oxygen species free radicals: Effects on panel properties. Journal of Beijing Forestry University, 31(2): 119–121. [in Chinese] ) |
| [] |
金剑, 康文丽, 生吉萍, 等. 2010. 云芝(Coriolus versicolor) 木质素过氧化物酶(LiP) 酶学性质分析. 食品科学, 31(17): 224–227.
( Jin J, Kang W L, Sheng J P, et al. 2010. Enzymological Characteristics of Lignin Peroxidase (LiP) from Coriolus versicolor. Food Science, 31(17): 224–227. [in Chinese] ) |
| [] |
孔令营, 郭道森, 赵博光, 等. 2010. 荧光假单胞菌GcM5-1A胞外木质素过氧化物酶的初步纯化及性质研究. 北京林业大学学报, 32(3): 112–116.
( Kong L Y, Guo D S, Zhao B G., et al. 2010. Preliminary purification and characterization of extracellular lignin peroxidase from Pseudomonas fluorescens GcM5-1A. Journal of Beijing Forestry University, 32(3): 112–116. [in Chinese] ) |
| [] |
李阿敏, 李国庆, 常艳, 等. 2015. 白腐菌降解木质素的研究进展. 食药用菌, 23(2): 95–101.
( Li A M, Li G Q, Chang Y, et al. 2015. Research progress on lignin degradation by white rot fungi. Edible and medicinal mushrooms, 23(2): 95–101. [in Chinese] ) |
| [] |
宋安东, 张百良, 吴坤, 等. 2005. 杂色云芝产木质纤维素酶及对稻草秸秆的降解. 过程工程学报, 5(4): 414–419.
( Song A D, Zhang B L, Wu K, et al. 2005. Production of lignocellulolytic enzymes and rice straw biodegradation by Coriolus versicolor. The Chinese Journal of Process Engineering, 5(4): 414–419. [in Chinese] ) |
| [] |
苏小军, 熊兴耀, 谭兴和, 等. 2009. 黑曲霉AF-1固态发酵生产生淀粉酶的条件优化. 湖南农业大学学报:自然科学版, 35(2): 208–212.
( Su X J, Xiong X Y, Tan X H, et al. 2009. Optimization of raw-starch-hydrolysing amylase production by Aspergillus niger AF-1 in solid state fermentation. Journal of Hunan Agricultural University:Natural Sciences, 35(2): 208–212. [in Chinese] ) |
| [] |
王娟, 宗学刚. 2010. 漆酶处理三倍体毛白杨APMP及对其中残余木素作用的研究. 造纸化学品, 22(1): 15–20.
( Wang J, Zong X G. 2010. Treatment of APMP of triploid of Populus tomentosa with laccase and its reaction with residual lignin of APA. Paper Chemicals, 22(1): 15–20. [in Chinese] ) |
| [] |
王敏. 2011. 白腐菌降解木质素研究进展. 衡水学院学报, 13(1): 51–53.
( Wang M. 2011. Progress of research on white rot fungi degradating lignin. Journal of Hengshui University, 13(1): 51–53. [in Chinese] ) |
| [] |
王维乐. 2011. Paraconiothyrium variabile GHJ-4漆酶的发酵、分离纯化及其酶学性质的研究.泰安:山东农业大学硕士学位论文. ( Wang W L. 2011. Fermentation, purification and characterization of laccase from Paraconiothyrium variabile GHJ-4. Tai'an: MS thesis of Shandong Agricultural University. [in Chinese][in Chinese]) |
| [] |
吴会广. 2008. Rhizoctonia sp. SYBC-M3产锰过氧化物酶发酵条件优化及酶学性质研究.无锡:江南大学硕士学位论文. ( Wu H G. 2008. Optimization of Rhizoctonia sp. SYBC-M3 fermentation for manganese peroxidase production and the enzyme characterization. Wuxi: MS thesis of Jiangnan University. [in Chinese][in Chinese]) |
| [] |
肖楚, 刘佳, 许修宏. 2011. 黑木耳漆酶酶学性质的研究. 中国农学通报, 27(25): 158–161.
( Xiao C, Liu J, Xu X H. 2011. Studies on enzymatic properties of laccase from Auricularia. Chinese Agricultural Science Bulletin, 27(25): 158–161. [in Chinese] ) |
| [] |
徐淑霞, 张跃灵, 张世敏, 等. 2007. 黄孢原毛平革菌过氧化物酶的分离、纯化和酶学特性研究. 农业环境科学学报, 26(1): 295–300.
( Xu S X, Zhang Y L, Zhang S M., et al. 2007. Purification and properties of peroxidase from Phanerochaete chrysosporium. Journal of Agro-Environment Science, 26(1): 295–300. [in Chinese] ) |
| [] |
杨暖. 2009.绿色糖单孢菌木质素过氧化物酶发酵工艺、纯化及酶学性质研究.北京:北京林业大学硕士学位论文. ( Yang N.2009. Studies on fermentation conditions, purification and characteristics of lignin peroxidases from Saccharomonospora viridis. Beijing: MS thesis of Beijing Forestry University. [in Chinese][in Chinese]) |
| [] |
尤纪雪, 陈星星, 李雨楠, 等. 2008. 漆酶-木聚糖酶体系直接降解木质素的研究. 纤维素科学与技术, 16(2): 12–17.
( You J X, Chen X X, Li Y N., et al. 2008. Study on direct degradation of lignin with laccase/xylanase system. Journal of Cellulose Science and Technology, 16(2): 12–17. [in Chinese] ) |
| [] |
喻云梅, 刘赟, 翁恩琪, 等. 2005. 白腐真菌木质素降解酶的产生及其调控机制研究进展. 安全与环境学报, 5(2): 82–86.
( Yu Y M, Liu Y, Wang E Q, et al. 2005. Review on the production and regulation mechanism of ligninolytic enzymes of the white rot fungi. Journal of Safety and Environment, 5(2): 82–86. [in Chinese] ) |
| [] |
张连慧, 刘卫晓, 葛克山, 等. 2005. 变色栓菌产锰过氧化物酶的条件优化. 微生物学通报, 32(5): 98–102.
( Zhang L H, Liu W X, Ge K S, et al. 2005. The optimization of manganese peroxidase production by Trametes versicolor. Journal of Microbiology, 32(5): 98–102. [in Chinese] ) |
| [] |
张莉. 2009.白腐菌(Trametes pubescesMB89) 漆酶酶学性质及其对酚类化合物的降解特性研究.杨凌:西北农林科技大学博士学位论文. ( Zhang L. 2009. Characterstics of laccase from white rot rungus (Trametes pubescesMB89) and its use in phenolic compunds degradation.Yangling: PhD thesis of Northwest A & F University. [in Chinese][in Chinese]) |
| [] |
张文婷. 2011. Trametes trogii WT-1木质素降解作用的研究.泰安:山东农业大学博士学位论文. ( Zhang W T. 2011. Study on the lignin decomposition of Trametes trogii WT-1. Tai'an: PhD thesis of Shandong Agricultural University. [in Chinese][in Chinese]) |
| [] |
赵晓燕, 邢增涛, 邵毅, 等. 2012. 灰树花漆酶酶学性质的初步研究. 天然产物研究与开发, 24: 824–827.
( Zhao X Y, Xing Z T, Shao Y, et al. 2012. Preliminary study on enzyme property of Grifola frondosa extracellular laccase. Nat Prod Res Dev, 24: 824–827. [in Chinese] ) |
| [] |
周菲. 2011.产漆酶木霉ZF-2分离、发酵与初步应用研究.泰安:山东农业大学硕士学位论文. ( Zhou F. 2011. Isolating, fermentation and primary application by laccase from Trichoderma harzianum ZF-2. Tai'an:MS thesis of Shandong Agricultural University. [in Chinese][in Chinese]) |
| [] | Abrahão M C, Gugliotta A M, Silva R D, et al. 2008. Ligninolytic activity from newly isolated basidiomycete strains and effect of these enzymes on the azo dye orange Ⅱ decolourisation. Ann Microbiol, 58: 427–432. DOI:10.1007/BF03175538 |
| [] | Adler E. 1977. Lignin chemistry-past, present and future. Wood Sci Technol, 11(3): 169–218. DOI:10.1007/BF00365615 |
| [] | Gao H J, Wang Y W, Zhang W T, et al. 2011. Isolation, identification and application in lignin degradation of an ascomycete GHJ-4. Afr J Biotechnol, 10(20): 4166–4174. |
| [] | Gao H J, Chu X, Wang Y W, et al. 2013. Media optimization for laccase production by Trichoderma harzianum ZF-2 using response surface methodology. Microbiol Biotechnol, 23(12): 1757–1764. DOI:10.4014/jmb.1302.02057 |
| [] | Glenn J K, Gold M H. 1983. Decolorization of several polymeric dyes by the lignin-degrading basidiomycete Phanerochaete chrysosporium. Appl Environ Microbiol, 45(6): 1741–1747. |
| [] | Hatakka A. 1994. Lignin-modifying enzymes from selected white-rot fungi: production and role in lignin degradation. FEMS Microbiol Rev, 13(3): 125–135. |
| [] | Leonowicz A, Cho N S, Luterek J, et al. 2001. Fungal laccase: properties and activity on lignin. J Basic Microbiol, 41(3/4): 185–227. |
| [] | Orth A B, Royse D J, Tien M. 1993. Ubiquity of lignin-degrading peroxidases among various wood-degrading fungi. Appl Environ Microbiol, 59(12): 4017–4023. |
| [] | Wariishi H, Valli K, Gold M H. 1992. Manganese Ⅱ oxidation by manganese peroxidase from the basidiomycete Phanerochaete chrysosporium-kinetic mechanism and role of chelators. Journal of Biological Chemistry, 267(33): 23688–23695. |
 2017, Vol. 53
2017, Vol. 53

