文章信息
- 翟辉, 张海, 张超, 周旭
- Zhai Hui, Zhang Hai, Zhang Chao, Zhou Xu
- 黄土峁状丘陵区不同类型林分土壤微生物功能多样性
- Soil Microbial Functional Diversity in Different Types of Stands in the Hilly-Gully Regions of Loess Plateau
- 林业科学, 2016, 52(12): 84-91
- Scientia Silvae Sinicae, 2016, 52(12): 84-91.
- DOI: 10.11707/j.1001-7488.20161210
-
文章历史
- 收稿日期:2015-11-30
- 修回日期:2016-03-29
-
作者相关文章
土壤微生物是土壤生态系统的重要组成部分,其参与土壤有机质的分解和腐殖质的形成,是土壤养分转化和循环以及有机碳代谢的主要驱动力(Dick et al.,1997)。土壤微生物对外界条件如土地利用以及管理措施等变化十分敏感,能及时反映土壤状况(Bucher et al.,2005),同时监测土壤微生物群落状态和功能也能够很好地评价植被恢复的效果(刘占锋等,2007)。反映土壤微生物群落状态和功能的指标通常包括土壤微生物量和微生物群落代谢多样性(Rogers et al.,2001),其中土壤微生物群落多样性反映了群落总体的动态变化,它可以通过检测微生物碳源利用程度来反映。Biolog方法可测定土壤微生物对不同碳源的利用能力和代谢差异,在一定程度上能够反映土壤碳源转化和土壤微生物多样性情况(鲁顺保等,2012)。该方法由于简单、快速等优点已被广泛用于评价不同土壤类型、不同土地利用方式和不同植被恢复的土壤微生物群落多样性(Zheng et al.,2005; 张海涵等,2009; 张燕燕等,2010; 刘秉儒等,2013; 胡婵娟等,2014)。
黄土峁状丘陵区是我国生态脆弱、水土流失严重的区域。在近几年大规模的退耕还林工程中营造了大量的坡地人工林,使该地区保留了大量立地条件、树种迥然不同的植被类型。研究表明,植物对土壤环境的重要影响之一是改变土壤微生物群落特征,且不同恢复植被对土壤微生物的影响存在差异(Söderberg et al.,,2002)。因此, 研究植被、微生物和土壤环境之间关系能更好地了解植被与土壤微生物之间的相互作用及植被恢复对土壤环境生物学方面的改善状况(向泽宇等,2014)。近几年关于该地区的研究,主要集中在植被恢复后土壤理化性质的变化特征、营养状况(Zhu et al.,2010; 隋媛媛等,2011; 王凯博等,2012)以及微生物区系特征方面(张文婷等,2008; Zhang et al.,2012),而关于土壤微生物对植被恢复的响应以及不同植被恢复的土壤微生物代谢活性的研究较少(Zhang et al.,2013)。本试验在陕西省米脂县境内选取退耕还林中的主栽树种柠条(Caragana korshinskii)、刺槐(Robinia pseudoacacia)、油松(Pinus tabulaeformis)、侧柏(Platycladus orientalis)、新疆杨(Populus alba var. pyramidalis)等植被类型下土壤微生物为研究对象,以撂荒坡地为对照。利用Biolog-ECO微平板培养法探讨不同类型林分下土壤微生物群落代谢多样性,旨在从微生物的角度对当地典型植被类型做出评价,为该地区植被恢复提供参考。
1 材料与方法 1.1 研究区概况试验区位于陕西省米脂县泉家沟(37°46′—38°50′N,109°49′—110°18′E),属黄土高原峁状丘陵区,平均海拔1 049 m。气候属半干旱大陆性季风气候,年平均气温8.3 ℃,≥10 ℃的年平均积温3 400 ℃,年日照时数2 716 h,无霜期165天,干燥度1.14,年降雨量450 mm左右,多集中在7—9月,占到年降雨量的70%以上,每年有相当一部分降水形成径流流失。土壤为黄绵土,土层深厚,坡地自然植被群落稀疏。
1.2 样品采集于2012年6月下旬选取5块生长状况和立地条件较为一致的造林树种样地,即柠条、刺槐、油松、侧柏和新疆杨人工林,林龄均为10年,同时选取撂荒坡地为对照。每块样地随机设置3个5 m×5 m样方,每个样方用梅花形布点法取5个样点,除去表面可见的动物和植物残体,采集0—20 cm深5个点的土壤混合样,将每块样地采集的15个样点,每5个样点的土壤混合均匀得到3个平行样,装入无菌袋中带回实验室,置于4 ℃冰箱保存,用于土壤微生物功能多样性的测定。样地基本情况见表 1。
|
|
称取相当于5 g干质量的新鲜土样加入至装有45 mL、0.85%NaCl无菌溶液的150 mL三角瓶中,摇床振荡30 min,转速为180 r·min-1。将得到的微生物悬浮液采用10倍稀释法稀释至浓度为10-3。在超净工作台上,接种微生物悬浮液于生态测试板中,每孔150 μL,每样1板,每板3次重复。将接种后的测试板加盖在30 ℃生化培养箱中连续培养240 h,每隔24 h用Biolog自动读数装置在590 nm下读数(张卫娟等,2011)。
Biolog-ECO微平板孔中溶液吸光值平均颜色变化率(average well color development,AWCD)的计算公式如下:
| ${\text{AWCD = }}\Sigma \left( {{C_i} - R} \right)/n{\text{。}}$ |
式中,Ci为各反应孔在590 nm的吸光度值,R为Biolog-Eco板对照孔A1的吸光度值,n为反应孔数,Biolog-Eco板n值为31,Ci-R小于零的孔,计算中记为零,即Ci-R≥0。
Simpson指数D=1-∑ Pi2,
Shannon指数H=-∑ Pi ×(lnPi ),
McIntosh 指数E=H/lnS。
式中,Pi为第i孔的相对吸光值与所有整个微平板的相对吸光值总和的比值 (Ci-Ri)/ ∑(Ci-Ri); S为颜色发生变化的孔数(AWCD>0.2代表该孔碳源被利用)(徐万里等,2015)。
1.4 数据处理与分析数据分析在 SPSS 21.0 中进行,采用方差分析和LSD 比较不同类型林分土壤微生物群落多样性的差异性,显著性水平设定为α=0.05,利用Pearson相关系数评价Shannon指数、Simpson指数和McIntosh指数与土壤理化性质(有机质和全氮)的相关关系,相关图表制作在 Excel 2010中完成。
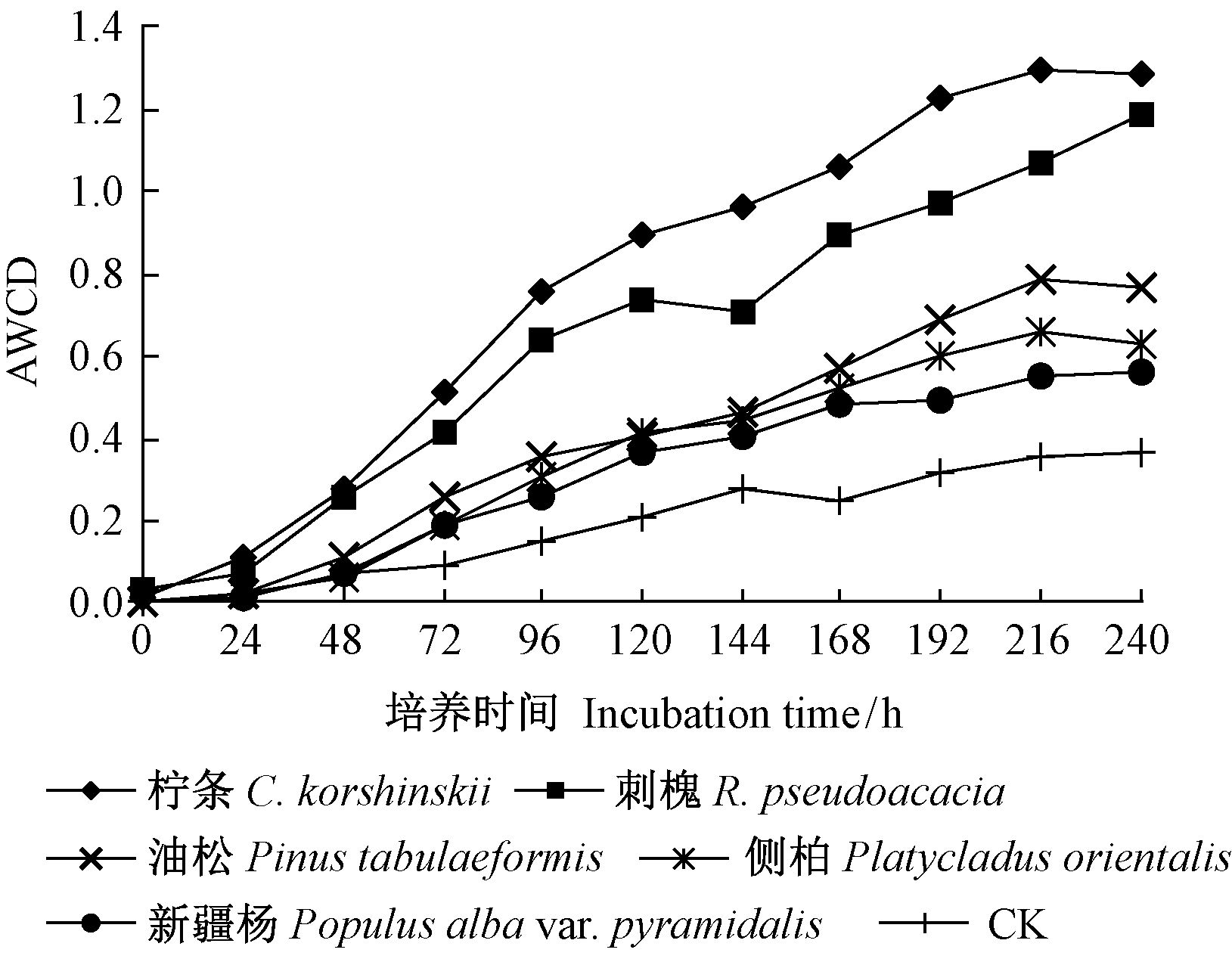
2 结果与分析 2.1 土壤微生物群落AWCD值的动态变化AWCD值反映了微生物的代谢活性,是土壤微生物群落利用单一碳源能力的一个重要指标(Zabinski et al.,1997)。计算不同类型林分土壤AWCD值的3次重复平均值,绘制AWCD值随培养时间的动态变化曲线。由图 1可知,每隔24 h测定的AWCD值随着培养时间的延长均呈增大趋势,表明5种类型林分土壤微生物利用碳源的量随着培养时间的延长逐渐增大,且各类型林分土壤微生物利用碳源的量均大于对照。土壤微生物群落的AWCD值均在24~96 h内迅速升高,随后持续缓慢地升高直到培养时间结束。AWCD值的快速增加表明微生物进入指数生长期,碳源被大量利用。在整个培养过程中,不同类型林分土壤微生物群落的AWCD值存在明显差异,大小顺序依次为: 柠条林>刺槐林>油松林>侧柏林>新疆杨林>对照,即柠条林土壤微生物代谢活性最强,刺槐林次之,而油松林、侧柏林和新疆杨林土壤微生物代谢活性相对较弱。
|
图 1 不同类型林分土壤微生物群落AWCD随培养时间的变化 Fig.1 Changes of soil AWCD in different forest types with incubation time |
Shannon指数(H)、Simpson指数(D)和McIntosh指数(E)是表征群落多样性的常用指数,是研究群落物种数及其个体数和分布均匀程度的综合指标,是目前应用最为广泛的群落多样性指数(陈宏灏等,2011)。参考贾夏等(2013)的研究结果,本试验采用Biolog-ECO微平板培养96 h的数据进行微生物代谢多样性分析。由表 2可知,各类型林分土壤微生物多样性指数均较对照有所提高,但不同类型林分土壤微生物群落代谢多样性用不同指数表示时存在差异。柠条林土壤Shannon指数和Simpson指数显著高于刺槐林、油松林、新疆杨林和侧柏林(P<0.05),表明柠条林土壤微生物群落多样性以及种群丰富度较高。刺槐林土壤McIntosh指数显著高于其他4种类型林分(P<0.05),表明刺槐林土壤微生物分布相对均匀。
|
|
本研究中所用的Biolog-ECO板的31种碳源可以分为6类,包括糖类、氨基酸类、羧酸类、多聚物类、芳香化合物类和胺类。表 3为Biolog-ECO微平板培养96 h每类碳源的AWCD平均值。由表 3可知,5种类型林分土壤微生物对6类碳源的利用率均高于对照,而不同类型林分土壤微生物对6类碳源利用能力的大小差异显著。刺槐林土壤微生物对糖类利用率最高,柠条林次之,油松林、新疆杨林和侧柏林较低。土壤微生物对氨基酸类碳源利用率最大的为柠条林,刺槐林和油松林次之,侧柏林和新疆杨林较低。柠条林和刺槐林土壤微生物对羧酸类利用率最高,其次是油松林、侧柏林和新疆杨林。侧柏林土壤微生物对多聚物类利用率最高,柠条林次之。不同类型林分土壤微生物对多酚类和胺类的利用率均表现为柠条和刺槐林较高,其余林地之间差异不显著(P>0.05)。总体而言,在5种林分中柠条林和刺槐林土壤微生物对主要碳源利用率较高,油松林、侧柏林和新疆杨林土壤微生物对主要碳源利用率较低。糖类是5种林分土壤微生物的主要碳源,其次为氨基酸类、羧酸类和多聚物类,多酚类和胺类利用率最小。
|
|
Biolog-ECO微平板中含有31种碳源,31种碳源的测定结果形成了描述微生物群落代谢特性的多元向量,不易直接比较。通过主成分分析可以用点的位置直观地反映出不同微生物群落的代谢特征。利用培养96 h的AWCD值,对不同类型林分土壤微生物利用单一碳源特性进行主成分分析,同时提取特征值大于1的主成分的特征根及方差贡献率。本研究共提取出4个主成分,累计贡献率达97.8%。其中第1主成分(PC1)的特征根为13.32,方差贡献率为43.0%; 第2主成分(PC2)的特征根为8.23,方差贡献率为26.5%; 第3主成分(PC3)的特征根为3.96,方差贡献率为12.8%; 其余2个主成分贡献率小于10%。从中提取可以聚集单一碳源变量的数据变异(累计方差贡献率)为69.5%的前2个主成分PC1和PC2进行分析,以PC1为横轴,PC2为纵轴,以不同类型林分31种碳源底物利用情况在2个主成分上的得分值为坐标作图,得到土壤微生物碳源利用主成分分析图(图 2)。由图 2可见,在PC1轴上,刺槐林和柠条林分布在正方向,油松林、新疆杨林、侧柏林和撂荒地分布在负方向; 在PC2轴上,柠条林和侧柏林分布在正方向,而刺槐林、油松林、新疆杨林和对照分布在负方向。由此表明柠条林、刺槐林和侧柏林的土壤微生物群落有各自独特的碳源利用模式,且柠条林土壤微生物群落对碳源的利用能力最强,而油松林、新疆杨林和对照的土壤微生物群落具有相似的碳源利用特征。

|
图 2 不同类型林分土壤微生物群落对碳源代谢的主成分分析 Fig.2 Principal components analysis(PCA)of soil microbial metabolic profiles in different forest types |
初始载荷因子反映主成分与碳源利用的相关系数,载荷因子越高,表示该碳源对主成分的影响越大。由表 4可知,对PC1贡献较大的碳源有20种,其中糖类占7种,氨基酸类占4种,羧酸类和多聚物类各占3种,胺类占2种,多酚类占1种,可见影响PC1的主要为糖类和氨基酸类; 对PC2贡献大的碳源有17种,其中糖类占5种,羧酸类占4种,多聚物类占3种,氨基酸类和多酚类各占2种,胺类占1种,表明影响PC2的碳源主要为是糖类和羧酸类。
|
|
Biolog-ECO微平板中共有31种碳源,碳源每孔AWCD值的变化可反映土壤微生物群落代谢活性和碳源利用能力。AWCD值越大,表明土壤微生物群落代谢活性越强(Konopka et al.,1998)。研究表明不同的植被对土壤生态系统特别是土壤微生物有着显著的影响,植被的类型、数量和化学组成可能是土壤微生物多样性变化的主要推动力(Waid,1999)。本研究发现黄土峁状丘陵区5种类型林分土壤微生物群落的碳源利用量以及代谢活性均较对照显著提高,这是因为种植人工林后植物根际释放了大量的碳源,同时植被凋落物的分解增加了土壤中的有机质以及C、N、P等养分的含量,继而影响了土壤微生物群落的分布以及代谢活性。此外不同类型林分土壤微生物代谢活性不同,这一发现与Zhang等(2013)研究结果一致。Grayston等(2004)研究表明不同类型草原的土壤微生物群落结构以及活性不同,主要与提供给土壤的碳源类型以及含量的不同有关。植物根系对土壤微生物有显著影响,且根系分泌物对土壤微生物的分布有重要作用(Nayyar et al.,2009)。此外,土壤理化性质的改变可能导致土壤微生境的变化,因此土壤微生物的分布以及活性和多样性均受到影响(Pengthamkeerat et al.,2011)。
本文采用Shannon指数(H)、Simpson指数(D)和McIntosh指数(E)研究了不同类型林分土壤微生物群落对31种碳源利用的多样性。多样性指数值越大表明土壤微生物群落功能多样性越高,反之亦然。结果表明5种类型林分土壤Shannon指数(H)、Simpson指数(D)和McIntosh指数(E)均较对照有所提高,表明种植人工林增加了土壤微生物种群多样性以及种群丰富度和均匀度。Zhang等(2013)研究也发现植被群落能显著提高土壤微生物群落功能多样性。5种类型林分中柠条林和刺槐林土壤Shannon指数、Simpson指数和McIntosh指数值较大,表明柠条林和刺槐林土壤微生物功能多样性较高,可能与柠条林和刺槐林土壤有机质含量较高有关。因为由3种指数与有机质和全氮的相关性分析(表 5)可以看出,3种指数与土壤有机质均极显著相关,由此说明丰富的碳源为微生物提供了大量的营养来源,从而提高了微生物的多样性以及对碳源的利用能力。此外,柠条和刺槐属于豆科植物,有研究表明豆科植物可显著增进微生物群落规模和功能(Han et al.,2007)。
|
|
研究不同类型林分土壤微生物对不同碳源利用能力的差异,可深入了解微生物群落的结构组成(郑华等,2007)。本研究结果表明,5种类型林分土壤微生物对糖类、氨基酸类、羧酸类、多聚物类、多酚类以及胺类等6种碳源的利用率均高于对照,而不同类型林分土壤微生物对不同碳源的利用率不同,说明各类型林分的土壤微生物对糖类、氨基酸类、羧酸类、多聚物类、多酚类以及胺类的利用具有选择性。胡婵娟等(2009)研究也发现了类似的现象,其原因可能与植物的生理特性、光合产物以及根系分泌物等有关(Ladygina et al.,2010)。PCA分析表明,不同类型林分土壤微生物碳源利用特征出现分异,在主成分分离中起主要贡献作用的是糖类、氨基酸类和羧酸类。Peter等(2001)的研究也发现,葡萄糖和氨基酸是细菌和真菌等土壤微生物代谢利用的主要碳源。植被类型的不同导致植物群落结构发生了变化,而植物种类又影响了微生物多样性及土壤中的碳分配(Pignataro et al.,2012)。
本研究利用Biolog方法分析了黄土高原峁状丘陵区不同类型林分土壤微生物群落特征,但是Biolog方法主要针对可培养的细菌类群,对于不可培养的且具有特殊功能的微生物无法检测(张超等,2015)。尽管Biolog分析法存在一定缺陷,但它仍然是研究土壤微生物代谢功能的一种快速有效方法。由于土壤微生物的复杂性和土壤中绝大多数微生物不可培养,仍需结合其他检测方法开展土壤微生物群落功能类群研究。
| [] |
陈宏灏, 张蓉, 张怡, 等. 2011. 压砂地土壤微生物群落功能多样性分析. 土壤通报 , 42 (1) : 51–55.
( Chen H H, Zhang R, Zhang Y, et al.2011. Analysis of microbial community function diversity in gravel-mulched field. Chinese Journal of Soil Science , 42 (1) : 51–55. [in Chinese] ) |
| [] |
胡婵娟, 傅伯杰, 刘国华, 等. 2009. 黄土丘陵沟壑区典型人工林下土壤微生物功能多样性. 生态学报 , 29 (2) : 727–733.
( Hu C J, Fu B J, Liu G H, et al.2009. Soil microbial functional and diversity under typical artificial woodlands in the hilly area of the Loess Plateau. Acta Ecologica Sinica , 29 (2) : 727–733. [in Chinese] ) |
| [] |
胡婵娟, 郭雷, 刘国华. 2014. 黄土丘陵沟壑区不同植被恢复格局下土壤微生物群落结构. 生态学报 , 34 (11) : 2986–2995.
( Hu C J, Guo L, Liu G H.2014. Soil microbial community structure under different vegetation restoration patterns in the loess hilly area. Acta Ecologica Sinica , 34 (11) : 2986–2995. [in Chinese] ) |
| [] |
贾夏, 董岁明, 周春娟. 2013. 微生物生态研究中Biolog Eco微平板培养时间对分析结果的影响. 应用基础与工程科学学报 , 21 (1) : 10–19.
( Jia X, Dong S M, Zhou C J.2013. Effects of biolog eco-plates incubation time on analysis results in microbial ecology researches. Journal of Basic Science and Engineering , 21 (1) : 10–19. [in Chinese] ) |
| [] |
刘秉儒, 张秀珍, 胡天华, 等. 2013. 贺兰山不同海拔典型植被带土壤微生物多样性. 生态学报 , 33 (22) : 7211–7220.
( Liu B R, Zhang X Z, Hu T H, et al.2013. Soil microbial diversity under typical vegetation zones along an elevation gradient in Helan Mountains. Acta Ecologica Sinica , 33 (22) : 7211–7220. DOI:10.5846/stxb [in Chinese] ) |
| [] |
刘占锋, 刘国华, 傅伯杰, 等. 2007. 人工油松林恢复过程中土壤微生物生物量C、N的变化特征. 生态学报 , 27 (3) : 1011–1018.
( Liu Z F, Liu G H, Fu B J, et al.2007. Dynamics of soil microbial biomass C, N along restoration chronosequences in pine plantations. Acta Ecologica Sinica , 27 (3) : 1011–1018. [in Chinese] ) |
| [] |
鲁顺保, 郭晓敏, 芮亦超, 等. 2012. 澳大利亚亚热带不同森林土壤微生物群落对碳源的利用. 生态学报 , 32 (9) : 2819–2826.
( Lu S B, Guo X M, Rui Y C, et al.2012. Utilization of carbon sources by the soil microbial communities of different forest types in subtropical Australia. Acta Ecologica Sinica , 32 (9) : 2819–2826. DOI:10.5846/stxb [in Chinese] ) |
| [] |
隋媛媛, 杜峰, 张兴昌. 2011. 黄土丘陵区撂荒群落土壤速效养分空间变异性研究. 草业学报 , 20 (2) : 76–84.
( Sui Y Y, Du F, Zhang X C.2011. Spatial heterogeneity of available soil nutrients in abandoned ole-field communities in the Loess Hilly Region. Acta Prataculturae Sinica , 20 (2) : 76–84. [in Chinese] ) |
| [] |
王凯博, 时伟宇, 上官周平. 2012. 黄土丘陵区天然和人工植被类型对土壤理化性质的影响. 农业工程学报 , 28 (15) : 80–86.
( Wang K B, Shi W Y, Shangguan Z P.2012. Effects of natural and artificial vegetation types on soil properties in Loess Hilly region.. Transactions of the Chinese Society of Agricultural Engineering , 28 (15) : 80–86. [in Chinese] ) |
| [] |
向泽宇, 张莉, 张全发, 等. 2014. 青海不同林分类型土壤养分与微生物功能多样性. 林业科学 , 50 (4) : 22–31.
( Xiang Z Y, Zhang L, Zhang Q F, et al.2014. Soil nutrients and microbial functional diversity of different stand types in Qinghai province. Scientia Silvae Sinicae , 50 (4) : 22–31. [in Chinese] ) |
| [] |
徐万里, 唐光木, 葛春辉, 等. 2015. 长期施肥对新疆灰漠土土壤微生物群落结构与功能多样性的影响. 生态学报 , 35 (2) : 468–477.
( Xu W L, Tang G M, Ge C H, et al.2015. Effects of long-term fertilization on diversities of soil microbial community structure and function in grey desert soil of Xinjiang. Acta Ecologica Sinica , 35 (2) : 468–477. [in Chinese] ) |
| [] |
张超, 刘国彬, 薛萐, 等. 2015. 黄土丘陵区不同植被类型根际微生物群落功能多样性研究. 草地学报 , 23 (4) : 710–717.
( Zhang C, Liu G B, Xue S, et al.2015. Functional diversity of rhizosphere microbial community of different vegetation types in the hilly-gully region of Loess Plateau. Acta Agrestia Sinica , 23 (4) : 710–717. [in Chinese] ) |
| [] |
张红, 吕家珑, 曹莹菲, 等. 2014. 不同植物秸秆腐解特性与土壤微生物功能多样性研究. 土壤学报 , 51 (4) : 743–752.
( Zhang H, Lü J L, Cao Y F, et al.2014. Decomposition characteristics of different plant straws and soil microbial functional diversity. Acta Pedologica Sinica , 51 (4) : 743–752. [in Chinese] ) |
| [] |
张海涵, 唐明, 陈辉. 2009. 黄土高原典型林木根际土壤微生物群落结构与功能特征及其环境指示意义. 环境科学 , 30 (8) : 2432–2437.
( Zhang H H, Tang M, Chen H.2009. Characterization of soil microbial community function and structure in rhizosphere of typical tree species and the meaning for environmental indication in the Loess Plateau. Environmental Science , 30 (8) : 2432–2437. [in Chinese] ) |
| [] |
张卫娟, 谷洁, 刘强, 等. 2011. 重金属Zn对猪粪堆肥过程中微生物群落的影响. 环境科学学报 , 31 (10) : 2260–2267.
( Zhang W J, Gu J, Liu Q, et al.2011. Effects of heavy metal Zn on microbial community during pig manure composting. Acta Scientiae Circumstantiae , 31 (10) : 2260–2267. [in Chinese] ) |
| [] |
张文婷, 来航线, 王延平, 等. 2008. 黄土高原不同植被坡地土壤微生物区系特征. 生态学报 , 28 (9) : 4228–4234.
( Zhang W T, Lai H X, Wang Y P, et al.2008. Microbial populations in different vegetation in sloping field on the Loess Plateau. Acta Ecologica Sinica , 28 (9) : 4228–4234. [in Chinese] ) |
| [] |
张燕燕, 曲来叶, 陈利顶, 等. 2010. 黄土丘陵沟壑区不同植被类型土壤微生物特性. 应用生态学报 , 21 (1) : 165–173.
( Zhang Y Y, Qu L Y, Chen L D, et al.2010. Soil microbial properties under different vegetation types in Loess hilly region. Chinese Journal of Applied Ecology , 21 (1) : 165–173. [in Chinese] ) |
| [] |
郑华, 陈法霖, 欧阳志云, 等. 2007. 不同森林土壤微生物群落对Biolog-GN板碳源的利用. 环境科学 , 28 (5) : 1126–1130.
( Zheng H, Chen F L, Ouyang Z Y, et al.2007. Utilization of different carbon sources types in Biolog-GN microplates by soil microbial communities from four forest types. Environmental Science , 28 (5) : 1126–1130. [in Chinese] ) |
| [] | Bucher A E, Lanyon L E.2005. Evaluating soil management with microbial community-level physiological profiles. Applied Soil Ecology , 29 : 59–71. DOI:10.1016/j.apsoil.2004.09.007 |
| [] | Dick R P. 1997. Soil enzyme activities as integrative indicators of soil health. Biological Indicators of Soil Health,121-156. |
| [] | Grayston S J, Campbell C D, Bardgett R D, et al.2004. Assessing shifts in microbial community structure across a range of grasslands of differing management intensity using CLPP, PLFA and community DNA techniques. Applied Soil Ecology , 25 (1) : 63–84. DOI:10.1016/S0929-1393(03)00098-2 |
| [] | Han X M, Wang R Q, Liu J, et al.2007. Effects of vegetation type on soil microbial community structure and catabolic diversity assessed by polyphasic methods in North China. Journal of Environmental Sciences , 19 : 1228–1234. DOI:10.1016/S1001-0742(07)60200-9 |
| [] | Konopka A, Oliver L, Turc R F.1998. The use of carbon substrate utilization patterns in environmental and ecological microbiology. Microbial Ecology , 35 (2) : 103–115. DOI:10.1007/s002489900065 |
| [] | Ladygina N, Hedlund K.2010. Plant species influence microbial diversity and carbon allocation in the rhizosphere. Soil Biology & Biochemistry , 42 (2) : 162–168. |
| [] | Nayyar A, Hamel C, Lafond G, et al.2009. Soil microbial quality associated with yield reduction in continuous-pea. Applied Soil Ecology , 43 (1) : 115–121. DOI:10.1016/j.apsoil.2009.06.008 |
| [] | Pengthamkeerati P, Motavalli P P, Kremer R J.2011. Soil microbial activity and functional diversity changed by compaction, poultry litter and cropping in a claypan soil. Applied Soil Ecology , 48 (1) : 71–80. DOI:10.1016/j.apsoil.2011.01.005 |
| [] | Peter C, Simon P W, Jonathan M A.2001. Effects of fungal inocula on the decomposition of lignin and structural polysaccharides in Pinus sylvestris litter. Biology and Fertility of Soils , 33 (3) : 246–251. DOI:10.1007/s003740000315 |
| [] | Pignataro A, Moscatelli M C, Mocali S, et al.2012. Assessment of soil microbial functional diversity in a coppiced forest system. Applied Soil Ecology , 62 : 115–123. DOI:10.1016/j.apsoil.2012.07.007 |
| [] | Rogers B F, Tate Ó R L.2001. Temporal analysis of the soil microbial community along a top sequence in Pineland soils. Soil Biology & Biochemistry , 33 : 1389–1401. |
| [] | Söderberg K H, Olsson P A, Bååth E.2002. Structure and activity of the bacterial community in the rhizosphere of different plant species and the effect of arbuscular my corrhizal colonization. FEMS Microbiology Ecology , 40 (3) : 223–231. DOI:10.1111/fem.2002.40.issue-3 |
| [] | Waid J S.1999. Does soil biodiversity depend upon metabiotic activity and influences. Applied Soil Ecology , 13 : 151–158. DOI:10.1016/S0929-1393(99)00030-X |
| [] | Zabinski C A, Gannon J E.1997. Effects of recreational impacts on soil microbial communities. Environmental Management , 21 (2) : 233–238. DOI:10.1007/s002679900022 |
| [] | Zhang C, Liu G B, Xue S.2012. Rhizosphere soil microbial properties on abandoned croplands in the Loess Plateau. European Journal of Soil Biology , 50 : 127–136. DOI:10.1016/j.ejsobi.2012.01.002 |
| [] | Zhang C, Xue S, Liu G B, et al.2013. Effect of different vegetation types on the rhizosphere soil microbial community structure in the Loess Plateau of China. Journal of Integrative Agriculture , 12 (11) : 2103–2113. DOI:10.1016/S2095-3119(13)60396-2 |
| [] | Zhang H F, Li G, Song X L, et al.2013. Changes in soil microbial functional diversity under different vegetation restoration patterns for Hulunbeier Sandy Land. Acta Ecologica Sinica , 33 (1) : 38–44. DOI:10.1016/j.chnaes.2012.12.006 |
| [] | Zheng H, Ouyang Z Y, Wang X K, et al.2005. Effects of regenerating forest cover on soil microbial communities:A case study in hilly red soil region, Southern China. Forest Ecology and Management , 217 (2/3) : 244–254. |
| [] | Zhu B B, Li Z B, Li P, et al.2010. Soil erodibility, microbial biomass, and physical-chemical property changes during long-term natural vegetation restoration:a case study in the Loess Plateau, China. Ecological Research , 25 : 531–541. DOI:10.1007/s11284-009-0683-5 |
 2016, Vol. 52
2016, Vol. 52

