文章信息
- 王启业, 王义强, 田宇, 彭牡丹, 陈章靖, 陆利
- Wang Qiye, Wang Yiqiang, Tian Yu, Peng Mudan, Chen Zhangjing, Lu Li
- 基于杨木发酵产异丁醇大肠杆菌工程菌构建
- Construction of Engineering Escherichia coli Strains Used for Isobutanol Production from Poplar Hydrolysate Fermentation
- 林业科学, 2015, 51(7): 157-164
- Scientia Silvae Sinicae, 2015, 51(7): 157-164.
- DOI: 10.11707/j.1001-7488.20150718
-
文章历史
- 收稿日期:2014-01-02
- 修回日期:2015-04-14
-
作者相关文章
2. 经济林培育与保护教育部重点实验室 长沙 410004;
3. 国家林业局生物乙醇研究中心 长沙 410004
2. Key Lab of Non-Wood Forest Nurturing and Protection of National Ministry of Education Changsha 410004;
3. Bio-Ethanol Research Center of State Forestry Administration Changsha 410004
随着全球环境问题及能源危机的不断加剧,生物燃料引起了人们的广泛关注,开发可替代生物燃料已成为世界各国提高能源安全、减排温室气体排放及应对气候变化的重要措施。利用木质纤维类生物质转化为生物燃料是一种非常有潜力的可持续能源发展战略。然而,近年来的研究重点主要集中在以工程酵母菌发酵木质纤维水解液生产燃料乙醇方面(Ho et al., 1998); 其他微生物,如运动发酵单胞菌(Zhang et al., 1995)、大肠杆菌(Escherichia coli)(Ohta et al., 1991)也被用于燃料乙醇的生产。尽管通过生物发酵生产乙醇已有相当长一段时间,且在生物燃料方面起着重要的作用,但由于其热值低、吸湿性强、不易管道输送等不足限制了其发展。相比之下,高级醇具有热值高、不易吸水、挥发性低等特点,将成为新一代生物燃料替代物。近年来,代谢工程及合成生物学被应用于生物能源的生产,通过构建重组微生物发酵来生产丁醇、1-丙醇、异丁醇、2-甲基-1-丁醇、3-甲基-1-丁醇等高级醇在大肠杆菌中得以成功实现(Atsumi et al., 2008a; 2008b; 2008c; Shen et al., 2008; Cann et al., 2008; Connor et al., 2008)。与其他高级醇相比,异丁醇拥有更高的辛烷值,还能用于除燃料工业以外的其他行业;且生物异丁醇的生产工艺与生物乙醇的生产工艺极为相似,现有的燃料乙醇生产设备只需稍加改造便可转而生产生物异丁醇。因此,异丁醇被认为是一种极具发展潜力的生物燃料替代物(Atsumi et al., 2008a;2008b; 2008c; Dellomonaco et al., 2010),通过生物技术途径生产异丁醇,符合绿色、可持续能源生产的要求(Fava et al., 2012)。Atsumi等(2008c)通过基因工程和代谢工程手段对大肠杆菌进行了改造,使其能够利用氨基酸的生物合成途径合成长链醇类如异丁醇(图 1)。近来,通过该途径生物合成异丁醇的其他宿主工程菌,如酿酒酵母(Saccharomyces cerevisiae)、枯草芽孢杆菌(Bacillus subtilis)、谷氨酸棒状芽胞杆菌(Corynebacterium glutamicum)、解纤维素梭菌(Clostridium celluldyticum)等也取得了较好的进展(Blombach et al., 2011; Smith et al., 2010; Li et al., 2011; Higashide et al., 2011; Chen et al., 2011)。但遗憾的是,大多数生产菌株需要在厌氧或是氧限制条件下通过其固有的氧化还原平衡代谢途径来生产相应代谢产物,故易导致这些工程菌的底物利用范围有限、原料利用率低和生产效率不高。本文以能代谢C6/C5糖的模式工业微生物大肠杆菌作为宿主菌种,通过构建产异丁醇大肠杆菌工程菌,实现氨基酸途径生物合成异丁醇关键酶基因adh2和kivd在大肠杆菌中的活性表达及杨木水解液发酵产异丁醇,以期为能利用木质纤维类生物质(水解液含C6,C5糖)发酵生产异丁醇提供一条新的途径。
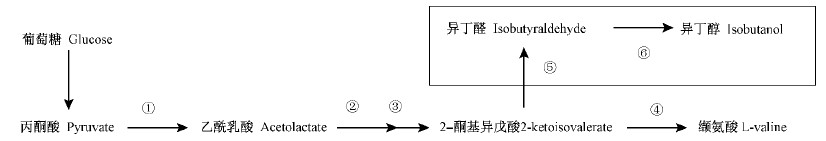 |
图 1 氨基酸途径生物合成异丁醇 Fig. 1 Amino acid pathway of isobutanol biosynthesis ①乙酰羟基酸合成酶Acetohydroxyacid synthase(AHAS); ②乙酰羟基酸异构还原酶Acetohydroxy isomeroreductase(AHAIR); ③二羟酸脱水酶Dihydroxyacid dehydratase(DHAD); ④脱氨基酶Transaminase B(TA);⑤酮酸脱羧酶2-ketoacid decarboxylase(KIVD); ⑥醇脱氢酶Alcohol dehydrogenase(ADH). |
1)质粒和菌株 酿酒酵母、大肠杆菌DH5α由中南林业科技大学国家林业局生物乙醇研究中心实验室提供; 乳酸乳球菌(Lactobacillus lactis)购于中国工业微生物菌种保藏管理中心(CICC); 亚克隆T载体pMD18-T载体、pSTV-29表达载体购于宝生物工程(大连)有限公司。
2)主要仪器和试剂 主要仪器有PCR仪(Bio-rad,美国)、小型垂直电泳槽(Bio-rad,美国)、气相色谱仪(日本岛津)、凝胶成像系统(SYNGENE)和核酸蛋白测定仪(Eppendorf)。主要试剂有DNA限制性内切酶(NEB)、DNA聚合酶(Taqplus)、T4连接酶等(Takara),DNA marker、蛋白marker、X-gal、寡核苷酸(dNTP)、DNA提取试剂盒、PCR产物纯化试剂盒、琼脂糖凝胶DNA回收试剂盒、质粒提取试剂盒等(天根生化科技有限公司),其他试剂均为分析纯。基因测序由南京金斯瑞生物科技有限公司完成。
3)培养基和培养条件 大肠杆菌培养和转化子筛选采用LB培养基,转化子筛选培养基添加氯霉素; 发酵培养基为添加10%杨木水解液(内含总还原糖为42 g·L-1)的LB培养基,同时以含42 g·L-1葡萄糖的LB培养基作为对照。培养条件为37 ℃、220 r·min-1。
1.2 目的基因片段的PCR扩增1)目的基因组DNA提取 用DNA提取试剂盒提取酿酒酵母和乳酸乳球菌的基因组DNA。
2)引物 根据NCBI中酿酒酵母 的adh2基因序列和乳酸乳球菌的kivd基因序列设计PCR引物(表 1),由南京金斯瑞生物科技有限公司合成。
|
|
3)PCR扩增 以酿酒酵母菌株总DNA和乳酸乳球菌菌株总DNA为模板,分别扩增异丁醇生物合成途径关键酶基因adh2和kivd。采用50 μL扩增体系,扩增条件: 94 ℃ 3 min; 94 ℃ 30 s,Tm 30 s,72 ℃1.5 min,30个循环; 72 ℃10 min。
1.3 重组质粒pSTV-29-adh2/pSTV-29-kivd/pSTV-29-adh2-kivd的构建胶回收纯化的adh2基因经双酶切后插入到Sma I/BamH I酶切位点上得表达质粒pSTV-29-adh2; kivd基因插入到pSTV-29的Sma I酶切位点上得表达质粒pSTV-29-kivd; 最后将酶切后的kivd基因插入pSTV-29-adh2质粒中,构建一个包含异丁醇合成途径关键酶基因的重组质粒pSTV-29-adh2-kivd (图 2)。酶切采用37 ℃水浴酶切5 h,16 ℃过夜。将连接产物转化至大肠杆菌DH5α感受态细胞中,菌落经双酶切鉴定后挑取阳性重组子送样测序。
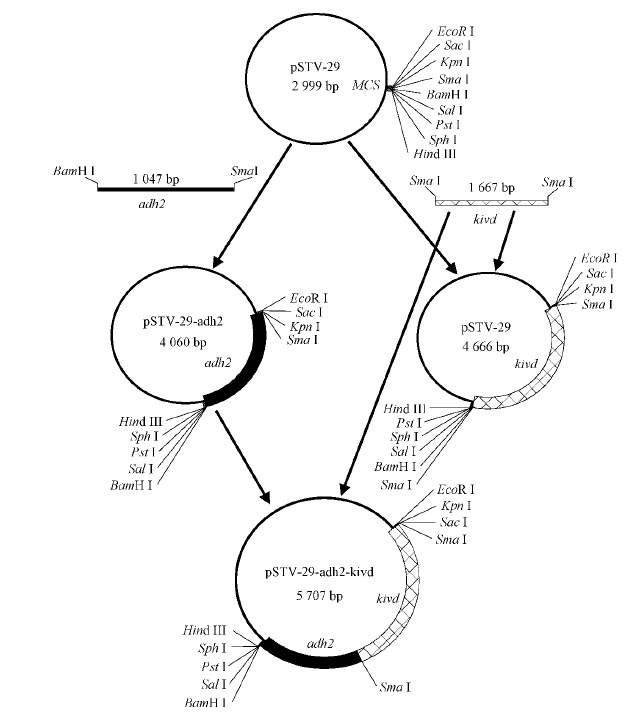 |
图 2 重组质粒pSTV-29-adh2/pSTV-29-kivd/pSTV-29-adh2-kivd构建过程 Fig. 2 The establishment process of recombinant plasmid pSTV-29-adh2/pSTV-29-kivd/pSTV-29-adh2-kivd |
重组菌E.coli DH5α在氯霉素终浓度为34 μg·mL-1的LB液体培养基中37 ℃、220 r·min-1摇床培养OD600到0.4~0.6,添加IPTG使其终浓度为1 mmol·L-1,诱导表达12 h,以带有空质粒pSTV-29的E.coli DH5α作为空白对照。收集菌体提取蛋白,采用5%浓缩胶和10%分离胶的SDS-PAGE分析蛋白表达量;同时使用 BCA 蛋白定量试剂盒测定蛋白含量,重复测定3次,结果取平均值。
1.5 重组菌E.coli DH5α发酵生产异丁醇以重组菌E.coli DH5α作为发酵菌株,添加10%杨木水解液的LB培养基、添加42 g·L-1葡萄糖的LB培养基和未添加任何碳源的LB培养基为发酵培养基,进行摇瓶发酵试验。种子培养基以1∶50的比例接种到250 mL的锥形瓶中,220 r·min-1、37 ℃培养至OD600为0.4~0.6时,加入IPTG至终浓度为1 mmol·L-1,继续培养24 h,采用气相色谱法测定异丁醇的产量。
1.6 目的产物检测方法采用气相色谱测定发酵液中异丁醇的含量。气相色谱条件为色谱柱: 安捷伦HP-INNOWAX,30 m×0.25 mm; 检测器: FID,N2为载气,流速为35 mL·min-1,H2流速为35 mL·min-1,空气流速为350 mL·min-1; 初始柱温45 ℃,保留1 min,然后以5 ℃·min-1升至150 ℃,保留2 min; 进样口温度为180 ℃,检测器温度为200 ℃,进样量为1 μL,分流比为1∶60,外标法定量测定。
2 结果与分析 2.1 重组质粒pSTV-29-adh2/pSTV-29-kivd/pSTV-29-adh2-kivd的构建转化成功的阳性重组子pSTV-29-adh2,pSTV-29-kivd和pSTV-29-adh2-kivd经菌液PCR和酶切双重验证后,送往南京金斯瑞生物科技有限公司测序,其结果表明adh2和kivd基因序列与NCBI中相应基因序列完全一致,可见克隆的基因片段为正确的目的基因片段。阳性重组子pSTV-29-adh2,pSTV-29-kivd和pSTV-29-adh2-kivd菌液PCR和酶切结果如图 3和图 4所示。可以看出,各片段大小与目的基因大小(adh2基因1 067 bp、kivd基因1 667 bp)和质粒载体大小(2 999 bp)相符,表明表达载体pSTV-29-adh2,pSTV-29-kivd和pSTV-29-adh2-kivd构建成功。
 |
图 3 重组质粒pSTV-29-adh2/pSTV-29-kivd/pSTV-29-adh2-kivd菌液PCR检测 Fig. 3 Electropherogram of recombinant plasmid pSTV-29-adh2/pSTV-29-kivd/pSTV-29-adh2-kivd in bacterial liquid culture M:500 bp DNA maker; A(1-8):pSTV-29-adh2; B(1-8):pSTV-29-kivd; C(1-14):pSTV-29-adh2-kivd(1和8、2和9、…、6和13、7和14分别指同一重组质粒 1 and 8,2 and 9,…,6 and 13,7 and 14 for the same recombinant plasmid,respectively). |
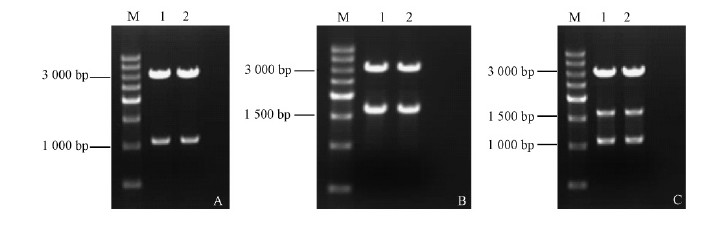 |
图 4 重组质粒pSTV-29-adh2/pSTV-29-kivd/pSTV-29-adh2-kivd酶切检测 Fig. 4 Electropherogram of the recombinant plasmid pSTV-29-adh2/pSTV-29-kivd/pSTV-29-adh2-kivd by restriction digestion M:500bp DNA maker; A(1-2):pSTV-29-adh2; B(1-2):pSTV-29-kivd; C(1-2):pSTV-29-adh2-kivd. |
重组菌E.coli DH5α采用1 mmol·L-1的IPTG 37 ℃诱导12 h后提取粗酶液,经测定,E.coli-adh2,E.coli-kivd,E.coli-adh2-kivd菌株粗酶液中蛋白含量分别是(627±23),(518±16)和(713±19)mg·L-1。经SDS-PAGE电泳后结果如图 5所示。从图 5可以看出,2号泳在40 kD处出现明显的蛋白特征带,与adh2基因编码的乙醇脱氢酶蛋白分子质量大小相符; 3号泳道在70 kD处出现明显的蛋白特征条带,与kivd基因编码的2-酮酸脱羧酶蛋白分子质量大小相符; 4号泳道在40 kD和70 kD 2处出现明显的蛋白特征条带,而1号泳道(空白对照菌株)未出现任何蛋白特征条带。这表明已构建的pSTV-29-adh2-kivd表达载体在大肠埃希菌DH5α中同时表达了adh2和kivd基因的编码蛋白,即成功地构建了含有表达载体pSTV-29-adh2-kivd的重组菌株。
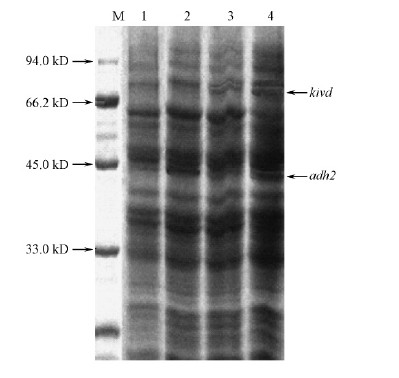 |
图 5 重组菌的SDS-PAGE分析 Fig. 5 SDS-PAGE analysis of the recombinant strains M:Maker;1: pSTV-29-adh2空载体 Blank carrier pSTV-29;2: pSTV-29-adh2蛋白表达pSTV-29-adh2 protein expression;3:pSTV-29-kivd蛋白表达pSTV-29-kivd protein expression; 4:pSTV-29-adh2-kivd蛋白表达pSTV-29-adh2-kivd protein expression. |
本试验以添加10%杨木水解液(内含总还原糖含量约42 g·L-1)的LB培养基为发酵培养基,连续培养24 h,气相色谱检测发酵液中异丁醇含量。结果如图 6所示,其中第2个峰(面积为7 074)为异丁醇。通过气相检测发现,只有串联了adh2基因和kivd基因的重组菌株E.coli DH5α-pSTV-29-adh2-kivd才能够合成异丁醇,而只导入pSTV-29-adh2的E.coli DH5α由于缺乏2-酮基脱羧酶的作用,发酵液中没有异丁醇,同样只导入pSTV-29-kivd的E.coli DH5α由于缺乏醇脱羧酶的作用无法将异丁醛转化成异丁醇。这说明只有乙醇脱羧酶和2-酮基脱羧酶在重组菌体内同时表达时才能合成异丁醇,最高产量为0.14 g·L-1。同时以添加42 g·L-1葡萄糖的LB培养基和未添加任何碳源的LB培养基为对照,经检测,含42 g·L-1葡萄糖的LB培养基发酵得到异丁醇的产量为4.1 g·L-1,未添加任何碳源的LB培养基中未检测出异丁醇。
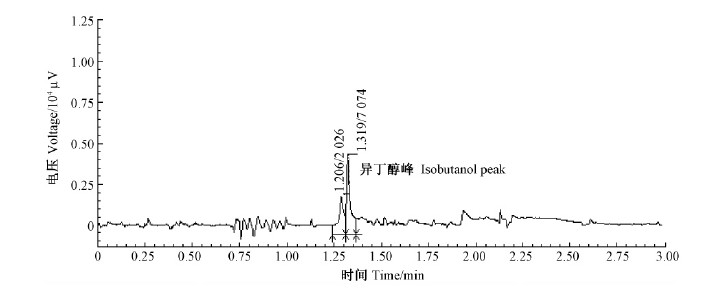 |
图 6 重组菌pSTV-29-adh2-kivd发酵产物的气相色谱分析 Fig. 6 Gas chromatography profiles analysis of fermentation product for recombinant strain pSTV-29-adh2-kivd |
本试验通过基因工程手段对大肠杆菌中缬氨酸途径进行改造,以酿酒酵母总DNA和以乳酸乳球菌总DNA为模板,成功构建了异丁醇合成途径关键酶基因的重组表达载体pSTV-29-adh2-kivd,并对重组菌E.coli DH5α pSTV-29-adh2-kivd进行了IPTG诱导和蛋白表达。同时以该重组菌为发酵菌种,以杨木水解液为原料进行摇瓶发酵得异丁醇,产量约为0.14 g·L-1,成功构建出了能产异丁醇的大肠杆菌工程菌,但异丁醇产量有待进一步提高。
Atsumi等(2008c)在大肠杆菌中对来自酿酒酵母的aro10,pdc6,thi3,乳酸乳球菌的kivd和丙酮丁醇梭菌的pdc等脱羧酶编码基因进行了比较,结果表明aro10和kivd具有最广泛的底物,且在异丁醇的生物合成过程中,kivd编码的脱羧酶活性最高,对缬氨酸代谢过程中的2-酮基异戊酸脱羧酶的专一性很强,故本试验选取kivd基因作为目的基因之一进行研究。但从SDS-PAGE电泳结果可以看出,kivd基因的表达量不高,这可能是导致异丁醇产量低的一个重要因素,说明编码2-酮酸脱羧酶基因(kivd)可能是生物合成异丁醇途径中的一个关键酶基因,这与潘超强等(2012)研究结果相似。因为2-酮酸脱羧酶催化缬氨酸途径中2-酮基异戊酸生成异丁醛,改变了缬氨酸原有的代谢途径,kivd基因新的异丁醇合成途径中引入的第一个酶基因,其表达量及催化活性直接影响了异丁醛的合成量,而异丁醛是异丁醇的合成底物,因此可以认为kivd基因是异丁醇新合成途径中的关键酶之一。如果能够大幅度提高现有kivd基因的表达或采用高酶活菌株的kivd基因构建表达质粒,并结合性能优良的大肠杆菌宿主与优化培养条件等措施,应该可以大幅度提高异丁醇产量。
郭媛(2010)将酿酒酵母菌株中的2-酮酸脱酸酶基因(aro10)及乙醇脱氢酶基因(adh2)导入工程菌,同时敲除了pflB,frdAB和fnr 3个旁路基因以阻断乙醇和丙酮的生物合成,成功地构建了可以利用蔗渣生产异丁醇的工程菌菌株。Savrasova等(2011)成功将乙酰羟酸合成酶、乙酰羟酸同分异构体还原酶(ilvC)、二羟酸脱羧酶(ilvD)、2-酮基异戊酸脱羧酶(kivd)和乙醇脱氢酶(adh2)等基因引入大肠杆菌,构建了工程菌,结果表明该工程菌可以利用葡萄糖产生异丁醇,在有氧条件下异丁醇产量达到1.5%。林丽华等(2011a;2011b)将2-酮基酸脱羧酶基因(kdcA)克隆到大肠杆菌缺失型突变株BW25113中,构建表达载体pSTV-29-alsS-ilvC-ilvD-kdcA,同时过量表达alsS,ilvC,ilvD基因,增加前体丙酮酸的量,经葡萄糖发酵24 h后,产率达到3 g·L-1。该研究组进一步将大肠杆菌缺失型突变株BW25113中的pflB,frdAB,fnr和AdhE 4个基因敲除,工程菌异丁醇产量达到4.2 g·L-1,提高了40%(郭媛等,2012)。潘超强等(2012)通过改造仅将2-酮基异酸脱羧酶基因(kivd)和醇脱氢酶基因(adhA)串联克隆到大肠杆菌中,利用葡萄糖发酵24 h后异丁醇的产量达到0.12 g·L-1。通过缬氨酸生物合成途径转化异丁醇过程中另一个关键基因是醛醇脱氢酶基因,编码醇脱氢酶,使异丁醛转化为异丁醇,因此,本试验同时选择了醇脱氢酶基因adh2作为研究对象,构建了基因工程菌E.coli DH5α-pSTV-29-adh2-kivd,并利用其以杨木水解液为底物进行发酵试验。结果显示,该工程菌可以利用木质纤维水解液中的糖类物质通过非发酵途径产生异丁醇,同时以与杨木水解液中总还原糖含量相等量的葡萄糖为碳源进行对照试验,该试验中异丁醇的产量提高了近3倍,工程菌试验比对照实验的异丁醇产量低,很有可能是因为工程菌并不能完全利用水解液中的各种还原糖。水解液中的还原糖主要有葡萄糖、木糖和阿拉伯糖,对照试验已证实,工程菌可以利用葡萄糖发酵转化异丁醇,因此,极有可能是工程菌并不能很好地利用木糖和阿拉伯糖。下一步应对水解液发酵前后各还原糖的含量及利用情况进行定量测定,以明确具体原因。
在后续的工作中,笔者将对现有基因工程菌进行发酵过程优化,筛选出发酵的最优温度、时间、pH、底物最佳浓度等,提高异丁醇的产量,使其能高效利用木质纤维类生物质原料发酵产异丁醇,降低生产成本,提高生产效益; 通过基因工程与代谢工程,利用合成生物学的理念,构建能利用木质纤维水解液中不同碳源合成异丁醇新途径,提高关键基因的表达量,同时抑制副产物相关基因的表达,提高丙酮酸含量,增加2-酮异戊醇的生物合成量,使碳源更多流向异丁醇代谢途径(Atsumi et al.,2010)。进一步构建NADH再生途径,以及添加提供NADH的辅助碳源来缓解NADH供应不足的限制,实现异丁醇产量的提高。
| [1] |
郭媛. 2010. 通过非发酵途径改造构建利用蔗渣产异丁醇宿主菌株的研究. 南宁:广西大学硕士学位论文. (Guo Y. 2010.Research on construction of a host strain used in bagasse butanol production by engineering non-fermentative pathway. Nanning: MS thesis of Guangxi University.[in Chinese])(  1) 1)
|
| [2] |
郭媛,林丽华,黄日波,等. 2012. 基因敲除提高大肠杆菌工程菌生产异丁醇产量的研究. 生物技术通报,(7):170-175. (Guo Y, Lin L H, Huang R B, et al. 2012. Influence of isobutanol production in gene defective mutant of Escherichia coli. Biotechnology Bulletin, (7):170-175[in Chinese]).(  1) 1)
|
| [3] |
林丽华,郭 媛,庞 浩,等. 2011a. 大肠杆菌中表达关键基因产异丁醇的研究. 生物技术,21(3):19-23. (Lin L H, Guo Y, Pang H,et al. 2011a. Research of isobutanol production in Escherichia coli expressing of the key genes. Biotechnology, 21(3):19-23[in Chinese]).(  1) 1)
|
| [4] |
林丽华,郭 媛,庞 浩,等. 2011b. 产异丁醇大肠杆菌工程菌的构建. 生物技术通报,8( 3):208-212. (Lin L H, Guo Y, Pang H,et al. 2011b. The construction of recombinant E.coli producing isobutanol Biotechnology Bulletin, 8( 3):208-212[in Chinese]).(  1) 1)
|
| [5] |
潘超强,高 强,郑春阳,等. 2012. 产异丁醇关键基因在大肠杆菌中表达的研究. 微生物学通报,39(7): 912-920. (Pan C Q, Gao Q, Zhen C Y,et al. 2012. Coexpression of two essential isobutanol synthesis genes in Escherichia coli. Microbiology China.39(7): 912-920[in Chinese]).(  2) 2)
|
| [6] |
Atsumi S,Liao J C. 2008a. Directed evolution of Methanococcus jannaschii citramalate synthase for biosynthesis of 1-propanol and 1-butanol by Escherichia coli. Appl Environ Microbiol,74(24): 7802-7808.( 2) 2)
|
| [7] |
Atsumi S,Cann A F,Connor M R, et al. 2008b. Metabolic engineering of Escherichia coli for 1-butanol production. Metab Eng,10(6): 305-311.( 2) 2)
|
| [8] |
Atsumi S,Hanai T,Liao J C. 2008c. Non-fermentative pathways for synthesis of branched-chain higher alcohols as biofuels. Nature,451(7174): 86-89.( 4) 4)
|
| [9] |
Atsumi S,Wu T Y,Eckl E M,et al. 2010. Engineering the isobutanol biosynthetic pathway in Escherichia coli by comparison of three aldehyde reductase/alcohol dehydrogenase genes. Appl Microbiol Biotechnol,85(3): 651-657.( 1) 1)
|
| [10] |
Blombach B,Riester T,Wieschalka S,et al. 2011. Corynebacterium glutamicum tailored for efficient isobutanol production. Appl Environ Microbiol,77(10): 3300-3310.( 1) 1)
|
| [11] |
Cann A F,Liao J C. 2008. Production of 2-methyl-1-butanol in engineered Escherichia coli. Appl Microbiol Biotechnol,81(1): 89-98.( 1) 1)
|
| [12] |
Connor M R,Liao J C. 2008. Engineering of an Escherichia coli strain for the production of 3-methyl-1-butanol. Appl Environ Microbiol,74(18): 5769-5775.( 1) 1)
|
| [13] |
Chen X,Nielsen K F,Borodina I,et al. 2011. Increased isobutanol production in Saccharomyces cerevisiae by overexpression of genes in valine metabolism. Biotechnol Biofuels,4(21): 21.( 1) 1)
|
| [14] |
Dellomonaco C,Fava F,Gonzalez R. 2010. The path to next generation biofuels: successes and challenges in the era of synthetic biology. Microb Cell Fact,9(3): 3.( 1) 1)
|
| [15] |
Fava F,Ohtake H,Pesaresi P. 2012. Biotechnology for a more sustainable environment decontamination and energy production. J Biotechnol,157(4): 443-445.( 1) 1)
|
| [16] |
Ho N W,Chen Z,Brainard A P. 1998. Genetically engineered Saccharomyces yeast capable of effective cofermentation of glucose and xylose. Appl Environ Microbiol,64(5): 1852-1859.( 1) 1)
|
| [17] |
Higashide W,Li Y,Yang Y,et al. 2011. Metabolic engineering of Clostridium cellulolyticum for production of isobutanol from cellulose. Appl Environ Microbiol,77(8): 2727-2733.( 1) 1)
|
| [18] |
Li S,Wen J,Jia X. 2011. Engineering Bacillus subtilis for isobutanol production by heterologous Ehrlich pathway construction and the biosynthetic 2-ketoisovalerate precursor pathway overexpression. Appl Microbiol Biotechnol,91(3): 577-589.( 1) 1)
|
| [19] |
Ohta K,Beall D S,Mejia J P, et al. 1991. Genetic improvement of Escherichia coli for ethanol production: chromosomal integration of Zymomonas mobilis genes encoding pyruvate decarboxylase and alcohol dehydrogenase II. Appl Environ Microbiol,57(4): 893-900.( 1) 1)
|
| [20] |
Shen C R,Liao J C. 2008. Metabolic engineering of Escherichia coli for 1-butanol and 1-propanol production via the keto-acid pathways. Metab Eng,10(6): 312-320.( 1) 1)
|
| [21] |
Smith K M,Cho K M,Liao J C. 2010. Engineering Corynebacterium glutamicum for isobutanol production. Appl Microbiol Biotechnol,87(3): 1045-1055.( 1) 1)
|
| [22] |
Savrasova E A,Kivero A D,Shakulov R S,et al. 2011. Use of the valine biosynthetic pathway to convert glucose into isobutanol. J Ind Microbiol Biotechnol,38(9): 1287-1294.( 1) 1)
|
| [23] |
Zhang M,Eddy C,Deanda K,et al. 1995. Metabolic engineering of a pentose metabolism pathway in ethanologenic Zymomonas mobilis.Science, 267(5195): 240-243.( 1) 1)
|
 2015, Vol. 51
2015, Vol. 51

