文章信息
- 黄秋娴, 赵顺, 刘春梅, 李玉灵
- Huang Qiuxian, Zhao Shun, Liu Chunmei, Li Yuling
- 遮荫处理对铁尾矿基质臭柏实生苗快速叶绿素荧光特性的影响
- Effects of Shading Treatments on Chlorophyll Fluorescence Characteristics of Sabina vulgaris Seedlings Grown in Iron Tailings Media
- 林业科学, 2015, 51(6): 17-26
- Scientia Silvae Sinicae, 2015, 51(6): 17-26.
- DOI: 10.11707/j.1001-7488.20150603
-
文章历史
- 收稿日期:2014-08-03
- 修回日期:2015-01-12
-
作者相关文章
2. 广州草木蕃环境科技有限公司 广州 510000
2. Guangzhou Environment Technology Co. Ltd. Guangzhou 510000
光是植物光合作用所必需的条件,当植物吸收的光能超出光合机构所能利用的范围时,便会导致光抑制和光合机构的光破坏(Demming et al.,1992)。叶绿素荧光动力学技术可以检测光合机构在光抑制下的内在变化。Kautsky等(1931)最先认识到光合原初反应和叶绿素荧光存在着密切关系。 后来在生物膜能量流动基础上建立了针对叶绿素荧光诱导曲线的数据分析和处理方法——JIP-test,为深入研究光合作用原初反应提供了有力而便捷的工具。通过JIP-test获得的结果能正确反映样品光合作用光系统Ⅱ的实际生理状态(Clark et al.,2000; Krüger et al.,1997; Srivastava et al.,1997),因此JIP-test已被广泛应用到植物胁迫生理学的诸多研究中。
臭柏(Sabina vulgaris)又名叉子圆柏、沙地柏等,为柏科(Cupressaceae)圆柏属(Sabina)植物,常绿匍匐针叶灌木,是一种耐旱、耐寒,生命力极强、适合防风固沙的古老树种,是退化土地生态环境恢复与重建的关键树种之一。已有学者对其自然分布、生长发育、生理特性、种群结构、群落动态、防风固沙、栽培抚育、开发利用等方面进行了深入的研究(李春艳等,2000;温国胜,2005;张国盛等,2001; 1999)。但目前对臭柏的研究多集中于个体生理生态对土壤干旱胁迫的响应(李玉灵,2009a; 2009b;王林和等,1998; 温国胜等,2004a; 2004b),而研究种子萌发的实生苗的光胁迫过程与其叶绿素荧光特性的相关内容较少。自然条件下,臭柏幼苗主要分布在乌柳(Salix cheilophila)灌丛内,幼龄时处于遮荫状态,光强较弱,随其生长,臭柏逐渐摆脱乌柳的荫蔽环境直至完全暴露于强光下,形成灌木纯林(王哲等,2007)。在此过程中,臭柏经历了由遮荫到强光的光照条件变化,臭柏是否受到光抑制,如何适应不同的光照环境或者说不同遮荫环境会对臭柏幼苗叶片的原初光化学反应和光系统Ⅱ的影响,还少有报道。叶绿素荧光动力学技术可以反映光合机构在光抑制下的内在变化,本研究利用快速叶绿素荧光诱导动力学测定和JIP-test数据分析方法,旨在探讨不同遮荫处理下臭柏幼苗叶片原初光化学反应的差异,明确臭柏在不同光照条件下的光保护机制,为臭柏光胁迫的研究提供理论依据。
植被恢复是铁尾矿生态修复的根本途径,造林技术是铁尾矿植被恢复的关键技术之一。近些年来,唐山迁安马兰庄政府尝试在铁尾矿上直接栽植臭柏大苗,保存率为35%,但尚未进行植苗造林试验。为了提高铁尾矿臭柏幼苗直接造林的可行性,又鉴于铁尾矿与臭柏天然分布的毛乌素沙地基质相近,本文选择铁尾矿作为盆栽试验基质,在探讨不同遮荫处理下臭柏幼苗荧光特性的同时,也为铁尾矿废弃地臭柏植苗造林技术提供一定的依据。
1 材料与方法 1.1 试验设计于2012年4月在河北农业大学标本园进行盆栽试验。试验材料来源于毛乌素沙地,选取生长良好、均为2年生的臭柏幼苗25株,所用铁尾矿砂采集于河北省唐山市迁安马兰庄镇。栽植盆大小为180 mm×190 mm,将25株盆栽臭柏幼苗置于自然条件下生长1个月后,再将其放在0(自然光),25%,50%,75%和90%5组不同的遮荫条件下培养,遮荫处理2个月后,进行快速叶绿素荧光特性的测定,栽植后保持一致的管理,灌水量以浇透为止。整个试验期间保证土壤水分充分供应。
1.2 测定方法采用连续激发式荧光仪Pocket-PEA(Hansatech,UK)对叶片快速叶绿素荧光诱导动力学曲线(O-J-I-P荧光诱导曲线)(Srivastava et al.,1997)进行测定,每个遮荫处理选取长势基本一致、生长健康的4株盆栽苗,以上部当年叶片作为供试叶片,测定前先将叶片暗适应15 min,每天测定时间为8:00—17:00,其间每隔2 h 测定1次。
1.3 JIP-test分析根据光系统Ⅱ能量流模型(Strasser et al.,1995a),天线色素吸收的能量有一部分被反应中心捕获用于光化学反应,驱动电子传递,其余的以叶绿素荧光和热能的形式散失。经过暗适应过程,一般的绿色植物叶绿素荧光(快相),显示明显的O-J-I-P期,获得的O-J-I-P荧光诱导曲线用于JIP-test分析(Srivastava et al.,1997)。分析时需知Fo(20 μs时荧光,O相)、Fk(300 μs时荧光,K相)、FJ(2 ms时荧光,J相)、Fm(最大荧光,P相)、RC(反应中心)、ABS(天线色素吸收的能量)、VJ(J点的相对可变荧光)、Mo(O-J-I-P荧光诱导曲线的初始斜率)和CS(单位面积)。
1)PSⅡ最大量子效率φPo=Fv/Fm=(Fm -Fo)/Fm;
2)以吸收光能为基础的性能指数 PIABS=(RC/ABS)×[φPo/(1-φPo)] ×[Ψo/(1 - Ψo)];
3)可变荧光 Fv占Fj -Fo振幅的比例Wk =(Fk-Fo)/(FJ-Fo);
4)捕获的激子将电子传递到电子传递链中QA-下游的其他电子受体的概率Ψo=1-Vj;
5)用于电子传递的量子产额φEo=[1-(Fo/Fm)] ×Ψo;
6)单位面积有活性的反应中心的密度RC/CS=φPo×(Vj/Mo)×(ABS/CS);
7)单位反应中心吸收(ABS/RC)、捕获(TRo/RC)、用于电子传递(ETo/RC)及热耗散掉的能量(DIo/RC)的计算为:
| $\begin{array}{l} ABS/RC = {M_o} \times \left( {1/{V_J}} \right) \times \left( {1/{\varphi _{Po}}} \right),\\ TR/RC = {M_o} \times \left( {1/{V_J}} \right),\\ E{T_o}/RC = {M_o} \times \left( {1/{V_J}} \right) \times {\Psi _o},\\ D{I_o}/RC = \left( {ABS/RC} \right) - \left( {T{R_o}/RC} \right); \end{array}$ |
8)单位面积吸收(ABS/CS)、捕获(TRo/CS)、用于电子传递(ETo/CS)和热耗散(DIo/CS)的光能计算:
| $\begin{array}{l} ABS/CS \approx {F_O},\\ T{R_o}/CS = {\varphi _{po}} \times \left( {ABS/CS} \right),\\ E{T_o}/CS = {\Psi _o} \times \left( {T{R_o}/CS} \right),\\ D{I_o}/CS = \left( {ABS/CS} \right) - \left( {T{R_o}/CS} \right); \end{array}$ |
式中VJ=(FJ-Fo)/(Fm-Fo),Mo=4×(FJ-Fo)/(Fm-Fo)。
用Excel 2003和SPSS 13.0软件进行数据统计分析。
2 结果与分析 2.1 遮荫处理对初始荧光(Fo)和最大荧光(Fm)的影响初始荧光Fo是PSⅡ反应中心全部开放时的荧光,它与PSⅡ天线色素内的最初激子密度、天线色素到PSⅡ反应中心的激发能传递速率的结构状态及叶绿素含量有关,而与光合作用光化学反应无关(白志英等,2011;Pandey et al.,2005)。由图 1A可知,随着遮荫率增加,初始荧光(Fo)呈减小趋势,除90%遮荫外,其他处理组初始荧光(Fo)变化波动较大。且全光照条件下与90%遮荫处理达到极显著差异水平(P<0.01),而与其他处理差异不显著(表 1)。全光照条件下Fo的增加可能是植物叶片PSⅡ反应中心出现可逆性失活或出现不易逆转的破坏,也可能是植物叶片类囊体膜受到损害,而且Fo增加量越多,类囊体膜受损程度就越严重。
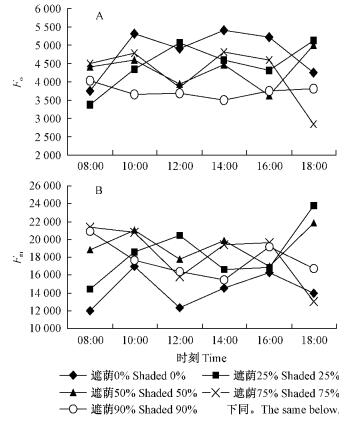 |
图 1 不同遮荫处理下臭柏叶片初始荧光(Fo)(A)和最大荧光(Fm)(B) Fig. 1 Minimal recorded fluorescence intenstity(Fo)(A) and maximal recorded fluorescence intenstity(Fm)(B)of S. vulgaris under different shading treatments |
最大荧光(Fm)是PSⅡ反应中心完全关闭时的荧光产量,是光合作用理论最大值。由图 1B可知,随着遮荫率增加,最大荧光(Fm)呈上升趋势,所有处理最大荧光(Fm)波动均较大,全光照条件下与50%遮荫组差异极显著(P<0.01),其他遮荫组之间无显著差异(表 1)。全光照条件下臭柏叶片Fm最小,有可能是强光胁迫对臭柏PSⅡ反应中心构成破坏。强光下Fm降低是光抑制的特征之一。
|
|
从图 2和表 2中可知,不同遮荫处理臭柏叶片对光能的吸收、转化、电子传递比率和热耗散的能量比率有不同影响。φPo反映了暗反应后的最大光化学效率,也表示PSⅡ最大量子效率,是指开放的PSⅡ反应中心捕获激发能的效率,与采用调制脉冲式荧光仪测定参数Fv/Fm相一致。图 2A表明,全光照条件下的φPo比其他所有遮荫处理都要小,且在中午12:00显著下降,达到全天最小值; 25%遮荫处理在14:00出现最小值,而其他遮荫处理φPo日变化都比较平稳,全光照条件下φPo日均值与其他遮荫处理差异极显著(P<0.01)(表 2)。
 |
图 2 不同遮荫处理下量子产额和能量分配比率 Fig. 2 The quantum yield and the energy distribution ratio of S. vulgaris under different shading treatments |
PIABS性能指数包含了RC/ABS,φPo,Ψo等3个独立的参数,可以更为准确地反映植物光合机构的状态。PIABS随着遮荫率的增加,变化幅度相对于φPo更大(图 2B)。全光照条件下PIABS依然最小,在14:00出现最小值,但其他遮荫处理之间PIABS差异也很大,50%遮荫组PIABS几乎是最大的,大致呈下降趋势,在14:00出现谷值,90%遮荫组日变化波动最剧烈,且在16:00达到最大峰值,25%与75%遮荫组日变化趋势相近,全光照条件PIABS日均值与25%遮荫组差异显著(P<0.05),与其他遮荫处理差异极显著(P<0.01),50%遮荫组与25%,75%遮荫组差异显著(P<0.05)(表 2)。
|
|
φDo用于热耗散的量子比率,全光照条件下最大,且在12:00受到光抑制时出现最大值,其他处理变化趋势相对平稳,在14:00略有升高(图 2C)。全光照条件下φDo日均值与其他遮荫处理差异极显著(P<0.01),25%与90%遮荫组差异显著(P<0.05),其他遮荫处理之间无显著差异(表 2)。
Ψo反映了在反应中心捕获的激子中,用来推动电子传递到电子传递链中QA下游的其他电子受体的激子占用来推动QA还原激子的比率,全光照条件下臭柏幼苗叶片光合机构在12:00受到光抑制(图 2D),肯定会阻碍电子传递到QA下游,电子传递能力降低,Ψo下降,且全光照条件下Ψo日均值与其他遮荫处理差异极显著(P<0.01),其他遮荫处理之间无显著差异(表 2)。
φEo用于电子传递的量子产额,反映了反应中心捕获的光能将电子传递到电子传递链中超过QA的其他电子受体的概率,随着遮荫率的增加,φEo呈上升趋势,全光照条件下φEo最小,且在12:00处亦出现最小值(图 2E),全光照条件下φEo日均值与其他处理组差异极显著(P<0.01),其他处理之间无差异(表 2)。
2.3 遮荫处理对比活性参数的影响随着遮荫率的增加,单位面积反应中心数量(RC/CSm)呈上升趋势(图 3A),全光照条件下RC/CSm最少,且与其他遮荫处理都呈极显著差异(P<0.01),而遮荫处理之间无显著差异。TRo/CSm(图 3B)和ETo/CSm(图 3C)反映单位面积捕获的光能和单位面积传递的光能,随遮荫率增加,都呈上升趋势,同样是全光照条件与遮荫处理组均呈极显著差异(P<0.01),遮荫处理之间无显著差异。而单位面积热耗散的光能(DIo/CSm)(图 3D)随遮荫率增加而呈下降趋势,全光照条件下DIo/CSm最大,与90%处理组呈极显著差异(P<0.01),其他遮荫处理之间无显著差异(表 3)。
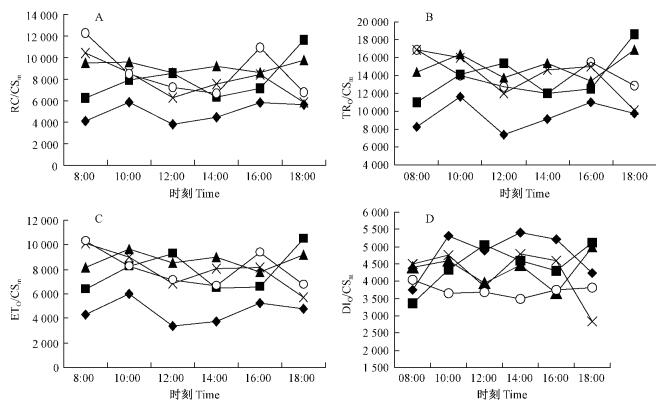 |
图 3 不同遮荫处理下对比活性参数 Fig. 3 Specific activity parameter of S. vulgaris under different shading treatment |
|
|
当PSⅡ的供体侧受到伤害时,经过极短的时间(在J点之前),叶绿素荧光强度就会上升,出现K点。WK为K相对可变荧光占FJ-FO振幅的比例,如图 4所示,全光照条件下,WK最大,变化较平缓。J相对可变荧光(VJ)表示PSⅡ初级受体QA被还原的程度,即QA-积累的程度(Strasser et al.,1995)。全光照条件下,VJ呈先上升后下降趋势,在12:00出现最大值,说明此时QA-出现很大积累,而8:00和18:00的VJ值相差不大,所有遮荫处理变化也较平缓,全光照条件与所有遮荫处理都呈极显著差异(P<0.01),而遮荫处理间无显著差异。MO是相对荧光的初始斜率,用来表示QA被还原的相对速率,从图中可知,MO和VJ的变化趋势是一致的。全光照条件下,QA被还原的相对速率比其他处理组都要快,QA-的积累也比较多,且全光照条件MO日均值与遮荫组之间均呈极显著差异(P<0.01),而遮荫处理间无显著差异(表 4)。
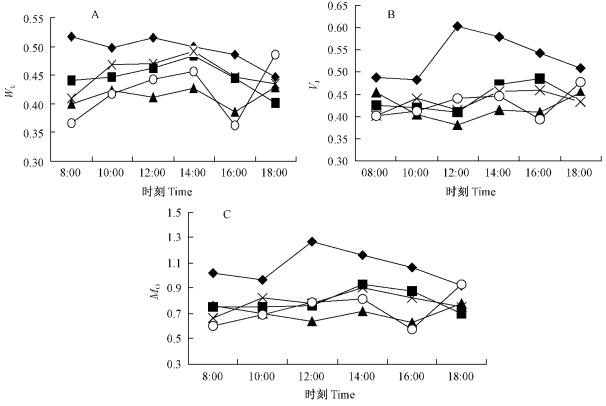 |
图 4 不同遮荫处理对PSⅡ供体侧和受体侧的影响 Fig. 4 Influence of donor side of PSⅡ and acceptor side of PSⅡ of S. vulgaris under different shading treatments |
|
|
快速叶绿素荧光诱导动力学曲线又称O-J-I-P曲线,是经Vt=(Ft-Fo)/(Fm-Fo)标准化之后的曲线,图 5为中午12:00时遮荫处理对臭柏O-J-I-P曲线的影响,12:00时全光照条件下O-J-I-P曲线与其他遮荫处理的曲线没有重合,在K点和J点处明显分开,且要高于其他遮荫处理,全光照条件下臭柏在K点和J点的相对可变荧光(Wk和VJ)均分别与其他遮荫处理差异达到显著(P<0.051)和极显著(P<0.01)水平(表 4)。臭柏在没有遮荫条件下O-J-I-P曲线变形为O-K-J-I-P曲线,即在曲线中在300 μs左右出现拐点K。
 |
图 5 遮荫处理对臭柏快速叶绿素荧光诱导动力学曲线的影响 Fig. 5 Effects of the fast induction curves of chlorophyll a fluorescence of S. vulgaris under different shading treatments |
PSⅡ对逆境胁迫非常敏感,因此,植物叶片的PSⅡ的光化学反应特性是衡量逆境胁迫对光合器官的有效指标(桂仁意等,2010; 贾永霞等,2011)。从表观指标Fo和Fm来看,不同遮荫处理下,Fo随遮荫率增加呈减小趋势,全光照条件下Fo的增加可能是植物叶片PSⅡ反应中心出现可逆性失活或出现不易逆转的破坏,也可能是植物叶片类囊体膜受到损害,而且Fo增加量越多,类囊体膜受损程度就越严重。而Fm随遮荫率增加呈上升趋势,全光照条件下臭柏Fm最小,有可能是强光胁迫对臭柏PSⅡ反应中心构成破坏。φPo表示PSⅡ有效光化学量子产量,反映开放的PSⅡ反应中心原初光能捕获效率(张守仁,1999),通常反映植物受抑制的程度。全光照条件下φPo最小,且在中午12:00出现最低值。而且只有PIABS在遮荫处理间统计检验差异显著,因此本研究同时也证实光合性能指数PIABS比φPo更敏感,能更好地反映胁迫对光合机构的影响(Appenroth et al.,2001; van Heerden et al.,2003)。
所以,全光照条件下Fo的增加和Fm的减小以及φPo的减小,说明植物受到光胁迫。而有研究表明,Fm大小与QA的氧化还原状态有关,也就是和反应中心的数量(RC/CSm)、反应中心捕获光能和传递光能指标(Tro/CSm,Eto/CSm)有关。RC/CSm,Tro/CSm、Eto/CSm随着遮荫率增加均呈上升的趋势。全光照条件下最小,说明强光胁迫使部分有活性的反应中心失活。在某些胁迫下,PSⅡ反应中心发生可逆失活,成为一个能量陷阱,能吸收光能但不能推动电子传递,一旦逆境解除,失活的反应中心又恢复活性(李鹏民等,2005)。叶绿素荧光快速诱导曲线拐点的变化反映了电子传递情况。研究表明,叶绿素荧光快速诱导曲线中K点的出现是放氧复合体(OEC)受伤害的标志,K点的相对可变荧光(Wk)代表放氧复合体被破坏的程度(Eggenberg et al.,1995; Strasser et al.,2004)。一般认为,K值的出现可以指示是放氧复合体完全被破坏与PSⅡ的电子门有关(Strasser,1997)。如图 4A和图 5所示,全光照条件WK比其他遮荫处理都要大,且与所有遮荫处理间有显著或极显著差异,全光照下快速叶绿素荧光诱导动力学曲线中K点与J点明显高于其他遮荫处理,说明在全光照条件下,臭柏的OEC受到了一定程度的伤害,即光合电子传递链中PSⅡ反应中心的供体侧受到了影响。J相相对可变荧光(VJ)反映PSⅡ反应中心受体侧QA被还原的情况,也表示在J点[QA-]/[总QA]的比例,VJ升高通常反映了QA-大量积累(Strasser et al.,1995b)。本研究中全光照条件下在12:00 VJ达到最大值,且与其他遮荫处理均有极显著差异(P<0.01),说明光抑制使VJ增加,造成大量QA-积累,阻碍了QA-往下的电子传递。PSⅡ供体侧和受体侧共同影响光合作用电子的传递能力(Krause et al.,1991)。Ψo主要反映了PSⅡ受体侧电子传递链的变化(李鹏民等,2005)。而PSⅡ反应中心供体侧受到伤害,受体侧的电子传递链受到抑制,才导致全光照条件下Ψo和φEo降低,这也同时导致φPo降低。
以上结果表明,全光照条件下,臭柏初始荧光(Fo)和最大荧光(Fm)减小,φPo降低,植物受到光抑制,而RC/CSm,Tro/CSm,Eto/CSm,PIABS,φPo的减小说明全光照条件下臭柏PSⅡ反应中心数量减少,反应中心捕获光能和传递光能能力下降,反应中心失活,叶绿素荧光快速诱导曲线表明全光照条件下电子传递受阻。所以,从叶绿素荧光、量子产额或能量分配比率、比活性参数、PSⅡ供体侧和受体侧各项指标和叶绿素荧光诱导曲线均表明全光照条件下臭柏受到了光抑制,且反应中心失活。
植物在光抑制条件下,光能捕获效率降低,必然会增加热耗散的比率,而臭柏在全光照条件下φDo极显著增加,且在中午12:00达到最大值,说明光抑制使全光照条件下臭柏叶片热耗散增加。研究表明,反应中心失活可能也是植物自身的一种保护机制(艾军勇等,2011)。有研究提出,高温可使部分反应中心降解或失活(Eggenberg et al.,1995)。Öquist等(1993)的试验证明,PSⅡ的光抑制程度与QA的还原程度密切相关,也就是说因为全光照条件下QA-积累阻碍电子传递链上电子向下传递,从而造成PSⅡ功能抑制,而PSⅡ的功能抑制会或使部分PSⅡ反应中心失活,转变为热耗散机构,耗散过剩光能。即使全光照条件下有活性的反应中心减少,但用于热耗散的比率还是最大的,随着光强增大,DIO/CSm增加。全光照条件下ABS/CSm的下降主要是光抑制使反应中心降解或失活,或是导致天线色素结构的改变并迫使天线色素降解,从而引起叶片捕获的光能下降,进而导致TRo/CSm和ETo/CSm减少。说明臭柏在遭受光抑制后,PSⅡ有活性的反应中心迅速作出反应,有活性反应中心的可逆性失活或降解失活,增加天线色素的热耗散、非辐射能量耗散等一系列机制来保护光合机构免受过量光能的危害。
其他遮荫处理组之间各项指标几乎没有显著差异。90%遮荫处理组与全光条件相比,其光合能力指标较大、热耗散指标较小,显现出较强的光捕捉特征,但其光合性能指数并非所有遮荫处理组中的最大值,说明由于光照不足,其光合作用也受到一定的影响。而50%遮荫处理Fm,PIABS的平均值最大,这说明该遮荫条件下臭柏叶片光抑制最小,光合能力最强,但其他指标与其他遮荫处理均未出现显著差异。只有全光照条件下,几乎所有指标均和其他遮荫处理组出现显著差异或极显著差异(表 1~4),臭柏幼苗若无遮荫措施,会受到光胁迫,所以臭柏选择在乌柳灌丛下度过其天然更新的最初阶段,而增加非辐射能量耗散途径达到光抑制防御的机制,又能使臭柏幼苗脱离乌柳灌丛的保护,完全暴露在全光照条件下,进而实现自身的不断生长、壮大。但就废弃地植苗造林来说,如果能采取一定的遮荫措施,将会提高造林成活率,本试验结果证实50%的遮荫率效果更佳。
| [1] |
艾军勇, 张道勇, 牟书勇,等. 2011.EDTA对波士顿蕨吸收Hg的影响及其光合响应. 应用与环境生物学报, 17(2): 219-222. (Ai J Y,Zhang D Y,Mu S Y,et al.2011. Effect of EDTA on accumulation and translocation of Hg in Nephrolepis exaltata and responses of Photosystem Ⅱ.Chinese Journal of Applied and Environmental, 17(2): 219-222[in Chinese]).(  1) 1)
|
| [2] |
白志英, 李存东, 赵金锋,等.2011.干旱胁迫对小麦代换系叶绿素荧光参数的影响及染色体效应初步分析. 中国农业科学, 44(1): 47-57. (Bai Z Y,Li C D,Zhao J F, et al.2011.Effect and preliminary analysis of chromosomal control on the chlorophyll fluorescence parameters of wheat substitution lines between synthetic hexaploid wheat and Chinese spring under drought stress. Scientia Agricultura Sinica, 44(1): 47-57[in Chinese]).(  1) 1)
|
| [3] |
桂仁意, 刘亚迪, 郭小勤,等.2010.不同剂量Cs-γ射对毛竹幼苗叶片叶绿素荧光参数的影响. 植物学报, 45(1): 66-72. (Gui R Y,Liu Y D,Guo X Q, et al.2010. Effects of dose of Cs-γ irradiation on chlorophyll fluorescence parameters for leaves of seedlings of Phyllostachys heterocycla 'Pubescens'. Chinese Bulletin of Botany, 45(1): 66-72[in Chinese]).(  1) 1)
|
| [4] |
贾永霞, 孙锦, 王丽萍,等.2011.低氧胁迫下黄瓜植物热耗散途径. 应用生态学报, 22(3): 707-712. (Jia Y X,Sun J,Wang L P, et al.2011. Thermal dissipation pathway in cucumber seedling leaves under hypoxia stress.Chinese Journal of Applied Ecology, 22(3): 707-712[in Chinese]).(  1) 1)
|
| [5] |
李春艳,王林和,慈忠玲. 2000.臭柏愈伤组织的诱导.内蒙古农业大学学报, 21(2): 58-62. (Li C Y,Wang L H,Ci Z L.2000. Induction of callus of Sabina vulgaris. Journal of Inner Mongola Institute of Agriculture and Animal Husbandry, 21(2): 58-62[in Chinese]).(  1) 1)
|
| [6] |
李鹏民,高辉远,Strasser R J. 2005.快速叶绿素荧光诱导动力学分析在光合作用研究中的应用. 植物生理与分子生物学学报, 31(6): 559-566. (Li P M,Gao H Y, Strasser R J.2005. Application of Chlorophyll a fluorescence transient in study of plant physiology under stress conditions. Journal of Plant Physiology and Molecular Biology, 31(6): 559-566[in Chinese]).(  2) 2)
|
| [7] |
李玉灵,朱帆,王俊刚,等. 2009a.水分胁迫下臭柏(Sabina vulgaris Ant.)光合特性和色素组成的季节变化.生态学报, 29(8): 4346-4352. (Li Y L,Zhu F, Wang J G, et al.2009a. Seasonal changes of photosynthetic characteristics and pigment composition of Sabina vulgaris Ant. under water stress. Acta Ecologica Sinica, 29(8): 4346-4352[in Chinese]).(  1) 1)
|
| [8] |
李玉灵,王玉魁,王俊刚,等.2009b.水分胁迫条件下臭柏匍匐茎的蒸腾和吸水特性.林业科学, 45(9): 48-52. (Li Y L,Wang Y K,Wang J G, et al.2009b. Transpiration and water uptake of Sabina vulgaris stolon under water stress. Scientia Silvae Sinicae, 45(9): 48-52[in Chinese]).(  1) 1)
|
| [9] |
王林和,张国盛,董智.1998.毛乌素沙地臭柏种子产量及更新的初步研究.林业科学, 34(6): 105-112. (Wang L H,Zhang G S,Dong Z.1998. A preliminary study on the seed yield and regeneration of Sabina vulgaris in Maowusu sandland. Scientia Silvae Sinicae, 34(6): 105-112[in Chinese]).(  1) 1)
|
| [10] |
王哲,张国盛,王林和,等.2007.毛乌素沙地天然臭柏群落有性更新的微生境特征.干旱区资源与环境, 21(4): 156-163. (Wang Z,Zhang G S,Wang L H, et al.2007. Microhabitat characteristics of natural regeneration of Sabina vulgaris community in Maowusu sandland. Journal of Arid Land Resources and Environment, 21(4): 156-163[in Chinese]).(  1) 1)
|
| [11] |
温国胜.2005.毛乌素沙地臭柏群落景观动态.浙江林学院学报, 22(2): 129-132. (Wen G S.2005. Dynamics of Sabina vulgaris phytocoenosis landscape in Maowusu Sandland. Journal of Zhejiang Forestry College, 22(2): 129-132[in Chinese]).(  1) 1)
|
| [12] |
温国胜,张国盛,吉川贤. 2004a.干旱胁迫对臭柏水分特性的影响.林业科学, 40(5): 84-87. (Wen G S,Zhang G S,Yoshikawa K.2004a. Effect of drought stress on water characteristics of Sabina vulgaris. Scientia Silvae Sinicae, 40(5): 84-87[in Chinese]).(  1) 1)
|
| [13] |
温国胜,吉川贤,张国盛,等.2004b.干旱胁迫条件下臭柏的生长.内蒙古农业大学学报, 25(1): 5-10. (Wen G S,Yoshikawa K,Zhang G S, et al.2004b. Growth of Sabina vulgaris under drought stress. Journal of Inner Mongolia Institute of Agriculture and Animal Husbandry, 25(1): 5-10[in Chinese]).(  1) 1)
|
| [14] |
张国盛,高润宏,王林和,等.2001.毛乌素沙地臭柏群落结构和生物多样性组成研究.内蒙古农业大学学报, 22(4): 88-91. (Zhang G S,Gao R H,Wang L H, et al.2001. Study on community structure and biodiversity of Sabina vulgaris of Maowusu. Journal of Inner Mongolia Institute of Agriculture and Animal Husbandry, 22(4): 88-91[in Chinese]).(  1) 1)
|
| [15] |
张国盛,李玉灵,王林和,等.1999.半干旱地区臭柏造林初步研究.内蒙古林学院学报,21 (1): 21-25. (Zhang G S,Li Y L,Wang L H, et al.1999. The preliminary study on Sabina vulgaris afforested in the semiarid region. Journal of Neimenggu Forestry College, 21(1): 21-25[in Chinese]).(  1) 1)
|
| [16] |
张守仁.1999.叶绿素荧光动力学参数的意义及讨论. 植物学通报, 16(4): 444-448. (Zhang S R.1999. A discussion on chlorophyll fluorescence kinetics parameters and their significance. Chinese Bulletin of Botany, 16(4): 444-448[in Chinese]).(  1) 1)
|
| [17] |
Appenroth K J, Stöckel J, Srivastava A, et al.2001.Multiple effects of chromate on the photosynthetic apparatus of Spirodela polyrhiza as probed by OJIP chlorophyll a fluorescence measurements. Environ Pollut, 115(1): 49-64.( 1) 1)
|
| [18] |
Clark A J, Landolt W, Bucher J B, et al.2000.Beech ( Fagus sylvatica) response to ozone exposure assessed with a chlorophyll a fluorescence performance index. Environ Pollut, 109(3): 501-507.( 1) 1)
|
| [19] |
Demming A B, Adams W W III. 1992.Photoprotection and other responses of plant to high light stress. Annu Rev Plant Physiol Plant Mol Biol, 43: 599-626.( 1) 1)
|
| [20] |
Eggenberg P, Rensburg L V, Krüger H J, et al. 1995.Screening criteria for drought tolerance in Nicotiana tabacum L derived from the polyphasic rise of the chlorophyll a fluorescence transient (O-J-I-P).//Mathis P. Photosynthesis: from Light to Biosphere. Dordrecht: KAP Press, 4: 661-664.( 2) 2)
|
| [21] |
Kautsky H, Hirsch A.1931. Neue versuche zur kohlensǎure-sssimilation. Naturwissenschaften, 19: 964.( 1) 1)
|
| [22] |
Krause G H, Weis E.1991. Chlorophyll fluorescence and photosynthesis: The basics. Annual Review of Plant Physiology Plant Molecular Biology, 42: 313-349.( 1) 1)
|
| [23] |
Krüger G H J, Tsimilli-Michael M, Strasser R J.1997. Light stress provokes plastic and elastic modifications in structure and function of photosystem Ⅱ in camellia leaves. Physiol Plant, 101(2): 265-277.( 1) 1)
|
| [24] |
Öquist G, Hurry V M, Huner N P A. 1993.The temperature dependence of the redox state of QA and susceptibility of photosynthesis to photoinhibition. Plant Physiol Biochem, 31(5): 683-691( 1) 1)
|
| [25] |
Pandey D M, Kang K H, Yeo U D.2005. Effects of excessive photon on the photosynthetic and violaxanthin de-epoxidase activity in the xanthophyll cycle of spinach leaf. Plant Science, 168(1): 161-166.( 1) 1)
|
| [26] |
Srivastava A, Guisse B, Greppin H. 1997.Regulation of antenna structure and electron transport in PSⅡ of Pisum sativum under elevated temperature probed by the fast polyphasic chlorophyll a fluorescence transient: OKJIP. Biochim Biophys Acta, 1320: 95-106.( 3) 3)
|
| [27] |
Strasser B J. 1997.Donor side capacity of photosystem Ⅱ probed by chlorophyll a fluorescence transient. Photosynthesis Research, 52: 147-155.( 1) 1)
|
| [28] |
Strasser B J, Strasser R J. 1995a.Measuring fast fluorescence transients to address environmental questions: the JIP test//Mathis P. Photosynthesis: from Light to Biosphere, vol. V. Kluwer Academic Publisher, The Netherlands, 977-980.( 2) 2)
|
| [29] |
Strasser R J, Tsimill-Michael M, Srivastava A. 2004.Analysis of the chlorophyll a fluorescence transient// Papageorgiou G, Govindjee. Advances in Photosynthesis and Respiration. Netherlands: KAP Press, 1-42.( 1) 1)
|
| [30] |
Strasser R J, Srivastava A. 1995b. Polyphasic chlorophyll a fluorescence transient in plant and cyanobacteria. Photochem Photobiol, 61: 32-42.( 1) 1)
|
| [31] |
van Heerden P D R, Tsimilli-Michael M, Krüger G H J, et al. 2003.Dark chilling effects on soybean genotypes during vegetative development: parallel studies of CO2 assimilation, chlorophyll a fluorescence kinetics O-J-I-P and nitrogen fixation. Physiol Plant, 117: 476-491.( 1) 1)
|
 2015, Vol. 51
2015, Vol. 51
