文章信息
- 黄增冠, 喻卫武, 罗宏海, 李昱飞, 戴文圣, 胡渊渊, 吴家胜
- Huang Zengguan, Yu Weiwu, Luo Honghai, Li Yufei, Dai Wensheng, Hu Yuanyuan, Wu Jiasheng
- 香榧不同叶龄叶片光合能力与氮含量及其分配关系的比较
- Photosynthetic Characteristics and Their Relationships with Leaf Nitrogen Content and Nitrogen Allocation in Leaves at Different Leaf Age
- 林业科学, 2015, 51(2): 44-51
- Scientia Silvae Sinicae, 2015, 51(2): 44-51.
- DOI: 10.11707/j.1001-7488.20150206
-
文章历史
- 收稿日期:2014-05-30
- 修回日期:2014-08-10
-
作者相关文章
2. 石河子大学农学院新疆生产建设兵团绿洲生态农业重点实验室 石河子 832003
2. Key Laboratory of Oasis Ecol-Agriculture of Xinjiang Production and Construction Crop College of Agricultural, Shihezi University Shihezi 832003
光合作用是植物生长发育的基础。果树干物质的90%~95%来源于光合作用,光合效率的高低可以反映出果树的生长发育水平(李天忠等,2008)。叶片是果树进行光合作用的主要器官,其生长发育和性状特征直接影响着果树的基本行为和功能。常绿植物在储存养分、适应贫瘠生境上有很大优势,主要原因是其叶片寿命可有效减少营养损失(Aerts,1995)。但常绿植物叶片由于其形成的年份、经历的环境条件及所处的发育阶段存在差异,使其资源分配模式和性状特征随叶龄变化而产生差别(Reich et al., 1991)。随着叶龄的增加,叶片的光饱和点(LSP)、光补偿点(LCP)、表观量子效率(AQY)均呈下降趋势(李勇等,2013)。凌丽俐等(2013)研究表明,纽荷尔脐橙(Citrus sinensis)2龄秋梢叶的叶绿素含量、光合相对电子传递速率均低于1龄春梢叶。叶片随叶龄变化的物质投资和分配格局是植物适应环境的重要途径之一(Silvertown et al., 1997)。叶片生长早期,为最大程度地获取光资源,需投资较多的生物量以优化同化器官,如扩展平均叶面积(mean leaf area,MLA)(Tilman,1988;Sulan,2000);相反,与早期生长的叶片相比,后期生长的叶片要经历更多复杂多变的环境胁迫,需要在抗机械胁迫和结构建造方面投资更多的生物量,从而维持叶片的停留和存活时间(Wilson et al., 1999;Gratani et al., 2000;Westoby et al., 2002)。植物叶片的氮含量与光合能力有很强的正相关性(Evans,1989;1996;Reich et al., 1994;张亚杰等,2004),老叶光合速率低是由于其叶氮含量、Rubisco/Chl比值低造成的(Warren et al., 2001)。因此,不同叶龄资源分配模式(尤其是氮素)对常绿植物的生长发育具有重要意义。
香榧(Torreya gr and is)是我国特有的珍稀干果,是集材用、药用、果用、油用和观赏于一体的经济树种。香榧是榧树的一个优良自然变异类型,常绿植物,叶片可以在枝干上存活较长时间,甚至几年。近年来有关研究主要集中在药用价值上(王向阳等,2005;Chen et al., 2006;徐超等,2012),香榧叶片光合特性的研究相对较少。Shen等(2014)对香榧幼苗光合作用与水分亏缺之间的关系进行了研究,但对不同叶龄叶片光合特性的差异及其与氮含量及分配关系的研究鲜见报道。明确香榧不同叶龄叶片光合特性差异及其形成机制,探寻通过调节物质投资和分配格局,对改善叶片光合性能、增加香榧果实产量具有重要意义。为此,本研究通过对不同叶龄香榧叶片的光响应和CO2响应曲线、叶绿素含量、叶氮含量及光合氮利用率等生化指标的测定,从表观光合特性和光合内部机构系统地揭示香榧叶片光合特性的生理机制,为进一步提高其丰产栽培技术提供理论依据。
1 材料与方法 1.1 试验材料试验于2013年10月在浙江省临安市浙江农林大学香榧山基地进行。试验区位于浙江省西北部,东临杭州余杭区,地理位置118°51′—119°52′ E,29°56′—30°23′ N,属于亚热带季风气候区,温暖湿润,光照充足,雨量充沛。供试材料为20年生香榧,对样地进行每木测量,计算出平均胸径和平均树高。选择胸径和树高与标准样地的平均胸径和平均树高比较接近、树冠良好的香榧植株为本研究的标准木。分别从树冠外围向东南伸展的顶枝(A)、侧枝(S)上选择当年生(C)叶片(萌芽后5个月)、1年生(C+1)叶片(萌芽后17个月)和2年生(C+2)叶片(萌芽后29个月)为代表性样枝。
1.2 试验方法 1.2.1 光响应曲线2013年10月选择晴朗天气,采用Li-6400便携式光合仪(美国Li-cor公司)测定不同叶位、不同叶龄香榧叶片的光响应曲线。测定时CO2浓度为400 μmol·mol-1(由CO2小钢瓶控制CO2浓度),叶室温度23~27 ℃,相对湿度约50%。采用自制人工光源,设定气体流速为500 μmol·s-1,光合有效辐射强度(PAR)梯度为1 904,1 573,1 262,959,763,575,433,198,130,0 μmol·m-2s-1。测定前用763 μmol·m-2s-1光强对叶片进行光诱导,使叶片活化。每个光强下稳定4 min记录数据,重复3~4次,取平均值作为测定结果。根据光合助手计算出光响应曲线饱和光强(LSP)、最大净光合速率(Pmax)、光补偿点(LCP)和暗呼吸速率(Rd)。所有的气体交换测定均在9:00—11:00完成。
1.2.2 CO2响应曲线选择光响应测定的叶片,控制光强为饱和光强以上(光强为763 μmol·m-2s-1),并在400 μmol·mol-1 CO2浓度下光诱导30 min,CO2浓度设置为:400,300,200,100和50 μmol ·mol-1,400,800,1 200,1 600和2 000 μmol ·mol-1CO2 浓度下测定Pn(净光合速率)。Vcmax(最大RuBP羧化速率)和Jmax(RuBP再生的光合电子传递速率)根据CO2响应曲线求得(Long et al., 2003)。所有的气体交换测定均在9:00—11:00完成。
1.2.3 叶绿素含量和比叶质量称取0.02 g鲜质量的不同叶龄叶片浸入盛有8 mL提取液(95%乙醇)的离心管中,密封避光低温浸提至叶片无色(高俊凤,2006)。用紫外分光光度计(UV2500,岛津)检测波长在665,649,470 nm处的吸光度值。记录所测叶片的鲜质量和面积,计算以叶片面积为基础的叶绿素含量。
气体交换测定完成后,将所测叶片收集,用扫描法测定叶面积(张小全等,2000),即将测定枝上的披针叶全部剪下,用透明胶带粘贴于复印纸上,并通过扫描仪(Epson扫描仪Perfection V370 Photo)求算出按针叶面积。然后将披针叶在85 ℃烘干至恒重,称量干质量。比叶质量(specific leaf weight,SLW,g·m-2)=干质量/叶面积。
1.2.4 叶片氮素含量及其在光合机构中的分配用凯氏定氮法测定单位干质量上的叶氮含量(NM)。以饱和最大光合速率(Pmax)与NM的比值表示光合氮利用效率(photosynthetic nitrogen utilization efficiency,PNUE)(Qing et al., 2012)。PNUE=Pn/NM。
植物叶氮在光合机构中的分配主要可分为3部分,即分配到RuBP羧化作用的氮素(NC,g·g-1)、分配到RuBP再生作用的氮素(NB,g·g-1)和分配到捕光组分的氮素(NL,g·g-1)。计算公式(Niinemets et al., 1997)如下:
$\begin{align} & {{N}_{\text{C}}}={{V}_{\text{cmax}}}/(6.25\times {{V}_{\text{cr}}}\times {{N}_{\text{M}}}\times \text{SLW}); \\ & {{N}_{\text{B}}}={{J}_{\text{max}}}/(8.06\times {{J}_{\text{mc}}}\times {{N}_{\text{M}}}\times \text{SLW}); \\ & {{N}_{\text{L}}}={{C}_{\text{C}}}/({{N}_{\text{M}}}\times {{C}_{\text{B}}}); \\ & {{N}_{\text{T}}}={{N}_{\text{C}}}+{{N}_{\text{B}}}+{{N}_{\text{L}}}. \\ \end{align}$
式中:CC为叶绿素含量;NM为单位干质量的叶氮含量;Vcr(Rubisco的比活度)、Jmc(以cyt f为基础的潜在光合电子流)和CB(整个叶片中叶绿素所绑定的类囊体复合体数量,即PSⅠ,PSⅡ和LHCⅡ的数量)为常数;6.25是氮素与Rubisco蛋白之间的转换系数;8.06为氮素与细胞色素f(cyt f)之间的转换系数。 1.3 数据分析采用SPSS软件进行统计分析,用光合助手(Photosynthesis)拟合曲线,采用Sigmaplot10.0作图。
2 结果与分析 2.1 光合-光响应曲线无论是顶枝(A)或侧枝(S),当年生(C)、1年生(C+1)和2年生(C+2)叶片对PAR的响应曲线基本一致(图 1)。当PAR在0~433 μmol·m-2s-1时,Pn随PAR的增强迅速增加,此时PAR是香榧叶片光合作用的主要限制因子;当PAR>433 μmol·m-2s-1时,Pn随PAR的增大其上升速度开始减慢,并逐渐趋于平缓,达到光饱和状态。
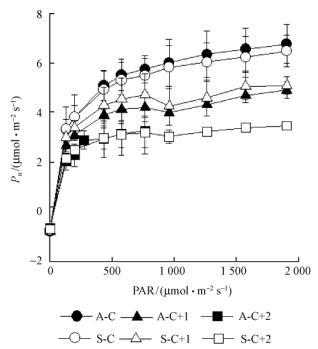 |
图 1 不同叶龄香榧叶片的光响应曲线 Fig. 1 Photosynthetic response curves of net photosynthetic rate (Pn) in leaves of different leaf age of T.grandis A-C:顶枝当年生叶片;A-C+1:顶枝1年生叶片;A-C+2:顶枝2年生叶片;S-C:侧枝当年生叶片;S-C+1:侧枝1年生叶片;S-C+2:侧枝2年生叶片。A-C: Current leaf of the apical branch; A-C+1: Current leaf +1 of the apical branch; A-C+2: Current leaf +2 of the apical branch; S-C: Current leaf of the side branch; S-C+1: Current leaf +1 of the side branch; S-C+2: Current leaf +2 of the side branch. |
对光合-光响应曲线采用非直角双曲线方程进行拟合,结果见表 1。同一叶位、不同叶龄之间,随着叶龄的增加,Pmax,LSP均呈逐渐下降趋势,其中2年生(C+2)叶片显著低于当年生(C)叶片。同一叶龄、不同叶位之间,除侧枝1年生(C+1)叶片的LSP显著高于顶枝1年生(C+1)叶片外,其余叶龄的顶枝(A)与侧枝(S)叶片之间的LSP无显著差异。
|
|
同一叶位、不同叶龄之间,随着叶龄的增加,叶片的Chla,Chlb及Chl(a+b)含量均呈下降趋势,其中顶枝(A)2年生(C+2)和1年生(C+1)叶片的Chl(a+b)含量分别比当年生(C)叶片下降了23.6%和12.1%;侧枝(S)2年生(C+2)和1年生(C+1)叶片的Chl(a+b)含量分别比当年生(C)叶片下降了18.7%和10.7%。同一叶龄、不同叶位之间,除侧枝(S)2年生(C+2)叶片显著高于顶枝(A)2年生(C+2)叶片外,其他叶龄的顶枝(A)与侧枝(S)叶片之间的Chla,Chlb及Chl(a+b)含量无显著差异(图 2)。
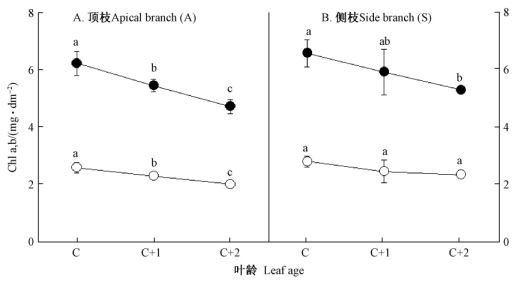 |
图 2 不同叶龄香榧叶片的叶绿素含量 Fig. 2 The chlorophyll contents in leaves of different leaf age of T. grandis ●: Chla;○: Chlb. 不同字母表示在0.05水平上差异显著。 Different letters denote significant differences at 0.05 level. |
同一叶位、不同叶龄之间,随着叶龄的增加,叶片的Vcmax呈下降趋势,其中顶枝(A)中,1年生(C+1)和2年生(C+2)叶片分别比当年生(C)叶片下降了13.86%和37.62%;侧枝(S)中,1年生(C+1)和2年生(C+2)叶片分别比当年生(C)叶片下降9.2%和27.56%。同一叶位、不同叶龄之间,随着叶龄的增加,叶片的Jmax呈下降趋势,其中顶枝(A)中,1年生(C+1)和2年生(C+2)叶片分别比当年生(C)叶片下降13.06%和39.45%;侧枝(S)中,1年生(C+1)和2年生(C+2)叶片分别比当年生(C)叶片下降了9.7%和27.42%。同一叶龄、不同叶位之间,顶枝(A)与侧枝(S)叶片之间的Vcmax,Jmax无显著差异(表 2)。
|
|
同一叶位、不同叶龄之间,随着叶龄的增加,香榧叶片NM呈逐渐下降趋势。同一叶龄、不同叶位之间,顶枝(A)与侧枝(S)叶片之间的NM无显著差异。同一叶位、不同叶龄之间,随着叶龄的增加,PC和NB均呈下降趋势。在顶枝(A)中,NL在不同叶龄之间无显著差异,但是侧枝(S)中,1年生(C+1)和2年生(C+2)的NL显著低于当年生(C)叶片。同一叶龄、不同叶位之间,顶枝(A)与侧枝(S)叶片之间的NC,NB,NL无显著差异(表 3)。
|
|
香榧叶片Pmax与NC,NB,NL,NT均呈极显著相关(表 4),表明随着叶龄的增加,香榧叶片的光合速率下降与其氮素含量及其分配到光合机构的氮素少有关。
|
|
同一叶位、不同叶龄之间,随着叶龄的增加,叶片SLW呈增大趋势,其中当年生(C)叶片的SLW显著低于1年生(C+1)和2年生(C+2)叶片,而1年生(C+1)与2年生(C+2)之间无显著差异。同一叶龄、不同叶位之间,顶枝(A)与侧枝(S)叶片之间的SLW无显著差异(图 3)。
 |
图 3 不同叶龄香榧叶SLW的变化 Fig. 3 SLW changes of different leaf age of T. grandis 不同字母表示同一叶位、不同叶龄之间在0.05水平上差异显著, ns表示同一叶龄、不同叶位之间无显著性差异。Different letters denote significant differences under different leaf age at the same position at 0.05 level, ns denote no significant differences under different position at the same leaf age.下同。The same below. |
同一叶位、不同叶龄之间,随着叶龄的增加,叶片的PNUE呈下降趋势,其中当年生(C)叶片的PNUE显著高于1年生(C+1)和2年生(C+2)叶片,1年生(C+1)与2年生(C+2)叶片之间的PNUE无显著差异;顶枝(A)和侧枝(S)之间的PNUE同样无显著差异(图 4A)。香榧叶片的PNUE与其SLW呈显著负相关关系(图 4B)。
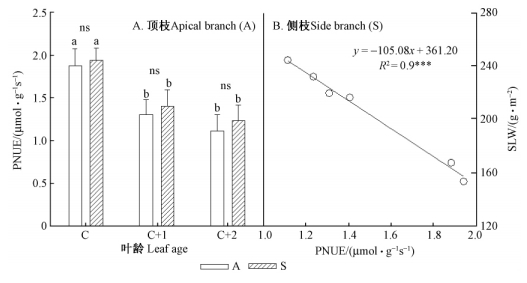 |
图 4 不同叶龄香榧叶片PNUE及其与SLW之间的相关性 Fig. 4 PNUE and its relationship to SLW in leaves of different leaf age of T.grandis |
衡量叶片光合能力的重要指标是最大净光合速率(张小全等,2001;霍宏等,2007)。研究表明,18年生杉木(Cunninghamia lanceolata)中龄林不同季节和部位针叶的Pmax均表现为当年生大于1年生、1年生大于2年生的趋势(张小全等,2001)。王兵等(2006)研究表明,随着叶龄的增加,丝栗栲(Castanopsis fargesii)叶片和苦槠栲(C.sclerophylla)叶片的净光合速率显著下降。本研究也发现,随着叶龄的增加,香榧叶片的Pmax呈下降趋势(表 1),这表明当年生叶片的光合能力较强,并且在傍晚和早晨等弱光条件仍能有效地进行光合作用,这对香榧产量形成具有重要的意义。植物叶片的LCP和LSP反映了植物对光照条件的要求,是判断植物耐阴性的重要指标。大体上阴性植物的LCP小于20 μmol·m-2s-1,LSP为500~1 000 μmol·m-2s-1或更低,而阳性植物的LCP为50~100 μmol·m-2s-1,LSP为1 500~2 000 μmol·m-2s-1或更高(蒋高明,2004)。本研究结果表明,香榧叶片的LCP为17.35~24.13 μmol·m-2s-1,LSP为345.97~513.97 μmol·m-2s-1,表现出阴生植物的光合特性,且当年生叶片的LSP值较高,表明当年生叶片对强光的适应能力强。
叶片光合能力的大小,通常与叶绿素含量、酶活性有关。随着叶龄的增加,纽荷尔脐橙叶片的叶绿素含量呈降低趋势(凌丽俐等,2013)。本研究中,1年生和2年生叶片的叶绿素含量显著低于当年生叶片,且顶枝叶片随叶龄增加的下降幅度大(图 2),这可能是顶枝叶片光合速率下降快的原因之一。研究表明,Vcmax与Rubisco含量具有显著相关性(Björkman,1968;1981;von Caemmerer et al., 1981)。与当年生叶片相比,1年生叶片的Vcmax下降了42%~44%(Whitehead et al., 2011)。本研究结果显示,与当年生叶片相比,1年生和2年生叶片的Vcmax,Jmax有明显的下降趋势,表明随着叶龄的增加,香榧叶片中的Rubisco含量逐渐降低、RuBP的再生速率受到抑制(表 2),这可能也是Pmax随叶龄增加降低的主要原因之一。而且,随着叶龄的增加,顶枝叶片的Vcmax,Jmax的下降幅度大于侧枝叶片,这可能是由于侧枝是结果枝,随着叶龄的增加,顶枝会先将氮素等营养元素优先供给侧枝叶片,导致顶枝叶片较侧枝叶片衰老速率较快的缘故。
植物叶片的氮含量与光合能力有很强的正相关性,因为通常叶氮含量中约有一半分配到光合机构中,如卡尔文循环和类囊体相关的酶(Evans,1989; 1996;Reich et al., 1994;张亚杰等,2004)。叶片单位干质量的氮含量与叶片寿命呈显著的正相关关系(Reich et al., 1999)。Yamashita等(2002)研究发现,叶片成熟后光合速率和叶氮含量逐渐降低。本研究中,随着叶龄的增加,香榧叶片的NM呈下降趋势,且叶片的NC,NB,NT均呈下降趋势,这表明分配到光合机构的氮素减少。另外,香榧叶片光合速率与氮素及其各组分均呈显著正相关(表 4),表明随着叶龄的增加,香榧叶片的光合速率下降主要由于其体内的N元素含量降低,从而降低PNUE(图 4A)。侧枝的NM要略高于顶枝,这可能是顶枝叶片较侧枝叶片衰老速率相对较快的原因。
理论上讲,高SLW植物叶片的细胞壁组分和碳含量较高,而其水分含量、叶片氮含量较低,因此大部分研究认为叶片光合与氮含量均与SLW相关(Meziane et al., 2001; Takashhna et al., 2004)。本研究结果显示,随着叶龄的增加,香榧叶片的SLW呈增加趋势(图 3),这可能是由于1年生和2年生叶片中大量氮素会流向其细胞壁上(Takashhna et al., 2004),使细胞获得更多的机械保护以抵御外界环境的变化,从而导致分配到Rubisco、捕光色素蛋白的氮元素减少(Onoda et al., 2004),这从香榧叶片的PNUE与其SLW呈显著负相关关系的分析(图 4B)中得到了进一步证实,与前人的研究结论(Hikosaka,2004;Onoda et al., 2004;Takashhna et al., 2004)一致。因此,随着叶龄的增加,香榧叶片分配到细胞壁的氮素增加,而分配到光合机构的氮素减少,可能是导致香榧不同叶龄叶片的Pn,PNUE产生差异的主要原因。
| [1] |
高俊凤. 2006. 植物生理学. 北京: 高等教育出版社, 74-77. (Gao J F. 2006. Plant physiology. Beijing: Higher Education Press, 74-77.[in Chinese])(  1) 1)
|
| [2] |
霍 宏, 王传宽. 2007. 冠层部位和叶龄对红松光合蒸腾特性的影响. 应用生态学报, 18(6): 1181-1186. (Huo H, Wang C K. 2007. Effects of canopy position and leaf age on photosynthesis and transpiration of Pinus koraiensis. Chinese Journal of Applied Ecology. 18(6): 1181-1186[in Chinese]).(  1) 1)
|
| [3] |
蒋高明. 2004. 植物生理生态学. 北京: 高等教育出版社, 65-66. (Jiang G M. 2004. Plant ecophysiology. Beijing: Higher Education Press House, 65-66.[in Chinese])(  1) 1)
|
| [4] |
李天忠, 张志宏. 2008. 现代果树生物学. 北京: 科学出版社, 141. (Li T Z, Zhang Z H. 2008. Modern fruit biology. Beijing: Science Press, 141.[in Chinese])(  1) 1)
|
| [5] |
李 勇, 韩海荣, 康峰峰, 等. 2013. 油松人工林冠层光合生理特性的空间异质性. 东北林业大学学报, 41(4): 32-35. (Li Y, Han H R, Kan F F, et al. Spatial heterogeneity of photosynthetic characterisitics of Pinus tabulaeformis canopy. Journal of Northeast Forestry University, 41(4): 32-35[in Chinese]).(  1) 1)
|
| [6] |
凌丽俐, 彭良志, 王男麒, 等. 2013. 缺镁胁迫对纽荷尔脐橙叶绿素荧光特性的影响. 生态学报, 33(1):71-78. (Ling L L, Peng L Z, Wang N Q, et al. 2013. Influence of magnesium deficiency on chlorophyll fluorescence characteristic in leaves of Newhall navel orange. Acta Ecologica Sinica, 33(1): 71-78[in Chinese]).(  2) 2)
|
| [7] |
王 兵, 赵广东, 李少宁, 等. 2006. 江西大岗山常绿阔叶林优势种丝栗栲和苦槠栲光合日动态特征研究. 江西农业大学学报, 27(4): 576-579. (Wang B, Zhao G D, Li S N, et al. 2006. Diurnal photosynthetic change characteristics of the dominant species Castanopsis fargesii and Castanopsis sclerophylla in evergreen broad-leaved forest in dagangshan mountain, Jiangxi Province. Acta Agriculturae Universitis Jiangxiensis, 27(4): 576-579[in Chinese]).(  1) 1)
|
| [8] |
王向阳, 修丽丽. 2005. 香榧的营养和功能成分综述. 食品研究与开发, 26 (2): 20-22. (Wang X Y, Xiu L L. 2005. Review: the nutritional and functional components of Torreya grandis. Food Research and Development, 26(2): 20-22[in Chinese]).(  1) 1)
|
| [9] |
徐 超, 王鸿飞, 邵兴锋, 等. 2012. 香榧子油抗氧化活性及降血脂功能研究. 中国粮油学报, 27(8): 43-47. (Xu C, Wang H F, Shao X F, et al. 2012. Study on antioxidant activity and reducing blood fat function of kaga oil. Journal of the Chinese Cereals and Oils Association, 27(8): 43-47[in Chinese]).(  1) 1)
|
| [10] |
张小全, 徐德应. 2000. 杉木中龄林不同部位和叶龄针叶光合特性的日变化和季节变化. 林业科学, 36(3):19-26. (Zhang X Q, Xu D Y. 2000. Seasonal changes and daily courses of photosynthetic characteristics of 18-year-old Chinese fir shoots in relation to shoot ages and positions within tree crown. Scientia Silvae Sinicae, 36(3): 19-26[in Chinese]).(  1) 1)
|
| [11] |
张小全, 徐德应. 2001. 18年生杉木不同部位和叶龄针叶光响应研究. 生态学报, 21(3): 409-414. (Zhang X Q, Xu D Y. 2001. Light responses of 18-year-old China fir shoots in relation to shoot ages and positions within crown. Acta Ecologica Sinica, 21(3): 409-414[in Chinese]).(  2) 2)
|
| [12] |
张亚杰, 冯玉龙. 2004. 不同光强下生长的两种榕树叶片光合能力与比叶重、 氮含量及分配的关系. 植物生理与分子生物学学报, 30(3): 269-276. (Zhang Y J, Feng Y L. 2004. The relationships between photosynthetic capacity and lamina mass per unit area, nitrogen content and partitioning in seedlings of two Ficus species grown under different irradiance. Acta Photophysiologica Sinica, 30(3): 269-276[in Chinese]).(  2) 2)
|
| [13] |
Aerts R. 1995. The advantages of being evergreen. Trends in Ecology and Evolution, 10: 402-407.( 1) 1)
|
| [14] |
Björkman O.1968. Carboxydismutase activity in shade-adapted and sun-adapted species of higher plants. Physiologia Plantarum, 21(1):1-10.( 1) 1)
|
| [15] |
Björkman O. 1981. Response to different quantum flux densities//Lange O L, Nobel P S, Osmond C B, et al. Physiological plant ecology I. responses to the physical environment, encyclopedia of plant physiology, new series. Springer-Verlag: Berlin, 57-107.( 1) 1)
|
| [16] |
Chen B Q, Cui X Y, Zhao X, et al. 2006. Antioxidative and acute antiinflammatory effects of Torreya grandis. Fitoterapia, 77(4): 262-267.( 1) 1)
|
| [17] |
Evans J R. 1989. Photosynthesis and nitrogen relationship in leaves of C3 plants. Oecoliogia, 78:9-19.( 2) 2)
|
| [18] |
Evans J R. 1996. Developmental constraints on photosynthesis: effects of light and nutrition//Baker N R. Photosynthesis and the environment. Netherlands: Kluwer Academic Publisher, 5: 281-304.( 2) 2)
|
| [19] |
Gratani L, Bombelli A. 2000. Correlation between leaf age and other leaf traits in three Mediterranean maquis shrub species: Quercus ilex, Phillyrea latifolia and Cistus incanus. Environmental and Experimental Botany, 43: 141-153.( 1) 1)
|
| [20] |
Hikosaka K. 2004. Interspecific difference in the photosynthesis-nitrogen relationship:patterns, physiological causes, and ecological importance. Journal of Plant Research, 117(6): 481-494. ( 1) 1)
|
| [21] |
Long S P, Bernacchi C J. 2003. Gas exchange measurements, what can they tell us about the underlying limitations to photosynthesis Procedures and sources of error. Journal of Experimental Botany, 54(392): 2393-2401.( 1) 1)
|
| [22] |
Meziane D, Shipley B. 2001. Direct and indirect relationships between specific leaf area, leaf nitrogen and leaf gas exchange-effects of irradiance and nutrient supply. Annual of Botany, 88: 915-927.( 1) 1)
|
| [23] |
Niinumets V, Tenhunen J D. 1997. A model separating leaf structural and physiological effects on carbon gain along light gradients for the shade-tolerant species Acer saccharum. Plant Cell Environ, 20: 845-866.( 1) 1)
|
| [24] |
Onoda Y, Hikosaka K, Hirose T. 2004. Allocation of nitrogen to cell walls decrease photosynthetic nitrogen-use efficiency. Functional Ecology, 18(3): 419-425.( 2) 2)
|
| [25] |
Qing H, Cai Y, Xiao Y, et al. 2012. Leaf nitrogen partition between photosynthesis and structural defense in invasive and native tall form Spartina alterniflora populations: effects of nitrogen treatments. Biological Invasions, 14(10):2039-2048.( 1) 1)
|
| [26] |
Reich P B, Ellsworth D S, Walters M B, et al.1999. Generality of leaf trait relationships: a test across six biomes. Ecology, 80:1955-1969.( 1) 1)
|
| [27] |
Reich P B, Walters M B, Ellsworth D S. 1991. Leaf age and season influence the relationships between leaf nitrogen, leaf mass per area and photosynthesis in maple and oak trees. Plant, Cell and environment, 14(3): 251-259. ( 1) 1)
|
| [28] |
Reich P B, Walters M B, Ellsworth D S, et al. 1994. Photosynthesis-nitrogen relations in Amazonian tree species I. Patterns among species and communities. Oecologia, 97:62-72.( 2) 2)
|
| [29] |
Shen C H, Hu Y Y, Du X H, et al. 2014. Salicylic acid induces physiological and biochemical changes in Torreya grandia cv. merrillii seedlings under drought stress. Trees, 28: 961-970.( 1) 1)
|
| [30] |
Silvertown J, Franco F B, Harper J L. 1997. Plant life histories: ecology, phylogeny and Evolution. Cambridge University Press, Cambridge, UK, 11-18. ( 1) 1)
|
| [31] | Sultan S E. 2000. Phenotypic plasticity for plant development, function and life history. Trends in Plant Science, 5(12): 537-542. |
| [32] |
Takashhna T, Kkosaka K, Hirose T. 2004. Photosynthesis or persistence: nitrogen allocation in leaves of evergreen and deciduous Quercus species. Plant, Cell & Environment, 27(8): 1047-1054. ( 3) 3)
|
| [33] |
Tilman D. 1988. Plant strategies and the dynamics and structure of plant communities. Princeton University Press, Princeton, 360.( 1) 1)
|
| [34] |
von Caemmerer S, Farquhar G D. 1981. Some relationships between the biochemistry of photosynthesis and the gas exchange of leaves. Planta, 153(4): 376-387.( 1) 1)
|
| [35] |
Warren C R, Adams M A. 2001. Distribution of N, Rubisco and photosynthesis in Pinus pinaster and acclimation to light. Plant, Cell Environment, 24:597-609.( 1) 1)
|
| [36] |
Westoby M, Falster D S, Moles A T, et al. 2002. Plant ecological strategies: some leading dimensions of variation between species. Annual Review of Ecology and Systematics, 33:125-159. ( 1) 1)
|
| [37] |
Whitehead D, Barbour M M, Griffin K L, et al. 2011. Effects of leaf age and tree size on stomatal and mesophyll limitations to photosynthesis in mountain beech (Nothofagus solandrii var. cliffortiodes). Tree physiology, 31(9): 985-996.( 1) 1)
|
| [38] |
Wilson P J, Thompson K, Hodgson J G. 1999. Specific leaf area and leaf dry matter content as alternative predictors of plant strategies. New Phytologist, 143(1): 155-162. ( 1) 1)
|
| [39] |
Yamashita N, Koike N, Ishida A. 2002. Leaf ontogenetic dependence of light acclimation in invasive and native subtropical trees of different successional status. Plant Cell Environ, 25(10):1341-1356. ( 1) 1)
|
 2015, Vol. 51
2015, Vol. 51

