文章信息
- 宁虎森, 罗青红, 吉小敏, 朱雅娟, 孙慧瑛, 褚玲
- Ning Husen, Luo Qinghong, Ji Xiaomin, Zhu Yajuan, Sun Huiying, Zhu Ling
- 3种沙地植物光合碳同化对环境因子的生理响应
- Physiological Responses of the Photosynthetic Carbon Assimilation to Environmental Factors in three Sandy Plants
- 林业科学, 2014, 50(9): 173-179
- Scientia Silvae Sinicae, 2014, 50(9): 173-179.
- DOI: 10.11707/j.1001-7488.20140924
-
文章历史
- 收稿日期:2014-02-17
- 修回日期:2014-07-30
-
作者相关文章
2. 中国林业科学研究院荒漠化研究所 北京 100091;
3. 中国科学院新疆生态与地理研究所乌鲁木齐830011
2. Institute of Desertification, CAF 100091;
3. Xinjiang Institute of Ecology and Geography, Chinese Academy of Sciences Urumqi 830063
自然条件下植物光合作用受多个环境因子交互影响(余叔文等,1998),研究植物光合特性对环境因子的响应是评价植物在一定环境条件下的生长能力及适应能力的基础,因此,对研究植物生态环境适应性有着重要作用。荒漠生态系统作为高温、高光强(Arandal et al.,2001;Jiang et al.,2001)、水分亏缺(Guttermen,2001)等极端环境因素的聚集地,其植物光合、生长及分布受环境因子的影响更加强烈。关于荒漠地区植物光合对环境因子响应的研究较多(蒋高明等,2004;张盹明等,2009;靳甜甜等,2011;曹生奎等,2012),但有关新疆荒漠区沙木蓼(Atraphaxis bracteata) 、沙地桑(Morus alba)和罗布麻(Apoceynum venetum)的光合特性对环境因子的响应研究较少。
不同科的沙地植物沙木蓼、沙地桑和罗布麻,其原生大环境基本一致,作为重要的防风固沙植物材料,以及优质的饲用、药用植物资源在生态环境较好的半干旱气候带广泛种植,并取得较好的生态经济效益。本研究以这3种经济生态兼用植物为试验对象,比较分析3种植物幼苗光合碳同化对不同光强、CO2浓度、温度和湿度响应的生理机制,旨在为丰富新疆等相似气候区生态经济兼用植物种类的筛选和利用提供理论依据,同时为改善其光合过程,进一步提高植物光合生产力提供科学依据。
1 材料与方法 1.1 试验区概况试验地位于新疆博尔塔拉蒙古自治州精河县沙丘道班(83°32′ N,44°57′ E),属典型温带大陆性气候,年均日照时数达2 709.6 h,年均太阳总辐射值为128.8 kk·m2;年均气温7.2 ℃,最高43.1 ℃,最低-41.0 ℃;年均降水量90.9 mm,年均蒸发量1 423.9 mm,无霜期171天。试验区土壤为沙土,土质疏松,透水透气性好,地面以下0~60 cm土层土壤pH7.96,有机质质量分数为2.22 g·kg-1,全N、全P、全K质量分数分别为0.12,0.28,14.58 g·kg-1。
1.2 试验材料供试材料为沙木蓼、沙地桑和罗布麻的1年生幼苗,2013年4月沿南北向栽植,株行距0.5 m×1.0 m,每种植物栽植3个小区,每小区45株,小区随机排列。利用喷灌设施灌溉,缓苗阶段(4~5月)灌水周期定为3~5天,待6月苗木生长正常后延长至8~10天,采用统一的施肥、除草、中耕等田间管理措施。
1.3 试验方法在苗木生长旺盛的7月和生理活动趋于缓慢的9月,晴朗无云日,每个小区选长势基本一致的5株幼苗进行标记,用CIRAS-2型(英国,PP SSystems)便携式光合作用测定仪,对向阳面的健康功能叶进行测定,每种植物测定15片叶。
1)光合日变化测定方法7月连续3天晴朗日的10:00—20:00,每隔2 h分别测定3种植物的胞间CO2浓度(Ci)、蒸腾速率(Tr)、气孔导度(Gs)、净光合速率(Pn)等参数并计算气孔限制值(LS)=1-Ci/Ca,羧化效率(CE)=Pn/Ci,瞬间水分利用效率(WUE)=Pn/Ci,瞬间光能利用效率(LUE)=Pn/PAR×1 000。
2)光合响应曲线测定方法在苗木生长旺盛的7月和生理活动趋于缓慢的9月,在晴朗上午的8:30—11:30时段内(光照强度、温度和湿度相对稳定的,即叶片在自然光诱导下进行充分光启动后),开放式气路系统下,测定活体叶片净光合速率(net photosynthetic rate,Pn)、蒸腾速率(transpiration rate,Tr)等对光强、CO2浓度、温度、湿度的响应。
3)光合—光响应曲线(Pn-PAR)测定安装配套的CO2控制系统,将CO2浓度稳定为(380±10)μmol·mol-1,叶室相对湿度(relative huminity,RH)稳定在45%~55%间,叶温(leaf temperture,TL)控制在(30±2)℃,在预试验的基础上,利用LED人工光源控制叶室光合有效辐射(photosynthetic available radiation,PAR),设置PAR为2 000,1 800,1 600,1 400,1 200,1 000,800,600,400,300,200,100,50,0 μmol·m-2s-1共14个梯度,每一PAR梯度平衡120 s,记录光合参数值。
采用的直角双曲线的修正模型(叶子飘,2009)对Pn-PAR响应曲线进行拟合,计算出最大净光合速率(maximum net photosynthetic rate,Pmax)、暗呼吸速率(dark respiration rate,Rd)、光补偿点(light compensation point,LCP)和光饱和点(light saturation point,LSP)、表观量子效率(apparent quantum yield,AQY)。
4)光合—胞间CO2浓度响应曲线(Pn-Ci)测定采用CO2控制系统提供气源,将叶室内CO2气体控制为50,100,200,300,500,700,900,1 200,1 500 μmol·mol-1共9个浓度水平,每个浓度梯度保持10 min,测前将叶温调为(30±1)℃,RH调为45%~55%,利用人工光源设定PAR为1 200 μmoL·m-2s-1。
利用SPASS对Pn-Ci曲线进行拟合(Farquhar et al.,1982),并计算最大净光合速率(Pmax)、光呼吸速率(light respiration rate,RP)、CO2饱和点(CO2 saturation point,CSP)和CO2补偿点(CO2 compensation point,CCP)等特征参数。并对Ci为50~400 μmol·mol-1的Pn值进行线性回归(蔡时青等,2000),得出羧化效率(carboxylation efficiency,CE)。
5)光合—温度响应曲线(Pn-T)测定采用CO2控制系统设置CO2浓度为(380±10)μmol·mol-1,TL设置为20,25,30,35,40 ℃共5个水平。测定中,使用人工光源控制PAR为1 200 μmol·m-2s-1,RH为45%~55%,每个温度梯度下适应5 min(Battaglia et al.,1996)后读取测值,并通过Pn/Tr求得瞬时水分利用效率(water utilization efficiency,WUE)。
6)光合—湿度响应曲线(Pn-H)测定安装CO2控制系统提供CO2气源,浓度控制为(380±10)μmol·mol-1,叶温控制为(30±1)℃,将人工光源PAR设定为1 200 μmol·m-2s-1,设定叶室RH为100%,90%,80%,70%,60%,50%,40%,30%,20%,10%,0%,每个湿度水平平衡5 min后记录Pn,Tr等数值。
7)瞬时光合参数的测定与上述光合响应曲线测定日期相近,利用自然光,在上午8:30—11:30时段内,用外接缓冲瓶控制CO2浓度保持相对稳定,测定3种植物在自然气候条件下的Pn,同步记录PAR,Ta,RH以及叶面蒸汽压水分亏缺(Vpd)等气象参数。测定数据用于光合参数与气象因子的相关性分析。
1.4 数据统计分析用统计分析软件SPASS 18.0和Excel 2003进行试验数据分析和作图,采用单因素方差分析(One-way ANOVA)揭示同一植物在7月和9月的光合特征参数的差异;用Duncan多重比较检验3种植物种间光合特征参数的差异。
2 结果与分析 2.1 3种植物光合生理特性对光合有效辐射的响应Pn-PAR响应曲线拟合结果如图 1所示,3种植物曲线拟合度R2均达到了0.986以上。从曲线的走势来看,无论是植物长势较旺的7月,还是生理活动开始减缓的9月,低PAR下3种植物的Pn均随PAR的增大而递增,而当PAR≥ 1 200 μmol·m-2s-1之后Pn逐渐趋于平缓。PAR在600~2 000 μmol·m-2·s-1范围内,2月参试植物的Pn排序分别为沙木蓼>沙地桑>罗布麻和沙木蓼>罗布麻>沙地桑,即沙木蓼的Pn始终比其他2种植物高,罗布麻在9月的Pn高于7月。
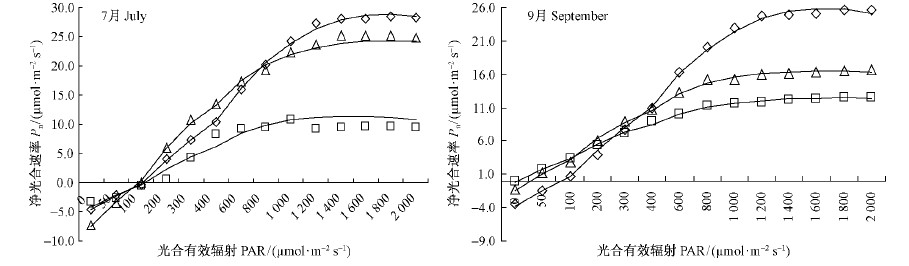 |
图 1 7月和9月3种沙地植物的净光合速率对光合有效辐射的响应 Fig. 1 The response curves of the net photosynthetic rate(Pn) to the photosynthetic available radiation(PAR) of the leaves of three sandy plants in July and September ◇沙土蓼Atraphaxis bracteata □沙地桑Morus alba △罗布麻Apoceynum venetum 下同。The same below. |
用直角双曲线的修正模型计算出3种沙地植物光响应特征参数(表 1),比较植物种间的差异发现,7和9月,沙地桑的LSP都最高,Pmax则是沙木蓼的最高,说明沙地桑的光合作用对强光的利用能力强,而沙木蓼潜在的光合能力最大。7月罗布麻的LCP较其他2种植物高,表明对弱光的利用能力较强,9月则大幅降低,而沙木蓼的LCP随生长月份变化的幅度较小。对同种植物不同月份生长期的差异比较可知,与7月相比,9月罗布麻的LSP显著上升,LCP极显著下降,说明罗布麻在初秋光合作用的光适应幅有增大的趋势。随着秋季的临近,气温开始缓慢降低、光强逐渐减弱,沙地桑的LCP和Pmax都(极)显著降低。
|
|
由图 2可知,2月3种沙地植物的Pn-Ci实测值与拟合值相似度较高(R2≥0.997),Pn与Ci均表现出正相关的关系,曲线呈现出先缓慢上升达饱和点后逐渐趋平的走势。但不同月份间差异较大,7月沙木蓼的Pn-Ci曲线位于最上方,沙地桑次之,罗布麻最次;而至9月,罗布麻的光合碳同化对二氧化碳的利用能力明显上升,主要表现在罗布麻Pn-Ci曲线的位置上调至最上方。
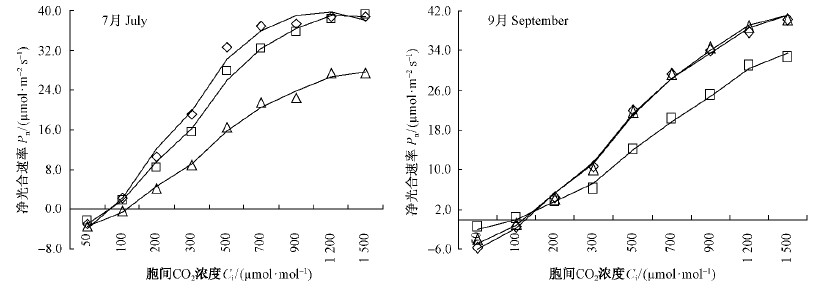 |
图 2 7月和9月3种沙地植物净光合速率对胞间二氧化碳浓度的响应 Fig. 2 The response curves of the net photosynthetic rate(Pn) to the intercellular CO2 concentration(Ci) of the leaves of three sandy plants in July and September |
由表 2可知,2月中各植物的Pn-Ci曲线特征参数表现出较大差异。7月罗布麻的CSP和CCP显著高于沙木蓼;9月沙木蓼的CSP和CCP值最大,且对应的Pmax,CE和Rp也较大。与7月相比,9月3种植物的CSP和Pmax都有所增大,CE则下降,说明随着秋季的到来,3种植物利用低浓度CO2进行光合碳同化的能力在减弱,而对高浓度CO2的利用能力在增强,3种植物中罗布麻的Pn对高浓度CO2的利用能力最强,具有最高的Pmax。
|
|
3种植物在7月的Pn-T和WUE-T曲线变化特征如图 3。Pn-T曲线波动较小,WUE-T曲线波幅较大。同一温度下,3种植物以沙木蓼的Pn值最大;在温度上升过程中,沙木蓼的Pn值降幅也最大,20与40 ℃对应的Pn差值达4.4,说明在相同温度下,该植物的光合碳同化能力较强,光合碳同化受温度的影响较大。罗布麻的Pn-T曲线最为平缓,温度从20 ℃升至40 ℃过程中,Pn值变化很小,且Pn较大值出现在低温区。沙木蓼的最大Pn值出现在35 ℃附近。另外,从WUE-T的弯曲程度来看,温度对3种沙地植物水分利用效率有较大影响,且对沙地桑和沙木蓼的影响程度明显高于罗布麻。
 |
图 3 7月3种沙地植物净光合速率、水分利用效率对叶温的响应 Fig. 3 The response curves of the net photosynthetic rate and water use efficiency to temperture of the leaves of three sandy plants in July |
3种沙地植物在7月的Pn-H和WUE-H曲线特征如图 4,随着环境湿度的增加,沙木蓼和沙地桑叶片的Pn值变幅不大,且Pn始终较大,罗布麻Pn的变幅较大,且Pn值始终较小。3种植物的WUE整体均随着环境湿度的增加而上升,且沙木蓼和沙地桑的WUE-H曲线走势相近,均呈近直线递增的趋势,沙地桑则呈曲线上升。3种植物以沙木蓼的WUE最高,罗布麻最低,沙地桑介于中间。
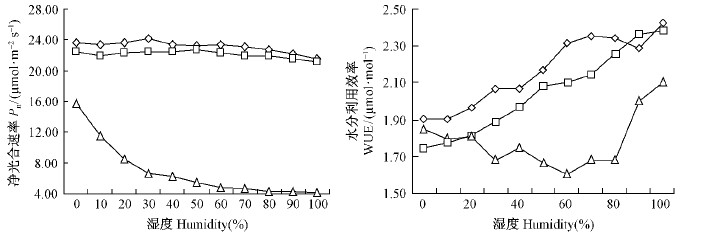 |
图 4 7月3种沙地植物净光合速率、水分利用效率对相对湿度的响应 Fig. 4 The response curves of the net photosynthetic rate and water use efficiency to relative humidity of the leaves of three sandy plants in Jul |
对7月和9月3种植物的光合参数与气象指标的相关性进行分析,结果见表 4。就Pn而言,仅沙木蓼的RH与之表现出极显著正相关关系,沙地桑的PAR与之表现出显著正相关关系,4种生态因子对罗布麻的Pn影响较小。同时,3种沙地植物的Tr与Ta,RH呈显著或极显著正相关。另外,4种气象因子中,Ta对3种植物的Gs影响均较大,而对罗布麻和沙木蓼的Gs影响较大的还有Vpd。整体来看,3种沙地植物的Pn受气象因子的影响较小,Tr和Gs与气象因子的关系更为密切,受气象因子影响的程度较重。
|
|
不同植物对环境条件变化响应存在显著差异,这种差异是植物生存和竞争策略的一部分,并显著影响植物的资源获取、利用和分配(孙伟等,2004)。而本研究结果也显示,3种沙地植物叶片的光合碳同化对光照强度、二氧化碳浓度和温度、湿度的响应过程及机制也不同。
3.1 3种沙地植物光合碳同化对光强的响应梁开明等(2008)的研究显示多数阳性植物的光饱和点(LSP)为1 500~2 000 μmol·m-2s-1、光补偿点(LCP)为50~100 μmol·m-2s-1。蒋高明等(2004)的研究认为阳生草本的最大净光合速率(Pmax)一般为15~30 μmol·m-2s-1,表观量子效率(AQY)为0.04~0.07。本研究中,3种沙地植物的LSP,LCP,Pmax及AQY均在上述范围内甚至高于阈值的上限,表明3种植物利用强光的能力较高,向阳性较强,在受到强光刺激时不易发生光抑制,能耐受高温,但不同植物种间仍有差异。与沙木蓼和罗布麻相比,沙地桑具有较高AQY和LSP,说明其具有更宽的光强生态幅和更强的弱光利用能力,但在相同光强条件下,沙地桑的净光合速率明显较低。这可能由于不同生长结构植物长期适应沙区强光辐射,即叶片较大或者光合面积较大的沙地桑光合碳同化对光能利用效率低,而叶片较小或光合面积较小的沙木蓼和罗布麻等植物类型对光能的利用效率反而更高。
3.2 3种沙地植物光合碳同化对二氧化碳浓度的响应CO2浓度缓慢升高的过程中,3种沙地植物的Pn也随之上升,这与Sims等(1999)和Ward等(1999)的研究结论CO2浓度增加在短期内能促进植物的光合作用一致。同时,3种植物CO2补偿点(CCP)均大于80 μmol·mol-1,比一般植物的CCP(30~70 μmol·mol-1)上限值高(潘瑞炽,2004),说明自然环境中3种植物的CO2同化能力较弱,不利于光合产物的积累。与沙木蓼和沙地桑相比,罗布麻具有更高的CSP、较低的CCP和较大的CE,说明它的光合作用具有更宽的CO2浓度适应生态幅,对低浓度的CO2有较强的转化能力。本研究仅在PAR为1 200 μmol·m-2s-1的条件下,分析了CO2浓度对3种植物光合碳同化的影响,而对不同PAR强度下各植物的光合生理变化尚需深入研究。
3.3 3种沙地植物光合碳同化对温度和湿度的响应温度对光合作用系统有双重效应,它影响光合生化反应的同时,也影响叶片与大气之间CO2和H2O的交换,即影响光合作用的物理过程(Charles et al.,1981;Gatherum et al.,1967)。从有关环境温度对光合作用影响的研究结果可知,不同种类植物对光合温度的敏感性差异较大(Battaglia et al.,1996;项文化等,2004;张小全等,2002)。温度对净光合速率和水分利用效率的影响在3种沙地植物间存有差异,沙地桑的光合作用对温度的生态适应幅较宽,且水分利用效率较高;沙木蓼的光合速率及水分利用效率受高温影响较大;罗布麻的光合作用对温度变化不敏感。
空气相对湿度(RH)对光合作用的效应与土壤湿度有相似性,干燥的空气导致叶片失水,并关闭气孔(张小全等,2002)。某些针叶树种的针叶随空气的蒸汽压差的提高,会导致光合速率的直线下降(Sandford et al.,1986),而本试验中罗布麻也表现出相似的变化趋势,即随着空气湿度的增大,净光合速度降低。本研究各生理生态指标对温度、湿度的响应值只是瞬时效应,有学者认为(Battaglia et al.,1996),光合作用的瞬时效应是基于对环境温度、湿度的适应,当环境温度、湿度瞬间偏离最适温度和湿度后,将导致光合酶的活性下降;当恢复到最适温、湿度时,光合能力又接近最大值。而本研究中3种植物对温度、相对湿度的适应只限于短时间处理,环境长期恒定的温度或湿度对碳同化过程的影响机制,还有待于进一步研究。
| [1] |
曹生奎, 冯起. 2012. 胡杨光合蒸腾与影响因子间关系的研究. 干旱区资源与环境, 26(4) : 155-159.( 1) 1)
|
| [2] |
蔡时青, 许大全. 2000. 大豆叶片CO2补偿点和光呼吸的关系. 植物生理学报, 26(6) : 545-550.( 1) 1)
|
| [3] | 蒋高明, 常杰, 高玉葆, 等. 2001. 植物生理生态学.北京:高等教育出版社, 65-67. |
| [4] |
蒋高明, 朱桂杰. 2004. 高温强光环境条件下3种沙地灌木的光合生理特点. 植物生态学报, 25(5) : 525-531.( 2) 2)
|
| [5] |
靳甜甜, 傅伯杰, 刘国华, 等. 2011. 不同坡位沙棘光合日变化及其主要环境因子. 生态学报, 1(7) : 1783-1793.( 1) 1)
|
| [6] |
梁开明, 曹洪麟, 徐志防, 等. 2008. 台湾青枣及野生种的光合作用日变化及光响应特征. 园艺学报, 35(6) : 793-798.( 1) 1)
|
| [7] |
潘瑞炽. 2004. 植物生理学.5版. 北京: 高等教育出版社, 80-81.( 1) 1)
|
| [8] |
孙伟, 王德利, 王立. 2004. 贝加尔针茅不同枝条叶片蒸腾特性与水分利用效率对瞬时CO2和光照变化的响应. 生态学报, 24(11): 2437-2443.( 1) 1)
|
| [9] |
项文化, 田大伦, 闫文德. 2004. 白栎光合特性对二氧化碳浓度增加和温度升高的响应. 浙江林学院学报, 21(3) : 247-253.( 1) 1)
|
| [10] |
叶子飘, 于强. 2009. 植物气孔导度的机理模型. 植物生态学报, 33(4) : 772-782.( 1) 1)
|
| [11] |
余叔文, 汤章城. 1998. 植物生理与分子生物学.2版. 北京: 科学出版社, 567-569.( 1) 1)
|
| [12] |
张小全, 徐德应. 2002. 温度对杉木中龄林针叶光合生理生态的影响. 林业科学, 38(3) : 27-33.( 2) 2)
|
| [13] |
张盹明, 唐进年, 徐先英, 等. 2009. 两种蒿属植物的光合特性研究. 西北农业学报, 18(2): 163-168.( 1) 1)
|
| [14] |
Arandal, Gil L, Pardos J. 2001. Effects of thinning in a Pinus sylvestris L. stand on foliar water relations of Pagus sylvatica L seedlings planted within the pinewood. Trees Structure and Function, 15(6):358-364.( 1) 1)
|
| [15] |
Battaglia M, Beadle C, Loughhead S. 1996. Photosynthetic temperature responses of Eucalyptus globulus and Eucalyptus nitens. Tree Physiology, 16(1-2):81-89.( 3) 3)
|
| [16] |
Charles-Edwards D A. 1981. The mathematics of photosynthesis and productivity.London: Academic Press Inc. ( 1) 1)
|
| [17] |
Farquhar G D, Sharkey T D. 1982. Stomatal conductance and photosynthesis.Ann Res Plant Physiol,33:317-345.( 1) 1)
|
| [18] |
Gatherum G E, Gordon J C, Broerman B F S. 1967. Effects of clone and light intensity on photosynthesis, respiration and growth of Aspen-poplar hybrids. Silvae Genet. 16(4) : 128-132.( 1) 1)
|
| [19] |
Guttermen Y. 2001. Plants in the deserts of the Middle East.Botany K H. Ann Bot (lond), 89(4) : 501.( 1) 1)
|
| [20] |
Jiang G M, Zhu G J. 2001. Different patterns of gas exchange and photochemical efficiency in three sandy shrub species under two natural temperatures and irradianccs in Mu Us Sandy Area of China. Photosynthetica, 39(2) : 257-262.( 1) 1)
|
| [21] |
Sims D A, Cheng W, Luo Y, et al. 1999. Photosynthetic acclimation to elevated CO2 in a sunflower canopy. J Exp Bot, 50(334) : 645-653.( 1) 1)
|
| [22] |
Ward J K, Strain B R. 1999. Elevated CO2 studies:past, present and future.Tree Physiology, 19(4/5) : 211-220.( 1) 1)
|
| [23] |
Sandford A P, Javrvis P G.1986. Stomatal response to humidity in selected conifers. Tree Physiology, 2(1/2/3) : 89-103.( 1) 1)
|
 2014, Vol. 50
2014, Vol. 50
