文章信息
- 梁超琼, 曹支敏, 陈敏, 周雪
- Liang Chaoqiong, Cao Zhimin, Chen Min, Zhou Xue
- 杨树水泡型溃疡病菌培养性状、无性型与分子系统学分析
- Cultural Characteristics, Anamorph and DNA Phylogeny of Botryosphaeria dothidea Causing Poplar Canker
- 林业科学, 2014, 50(4): 66-76
- Scientia Silvae Sinicae, 2014, 50(4): 66-76.
- DOI: 10.11707/j.1001-7488.20140410
-
文章历史
- 收稿日期:2013-04-07
- 修回日期:2014-03-03
-
作者相关文章
杨树(Populus)是一种适应性强、分布极广的树种,为我国北方栽植面积最大的速生用材林树种,具有重要的生态和经济价值。随着杨树人工林的大面积的发展,杨树病虫害大量产生,其中,水泡型溃疡病是杨树重要的枝干病害,常导致杨树幼树枯死并限制成树的生长,严重影响杨树人工林的培育,一定程度上制约着我国林业及生态环境建设的稳定发展。杨树水泡型溃疡病由子囊菌门(Ascomycota)、葡萄座腔菌目(Botryosphaeriales)的葡萄座腔菌(Botryosphaeria dothidea)侵染所致(张星耀等,2003; Grasso et al.,2010),该真菌寄主范围广泛,可引起包括杨树在内的多种林木溃疡、枝枯、流胶和果腐等病害(吴小芹等,2001)。
葡萄座腔菌在自然条件下多以无性型出现在杨树等寄主上,但葡萄座腔菌属无性型复杂多样,如Dothiorella,Diplodia 和Fusicoccum 等(Denman et al.,2000)。关于葡萄座腔菌的无性型类型仍存在争议(张星耀等,1999; 2000; 王金利等,2007; 余仲东等,2010; Slippers et al.,2004; Kirk et al.,2008),该病菌的无性型存在着生理与致病性变异(刘会香等,1997; 张星耀等,2008)。因此,深入开展杨树水泡型溃疡病病原菌系统学及其致病性分化研究,具有重要的理论与实践意义。
目前,国内外学者对于Botryosphaeriaceae 真菌分类研究除仍主要依据此类真菌有性型、无性型形态学特征外,更多是采用多种分子系统学研究方法。这些技术包括SSR,ISSR,RAPD,RFLP和AFLP等多种分子标记(王金利等,2003; 2007; 余仲东等,2000; 2004; 张星耀等,1999; 2000)。多个研究都采用rDNA的保守区域(如ITS,LSU,18S rDNA,28S rDNA基因等)、β-微管蛋白和EF-1a 基因序列对树木溃疡病病原菌进行鉴定并分析其系统发育关系(余仲东等,2010; Slippers et al.,2004; Phillips et al.,2005; Crous et al.,2006)。本研究首次对发生在陕西、甘肃等地的杨树水泡型溃疡病菌进行调查分析,在形态学鉴定的基础上,利用rDNA-ITS 序列、β-微管蛋白基因和EF-1α基因序列分析不同地域菌系间的系统发育关系,以期为西北地区杨树溃疡病菌分子系统及其地理分化提供理论依据。
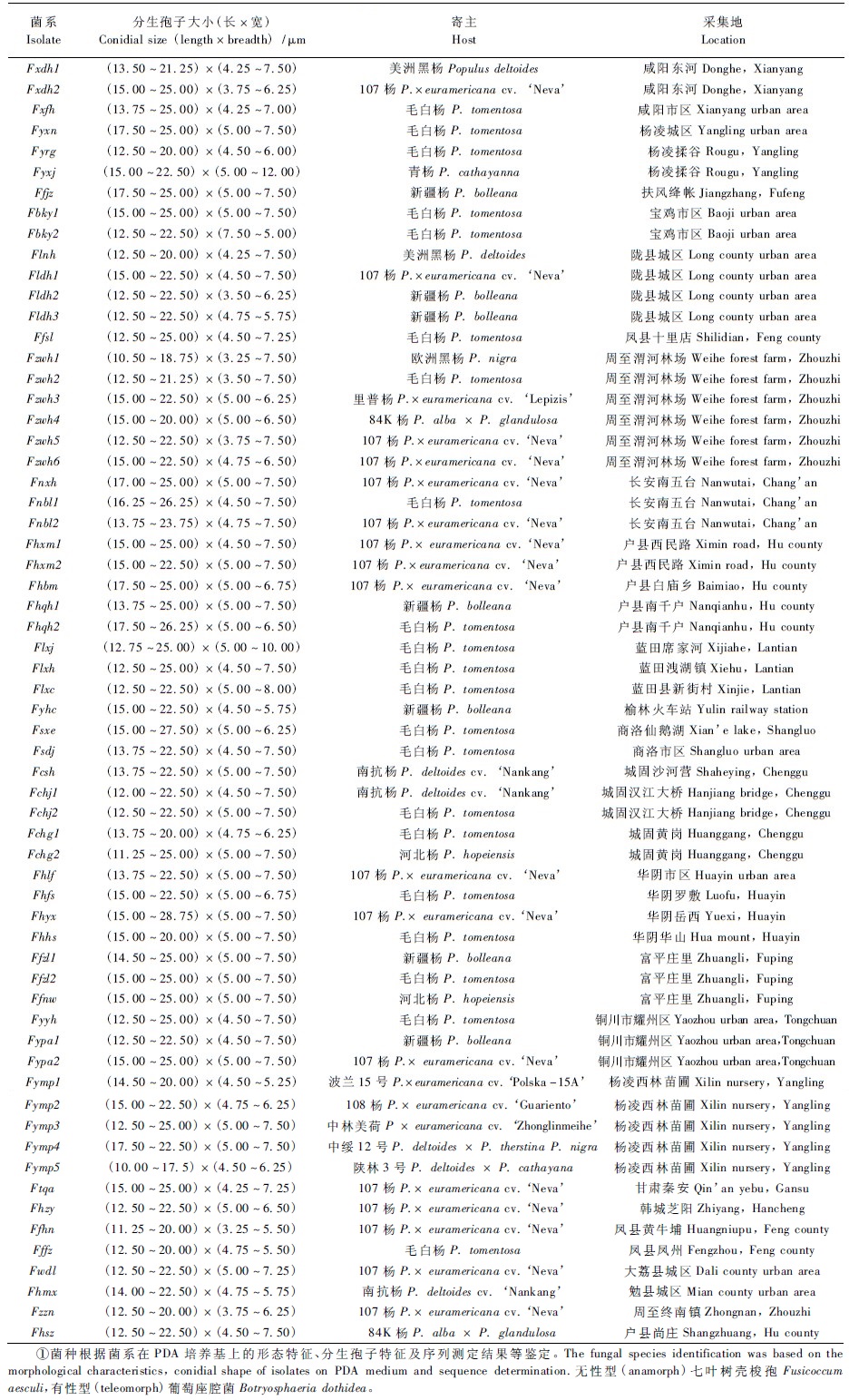
1 材料与方法 1.1 试验材料2011年5月—2012年10月分别在陕西省西安市、宝鸡市、榆林市、汉中市和甘肃省天水市等地设立调查、采集点,随机抽样法采集各杨树品种具有典型水泡型溃疡病症状的树皮组织,按常规方法分离、纯化并保存菌种,选取其中56个杨树水泡型溃疡病菌菌系及西北农林科技大学森林病理实验室2009年保存6个杨树水泡型溃疡病菌菌系,共计62株作为本研究试验菌系(表 1)。
|
|
将62个菌系接种到PDA培养基(马铃薯200 g,葡萄糖20 g,琼脂粉16 g,水1 000 mL)上,置于27 ℃恒温培养箱中黑暗培养,观察并比较菌落形态、颜色变化、气生菌丝表面特征及产孢情况等,在Olympus 显微镜(CX31RTSF,配DP-25数码相机)下不同视野中随机挑选50个分生孢子测量其大小并进行显微照相。依据各菌系在PDA培养基上的形态特征、分生孢子个体发育类型和分生孢子形态与大小鉴定各菌系培养物无性型的分类地位(向玉英等,1981; 邵力平等,1984; 钟兆康,1985; 杨旺,1996; Sutton,1980; Slippers et al.,2004)。
1.2.2 菌丝体收集将经过无性型形态鉴定后的62个菌系活化于PDA培养基上,27 ℃黑暗培养5天。用直径5 mm 的打孔器沿菌落边缘打取7块菌饼,置入马铃薯葡萄糖液体培养基(PDB,马铃薯200 g,葡萄糖20 g,水1 000 mL)中,27 ℃、120 r·min-1震荡培养5.5天后收集菌丝团,用无菌水冲洗3次,无菌滤纸吸干水分,再用无菌滤纸包裹收集到的菌丝,置40 ℃烘箱中烘干,- 20 ℃保存备用。
1.2.3 DNA提取称取冷冻干燥菌丝约0.06 g放入无菌研钵中,迅速加入适量液氮用研磨棒研磨至粉末状后转入2 mL 离心管中。真菌基因组DNA提取采用CTAB法,参照张颖慧等(2008)、孙立夫等(2009)、姜自如等(2012)方法并做相应改进。模板DNA检测采用琼脂糖凝胶电泳法。
1.2.4 PCR扩增和测序采用通用引物ITS1(5'>TCCGTAGGTGAACCTGCGG<3'),ITS4(5'>TCCTCCGCTTATTGATATGC<3')(White et al.,1990)对核糖体内部转录间隔区ITS1 -5.8 S-ITS4序列进行扩增。扩增体系为25 μL,包括DNA模板1μL,ITS1 1μL,ITS41 μL,2 × Tap Master Mix 7.5 μL,ddH2 O14.5μL。PCR反应程序为: 94 ℃预变性2 min,55 ℃停留40 s; 93 ℃变性1 min,51℃退火30 s,72 ℃延伸1 min 30 s,共35个循环; 72 ℃再延伸10 min,4 ℃终止反应保存。分别用引物Bt2a(5' > GGTAACCAAATCGGTGCTGCTTTC < 3')/Bt2b(5' > ACCCTCAGTGTAGTGACCCTTGG C<3')和EF1-728F(5' > CATCGAGAAGTTCGAGAAGG <3')/EF1-986R(5' > TACTTGAAGGAACCCTTACC <3')对β-tubulin 基因和EF-1α基因序列进行扩增(White et al.,1990; Glass et al.,1995; Carbone et al.,1999)。扩增体系均为25 μL,包括DNA模板1 μL,正反向引物各1 μL,2 × Tap Master Mix 7 μL,ddH2O 15 μL。PCR反应程序为: 94 ℃预变性5 min; 94 ℃变性30 s,58 ℃退火30 s,72 ℃延伸1 min,共35个循环; 72 ℃再延伸7 min,4 ℃终止反应保存(冯小慧等,2012)。操作均在冰上进行。
扩增产物置4 ℃冰箱中保存。取5 μL PCR产物样品,以Marker DL2000为分子质量标准,在2%琼脂糖凝胶中100 V 稳压电泳约45 min,EB 染色15 min后观察电泳结果。所有PCR产物由上海生物工程公司进行序列测定,测序引物与扩增引物相同。
1.2.5 序列分析及系统发育树构建将所有检测序列提交GenBank,经Blast 同源性比较,根据比对的期望值(expect values)、提交序列与参比序列的一致度(identities)以及空位(gaps)综合判断每一个Blast 结果后选择参比序列。从GenBank 搜集到18条Botryosphaeria spp.基因序列作为参比序列(表 2)。
|
|
将检测序列和参比序列以FASTA 格式编辑成为一个文本文档,用Clustalx2和BioEdit 软件分别校正比对68个rDNA-ITS 序列、69个β-tubulin 基因序列和70个EF-1α基因序列,并将开始和末尾处长短不同的序列剪切整齐,得到聚类的碱基序列矩阵。用Tajima-Nei 法检测序列中性突变的稳定性。使用MEGA5.05软件中的“Sequence DataExplorer”分析构建系统树所使用序列的统计学特征(赵嘉平,2007),如序列的保守区、可变区等。分别以Fusarium solani,F.oxysporum和F.proliferatum 3种镰刀菌作为rDNA-ITS,β-tubulin和EF-1α基因序列的外类群(表 2),采用p-距离对3种基因序列进行NJ 聚类分析,以自展法(bootstrap)检测,重复1 000次(Felsenstein,1985),构建邻接树(neighborjoiningtree)。
2 结果与分析 2.1 供试菌系培养性状与无性型形态杨树水泡型溃疡病菌在PDA培养基上生长3天时菌落呈污白色绒毛状,气生菌丝发达。培养第4天起出现浅墨绿色色素沉淀,呈散点状或环状分布。多数菌系菌落在生长中后期(7 ~ 10天)呈现灰色、灰黑色至墨黑色,中央菌丝稠密、棉絮状,向上生长呈喷泉状可达培养皿盖,菌丝层较厚,部分倒伏,边缘菌丝灰色、较稀疏,呈辐射状生长。菌系Fhbm和Fzwh3生长中后期菌落呈平伏状,并有明显环状色素沉淀。依据27 ℃下PDA培养基上生长8天的菌落特征将供试菌系划分为2个菌落类群: 类群Ⅰ为典型喷泉状菌落,包括除菌系Fhbm和Fzwh3以外的60个菌系,如菌系Fbky2,Fhqh2等; 类群Ⅱ为平伏状菌落,包括菌系Fhbm和Fzwh3(图 1)。
 |
图 1 杨树水泡型溃疡病菌在PDA 上的菌落形态特征
Fig. 1 Colonial characteristics of poplar blister canker’s pathogenic fungus isolates on PDA medium
菌落类群ⅠColonial groupⅠ: 菌系Fbky2,Fhqh2 Isolates Fbky2,Fhqh2; 菌落类群Ⅱ Colonial groupⅡ: 菌系Fhbm,Fzwh3 Isolates Fhbm,Fzwh3. |
多数供试菌系在PDA培养基上培养15 ~ 45天可产生分生孢子,全壁芽殖型(holoblastic)发育,无色、单胞,纺锤形至不规则纺锤形(近棒状),基部平截或钝圆,细胞内含颗粒状物; 分生孢子大小为(12.5 ~ 25.0)μm ×(3.5 ~ 7.5)μm,菌系之间并无显著差异(表 1)。此外,多数菌系(如Fbky2,Fyxj,Fchj1等)可同时产生无色、杆状的小分生孢子(microconidia)(图 2)。采自户县白庙乡的菌系Fhbm和杨凌菌系Fyxn在PDA上难以产生分生孢子,经对这2个菌系采用划伤菌丝、近紫外光诱导等处理方法使其在PDA上培养20天左右产生分生孢子,且较大。
 |
图 2 杨树水泡型溃疡病菌分生孢子形态
Fig. 2 Conidium morphology of poplar blister canker’s pathogen isolates
分生孢子与小分生孢子Conidia and microconidia: 菌系Fbky2,Fxdh1,Fchj1,Fyrg 和Fyxn isolates Fbky2,Fxdh1,
Fchj1,Fyxn and Fyrg; 分生孢子Conidia: 菌系Flxy,Fzwh3,Fxdh2 和Fhbm Flxy,Fzwh3,Fxdh2 and Fhbm. |
依据各菌系所产生的分生孢子个体发育及其形态大小,认定均为七叶树壳梭孢(Fusicoccuma esculi),与Slippers等(2004)及Crous等(1999)所描述的Botryosphaeria dothidea无性型形态相符合。
2.2 rDNA-ITS,β-tubulin,EF-1α基因PCR扩增及序列测定与比对供试62个杨树溃疡病菌菌系的rDNA-ITS-PCR产物直接测序长度为514 ~ 560 bp,平均GC 含量54% ; β-tubulin 基因PCR产物直接测序长度为417~ 437 bp,平均GC 含量58% ; EF-1α基因PCR产物直接测序长度为265 ~ 280 bp,平均GC 含量57%。将供试菌系的rDNA-ITS,β-tubulin,EF-1α基因序列在GenBank 数据库进行Blast 同源比较,显示所有试验菌系均为葡萄座腔菌,与其相似率在97%以上,该结果与形态学鉴定结果一致。
2.3 DNA序列矩阵的特征分析对供试菌系68个rDNA-ITS 序列、69个β-tubulin序列和70个EF-1α序列进行多重比对分析表明,在rDNA-ITS 序列构成的碱基序列矩阵中,包括空位在内共有469个碱基位点,其中保守位点(conserved sites)328个,可变位点(variable sites)119个,简约信息位点(parsim-Info sites)31个,单一位点(singleton sites)88个。β-tubulin 分析数据包括空位在内共有393个碱基位点,其中保守位点92个,可变位点282个,简约信息位点58个,单一位点224个。EF-1α分析数据包括空位在内共有266个碱基位点,其中保守位点90个,可变位点168个,简约信息位点55个,单一位点102个。
2.4 rDNA-ITS,β-tubulin,EF-1α序列的聚类分析分析(表 3)显示,rDNA-ITS,β-tubulin和EF-1α基因序列的Tajima-Nei 检验值分别为- 2.764 298,- 2.740 716和- 2.423 210,核苷酸多样性值分别为0.011 945,0.035 355和0.041 348,说明各种基因序列无明显多样性,且进化稳定。rDNA-ITS,β-tubulin和EF-1α序列系统发育树的分支长度值(sum of branch lengths,SBL)或进化距离依次为0.276 304 25,0.891 805 17和0.779 918 73。
|
|
聚类分析结果表明:供试菌系在基于rDNA-ITS序列的系统发育树(图 3)中可分为2个类群: GroupⅠ包括了Fyxj,Fzzn,Fymp2,Fhzy,Fymp1,Fchj1,Fsdj,Fzwh1,Fyyh,Fzwh5,Ftqa,Fypa2,Fhqh1,Fymp5,Fnbl2,Fbky1,Ffhn,Fhhs,Fhyx,Ffzl1,Fypa1,Fzwh2,Fzwh6,Fhfs,Flxc,Fchg2,Fhxm2,Fwdl,Fnxh,Ffnw,Fcsh,Fhbm,Fhqh2,Fzwh4,Fchj2,Ffsl,Ffjz,Fsxe,Fymp3,Fldh3,Flnh,Fhmx,Fldh2,Fchg1,Fyrg,Fymp4,Flxh,Fnbl1,Fffz,Ffzl2,Fhsz,Fxfh,Flxj,Fzwh3,Fbky2,Fhxm1,Fyhc,Fhlf,Fyxn,Fxdh2和Fxdh2 共61个Fusicoccum aesculi 菌系,均与GenBank 中报道的3条Botryosphaeria dothidea 序列聚在一起; 而来自宝鸡陇县的菌系Fldh1独立成群。诸菌系与葡萄座腔菌属已知种B.parva,B.ribis关系明显较远。β-tubulin 基因序列的聚类分析结果见图 4。参试的62个菌系按照序列分析形成3个不同的分支类群: GroupⅠ包括Fsxe,Fyhc,Fhsz,Fchg1,Fhfs,Ffhn,Fzwh1,Fhbm,Fsdj,Fldh2,Fymp4,Fzwh2,Fwdl,Fyyh,Fhzy,Fhmx,Fhlf,Fymp5,Fzzn,Ffzl2,Fypa2,Fnxh,Fhqh1,Ftqa,Fzwh6,Fypa1,Fnbl2,Fhxm2,Ffjz,Fhxm1,Fzwh3,Fymp1,Fymp3,Ffnw,Fymp2,Fbky2,Fchj2,Flxh,Fcsh,Flnh,Fchg2,Flxj,Fhqh2,Flxc,Fxdh2,Fxdh2,Fhyx,Fffz,Fxfh,Ffzl1,Fhhs,Fbky1,Fnbl1,Fldh1和Fzwh5共55个菌系序列及来自GenBank中的4条B.dothidea 序列; GroupⅡ包括菌系Fchj1,Ffsl,Fldh3和Fzwh4; GroupⅢ包括采自杨凌的Fyrg,Fyxj和Fyxn 3个菌系。表明参试菌系系统发育与B.ribis 不同。
 |
图 3 62个供试菌系β-tubulin基因序列的p-距离NJ系统发育树(SBL= 0.891 805 17)
Fig. 3 Phylogenetic tree generated by p-distance NJ analysis using the β-tubulin gene sequence data for 62 isolates
|
 |
图 4 62个供试菌系β-tubulin基因序列的p-距离NJ系统发育树(SBL=0.891 805 17)
Fig. 4 Phylogenetic tree generated by p-distance NJ analysis using the β-tubulin gene sequence data for 62 isolates
|
EF-1α基因序列系统发育分析结果与β-tubulin基因序列分析大致相似(图 5),将参试62个F.aesculi菌系分为3个类群: GroupⅠ包括Fhsz,Fnxh,Fldh1,Fhqh2,Fbky2,Ffsl,Ffzl1,Fhxm1,Fzwh3,Fffz,Fhmx,Fymp4,Fzzn,Fzwh6,Fhbm,Fzwh1,Ffnw,Ffzl2,Fldh3,Ftqa,Fhhs,Fzwh2,Fnbl1,Fymp3,Fhfs,Fsdj,Ffjz,Fchj1,Fchj2,Fchg1,Fchg2,Ffhn,Fzwh5,Fnbl2,Fhzy,Fymp2,Fyyh,Fhyx,Fzwh4,Fymp5,Fhxm2,Fldh2,Fcsh,Flnh,Flxh,Fypa1,Fyhc,Fypa2,Fymp1,Fhqh1,Flxc,Fbky1,Fsxe,Fwdl,Fhlf,Flxj共56个菌系序列及GenBank 中报道的4条B.dothidea序列; GroupⅡ包括来自杨凌的Fyrg,Fyxj和Fyxn 3个菌系; GroupⅢ由咸阳的Fxfh,Fxdh2和Fxdh2 3菌系组成,显示与B.dothidea种内其他地域菌系亲缘关系较远。然而,所有参试菌系与B.parva,B.ribis关系仍然明显较远。
 |
图 5 62个供试菌系EF-1α基因序列的p-距离NJ系统发育树(SBL=0.779 918 73)
Fig. 5 Phylogenetic tree generated by p-distance NJ analysis using the EF - 1α gene sequence data for 62 isolates
|
从不同基因序列构建的3个NJ 系统发育树中可看出,采用p-距离对rDNA-ITS,β-tubulin,EF-1α基因进行测度得到的聚类结果基本一致。3个系统发育树中的GroupⅠ分别包括了61,55和56个供试菌系,占供试菌系总数的比例分别为98.3%,88.7%和90.3%,另外,β-tubulin 系统树GroupⅠ中的55个菌系和EF-1α系统树GroupⅠ中的56菌系均聚在rDNA-ITS系统树GroupⅠ中。来自杨凌的3个菌系Fyrg,Fyxj和Fyxn在β-tubulin,EF-1α基因序列构建的NJ树中均聚在一起,且独立成群,表明Fusicoccum aesculi种内菌系之间存在一定的遗传分化。
3 讨论Botryosphaeria dothidea是一种能引起杨树等树木溃疡病的重要葡萄座腔菌科真菌,长期以来国内外对其无性型的分类存在很大争议。1979年关于我国杨树水泡型溃疡病的病原菌鉴定报道以后,首次确认杨树水泡性溃疡病由真菌聚生小穴壳孢Dothiorella gregaria引起,其有性型为葡萄座腔菌B.dothidea,同物异名为B.ribis(向玉英等,1979;Arx et al.,1954; Witcher et al.,1963)。由于该病菌无性型较为常见,所以国内几乎所有的研究报道都以Dothiorella gregaria 作为病原菌(景耀等,1987;向玉英,1979; 向玉英等,1987; 杨旺,1996; 张星耀等,1999; 2003)。但Sutton(1980),Pennycook等(1985)和王金利等(2007)认为B.dothidea的无性型应为Fusicoccum aesculi,而不是D.gregaria。因为Dothiorella属真菌可在分生孢子器内产生暗色、双胞的分生孢子(Phillips et al.,2005; Crous et al.,2006)。本研究根据供试菌系在PDA培养基上的形态学特征、分生孢子特征并结合相关基因序列分析结果,将引起陕西、甘肃等地的杨树水泡型溃疡病的病原菌鉴定为七叶树壳梭孢( Fusicoccum aesculi),与有性型B.dothidea 相对应,此鉴定与国内外学者近年来的研究结果相符合。
本试验依据菌落特征将供试菌系划分为2个菌落类群: 类群Ⅰ为典型喷泉状菌落,类群Ⅱ为平伏状菌落。但从rDNA-ITS,β-tubulin和EF-1α基因序列系统进化树分类来看,不同菌落特征菌系之间并未表现明显差异。具有平伏状菌落特征的Fhbm,Fzwh3 2菌系均与大多数典型喷泉状菌落特征的菌系一起被聚在同一分子系统类群中(GroupⅠ),显示它们之间的亲缘关系很近,序列无差异。虽然培养性状与分生孢子形态特征为该病原真菌分类鉴定提供了基本依据,但试验菌系的培养性状易受培养基成分、培养温度和培养时间等因素影响,不同菌系之间、甚至同一菌系不同重复之间的形态特征都有一定差异,仅仅依靠培养特征并不足以对Botryosphaeria属真菌做出符合其亲缘关系的分类(赵嘉平等,2007),因此需要用分子系统学方法来验证形态学鉴定结果,此为Botryosphaeria spp.分类学研究趋势(Slippers et al.,2004)。
本研究中杨树水泡型溃疡病菌诸菌系3个基因位点的系统分析结果大致相似。所有供试菌系均与GenBank 中报道的Botryosphaeria dothidea序列聚在一起,而与B.parva和B.ribis亲缘关系远,该结果证实本研究根据培养学特征对杨树水泡型溃疡病菌种的鉴定结论是正确的。从rDNA-ITS 序列系统发育树来看,宝鸡陇县菌系Fldh1独立成群,与B.dothidea种内其他地域菌系的亲缘关系明显较远,但该菌系在β-tubulin和EF-1α系统树中均被划归GroupⅠ中,且在培养性状和分生孢子形态特征上与其他菌系并无差异。来自杨凌的3个菌系Fyrg,Fyxj和Fyxn 在β-tubulin,EF-1α基因序列构建的NJ树中均聚在一起,且独立成群; 咸阳的Fxfh,Fxdh2 和Fxdh23菌系也在EF-1α基因序列系统树中独立成群,表明Fusicoccum aesculi种内诸菌系间存在一定的遗传分化。杨凌揉谷菌系Fyrg和户县白庙菌系Fhbm 的培养性状表现特殊,即在PDA培养基上很难产生无性繁殖体; 接种证明周至菌系Fzwh、凤县菌系Ffhn及城固菌系Fcsh表现出较其他地域菌系强的致病性。这些表明F.aesculi在陕西存在一定的生理分化现象。但总的来看,供试菌系之间在培养性状、分生孢子形态及致病性等方面的差异与其分子系统发育类群分化并不存在明显对应关系,其机制还需进一步研究。
| [1] |
冯小慧, 张星耀, 严东辉. 2012. 杨树溃疡病病原的多重PCR检测技术. 林业科学, 48 (5): 73-77.( 1) 1)
|
| [2] |
姜自如, 张刚龙, 曹支敏, 等. 2012. 陕西省杨树溃疡病菌地理种群研究. 西北林学院学报, 27 (2): 102-108.( 1) 1)
|
| [3] |
景耀, 刘会香. 1987. 杨树和核桃溃疡病菌的交叉接种试验. 森林病虫通讯, (2): 11-13.( 1) 1)
|
| [4] |
刘会香, 景 耀, 赵仕光, 等. 1997. 杨树溃疡病菌三菌系形态和生理学特性的研究. 西北林学院学报, 12 (3): 18-23.( 1) 1)
|
| [5] |
邵力平, 沈瑞祥, 张素轩. 1984. 真菌分类学. 北京: 中国林业出版社.( 1) 1)
|
| [6] |
孙立夫, 张艳华, 裴克全. 2009. 一种高效提取真菌总DNA的方法. 菌物学报, 28 (2): 299-302.( 1) 1)
|
| [7] |
王金利, 贺 伟, 秦国夫, 等. 2007. 树木溃疡病重要病原葡萄座腔菌属、种及其无性型研究. 林业科学研究, 20 (1): 21-28.( 3) 3)
|
| [8] |
王金利, 秦国夫, 贺 伟, 等. 2003. 葡萄座腔菌属及其相关真菌的系统学研究进展. 中国森林病虫, 22 (3): 32-36.( 1) 1)
|
| [9] |
吴小芹, 何月秋, 刘忠华. 2001. 葡萄座腔菌属所致树木溃疡病发生与研究. 南京林业大学学报, 25 (1): 61-66.( 1) 1)
|
| [10] |
向玉英. 1987. 杨树病害及其防治. 北京: 中国林业出版社.( 1) 1)
|
| [11] |
向玉英, 花晓梅, 赵经周. 1979. 杨树水泡型溃疡病的病原鉴定. 微生物学报, 19 (1): 57-63.( 2) 2)
|
| [12] |
向玉英, 花晓梅, 赵经周, 等. 1981. 杨树溃疡病的发生及病原菌的生物学特性的研究. 植物病理学报, 11 (4): 27-33.( 1) 1)
|
| [13] |
杨旺. 1996. 森林病理学. 北京: 中国林业出版社.( 2) 2)
|
| [14] |
余仲东, 曹支敏, 张星耀. 2000. 真菌核糖体基因间隔区研究概况. 西北林学院学报, 15 (2): 107-112.( 1) 1)
|
| [15] |
余仲东, 曹支敏, 张星耀. 2004. 杨树溃疡病、苹果轮纹病等病原菌的ITS-rDNA-RFLP解析. 中国森林病虫, 23 (2): 15-17.( 1) 1)
|
| [16] |
余仲东, 赵官成, 淡静雅, 等. 2010. 葡萄座腔菌属ITS-nrDNA的分子系统学分析. 菌物学报, 29 (2): 285-293.( 2) 2)
|
| [17] |
张星耀, 骆有庆. 2003. 中国森林重大生物灾害. 北京: 中国林业出版社.( 2) 2)
|
| [18] |
张星耀, 赵嘉平, 梁 军, 等. 2008. 树木枝干溃疡病菌致病力分化研究. 中国森林病虫, 27 (1): 1-4.( 1) 1)
|
| [19] |
张星耀, 赵仕光, 朴春根, 等. 1999. 树木溃疡病病原真菌类群分子遗传多样性研究Ⅰ——小穴壳属、疣壳孢属、壳囊孢属、盾壳霉属分类地位的分子证明. 林业科学, 35 (3): 34-40.( 3) 3)
|
| [20] |
张星耀, 赵仕光, 吕 全, 等. 2000. 树木溃疡病病原真菌类群分子遗传多样性研究Ⅱ——Botryosphaeria属28SrDNA-PCR-RFLP和RAPD解析. 林业科学, 36 (2): 75-81.( 2) 2)
|
| [21] |
张颖慧, 魏东盛, 邢来君, 等. 2008. 一种改进的丝状真菌DNA提取方法. 微生物学通报, 35 (3): 466-469.( 1) 1)
|
| [22] |
赵嘉平. 2007. 树木溃疡病菌-葡萄座腔菌属及其相关真菌系统分类研究. 北京: 中国林业科学研究院博士学位论文.( 1) 1)
|
| [23] |
赵嘉平, 梁军, 吕全, 等. 2007. 葡萄座腔菌属系统分类评述. 林业科学研究, 20 (3): 415-422.( 1) 1)
|
| [24] |
钟兆康. 1985. 几种杨树溃疡病的识别与防治, 林业科技通讯, (6): 28-31.( 1) 1)
|
| [25] |
Arx J A von, Müller E. 1954. Die Gattungen der amerosporen Pyrenomyceten. Beitruge zur Kryptogamenflora der Schweiz, 11(1): 1-434.( 1) 1)
|
| [26] |
Carbone I, Anderson J B, Kohn L M. 1999. A method for designing primer sets for speciation studies in filamentous ascomycetes. Mycologia, 91 (3): 553-556.( 1) 1)
|
| [27] |
Crous P W, Palm M E. 1999. Reassessment of the anamorph genera Botryodiplodia, Dothiorella and Fusicoccum. Sydowia, 51 (2): 167-175.( 1) 1)
|
| [28] |
Crous P W, Slippers B, Wingfield M J, et al. 2006. Phylogenetic lineages in the Botryosphaeriaceae. Studies in Mycology, 55(1): 235-253.( 2) 2)
|
| [29] |
Denman S, Crous P W, Tavlor J E, et al. 2000. An overview of the taxonomic history of Botryosphaeria and a re-evaluation of its anamorphs based on morphology and ITS rDNA phylogeny. Studies in Myxology, 45: 129-140.( 1) 1)
|
| [30] |
Felsenstein J. 1985. Confidence intervals on phylogenetics: an approach using bootstrap. Evolution, 39 (4): 783-791.( 1) 1)
|
| [31] |
Glass N L, Donaldson G C. 1995. Development of primer sets designed for use with the PCR to amplify conserved genes from filamentous Ascomycetes. Applied and Environment Microbiology, 61 (4): 1323-1330.( 1) 1)
|
| [32] |
Grasso F M, Granata G. 2010. First report of Botryosphaeria dothidea associated with dieback of aspen (Populus tremula) in Italy. Plant Pathology, 59 (4): 807.( 1) 1)
|
| [33] |
Kirk P M, Cannon P F, Minter D W, et al. 2008. Dictionary of the Fungi (10th Edition). CABI Europe-UK, 100.( 1) 1)
|
| [34] |
Pennycook S R, Samuels G J. 1985. Botryosphaeria and Fusicoccum species associated with ripe fruit rot of Actinidia deliciosa (kiwifruit) in New Zealand. Mycotaxon, 24: 445-458.( 1) 1)
|
| [35] |
Phillips A J L, Alves A, Correia A, et al. 2005. Two new species of Botryosphaeria with brown, 1-septate ascospores and Dothiorella anamorphs. Mycologia, 97(2): 513-529.( 2) 2)
|
| [36] |
Slippers B, Crous P W, Denman S, et al. 2004. Combined multiple gene genealogies and phenotypic characters differentiate several species previously identified as Botryosphaeria dothidea. Mycologia, 96 (1): 83-101.( 5) 5)
|
| [37] |
Sutton B C. 1980. The Coelomycetes. Commonwealth Mycological Institute, Kew, UK, 1-696.( 2) 2)
|
| [38] |
White T J, Bruns T, Lee S, et al. 1990. Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenetics.//Innis M A, Gelfand D H, Snisky J J, et al. PCR Protocols: a sequencing guide to methods and applications. San Diego: Academic Press, 315-322.( 2) 2)
|
| [39] |
Witcher W, Clayton N. 1963. Blueberry stem blight caused by Botryosphaeria dothidea (B.ribis). Phytopathology, 53: 705-712.( 1) 1)
|
 2014, Vol. 50
2014, Vol. 50