文章信息
- 赵娜, 孟平, 张劲松, 陆森, 程志庆
- Zhao Na, Meng Ping, Zhang Jinsong, Lu Sen, Cheng Zhiqing
- 华北低丘山地不同土地利用条件下的土壤呼吸比较
- Comparison of Soil Respiration under Various Land Uses in Hilly Area of Northern China
- 林业科学, 2014, 50(2): 1-7
- Scientia Silvae Sinicae, 2014, 50(2): 1-7.
- DOI: 10.11707/j.1001-7488.20140201
-
文章历史
- 收稿日期:2013-09-22
- 修回日期:2014-01-03
-
作者相关文章
2. 国家林业局林木培育重点实验室 北京 100091
2. Key Laboratory of Tree Breeding and Cultivation of State Forestry Administration Beijing 100091
全球气候变暖及其影响已成为当前全世界关注的焦点,其中最重要的温室气体CO2在大气中的含量以每年0.4%的速度在增长(陈泮勤等,2004)。土壤呼吸是陆地碳循环中仅次于全球总初级生产力的碳通量途径(Raich et al.,1995),平均每年向大气释放60~110 PgC(Bond-Lamberty et al.,2010),超过化石燃料释放碳的11倍(Marland et al.,1994),是陆地碳循环中最大的碳源(Raich et al.,2002),且其细微变化有可能引起大气CO2浓度的明显改变。研究表明,土壤呼吸对全球气候变化响应明显(Boone et al.,1998),且具有反馈作用(Davidson et al.,2006)。
土地利用方式变化通过改变辐射特征、植物的蒸腾作用等影响土壤温湿度(Raich et al.,1995),使土壤有机质含量、微生物的组成和活性、根系生物量等发生改变,从而影响土壤呼吸过程(骆亦其等,2007),并直接影响陆地生态系统碳循环过程,最终导致生态系统碳源汇功能的变化。20世纪90年代全球土地利用变化向大气排放了1.6 PgC·a-1,仅次于化石燃料燃烧释放的碳(7.2 PgC·a-1),是大气中的第二大人为碳源(Raich et al.,1995)。因此,系统研究土地利用变化所引起的土壤呼吸变化一直是生态学、农学及林学等相关学科重点关注的研究内容。
近20年来,我国对生态脆弱重点区域(如“三北”、长江中上游等地区)进行生态恢复与重建,土地利用方式也发生了较大改变,与此同时构建形成了具生态效益的多龄级人工林。林龄在森林碳库分配及不同生态系统碳通量差异中扮演着重要角色,其差异会引起森林生态系统碳平衡的变化,进而形成不同的土壤呼吸特征(Baggs,2006)。相关研究表明,人工林林龄与森林碳通量之间的关系存在极大的不确定性(Singh et al.,1977),土壤CO2通量随林龄变化呈现出复杂的格局。刺槐(Robinia pseudoacacia)属植被恢复的先锋树种,且具有固氮、改良土壤的作用,是华北低丘山地主要退耕造林树种之一。但在该区域,不同土地利用条件下(特别是退耕还林工程的实施所引起的)土壤碳循环过程的变化研究至今仍较罕见。因而,系统地分析退耕地内多龄级刺槐人工林的土壤呼吸及碳循环过程,对评价该区域的生态系统碳循环与退耕还林生态效益都具有重要意义。本研究依托森林生态定位监测系统,对华北南部低丘山地的退耕还林重点区域进行定量观测,以撂荒地和农田为对照,分析退耕后不同林龄刺槐林地的土壤呼吸动态变化特征及其与环境因子的关系,为评估该区域的退耕还林碳效益与生态效益提供理论依据。
1 研究区概况本研究在河南省济源市黄河小浪底森林生态系统研究站(112° 28' E,35° 01' N)进行。研究区位于华北南部低山丘陵退耕还林工程区内,南邻黄河小浪底水利枢纽工程,北依太行山南麓,是典型的低山丘陵石质山区,属暖温带大陆性季风气候。试验区全年日照2 367.7 h;多年平均降水量641.7 mm,6—9月降水量占全年的68.3%;土壤以石灰岩风化母质淋溶性褐色土为主,土层厚度为50~80 cm。研究区内有农田、农田撂荒地和多龄级退耕人工林地等多种土地利用类型。
2 研究方法 2.1 试验设计2011年12月,遵循试验样地与周边环境一致性原则,避开林缘带状区域,在土壤类型、地势起伏及海拔相近的半阳坡研究区内,选取农田(CL)、农田撂荒地(AL)、退耕10年刺槐人工林地(R10)和退耕43年刺槐人工林地(R43)4种土地利用类型为研究对象,并在每种土地利用条件下各设置3个20 m×33 m固定样地。其中,农田的种植制度为冬小麦(Triticum aestivum)与夏玉米(Zea mays)轮作;农田撂荒地内的主要植被为构树(Broussonetia papyrifera)和狗尾草(Setaira viridis);退耕刺槐人工林内的主要植被为刺槐,林下植被主要为扁担木(Grewia biloba var. parviflora)、蛇莓(Duchesnea indica)和狗尾草等。4种土地利用类型概况见表 1。
|
|
2012-03—2013-02,利用基于红外分析法的Li-8100土壤呼吸自动测量系统(Li-cor.,USA)观测不同土地利用条件下的土壤呼吸速率变化。本研究中,在每种土地利用条件下的每块样地内分别随机设置了9个土壤呼吸测定点。在每个测定点处,将PVC环(直径9 cm,高9 cm)纵向插入土中7 cm,露出地表 2 cm,待PVC环与土壤接触紧密后(平衡7天)进行土壤呼吸测定。在测定期内,每月初与月末各观测1次,观测时段均为9∶ 00—11∶ 00(Maestre et al.,2003)。
在观测土壤呼吸速率的同时,同步采用土壤温湿度计W. E. T Sensor(ΔT device,UK)测定5 cm深处的土壤温度(Ts)、土壤体积含水率(W)和电导率(ECp)。同时采集每个测定土壤呼吸速率PVC环附近的土壤,采样深度分别为0~5,5~10和10 ~20 cm,用于土壤有机质含量测定。
2.3 数据分析运用SPSS 18.0软件完成方差分析与回归分析,并利用Excel绘制图像。采用方差分析中的单因素ANOVA方法,运用LSD方法检验不同土地利用方式下的土壤有机质含量(0~10 cm)、土壤温度(Ts)、土壤水分(W)、土壤电导率(ECp)和土壤呼吸速率(Rs)均值间是否存在差异。运用回归分析中的曲线估计讨论土壤呼吸与土壤温度、土壤水分含量及土壤电导率间的回归模型和曲线拟合度。
本研究运用van't Hoff模型来定量模拟土壤呼吸和土壤温度间的关系,该模型如下(Lloyd et al.,1994):
| ${R_{\rm{s}}} = {R_0}{{\rm{e}}^{b{T_s}}}$。 | (1) |
式中: Rs为土壤呼吸速率(μ mol·m-2 s-1);R0为土壤温度为0℃时的土壤呼吸速率;b为模型参数;Ts为土壤温度(℃)。
土壤呼吸速率对温度变化的敏感度通常用Q10值来描述(骆亦其等,2007),Q10值定义为温度每升高10℃土壤呼吸速率所增加的倍数,即:
| ${Q_{{\rm{10}}}} = {R_{{T_0} + 10}}{\rm{/}}{R_{{T_0}}}$。 | (2) |
式中: RT0和RT0+10分别是参比温度T0和温度为T0+10℃时的呼吸速率。依据地温与土壤呼吸速率间的拟合函数,可对Q10值进行估算(Lee et al.,2003):
| ${Q_{{\rm{10}}}} = {{\rm{e}}^{10b}}$。 | (3) |
由表 2可知,退耕43年刺槐林0~10 cm土层土壤有机质含量显著高于其他土地利用条件,且随着退耕年限增加,刺槐人工林0~10 cm土层土壤有机质含量增加显著。与农田相比,退耕10年和43年刺槐林0~5 cm土层的土壤有机质含量分别是农田的1.6和3.9倍。此外,研究发现退耕刺槐林和撂荒地的土壤有机质分布具有明显的表聚性(0 ~10 cm);随着土层深度增加,退耕刺槐林和撂荒地的土壤有机质含量逐渐降低。而农田由于频繁翻耕,其土壤有机质含量随土层的变化不明显。
|
|
2012-03—2013-02,退耕43年刺槐林、退耕10年刺槐林、撂荒地及农田的月均土壤温度均呈现明显的单峰季节变化曲线(图 1)。各土地利用条件下5 cm深处土壤温度的最小值均出现于1月;除农田外,其他土地利用条件下的土壤温度均在7月达到全年最大值。除冬季差异不显著外,农田在全年各月份的土壤温度均高于2个退耕刺槐林(P<0.05),同时退耕43年刺槐林的月均温高于退耕10年刺槐。由于试验测定期内的5—6月气温较高而降雨较少,因此造成各土地利用条件下的土壤体积含水量大幅降低;7月试验区进入雨季,土壤体积含水量于8月达到最大值;1月达全年最小值。除1月及4月外,退耕10年刺槐林的月均土壤体积含水量均高于农田(P<0.05),但退耕10年与43年刺槐林土壤体积含水量间差异不显著。除5和6月外,农田土壤电导率均显著高于退耕刺槐林(P<0.05),这与农田内施肥措施所引起的土壤盐分增加密切相关。
由图 1可知,退耕43年刺槐林、退耕10年刺槐林、撂荒地和农田的土壤呼吸速率变化趋势与5 cm深处土温变化趋势基本一致。随着土壤温度升高,土壤呼吸速率也逐渐上升,退耕43年刺槐林、退耕10年刺槐林和撂荒地的土壤呼吸速率均在7月达到最大,随后逐渐下降。农田土壤呼吸速率出现2次峰值(4和9月),这是由于在4月,冬小麦正处于拔节期,小麦根系生长迅速,呼吸旺盛(3.56 μmol·m-2s-1);而到9月玉米成熟,土壤呼吸再次达到峰值(3.27 μmol·m-2 s-1)。6月的农田土壤呼吸速率较低,主要由于小麦在该月上旬收获,而玉米在6月下旬刚播种。在冬季,由于气候寒冷,植被处于休眠状态,因此各土地利用条件下土壤呼吸最小值均出现于温度较低的1月。2,3月农田土壤呼吸速率值均显著高于退耕刺槐林(P<0.05);而在5—10月,退耕43年刺槐林土壤呼吸速率显著高于农田;冬季各土地利用条件下土壤呼吸速率差异不显著。退耕10年刺槐林月均土壤呼吸速率在测定期内均低于其他土地利用条件。4种土地利用条件下年均土壤呼吸速率表现为撂荒地>退耕43年刺槐林>农田>退耕10年刺槐林(P<0.05),这是由于退耕刺槐林在幼林阶段土壤CO2排放较少,随着林龄增加,土壤固碳能力增加,土壤CO2排放量也逐渐增大。
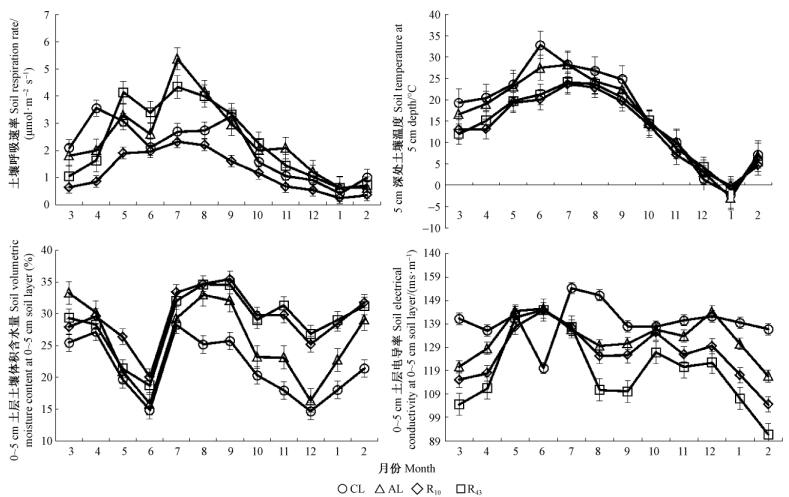 |
图 1 4 种土地利用条件下土壤呼吸速率、 5 cm 深处土壤温度、0 ~ 5 cm 土层土壤体积含水量和 0 ~ 5 cm 土层电导率的季节变化
Fig. 1 Seasonal variation of soil respiration rate,soil temperature at 5 cm depth,soil moisture content and soil electrical conductivity at 0 ~ 5 cm soil layer under four land uses
|
4种土地利用条件下土壤呼吸速率与土壤温度间均极显著指数相关(P<0.01,图 2),5 cm深处土壤温度可以解释各土地利用条件下土壤呼吸速率季节变化的53.67%~79.50%。退耕10年刺槐林、退耕43年刺槐林、撂荒地和农田的土壤呼吸温度敏感系数(Q10)分别为2.53,2.47,2.06和1.56,可见退耕刺槐人工林和撂荒地的土壤CO2排放对温度变化的敏感度显著高于农田。
 |
图 2 土壤呼吸速率与土壤温度的关系
Fig. 2 Relationship between Rs and Ts for four land use types
|
SPSS相关分析(表 3)表明,4种土地利用条件下土壤呼吸速率与土壤体积含水量及土壤电导率间的相关性较低,线性回归模型的决定系数均低于0.2,表明4种土地利用条件下土壤呼吸受土壤体积含水量、电导率的影响作用较小。
|
|
本研究分别计算春(3—4月、翌年2月)、夏(5—7月)、秋(8—10月)和冬(11月至翌年1月)4个时期的Q10值。由表 4可见,除撂荒地外,其他土地利用条件下的Q10值随季节变化趋势相似,即Q10值均在夏季最低、冬季最高,说明在温度较低的冬季,土壤呼吸对温度变化的响应更加明显。表 4表明,Q10与季节平均地温负相关,但各样地在夏季的土壤呼吸速率与土壤温度的决定系数R2值均低于其余3个季节。土壤体积含水量通过影响土壤呼吸速率进而影响Q10值的季节变化。由于4种土地利用条件下的土壤体积含水量为0.15~0.35 cm3·cm-3,土壤水分较充足,且变化范围较小,不足以影响植物根系和土壤微生物的活动,难以区分出土壤含水量对Q10值的影响(张惠东等,2011),同时也存在土壤体积含水率对土壤呼吸速率的影响作用被其他影响因子所遮蔽的可能。
|
|
退耕还林还草措施在不同程度上可使土壤有机质含量得到恢复(彭文英等,2005)。在本研究中,退耕人工林0~5 cm土层的土壤有机质含量显著高于农田,这是由于林地土壤表层存在丰富的植物凋落物残体,其在分解过程中形成有机物质,补充了土壤碳库(Bouwman et al.,1995;董莉丽等,2009)。而传统种植方法对农田重收轻养,且翻耕措施显著地影响着土壤有机质含量,因此农田土壤有机质含量比较低(邱莉萍等,2006)。本研究发现,退耕仅10年的刺槐人工林其土壤表层有机质含量已接近自然恢复40年的撂荒地,这说明在该研究区域内,营造刺槐人工林是增强土壤固碳能力的有效方式;该结果和彭文英等(2005)关于刺槐人工林恢复土壤养分的能力优于撂荒地的结论一致。
土壤呼吸速率计算结果表明,退耕10年刺槐人工林的年平均土壤呼吸速率较农田降低40.69%,而退耕43年刺槐林的土壤CO2排放量则比农田增加了14.22%。这是由于在造林初期,来自森林的碳增加并不能抵消来自农田的碳分解,因而退耕人工林初期土壤呼吸速率一般较小(王春梅等,2007)。随着刺槐林龄的不断增长,土壤呼吸速率也逐渐增大,这与Wiseman等(2004)和Jiang等(2005)的研究结果一致,即土壤呼吸与刺槐根系的生长及土壤固碳能力密切相关。相关研究表明,不论在扰动还是非扰动系统内,土壤呼吸一般均与土壤有机质含量呈显著正相关(Chen et al.,2010)。在本研究区内,当农田退耕为林地后,林龄的增大不仅使树木根系变得庞大(表 1),根系呼吸增强,同时也增加了凋落物,使得土壤有机质含量得到提高,促进了土壤微生物的生长和呼吸。与刺槐林地相比,由于每年重复的耕作、施肥、播种和收获等田间管理措施,农田土壤结构和微生物群落受到了剧烈干扰,降低了土壤CO2释放速率(Larionova et al.,1998;Canadell et al.,2008)。
综合分析土壤温度、水分、电导率等环境因子对土壤呼吸的影响,研究发现4种土地利用条件下的土壤呼吸主要受土壤温度影响,土壤水分对土壤CO2排放的影响贡献率均较小,这与前人的研究结果(张劲松等,2008)相似。此外,一些研究(孙波等,1999;王效举等,1997)表明,与土壤性质密切相关的土壤电导率可以作为土壤质量综合评价的一个定量指标,因为土壤电导率可以综合反映土壤的水分状况、盐分浓度和微生物生长等多种性状。在不同土壤电导率下,微生物群落对盐胁迫和离子中毒的适应机制会发生变化,进而导致土壤气体的排放产生差异。一般地,当土壤湿度恒定时,随着土壤电导率的增大,土壤微生物呼吸减弱,土壤CO2排放量减少(Adviento-Borbe et al.,2006)。因而,本研究对土壤电导率对土壤呼吸的影响进行了分析,结果表明退耕10年刺槐林土壤呼吸与土壤电导率间虽存在显著相关,但R2值偏低,仅能解释土壤呼吸的15.3%,而其他土地利用条件下的土壤呼吸与土壤电导率间均无显著相关关系。因而,在本试验区内土壤电导率并不是影响土壤呼吸的关键因子。
Q10值反映着土壤呼吸对温度变化的敏感性。在本研究中,不同林龄刺槐林地的Q10均接近于全球中位值(约2.4)(Raich et al.,1992)。此外,本研究区域农田的Q10值显著低于退耕林地,考虑到退耕林地的高土壤碳储量和高Q10值,应尽量减少人类活动对该区域刺槐人工恢复林的干扰。一般地,Q10值存在显著的季节变异,随着增温时间的延长,土壤呼吸速率的增幅往往减小甚至停止,对温度变化的敏感程度降低,表现出温度适应性(Oechel et al.,2000)。在本研究中,4种土地利用类型的Q10值均随着温度降低而增大,呈现出显著的季节变异,这与Jassens等(2003)的研究结果一致,即Q10的季节变化与土壤温度负相关(王光军等,2008)。
以退耕还林为主的植被恢复工程对区域生态系统碳循环及温室气体排放产生了重大影响。本研究在华北南部低丘山区退耕还林地的试验表明,退耕还林措施可显著增加土壤有机质含量;且伴随着林龄增长,土壤固碳能力不断增强,林地内土壤呼吸速率也逐渐增大;在研究区域内,土壤呼吸速率主要受土壤温度影响,退耕刺槐林地的土壤呼吸速率对温度变化的敏感度高于农田。因而,气候变化引起的温度升高对退耕刺槐人工林的土壤呼吸影响远大于农田,人类活动应尽量避免对退耕人工林的过度干扰。
| [1] |
陈泮勤, 黄 耀,于贵瑞.2004.地球系统碳循环.北京:科学出版社.( 1) 1)
|
| [2] |
董莉丽,郑粉莉. 2009. 土地利用类型对土壤微生物量和有机质的影响. 水土保持学报,29(6): 10-15.( 1) 1)
|
| [3] |
骆亦其,周旭辉.2007. 土壤呼吸与环境. 姜丽芬,等.译. 北京: 高等教育出版社.( 2) 2)
|
| [4] |
彭文英,张科利,陈 瑶,等. 2005. 黄土坡耕地退耕还林后土壤性质变化研究. 自然资源学报,20(2): 272-278.( 2) 2)
|
| [5] |
邱莉萍,张兴昌. 2006. 子午岭不同土地利用方式对土壤性质的影响. 自然资源学报,21(6): 965-972.( 1) 1)
|
| [6] |
孙 波,赵其国. 1999. 红壤退化中的土壤质量评价指标与评价方法. 地理科学进展,18 (2): 118-128.( 1) 1)
|
| [7] |
王春梅,刘艳红,邵 彬. 2007. 量化退耕还林后土壤碳变化. 北京林业大学学报,29(3): 112-119.( 1) 1)
|
| [8] |
王光军,田大伦,朱 凡,等. 2008. 长沙樟树人工林生长季土壤呼吸特征. 林业科学,44(10): 20-24.( 1) 1)
|
| [9] |
王效举,龚子同. 1997. 红壤丘陵小区域水平上不同时段土壤质量变化评价和分析. 地理科学,17 (2): 141-148.( 1) 1)
|
| [10] |
张惠东,尤文忠,邢兆凯,等. 2011. 辽东山区天然次生林和落叶松人工林的土壤呼吸. 水土保持学报,25(3): 198-224.( 1) 1)
|
| [11] |
张劲松,孟 平,王鹤松,等. 2008. 华北石质山区刺槐人工林的土壤呼吸. 林业科学,44(2): 8-14.( 1) 1)
|
| [12] |
Adviento-Borbe M A A, Doran J W, Drijber R A, et al. 2006. Soil electrical conductivity and water content affect nitrous oxide and carbon dioxide emissions in intensively managed soils. Journal of Environmental Quality, 35 (6): 1999-2010.( 1) 1)
|
| [13] |
Baggs E M. 2006. Partitioning the components of soil respiration: a research Challenge. Plant and Soil, 284 (1/2): 1-5.( 1) 1)
|
| [14] |
Bond-Lamberty B, Thomson A. 2010. Temperature-associated increases in the global soil respiration record. Nature, 464 (7288): 579-582.( 1) 1)
|
| [15] |
Boone R D, Nadelhoffer K J, Canary J D, et al. 1998. Roots exert a strong influence on the sensitivity of soil respiration. Nature, 396 (6711): 570-572.( 1) 1)
|
| [16] |
Bouwman A F, Leemans R. 1995. The role of forest soils in the global carbon cycle//Mcfee W W, Kelly J M. Carbon forms and functions in forest soils. Madison, WI, USA: Soil Science Society of America, 503-525.( 1) 1)
|
| [17] |
Canadell J G, Raupach M R. 2008. Managing forests for climate change mitigation. Science, 320 (5882): 1456-1457.( 1) 1)
|
| [18] |
Chen S T, Huang Y, Zou J W, et al. 2010. Modeling interannual variability of global soil respiration from climate and soil properties. Agricultural and Forest Meteorology, 150 (4): 590-605.( 1) 1)
|
| [19] |
Davidson E A, Janssens I A. 2006. Temperature sensitivity of soil carbon decomposition and feedbacks to climate change. Nature, 440 (7081): 165-173.( 1) 1)
|
| [20] |
Jassens I A, Pilegaard K. 2003. Large seasonal changes in Q10 of soil respiration in a beech forest. Global Change Biology, 9 (6): 911-918.( 1) 1)
|
| [21] |
Jiang L, Shi F, Li B, et al. 2005. Separating rhizosphere respiration from total soil respiration in two larch plantations in northeastern China. Tree Physiology, 25 (9): 1187-1195.( 1) 1)
|
| [22] |
Larionova A A, Yermolayev A M, Blagodatsky S A, et al. 1998. Soil respiration and carbon balance of gray forest soils as affected by land use. Biology and Fertility Soil, 27 (3): 251-257.( 1) 1)
|
| [23] |
Lee K H, Jose S. 2003. Soil respiration and microbial biomass in a pecan-cotton alley cropping system in Southern USA. Agroforestry Systems, 58 (1): 45-54.( 1) 1)
|
| [24] |
Lloyd J, Taylor J A. 1994. On the temperature dependence of soil respiration. Functional Ecology, 8: 315-323.( 1) 1)
|
| [25] |
Maestre F T, Cortina J. 2003. Small-scale spatial variation in soil CO2 efflux in a Mediterranean semiarid steppe. Applied Soil Ecology, 23 (3): 199-209.( 1) 1)
|
| [26] |
Marland G, Boden T A, Andres R J. 1994. Globe, regional and national CO2 emissions//Boden T A, Kaiser D P, Sepanski R J, et al. Trends'93: a compendium of data on global change. Tennessee, USA: Carbon Dioxide Information Analysis Center, 505-584.( 1) 1)
|
| [27] |
Oechel W C, Vourlitis G L, Hastings S J, et al. 2000. Acclimation of ecosystem CO2 exchange in the Alaskan Arctic in response to decadal climate warming. Nature, 406 (6799): 978-981.( 1) 1)
|
| [28] |
Raich J W, Potter C S. 1995. Global patterns of carbon dioxide emissions from soils. Global Biogeochemical Cycles, 9 (1): 23-36.( 3) 3)
|
| [29] |
Raich J W, Potter C S, Bhagawati D. 2002. Interannual variability in global soil respiration. Global Change Biology, 8 (8): 800-812.( 1) 1)
|
| [30] |
Raich J W, Schlesinger W H. 1992. The global carbon dioxide flux in soil respiration and its relationship to vegetation and climate. Tellus B, 44 (2): 81-99.( 1) 1)
|
| [31] |
Singh J S, Gupta W H. 1977. Plant decomposition and soil respiration in terrestrial ecosystems. The Botanical Review, 43 (4): 449-529.( 1) 1)
|
| [32] |
Wiseman P E, Seiler J R. 2004. Soil CO2 efflux across four age classes of plantation loblolly pine (Pinus taeda L.) on the Virginia Piedmont. Forest Ecology and Management, 192 (2): 297-311.( 1) 1)
|
 2014, Vol. 50
2014, Vol. 50

