文章信息
- 孙妙, 杨周婷, 张存莉, 魏安智, 史伟
- Sun Miao, Yang Zhouting, Zhang Cunli, Wei Anzhi, Shi Wei
- 中国沙棘种子的水引发技术及其抗性生理效应
- Hydro-Priming Technique and Its Resistance Physiology Effect for Sea Buckthorn Seed
- 林业科学, 2014, 50(12): 32-39
- Scientia Silvae Sinicae, 2014, 50(12): 32-39.
- DOI: 10.11707/j.1001-7488.20141205
-
文章历史
- 收稿日期:2014-01-22
- 修回日期:2014-07-10
-
作者相关文章
2. 陕西海升果业股份有限公司渭南分公司 渭南 715206;
3. 西北农林科技大学林学院 杨凌 712100
2. Weinan Branch, Shaanxi Haisheng Fresh Fruit Juice Co. Ltd. Weinan 715206;
3. College of Forestry, Northwest A & F University Yangling 712100
种子引发也称种子渗透调节,是在控制条件下使种子缓慢定量吸水、为萌发提前进行生理准备的种子播前处理技术(Heydecker et al., 1973)。种子引发引起细胞周期蛋白的变化(Muchena et al., 1972; Garcia,1997),促进种子RNA以及细胞核DNA的合成(Davison et al., 1991; Sung et al., 1993),诱导与抗逆有关的基因表达(Gao et al., 1999),故能增强种子活力、缩短种子萌发时间,使出苗整齐均一,且能提高种子抗旱、抗寒及抗盐渍等能力(Song et al., 1999; Kaya et al., 2006)。
中国沙棘(Hippophae rhamnoides subsp. sinensis)是胡颓子科(Elaeagnaceae)沙棘属落叶灌木,具有较好的抗风沙、耐旱、耐瘠薄、耐盐碱及根瘤固氮的特性(李怀恩等,2007; 吴清风等,2002; 孙坤等,2012),是荒漠化防治和改善土壤质量的重要树种。但是其种子抗性不强,在干旱、盐碱等逆境条件下的发芽能力差、成活率低,必须先在适宜的条件下发芽、育苗,待幼苗长成后再进行人工栽植。因此,研究促进中国沙棘种子萌发与出苗的方法,提高种子萌发率、种子活力和抗逆性具有重要意义。沙棘种子萌发的相关研究主要集中在温度(孙坤等,2012)、渗透调节(张虎平等,2008)和药物浸种(郑蔚虹等,2003; 张俊风等,2010)等方面,而水引发对沙棘种子萌发的影响方面的研究还未有报道。本文对中国沙棘种子水引发的温度、时间和吸水量及它们对沙棘种子活力和幼苗抗性的生理效应进行了研究,为制定中国沙棘种子引发技术措施提供理论依据。
1 材料与方法 1.1 试验材料中国沙棘种子于2007年采自陕西省榆林市、宁夏固原市、甘肃省榆中县和内蒙古呼和浩特市。种子初始含水量分别为8.05%,9.03%,8.28%和9.34%; 千粒质量分别为2.575 8,2.968 4,2.598 3和3.021 6 g; 发芽率分别为15%,33%,26%和62%。
1.2 方法 1.2.1 引发加水量的确定根据预试验获得的吸水率曲线,确定种子引发的总加水量为种子初始质量的50%~75%,引发开始时的加水量为总水量的23%,3 h为23%、6 h为25%、12 h为14%和21 h为15%。设定6个总加水量梯度,即50%,55%,60%,65%,70%和75%,在引发时将水分批加入。
1.2.2 引发温度和时间的确定设 5(±1)℃,10(±1)℃,15(±1)℃ 3个温度梯度,将500 g沙棘种子装入2 000 mL的引发器(20 cm×10 cm×2 cm的加盖塑料盘)中,根据1.2.1的6个加水量梯度,在萌动时间内,将水分批加入引发器中。萌动是指种子缝合线靠近胚根的一端明显被胀裂,有的根端膨大,有的白色胚根尖端已突破内种皮。用塑料薄膜封口,扎10个孔径约为0.5 mm的小孔,用于种子呼吸。每个加水时间间隔期,充分摇动引发器(加无孔塑料膜及盖子摇动),以保证种子均匀吸水。每天观察种子,记录不同温度、水分组合条件下种子出现萌动的最初时间。
1.2.3 综合引发条件的确定将500 g沙棘种子装入引发器中,通过引发温度、加水量和时间的因素组合,确定种子引发的最佳条件。进行综合评价分析时,用T表示引发温度,W表示吸水量占种子初始质量的百分数,D表示引发时间。例如T10+W55+D7表示在10 ℃下,吸水量为种子初始质量的55%时,引发7天。引发加水结束后,每天从各引发器中取出150粒种子在20~30 ℃变温,低温无光照的条件下进行纸床发芽试验(ISTA,1999),每个处理3个重复,每个重复50粒种子(塔依尔等,2004),直至引发器中有萌动种子出现或引发种子的发芽率有大幅度的降低为止。发芽率的测定以种子出现0.2 cm长的胚根为标准。
依据综合评价指数(CEI)大小判断中国沙棘种子引发的最适温度、吸水量和引发时间,CEI数值越大,引发效果越好。
1.2.4 引发种子的发芽效果用水浸48 h的沙棘种子作对照(CK),引发甘肃、宁夏和内蒙古3个产地的种子,每个处理50粒种子,3次重复,进行纸床发芽试验,逐日统计发芽数,验证引发效果。
1.2.5 引发种子的生理变化随机称取各产地中国沙棘引发和对照种子0.3 g,4次重复,测定生理生化指标。可溶性糖含量采用蒽酮比色法测定,丙二醛含量采用硫代巴比妥酸比色法测定,脯氨酸含量采用茚三酮显色法测定(李合生,1999)。均采用UV-1700型可见紫外分光光度计测定。
1.2.6 干旱胁迫下引发种子的发芽和幼苗生长情况用聚乙二醇(PEG)6000调节溶液的渗透势,模拟干旱条件,对经过最佳水引发处理后的种子在0,-0.3,-0.6,-0.9和-1.2 MPa下进行纸床发芽试验。每个处理50粒种子,3次重复,每日更换滤纸,并向培养皿中加入5 mL的PEG溶液。统计最终发芽率、发芽指数、平均发芽时间和发芽5天时的根长、苗高及幼苗鲜质量。
1.2.7 盐胁迫下引发种子的发芽和幼苗生长情况采用NaCl分析纯来模拟盐胁迫环境,其浓度梯度设置为0,50,100,150和200 mmol·L-1。发芽试验方法同1.2.6。
1.2.8 数据处理最终发芽率(final germination percentage,Gp)=最终发芽种子数/供试种子数×100%; 发芽指数(germination index,GI)=∑(Gt/Dt)(Gt: 在时间t日的发芽数,Dt: 相应的发芽天数)(Maguire,1962); 综合评价指数(comprehensive evaluation index,CEI)=(Gp×100+GI)/2。
依据Ellis等(1981)的方法计算平均发芽时间(mean germination time,MGT),其计算公式为:MGT=∑Dn/∑n,n是种子在D天时的发芽数,D是种子开始发芽到统计发芽数时的天数。
所有数据均采用 Microsoft Excel输入,SPSS 13.0 统计软件进行One-way ANOVA方差分析,制图采用Microsoft Excel。
2 结果与分析 2.1 引发温度和时间不同的引发加水量和温度处理下种子的初始萌动时间见表 1。
|
|
由表 1可知,吸水量和引发时的温度都对种子的初始萌动时间有影响。在吸水量一样的情况下,种子的初始萌动时间随温度的上升而缩短。在温度一致的条件下,种子的初始萌动时间随吸水量的升高而缩短。在不同的温度与吸水量组合下,种子初始萌动的时间存在很大的差异。
在5 ℃的条件下,吸水量为种子初始质量的50%和55%时没有种子萌动,在60%和65%时13天才出现萌动种子,说明5 ℃与50%,55%吸水量的组合中,种子的生理活动停滞,据此,可将T5+W50和T5+W55的组合排除。
在10 ℃和15 ℃时,所设计的5种吸水量下均出现了种子萌动情况。当吸水量为75%时,所有温度下引发的种子,以及引发温度为15 ℃、吸水量为70%时的种子均在加水还没有结束时萌动,说明其吸水速度过快,极易造成种子吸胀伤害,故将各温度与75%吸水量的组合、15 ℃与70%吸水量的组合排除。因此,初步确定在5(±1)℃,10(±1)℃和15(±1)℃下,加水量为50%~75%,中国沙棘种子的引发时间为3~13天。
2.2 引发条件试验所设计的61个处理结果见表 2。 从表 2的统计可以看出,对照处理的种子发芽率为16%,位于总排序的第28位,有27个处理提高了种子的发芽率,且部分处理与对照有显著或极显著差异; 另外有32个处理降低了种子的发芽率,除T15+W60+D4与对照有显著差异(P<0.05)外,其余均没有达到显著水平。从发芽率来看,种子引发的适宜条件为: T10+W55+D7,T10+W60+D7,T15+W60+D6,T10+W55+D6。
|
|
有50个处理较对照增加了种子的发芽指数,并且有5个处理对种子发芽指数的提高达到了极显著水平(P<0.01)。从种子的发芽指数来看,种子引发的 适宜条件为: T10+W55+D7,T15+W60+D6,T15+W50+D6,T10+W60+D7,T10+W55+D6。
发芽率与发芽指数的评价结果并不完全相同,需要采用综合评价指数来分析引发结果。在所有的引发处理中,有5个处理的综合评价指数显著高于对照,它们的排序为: T10+W55+D7,T15+W60+D6,T10+W60+D7,T15+W50+D6,T10+W55+D6。因此可以确定中国沙棘种子的适宜水引发条件为: 10 ℃和15 ℃,吸水量为种子初始质量的50%~60%,引发时间为6~7天。
2.3 不同产地种子引发效果不同产地(宁夏、甘肃、内蒙古)种子的发芽率见图 1。3种不同产地的种子引发后均提高了种子的最终发芽率。其中T10+W55+D7引发处理的宁夏、甘肃和内蒙古产地的沙棘种子,与对照比较,其最终发芽率分别提高了26.5%,26.7%,21.2%,差异显著。
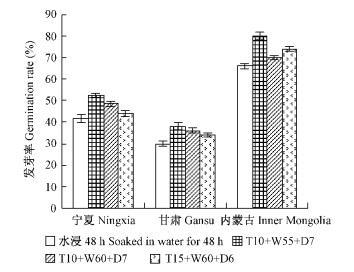 |
图 1 不同产地的中国沙棘种子的发芽率 Fig. 1 Seed germination of sea buckthorn from different sources |
结果表明: 吸水量为种子初始质量的55%、温度为10 ℃时引发7天可以显著提高中国沙棘种子的最终发芽率。
2.4 种子引发后生理变化 2.4.1 可溶性糖如图 2所示,陕西、宁夏、甘肃和内蒙古4个不同产地中国沙棘种子水浸48 h和水引发处理的可溶性糖含量都极显著低于处理前。水引发处理后,4个不同产地沙棘种子可溶性糖含量与对照比较分别提高40.14%,37.13%,33.57%,41.61%。除甘肃产沙棘种子以外,其余3个产地种子可溶性糖含量均极显著高于对照。
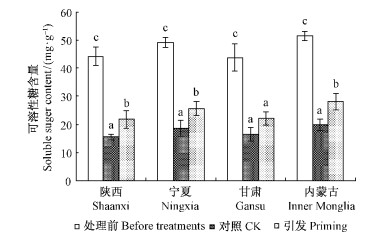 |
图 2 中国沙棘种子水引发前后可溶性糖含量的变化 Fig. 2 The content changes of soluble sugar in seeds of sea buckthorn before and after hydropriming 同一产地种子不同大写字母表示 处理间有显著差异(P<0.01)。 Defferent capital letters differ significantly at P<0.01 among treatments from the seeds of the same source.下同The same below. |
由图 3可知,除了水浸48 h的内蒙古产沙棘种子外,其余处理的种子丙二醛含量均显著低于处理前。陕西、宁夏、甘肃和内蒙古4个不同产地中国沙棘种子引发后丙二醛的含量比对照分别降低20.00%,20.42%,20.93%和20.80%,均达到极显著水平。
 |
图 3 中国沙棘种子水引发前后丙二醛含量的变化 Fig. 3 The content changes of MDA in seeds of sea buckthorn before and after hydropriming |
由图 4可知,陕西、宁夏、甘肃和内蒙古4个不同产地中国沙棘种子水浸48 h和水引发处理的脯氨酸含量均显著低于处理前。引发后4个不同产地中国沙棘种子脯氨酸的含量比对照分别提高35.91%,22.13%,35.77%和31.90%,均达到极显著水平。
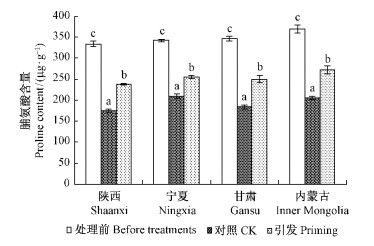 |
图 4 中国沙棘种子水引发前后脯氨酸含量的变化 Fig. 4 The content changes of proline in seeds of sea buckthorn before and after hydropriming |
由表 3可以看出,水引发种子与对照比较显著提高种子的发芽率和发芽指数,在正常的水分条件下分别提高8.24%和33.25%;在PEG浓度为-0.3 MPa时,提高72.73%和86.40%;在PEG为-0.6 MPa时,提高75.01%和65.43%;在PEG为-0.9 MPa时,对照的发芽完全受抑制,而水引发处理发芽率和发芽指数分别为8.67%和0.67;同时水引发将种子的临界萌发条件由-0.6 MPa提升到-0.9 MPa。
|
|
正常生长条件下,水引发种子的平均发芽时间比对照缩短21.47%,差异显著; 在干旱胁迫下,平均发芽时间与对照没有显著差异。
2.5.2 干旱胁迫下水引发对沙棘幼苗形态指标的影响由表 4可知,与对照比较,在正常水分和轻度干旱(-0.3 MPa)胁迫下,水引发种子的苗高显著增加,分别提高84.61%和11.33%,随着干旱的加剧,苗高显著降低;水引发种子幼苗的根长和鲜质量均显著增加,在正常的水分条件下分别提高46.35%和29.92%;在PEG浓度为-0.3 MPa时,提高61.31%和10.22%;在PEG为-0.6 MPa时,提高50.47%和38.40%;在PEG为-0.9 MPa时,幼苗不能正常生长。
|
|
由表 5可知,对照沙棘种子在非盐胁迫条件下的发芽率为68.67%,而100,150和200 mmol· L-1 NaCl胁迫下,对照种子的发芽率均显著低于非盐胁迫下的发芽率。水引发种子在0,50和100 mmol· L-1 NaCl胁迫下发芽率均显著高于非盐胁迫下的对照种子。并且,在不同浓度NaCl胁迫下,水引发种子的发芽率均显著高于相同浓度的对照种子。
|
|
100,150和200 mmol· L-1 NaCl胁迫下,沙棘对照种子的发芽指数均显著低于非盐胁迫下。水引发种子在150 mmol· L-1NaCl胁迫下发芽指数与非盐胁迫下的对照种子没有显著差异,其余浓度盐胁迫下,发芽指数均显著高于非盐胁迫的对照种子。并且,在不同的盐胁迫下,水引发种子的发芽指数均显著高于相同浓度的对照种子。
对照沙棘种子的平均发芽时间随着盐胁迫浓度的升高而延长。水引发种子,仅100和150 mmol· L-1处理与非盐胁迫下的对照种子无显著差异,其他各处理与非盐胁迫下的对照种子比较均显著缩短平均发芽时间。并且,在不同的盐胁迫下,水引发种子的平均发芽时间均显著少于相同浓度的对照种子。
随着NaCl浓度的增大,水引发和对照种子的发芽率和发芽指数都呈下降趋势。但是与对照比较,水引发显著提高种子的发芽率和发芽指数,缩短种子的平均发芽时间。
2.6.2 盐胁迫下水引发对沙棘幼苗形态指标的影响由表 6可知,对照和水引发种子幼苗的根长随盐胁迫浓度的升高呈下降趋势。经不同的盐胁迫后,水引发种子幼苗的根长均高于对照,且50和100 mmol· L-1NaCl胁迫下,水引发处理与对照之间差异显著。
|
|
对照和水引发处理的沙棘苗高也随盐胁迫浓度的升高而呈下降趋势。150和200 mmol· L-1NaCl胁迫下对照幼苗无法生存,而水引发种子幼苗能够正常生长,说明水引发能够提高沙棘幼苗在盐胁迫下的生存能力。在正常条件及50 mmol· L-1NaCl胁迫下,水引发能够显著增加苗高。
随盐浓度的升高,对照和水引发种子幼苗鲜质量变化趋势有所不同,对照种子幼苗呈下降趋势,而水引发种子幼苗呈先上升后下降的趋势,在50 mmol· L-1 NaCl胁迫时最高,显著高于其他处理。在不同的盐胁迫下,水引发种子幼苗的鲜质量均高于相同浓度盐胁迫的对照种子,且50,150和200 mmol· L-1NaCl胁迫与对照差异显著。
3 结论与讨论 3.1 水引发沙棘种子的最佳条件中国沙棘种子的水引发最佳条件为:吸水量为种子初始质量55%,在引发0,3,6,12和21 h时分别加入总水量的23%,23%,25%,14%和15%,温度为10 ℃(避光),引发时间为7天。用筛选出的最佳引发方法对不同产地的中国沙棘种子进行检验,均显著提高了种子的发芽率和发芽指数。
中国沙棘种子最佳引发温度是10 ℃,而以往采用的引发温度一般为15~20 ℃(Khan,1992),例如柳枝稷(Panicum virgatum NewJersey 50)在16 ℃条件下的引发效果更好(Madakkadze et al., 2000),这与本试验的研究结果有差异,这种差异可能与物种的生物学特性有关。引发还有生理锻炼的效应,对某些物种低温引发效果好(傅家瑞,1985;Heydecker et al., 1975)。
中国沙棘种子的最佳引发时间为7天。有文献报道,6种禾本科(Gramineae)在20 ℃下,PEG溶液中引发时间是7天或14天(Liu et al., 2008)。引发时间因植物种、品种或温度的不同而有所差异,种子的最佳引发时间的变化范围为2~21天(Khan et al., 1992),本文的研究结果与之相符。在引发处理过程中,种子胚根尖端细胞DNA复制也在增加,从而为种子萌发做准备(任淑娟等,2012)。某些种子需要更长的引发时间来完成引发过程,可能是由于这些种批种子活力较低(Sliwinska et al., 2002)。
3.2 引发提高种苗抗性机制种子萌发和幼苗早期生长阶段对环境胁迫最为敏感(Rahimi,2013),直接影响物种的总体适应性,植物能否在干旱和盐渍环境中生存,首先取决于它们能否发芽,以及发芽率的高低和发芽速度的快慢。据报道,水引发能够增强种子在盐胁迫下的渗透调节能力、提高成苗率和作物产量(Amooaghaie,2011; Pirasteh-Anosheh et al., 2011)。
本试验研究发现,水引发显著提高干旱胁迫和盐胁迫下中国沙棘种子的发芽率和发芽指数,以及幼苗的根长、苗高和鲜质量,缩短种子平均发芽时间,并将种子的干旱临界萌发条件由-0.6 MPa提升到-0.9 MPa,从而提高中国沙棘的整体适应性。
4个不同产地沙棘种子经对照和水引发处理后,可溶性糖含量都显著低于处理前,说明种子内部发生了一系列的生理生化变化,种子内部储藏的可溶性糖已被用于胚的生长或转化合成新的物质,为种子萌发和幼苗生长提供能量。可溶性糖既是细胞渗透调节剂,也是合成其他有机溶质的碳架和能量来源,还可在细胞内无机离子浓度高时起保护酶类的作用,可以看做是植物在胁迫条件下的一种适应机制(张春平等,2012)。在逆境环境中,其含量会增加,对于提高细胞汁液浓度、降低细胞水势、增强吸水等功能起着重要促进作用(Yokoi et al., 2002)。
丙二醛是膜脂过氧化作用的主要产物之一,其含量的高低和质膜透性的大小都是膜脂过氧化强弱和质膜破坏程度的重要指标(张春平等,2011)。经过水引发处理后,其含量显著低于对照处理,说明水引发能够缓解种子内的膜脂过氧化作用。
脯氨酸被认为是植物在渗透胁迫下容易积累的一种相溶渗透剂,具有调节细胞渗透平衡、提高细胞内渗透势、维持质膜结构完整性,增强细胞结构稳定性和阻止氧自由基产生的作用(杜锦,2010; Heydecker et al., 1977)。也有研究认为脯氨酸在植物体内不仅作为渗透调节剂调节渗透压,还起着改善植物微环境的作用,保证其他生化反应的正常进行(Hoque et al., 2007)。水引发与对照比较,显著提高种子脯氨酸含量,说明引发更能调节种子的渗透势,防止渗透胁迫对种子造成伤害(史雨刚等,2011)。
3.3 水引发技术在直播造林中应用的可行性原理上任何控制吸水的方法都可能成功完成对种子的引发。生物引发和膜引发是生产实践中比较成熟的引发技术,生物引发的技术难度大,投资高;膜引发技术只适合于表面有黏液的种子,应用范围狭窄,目前只有发达国家将该技术应用于高档蔬菜和花卉的引发(杨小环等,2009;Brocklehurst et al., 2008);对于荒漠化面积大、经济欠发达的国家,大面积推广应用水引发技术存在一定的困难。水引发对于不同物种的种子萌发和胚芽生长都具有重要作用。与其他引发技术相同,在盐胁迫和非盐胁迫下,水引发也能够普遍促进种子萌发和幼苗生长(Nawaz et al., 2013)。
水引发是一种既有效又经济简便的方法,有可能成为利用植被进行荒漠化治理的一项重要技术措施,值得在生产实践中进一步验证。
| [1] |
杜锦.2010.盐胁迫下不同基因型玉米的生物学特性及其遗传规律的研究.天津:天津农学院硕士学位论文.( 1) 1)
|
| [2] |
傅家瑞.1985.种子生理.北京:科学出版社.( 1) 1)
|
| [3] |
李怀恩,李刚军,张康,等.2007.沙棘柔性坝对土壤有机质改善作用的试验研究.水土保持通报,27(6): 1-4.( 1) 1)
|
| [4] |
李合生.1999.植物生理生化的试验原理和技术.北京:高等教育出版社.( 1) 1)
|
| [5] |
任淑娟,喻方圆,徐丽萍.2012.引发对马尾松种子细胞周期和发芽率的影响.南京林业大学学报:自然科学版,36(5): 51-55.( 1) 1)
|
| [6] |
史雨刚,孙黛珍,雷逢进,等.2011.种子引发对NaCl胁迫下小麦幼苗生理特性的影响.核农学报,25(2): 342-347.( 1) 1)
|
| [7] |
孙坤,吕小旭,苏雪,等.2012.不同温度下中国沙棘种子的萌发策略.西北师范大学学报:自然科学版,48(3): 86-89.( 2) 2)
|
| [8] |
塔依尔,杨梅花.2004.不同温度对沙棘种子萌发的影响.种子,23(9): 32-34.( 1) 1)
|
| [9] |
吴清风,田春杰,何兴元,等.2002.非豆科固氮树种—沙棘与微生物联合共生体的纯培养研究.生态学杂志,21(2): 22-23.( 1) 1)
|
| [10] |
杨小环,杨文秀,马金虎,等.2009.种子引发对大豆发芽和幼苗生理特性的影响.山西农业大学学报:自然科学版,29(6): 537-541.( 1) 1)
|
| [11] |
张春平,何平,刘海英,等.2012.外源性5-氨基乙酰丙酸对盐胁迫下决明子萌发及幼苗生理特性的影响.中草药,43(4): 161-170.( 1) 1)
|
| [12] |
张春平,何平,韦品祥,等.2011.外源5-氨基乙酰丙酸对盐胁迫下紫苏种子萌发及幼苗抗氧化酶活性的影响.中草药,42(6): 1194-1200.( 1) 1)
|
| [13] |
张虎平,樊新民,王华.2008.聚乙烯醇渗调对沙棘种子活力和出苗的影响.西北农业学报,17(1): 226-228.( 1) 1)
|
| [14] |
张俊风,李庆梅,段新芳,等.2010.壳聚糖对沙棘种子萌发的影响.种子,29(9): 33-37.( 1) 1)
|
| [15] |
郑蔚虹,冷建梅.2003.青霉素、过氧化氢和高锰酸钾浸种对沙棘种子萌发及幼苗生长的影响.种子,22(6): 22-23,30.( 1) 1)
|
| [16] |
Amooaghaie R.2011.The effect of hydro and osmopriming on alfalfa seed germination and antioxidant defenses under salt stress.African Journal of Biotechnology,10(33): 6269-6275.( 1) 1)
|
| [17] |
Anosheh H P,Sadeghi H,Emam Y.2011.Chemical priming with urea and KNO3 enhances maize hybrids(Zea mays L.)seed viability under abiotic stress.Journal of Crop Science and Biotechnology,14(4): 289-295.( 1) 1)
|
| [18] |
Brocklehurst P A,Dearman J.2008.Interactions between seed priming treatments and nine seed lots of carrot,celery and onion.I.Laboratory germination.Annals of Applied Biology,102(3): 577-584.( 1) 1)
|
| [19] |
Davison P A,Taylor R M,Bray C M.1991.Changes in ribosomal RNA integrity in leek(Allium porrum L.)seeds during osmopriming and drying-back treatments.Seed Science Research,1(1): 37-44.( 1) 1)
|
| [20] |
Ellis R H,Roberts E H.1981.The quantification of ageing and survival in orthodox seeds.Seed Science and Technology,9(2): 373-409.( 1) 1)
|
| [21] |
Gao Y P,Young L,Smith B P.1999.Characterization and expression of plasma and tonoplast membrane aquaporins in primed seed of Brassica napus during germination under stress conditions.Plant Molecular Biology,40(4): 635-644.( 1) 1)
|
| [22] |
Garcia C,Aguilar Z,Ramos V,et al. 1997.Molecular analysis of osmopriming and hormone accelerated seed germination.Plant Physiology,114(3): 1507-1507.( 1) 1)
|
| [23] |
Heydecker W,Higgins J,Gulliver R L.1973.Accelerated germination by osmotic seed treatment.Nature,246: 42-44.( 1) 1)
|
| [24] |
Heydecker W,Higgins J,Tumer Y J.1975.Invigoration of seeds.Seed Science and Technology,3: 881-888.( 1) 1)
|
| [25] |
Heydecker W,Coolbear P.1977.Seed treatments for improved performance survey and attempted prognosis.Seed Science and Technology,5: 353-425.( 1) 1)
|
| [26] |
Hoque M A,Okuma E,Banu M N,et al. 2007.Exogenous proline mitigates the detrimental effects of salt stress more than exogenous betaine by increasing antioxidant enzyme activities.Journal of Plant Physiology,164(5): 553-561.( 1) 1)
|
| [27] | International Seed Testing Association(ISTA).1999.International rules for seed testing.Seed Science and Technology,27(Supplement): 27-32,174-182. |
| [28] |
Kaya M D,Okcu G,Atak M,et al.2006.Seed treatments to overcome salt and drought stress during germination in sunflower(Helianthus annuus L.).European Journal of Agronomy,24(4): 291-295.( 1) 1)
|
| [29] |
Khan A A.1992.Preplant physiological seed conditioning.Horticultural Reviews,13: 131-181.( 2) 2)
|
| [30] |
Khan A A,Maguire J D,Abawi G S,et al.1992.Matriconditioning of vegetable seeds to improve stand establishment in early field plantings.Journal of the American Society for Horticultural Science,117(1): 41-47.( 2) 2)
|
| [31] |
Liu H X,Guo Z G,Wang Y R.2008.Optimal conditions for hydropriming Lucerne seeds.New Zealand Journal of Agricultural Research,51(1): 69-75.( 1) 1)
|
| [32] |
Madakadze I C,Prithviraj B,Madakadze R M,et al.2000.Effect of preplant seed conditioning treatment on the germination of switchgrass(Panicum virgatum L.).Seed Science and Technology,28(2): 403-411.( 1) 1)
|
| [33] |
Maguire J D.1962.Speed of germination-aid in selection and evaluation for seedling emergence and vigor.Crop Science,2(2): 176-177.( 1) 1)
|
| [34] |
Muchena S C,Grogan C O.1977.Effects of seed size on germination of corn(Zea mays L.)under simulated water stress conditions.Canadian Journal of Plant Science,57(3): 921-923.( 1) 1)
|
| [35] |
Nawaz J,Hussain M,Jabbar A,et al. 2013.Seed priming a technique.International Journal of Agriculture and Crop Sciences,6(20): 1373-1381.( 1) 1)
|
| [36] |
Rahimi A.2013.Seed priming improves the germination performance of cumin(Cuminum syminum L.)under temperature and water stress.Industrial Crops and Products,42:454-460.( 1) 1)
|
| [37] |
Sliwinska E,Jendrzejczak E.2002.Sugar-beet seed quality and DNA synthesis in the embryo in relation to hydration-dehydration cycles.Seed Science and Technology,30(3): 597-608.( 1) 1)
|
| [38] |
Song J J,Nada K,Tachibana S.1999.Ameliorative effect of polyamines on the high temperature inhibition of in vitro pollen germination in tomato(Lycopersicon esculentum Mill.).Scientia Horticulturae,80(3): 203-212.( 1) 1)
|
| [39] |
Sung F J M,Chang Y H.1993.Biochemical activities associated with priming of sweet corn seeds to improve vigor.Seed Science and Technology,21(1): 97-105.( 1) 1)
|
| [40] |
Yokoi S,Bressan R A,Hasegawa P M.2002.Salt stress tolerance of plants.JIRCAS Working Report,23(1): 25-33.( 1) 1)
|
 2014, Vol. 50
2014, Vol. 50

