文章信息
- 何云, 周义贵, 李贤伟, 苗宇, 范川, 陈栎霖
- He Yun, Zhou Yigui, Li Xianwei, Miao Yu, Fan Chuan, Chen Yuelin
- 台湾桤木林草复合模式土壤微生物量碳季节动态
- Seasonal Dynamics of Soil Microbial Biomass Carbon in Alnus formosana Forest-Grass Compound Models
- 林业科学, 2013, 49(7): 26-33
- Scientia Silvae Sinicae, 2013, 49(7): 26-33.
- DOI: 10.11707/j.1001-7488.20130704
-
文章历史
- 收稿日期:2013-04-02
- 修回日期:2013-06-02
-
作者相关文章
土壤微生物是土壤生态系统中养分源和汇的一个巨大的原动力,在植物凋落物分解、土壤能量转移、养分循环与平衡、土壤理化性质改善、林分发育及生态系统的长期稳定性中发挥着重要作用(Spedding et al.,2004;方丽娜等,2011;Sandra et al.,2012)。土壤微生物量是指土壤中体积小于50×103 μm3的生物总量,是活的土壤有机质组成部分,是土壤活性大小的重要标志,可以反映土壤同化和矿化程度(漆良华等,2008),是陆地生态系统中有机碳和有效营养元素循环的重要环节(Singh et al.,2010)。土壤微生物量碳一般只占土壤有机碳的1%~4%,但它是土壤有机碳最活跃的部分(Schlesinger,1990),是整个生态系统养分和能源循环的关键和动力,是植物所需养分的重要源和库(周建斌等,2001;漆良华等,2009)。
土壤微生物量碳动态变化是一个复杂的过程,在森林生态系统中,土壤微生物活力是土壤有机碳和土壤肥力循环的驱动力,而土壤微生物量会受到环境因子和土壤活性有机碳含量限制,如土地利用方式、植被因子、施肥措施和季节变化等(Devi et al.,2006;宋明伟等,2008;宇万太等,2008)。研究表明,土壤微生物对土壤温度(Frey et al.,2008)、养分(Allison et al.,2010)和水分有效性(Hawkes et al.,2011)等土壤特性十分敏感,导致不同森林生态系统土壤微生物量碳的季节变化不同(Devi et al.,2006;Edwards et al.,2006),即便在相同的气候条件和土壤类型下,不同植被的土壤微生物量碳仍然存在较大差异(Liu et al.,2012)。同时,作为土壤有机碳库和养分的重要指示指标,对土壤微生物量碳动态研究不仅能够了解土壤有机碳循环及转化过程,而且可以对土壤质量和肥力状况以及土地可持续利用进行综合评价(李新爱等,2006;周丽霞等,2007),为人工林经营和地力维护提供可靠依据。本试验在四川省丹棱县台湾桤木(Alnus formosana)退耕还林林地内实地定位,选取台湾桤木2种林草复合模式与台湾桤木自然模式,通过林下草种建植、采样、测试、分析,研究不同林草复合模式土壤有机碳和微生物量碳的季节动态,以期为该地区退耕还林的台湾桤木林地合理经营提供依据。
1 研究区概况研究区位于四川省丹棱县仁美镇飞龙村实施退耕还林工程营造的台湾桤木林地内(102° 57'~103°04' E,29°55'~29°59' N),海拔570~590 m。土壤为紫色土,土层厚30~40 cm。该区地处四川盆地西南边缘,冬干春旱,夏洪秋雨,阴天偏多,日照偏少。属于亚热带气候,年平均气温16.7 ℃,最冷月平均温度6.7 ℃,最热月平均温度为28.0 ℃。研究期间,年降水量1 233 mm,年均相对湿度82%。
2 材料与方法 2.1 样地设置2007年9月初在5年生台湾桤木退耕还林地内,设置面积相近、条件相似的3个小区,每个小区分别设置20 m×20 m样地3块,铲除杂草。在第一小区内播种多花黑麦草(Lolium multiflorum),播种量为30 kg·hm-2;第二小区内采用无性系扦插法建植扁穗牛鞭草(Hemarthria compress),扦插量1 400 kg·hm-2,根据当地扦插经验行距为47 cm,株距为15 cm;第三小区不播草作为对照(前期铲除杂草处理相同)。分别建立以下3种模式:台湾桤木+多花黑麦草复合模式(AL)、台湾桤木+扁穗牛鞭草复合模式(AH)、台湾桤木自然草模式(AN)。同时,在所建立的标准地内进行样地本底值调查(表 1)。2009年4月,对3种模式样地再次进行林龄、树高、胸径、林分郁闭度、草本层高度和盖度等调查(表 2)。对照区中主要自然草有麦冬(Ophitopogin japonicum)、风铃草(Campanula medium)、野胡萝卜(Daucas carota)、鸭儿芹(Cryptotaenia japonica)和繁缕(Stellaria media)。
|
|
|
|
分别在2009年4月(春)、7月(夏)和10月(秋)及2010年1月(冬)在3种模式12块样地中用内径10 cm、采样深度10 cm的土钻采集带根土柱,按0~10,10~20,20~30和30~40 cm的深度进行分层取样,每块样地随机选取5个样点,将相同层次混合均匀后,按四分法取样带回实验室。取部分土过2 mm筛,放置于冰箱中(4 ℃)用于测定微生物量碳含量,剩余部分自然风干后用于测定土壤有机碳含量。每个样品进行3次重复测定。
土壤有机碳含量的测定采用重铬酸钾氧化-外加热法(LY/1237—1999)。
土壤微生物量碳含量测定采用氯仿薰蒸浸提法(Brookes,1995),表达式为:
SMBC=EC/KEC。
式中: SMBC为土壤微生物量碳含量;EC为熏蒸土壤浸提测定的全碳含量与不熏蒸土壤浸提测定的全碳含量的差值;KEC为所浸提出来的微生物量碳占土壤微生物量碳的比例,即浸提效率,KEC取值0.38。Sparling(1992)研究发现,土壤微生物量碳是土壤有机碳库的重要成分,土壤微生物量碳占有机碳的比例是评价土壤的重要指标之一,因此将其命名为土壤微生物量熵。其计算公式是:
qSMB=SMBC/SOC。
式中: qSMB为土壤微生物量熵;SOC为土壤有机碳含量。 2.3 数据处理试验数据处理采用Office Excel 2003和SPSS16.0统计软件,3种模式土壤有机碳含量和微生物量碳含量的差异采用单因素方差(One-WayANOVA)和Duncan新复极差法进行分析。
3 结果与分析 3.1 土壤有机碳含量、微生物量碳含量随土层深度的变化综合分析四个季节土壤有机碳和土壤微生物量碳含量,随着土层加深,3种模式土壤有机碳含量和微生物量碳含量均呈现下降趋势。其中,台湾桤木自然模式下降程度最大,台湾桤木+扁穗牛鞭草模式下降程度最小。在30~40 cm土层中,台湾桤木+扁穗牛鞭草模式下土壤有机碳和微生物量碳含量分别占全部土层的18.327%和21.230%,台湾桤木+多花黑麦草模式的分别为17.136%和18.380%,台湾桤木自然模式下则分别只有15.163%和15.502%(表 3,4)。对2种林草模式和自然模式下土壤有机碳和微生物量碳含量进行方差分析,结果表明:在0~10 cm土层中,3种模式下土壤有机碳含量差异均极显著(P<0.01),而在10~20,20~30和30~40 cm土层中,3种模式差异性均不显著(P>0.05);在0~10和10~20 cm土层中,3种模式土壤微生物量碳含量差异则达到显著性水平(P<0.05),台湾桤木+扁穗牛鞭草模式土壤微生物量碳含量甚至极显著高于台湾桤木自然模式(P<0.01),而在20~30和30~40 cm土层中,3种模式土壤微生物量碳含量差异不显著(P >0.05)。说明通过林下种植草本植物,增加了对土壤有机质的供给,提供给土壤微生物的“源”相应增加,这种增加在土壤表层(0~10 cm)和亚表层(10~20 cm)表现十分明显,因此,土壤微生物量碳含量也会增加。
|
|
|
|
3种模式土壤有机碳含量在0~40 cm各土层中的季节动态见图 1。在各土层深度,从春季到冬季,2种林草模式与台湾桤木自然模式土壤有机碳含量季节动态均表现为“升-降-升”的变化趋势,即:土壤有机碳含量夏季最高,秋季最低,冬季和春季大致相同,但在土壤的表层(0~10 cm)和亚表层(10~20 cm),这种季节变化趋势不明显,尤其是台湾桤木+扁穗牛鞭草模式0~10和10~20 cm两土层土壤有机碳含量的季节变化不大,分别为(14.10±1.02)~(15.59±0.62)和(8.00±0.29)~(12.99±0.31)g·kg-1,各季节间差异不显著(P>0.05)。综合各土层土壤有机碳含量进行方差分析,在春季、夏季和冬季中,台湾桤木+扁穗牛鞭草模式、台湾桤木+多花黑麦草模式和台湾桤木自然模式土壤有机碳含量均有极显著差异(P<0.01)(表 5),而在秋季时则表现为台湾桤木+扁穗牛鞭草模式和台湾桤木+多花黑麦草模式之间土壤有机碳含量差异不显著(P>0.05),但是2种林草模式与台湾桤木自然模式土壤有机碳含量均有极显著差异(P<0.01)。其中台湾桤木+扁穗牛鞭草模式、台湾桤木+多花黑麦草模式下土壤有机碳含量分别是自然模式的1.24~1.55和1.16~1.30倍。说明林草复合模式可以显著增加土壤有机碳含量。
 |
图 1 各土层土壤有机碳含量季节动态
Fig. 1 Seasonal dynamics of soil organic carbon in different soil layer of three models
|
|
|
从春季到冬季,3种模式土壤微生物量碳含量季节动态均变现为“降-升-降”的变化趋势,与3种模式下土壤有机碳含量季节动态趋势基本相反(图 1,2)。各种模式土壤微生物量碳含量随季节变化规律明显,其值表现为秋季>春季>冬季>夏季(P<0.05)。3种模式在各个季节中土壤微生物量碳含量均有极显著差异(P<0.01)(表 6),且在各个季节土壤微生物量碳含量均表现为台湾桤木+扁穗牛鞭草模式最大,台湾桤木自然模式最小。其中台湾桤木+扁穗牛鞭草模式和台湾桤木+多花黑麦草模式下土壤微生物量碳含量分别是自然模式的1.50 ~2.95和1.23~1.80倍。说明林草复合模式不仅可以显著增加土壤微生物量碳的含量,而且增加的速率超过了土壤有机碳含量的增加速率,这可能与草本植物能迅速增加土壤中微生物数量有关。
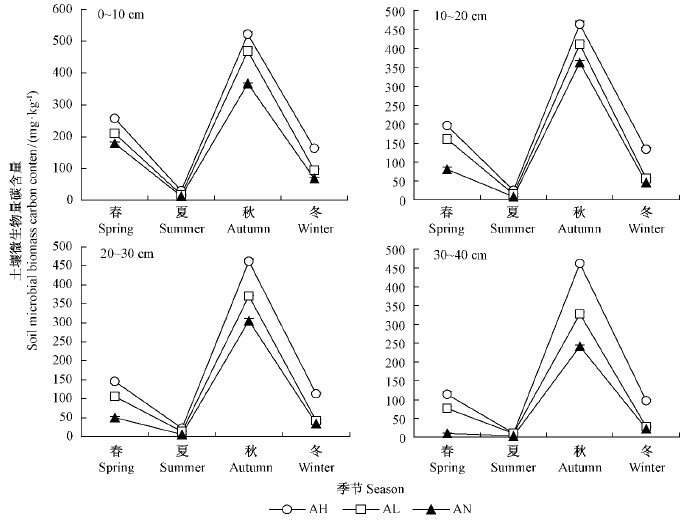 |
图 2 各土层深度土壤微生物量碳含量季节动态
Fig. 2 Seasonal dynamics of soil microbial biomass carbon content in different soil layer of three models
|
|
|
3种模式土壤微生物熵随季节变化规律明显,表现出与土壤微生物量碳含量随季节变化相同的规律(图 2,3),即秋季最大,夏季最小,且秋季时土壤微生物熵显著大于其余各季节(P<0.05)。对3种模式各季节微生物熵的方差分析表明,春季2种人工种植林草复合模式土壤微生物熵极显著大于自然模式(P<0.01),2种林草复合模式之间差异不显著(P>0.05);在秋季时3种模式之间土壤微生物熵差异均不显著(P>0.05);夏季和冬季,台湾桤木+扁穗牛鞭草模式与台湾桤木+多花黑麦草模式以及台湾桤木+扁穗牛鞭草模式与台湾桤木自然模式之间土壤微生物熵差异极显著(P<0.01),但台湾桤木+多花黑麦草模式与自然模式土壤微生物熵差异不显著(P>0.05)(表 7)。这可能与扁穗牛鞭草和多花黑麦草的生长特性有关。
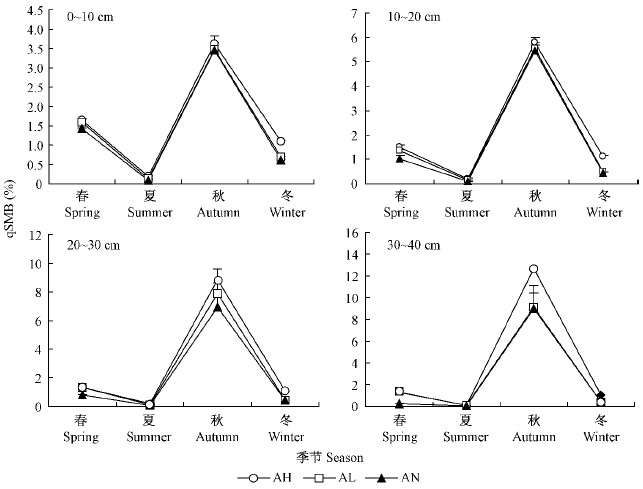 |
图 3 各土层深度土壤微生物熵的季节动态
Fig. 3 Seasonal dynamics of qSMB in different soil layer of three models
|
|
|
土壤有机碳含量和微生物量碳含量受到多种因素的影响。土层深度是影响土壤有机碳含量和土壤微生物量碳含量垂直分布的主要因素之一。本研究中3种台湾桤木林草模式土壤有机碳和土壤微生物量碳均随土层加深而减少,与已有研究结果相同(Arrouays et al.,1994;姜培坤,2005;Gobernaa et al.,2006;张洁等,2007)。台湾桤木的2种林草复合模式土壤有机碳和土壤微生物量碳含量高,且显著高于2007年9月调查的本底值(P<0.05),是因为林草模式下分布有台湾桤木细根与扁穗牛鞭草/黑麦草草根,草根的生长、周转迅速,可以显著提高土壤有机碳含量,提供给土壤微生物的“源”就增加(李贤伟等,2005;王巧等,2007;罗正华等,2008),势必会显著提高土壤微生物量碳的含量。但随土层深度增加,2种林草模式土壤有机碳与微生物量碳降低的程度显著低于台湾桤木自然模式,说明经人工引种草本植物,使得土壤有机碳和土壤微生物量碳的垂直分布更为有效,这主要与细根能改善土壤环境有关,而台湾桤木+扁穗牛鞭草模式与台湾桤木+多花黑麦草间的差异则主要是由草本的生长特征、细根深度及产量引起的(李贤伟等,2009)。
土壤有机碳和微生物量碳的季节性变化是一个复杂的过程。本研究表明,在3种模式各土层里土壤有机碳含量表现为夏季高于冬、春、秋三季,土壤微生物量碳含量则表现为秋季>春季>冬季>夏季(P<0.05)。这种趋势是由于春季到夏季气温逐渐升高,林木和草本根系生长及新陈代谢旺盛,根系周围大量的根系分泌物或溢泌产物、根组织的脱落物等根产物导致春季到夏季土壤有机碳的含量不断升高;而夏季适宜的水热条件大幅提高了土壤微生物活性(张崇邦等,2002)和植被、根系新陈代谢速率,使土壤微生物的周转速率提高,能耗加快,导致活性土壤微生物量碳蓄存积累量降低。从夏季到秋季,一方面,由于土壤温度较高,土壤微生物活性增加,导致土壤有机质分解加速(张金波等,2005),土壤有机碳含量呈现下降趋势;另一方面,土壤微生物生物量碳含量受干湿季变化的影响,雨季高于旱季(吴艺雪等,2009;张剑等,2009)。
在不同季节,2种林草模式下土壤有机碳和微生物量碳含量在表层和亚表层显著高于自然模式,2种林草复合经营模式的地表都比纯林自然模式覆盖了更多的植被,不仅增加了地上部分凋落物的数量,而且丰富了地下根系组成(罗正华等,2008),促进了土壤微生物的繁衍,增加了土壤中微生物数量,提高了微生物的活性(彭佩钦等,2005)。
本研究表明,各种模式微生物熵的季节变化规律表现出与土壤微生物量碳含量随季节变化相同的规律,即秋季最大,夏季最小,且秋季时微生物熵远大于其他各季节。除秋季外,其他各个季节土壤微生物熵均随土层深度的增加而降低。
| [1] |
方丽娜,杨效东,杜 杰.2006.土地利用方式对西双版纳热带森林土壤微生物生物量碳的影响.应用生态学报, 22(4):837-844.( 1) 1)
|
| [2] |
姜培坤. 2005. 不同林分下土壤活性有机碳库研究.林业科学, 41(1):10-13.( 1) 1)
|
| [3] |
李贤伟, 张 健,陈文德,等. 2005. 三倍体毛白杨—黑麦草复合模式细根和草根分布与生长特征.草业学报,14 (6):73-78.( 1) 1)
|
| [4] |
李贤伟, 张 健, 胡庭兴,等. 2009. 退耕还林理论基础及林草模式的实践应用. 北京: 科学出版社.( 1) 1)
|
| [5] |
李新爱,肖和艾,吴金水,等.2006. 喀斯特地区不同土地利用方式对土壤有机碳、全氮以及微生物生物量碳和氮的影响.应用生态学报,17(10):1827-1831.( 1) 1)
|
| [6] |
罗正华,李贤伟,袁渭阳,等. 2008. 台湾桤木幼林地细根生长及林地土壤抗蚀性分析.四川农业大学学报, 26 (3):245-250.( 2) 2)
|
| [7] |
彭佩钦, 张文菊, 童成立,等. 2005. 洞庭湖典型湿地土壤碳、氮和微生物碳、氮及其垂直分布.水土保持学报, 19(1):49-53.( 1) 1)
|
| [8] |
漆良华, 张旭东, 彭镇华,等.2008.湘西北退化侵蚀地植被恢复区土壤养分、微生物与酶活性的典范相关分析.林业科学,44(9):1-6.( 1) 1)
|
| [9] |
漆良华, 张旭东, 周金星,等.2009.湘西北小流域不同植被恢复区土壤微生物数量、生物量碳氮及其分形特征.林业科学,45(8):14-20.( 1) 1)
|
| [10] |
宋明伟, 李爱宗, 蔡立群,等. 2008. 耕作方式对土壤有机碳库的影响.农业环境科学学报, 27(2):622-626.( 1) 1)
|
| [11] |
王 巧,李贤伟,杨 渺,等. 2007. 光皮桦木-扁穗牛鞭草复合模式细根草根生物量及空间分布.四川农业大学学报, 25(3):430( 1) 1)
|
| [12] |
吴艺雪,杨效东,余广彬. 2009. 两种热带雨林土壤微生物生物量碳季节动态及其影响因素.生态环境学报,18 (2):658-663.( 1) 1)
|
| [13] |
宇万太, 赵 鑫, 马 强,等. 2008. 长期定位试验下施肥对潮棕壤活性碳库及碳库管理指数的影响.土壤通报,39 (3):540-543.( 1) 1)
|
| [14] |
张崇邦,金则新,施时迪. 2002. 浙江天台山几种林型下土壤细菌生理群生态分布的特性.植物生态学报, 26(3): 269-274.( 1) 1)
|
| [15] |
张 剑,汪思龙,王清奎,等. 2009. 不同森林植被下土壤活性有机碳含量及其季节变化.中国生态农业学报,17(1): 41-47.( 1) 1)
|
| [16] |
张 洁,姚宇卿,金 轲. 2007. 保护性耕作对坡耕地土壤微生物碳、氮的影响.水土保持学报, 21(4):127-129.( 1) 1)
|
| [17] |
张金波,宋长春,杨文燕. 2005. 小叶樟湿地表土水溶性有机碳季节动态变化及影响因素分析.环境科学学报, 25(10):1397-1402.( 1) 1)
|
| [18] |
周建斌, 陈竹君,李生秀. 2001. 土壤微生物量氮含量、矿化特性及其供氮作用.生态学报, 21(10):1718-1721.( 1) 1)
|
| [19] |
周丽霞,丁明懋. 2007. 土壤微生物学特性对土壤健康的指示作用.生物多样性,15(2):162-171.( 1) 1)
|
| [20] |
Allison S, Gartner T, Mack M, et al. 2010. Nitrogen alter carbon dynamics during early succession in boreal forest. Soil Biology Biochemistry, 42(9):1157-1164.( 1) 1)
|
| [21] |
Arrouays D, Pelissier P. 1994. Modeling carbon storage profiles in temperate forest humid loamy soils of France. Soil Science, 157(3):185-192.( 1) 1)
|
| [22] |
Brookes P C.1995.The use of microbial parameters in monitoring soil pollution by heavy metals. Biology and Fertility of Soils, 19(4):269-279.( 1) 1)
|
| [23] |
Devi N B, Yadava P S. 2006. Seasonal dynamics in soil microbial biomass C, N and P in a mixed-oak forest ecosystem of Manipur, Northeast India. Applied Soil Ecology, 31(3):220-227.( 2) 2)
|
| [24] |
Edwards K A, McCulloch J, Kershaw G P, et al. 2006. Sol microbial and nutrient dynamics in a wet Arctic sedge meadow in late winter and early spring. Soil Biology and Biochemistry, 38(9):2843-2851.( 1) 1)
|
| [25] |
Frey S D, Drijber R, Smith H, et al. 2008. Microbial biomass, functional capacity, and community structure after 12 years of soil warming. Soil Biology Biochemistry, 40(11):2904-2907.( 1) 1)
|
| [26] |
Gobernaa M, Sáncheza J, Pascualb J A, et al. 2006. Surface and subsurface organic carbon, microbial biomass and activity in a forest soil sequence. Soil Biology and Biochemistry, 38(8):2233-2243.( 1) 1)
|
| [27] |
Hawkes C V, Kivlin S N, Rocca J D, et al. 2011.Fungal community responses to precipitation. Globe Change Biology, 17(4):1637-1645.( 1) 1)
|
| [28] |
Liu L, Gundersen P, Zhang T, et al. 2012.Effect of phosphorus addition on soil microbial biomass and community composition in three forest type in tropical China. Soil Biology and Biochemistry,44(1):31-38.( 1) 1)
|
| [29] |
Sandra R D, Kathleen K T. 2012. The effect of fire on microbial biomass: a meta-analysis of field studies. Biogeochemistry, 109(1): 49-61.( 1) 1)
|
| [30] |
Schlesinger W H. 1990. Evidence from chronosequence studies for fl low carbon storage potential of soils. Nature, 348(15):232-234.( 1) 1)
|
| [31] |
Singh J S, Singh D P, Kashyap A K.2010. Microbial biomass C, N and P in disturbed dry tropical forest soil India. Pedosphere, 20(6):780-788.( 1) 1)
|
| [32] |
Sparling G P. 1992. Ratio of microbial biomass carbon to soil organic carbon as a sensitive indicator of changes in soil organic matter. Soil Research, 30(2):195-207.( 1) 1)
|
| [33] |
Spedding T A, Hamel C, Mehuys G R, et al. 2004. Soil microbial dynamics in maize growing soil under different tillage and residue management systems. Soil Biology and Biochemistry, 36(3):499-512.( 1) 1)
|
 2013, Vol. 49
2013, Vol. 49

