文章信息
- 杨升, 刘正祥, 张华新, 杨秀艳, 刘涛, 姚宗国
- Yang Sheng, Liu Zhengxiang, Zhang Huaxin, Yang Xiuyan, Liu Tao, Yao Zongguo
- 3个树种苗期耐盐性综合评价及指标筛选
- Comprehensive Evaluation of Salt Tolerance and Screening Identification Indexes for Three Tree Species
- 林业科学, 2013, 49(1): 91-98
- Scientia Silvae Sinicae, 2013, 49(1): 91-98.
- DOI: 10.11707/j.1001-7488.20130114
-
文章历史
- 收稿日期:2012-02-16
- 修回日期:2012-05-21
-
作者相关文章
2. 大港区农林畜牧局 天津 300270
2. Dagangqu Bureau of Agriculture, Forestry and Animal Husbandry Tianjin 300270
我国盐碱地总面积约1亿hm2以上,主要分布在东北和华北重要农产区、生态脆弱的西北内陆地区以及经济繁荣的沿海地带(马文月,2004)。盐分胁迫是植物在盐碱地上生长的主要限制因子。通过筛选植物耐盐性指标,选育出能在盐碱地上造林绿化的耐盐树种,对改善我国广大盐碱地的生态系统,改良盐碱地、减少土壤盐渍化危害具有重要意义。
目前,关于盐胁迫下植物的生理生化响应以及植物耐盐能力评价的研究较多,如孙海菁等(2009)研究了盐胁迫对6个树种的生长及生理指标的影响;倪细炉等(2010)对4种植物抗盐能力进行综合评价;张华新等(2008)研究了盐胁迫下11个树种的生理特性并利用隶属函数法对它们进行耐盐能力评价。同时,通过外源物质和转基因调控表达提高植物耐盐能力的研究也受到广泛重视(Lata et al.,2011;Ganege et al.,2010;Rania et al.,2010)。对植物耐盐性评价所选用的耐盐性指标不同,所得到的结果也存在差异,因此,需要对耐盐性指标进行筛选,寻找与耐盐性评价相关性较大的指标。张耿等(2007)对偃麦草属(Elytrigia)植物苗期耐盐性指标进行筛选,认为存活率、脯氨酸含量、丙二醛含量、生长胁迫指数、相对生长速度和K+/Na+对其耐盐性有显著影响。李庆贱等(2010)等初步筛选出Pn,Gs,Tr,Fv/Fm,Fv/Fo可作为白榆(Ulmus pumila)苗期耐盐碱评价的有效指标。李源等(2010)对紫花苜蓿(Medicago sativa)的研究认为可溶性糖含量、细胞质膜透性、丙二醛含量等指标可以直接作为耐盐评价指标。高膜稳定性、低Na+/K+、高渗透物质浓度等可作为黄瓜(Cucumis sativus)耐盐碱的有效选择标准(Jagesh et al.,2010)。在盐胁迫环境下植物生长、生理等指标是反映其对逆境适应性的重要指标,是评价植物耐盐性的重要信息,因此,对耐盐性指标进行筛选,建立耐盐评价体系是选育耐盐良种的重要工作。本文以卫矛(Euonymus alantus)、沙枣(Elaeagnus angustifolia)和美国白蜡(Fraxinusamericana)3个树种为材料,研究其盐胁迫下生长和生理响应,综合评价其耐盐能力,对耐盐性指标进行筛选,为建立植物耐盐评价体系和耐盐树种选育提供理论依据。
1 材料和方法 1.1 试验材料在北京房山区田各庄实验基地的大棚中进行盆栽控盐试验。试验材料为华北林业实验研究中心用种子繁殖的卫矛、沙枣和美国白蜡1年生实生苗,种子由格林种业公司从美国引进。盆的规格为37 cm×30 cm。4月份上盆,每盆1株,基质由腐殖土、草炭土和珍珠岩按照1: 3 : 1的比例混合而成,用80%的多菌灵进行消毒处理。缓苗2个月后,选取长势基本一致的苗木进行盐胁迫处理。
1.2 试验设计采用完全随机区组设计,共设6个盐分梯度(NaCl浓度mmol·L-1): 0,100,200,300,400,500。每个树种各梯度10株,3次重复。施盐方式采取多次施盐,逐级递增。当达到预期设定的盐浓度后,根据蒸发情况浇水,以平衡蒸发量,同时防治病虫害。花盆下垫塑料托盘,以便后期浇水时将流出的溶液及时倒回花盆内,防止盐分流失。盐胁迫处理40天,并且观测记录各树种的盐害症状。
1.3 测定的指标与方法株高的测定:每个树种各处理下随机选取5株,测定盐胁迫前后的株高H1和H2,株高生长量=H2-H1,株高相对生长量=盐处理的株高生长量/对照的株高生长量;盐胁迫结束后,每个树种各处理随机选取3株进行生物量测定,在105 ℃下杀青1 h,80 ℃烘干至恒质量,称干质量(精确到0.01 g)。
采集相同部位的功能叶,马上放入液氮中速冻,然后放在-70 ℃超低温冰箱中保存,用于各生理指标测定。叶绿素采用丙酮法测定;MDA采用硫代巴比妥酸法测定;SOD采用NBT光化还原法测定(郝建军等,2007)。脯氨酸采用酸性茚三酮法测定;可溶性糖采用蒽酮法测定(李合生等,2000)。Na+和K+含量参照王宝山(1995)和於丙军(2001)的方法,用原子吸收分光光度计法测定。膜透性(中国科学院上海植物生理研究所,1999)用相对电导率表示,取新鲜叶片,采用DDSJ-308电导仪测定。每个指标测定3次重复。
1.4 数据处理利用EXCEL2003对数据进行处理和绘制图表,以小区平均值为统计单位,用SPSS13.0进行数据标准化处理、相关性分析和主成分分析,并利用隶属函数法和主成分赋予权重法求出耐盐性的综合评价值,进行耐盐性排序。运用灰色关联分析进行指标筛选。
2 结果与分析 2.1 各树种在不同盐浓度下的盐害症状表现随着盐胁迫浓度的增加,供试树种的受害症状逐渐显现,但3个树种受害状况存在明显的差异(表 1)。NaCl浓度为100 mmol·L-1时,3个树种的生长状况均正常,说明它们均能忍耐一定的盐胁迫环境。在200 mmol·L-1条件下,受害症状开始出现,并存在一定的差异。在400 mmol·L-1处理水平,美国白蜡出现大量叶片干枯。在500 mmol·L-1盐浓度下,沙枣有明显的落叶现象,而卫矛只有少量落叶。由此可以初步评定3个树种的耐盐能力排序为:卫矛>沙枣>美国白蜡。
|
|
盐胁迫对植物生长具有直接的影响。从图 1可知:盐胁迫下3个树种的株高相对生长量和生物量均表现出随盐浓度的升高而降低的趋势。盐胁迫对美国白蜡的株高影响最明显,盐浓度达到200 mmol·L-1时其相对株高生长量比对照相比下降了93%;沙枣在400 mmol·L-1盐浓度下,与对照相比下降40%;卫矛相对株高生长量受盐胁迫影响较小,盐浓度达到500 mmol·L-1时仅下降了36%。在低盐浓度(≤200 mmol·L-1)下,3树种的生物量所受影响都较小。当盐浓度上升到500mmol·L-1时,与对照相比,沙枣的生物量减少最大,为43.0%,美国白蜡减少35.7%,卫矛减少最小,为33.1%。
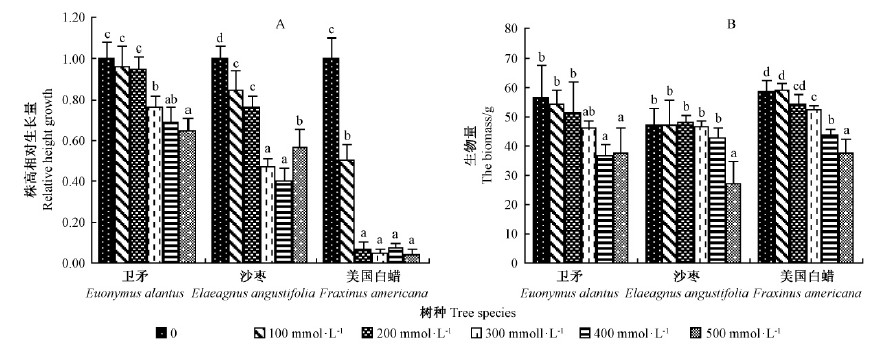 |
图 1 盐胁迫对相对株高生长量(A)和生物量(B)的影响
Fig. 1 Effect of salt stress on relative height growth (A) and biomass (B)
相同树种不同字母表示在P < 0.05水平上显著差异。Bars are mean values of three replicates±standard deviation. The same speciessharing a different letter are significantly different according to Duncan’s multiple range tests at the 0.05 probability level.下同 The same below. |
盐胁迫对植物的影响还表现在生理反应上。由表 2可知: 3个树种叶绿素含量均随盐浓度的升高逐渐减少,表明盐分胁迫可能会降低它们的光合能力。同时,随着盐胁迫的增强,膜透性、MDA含量和可溶性糖含量在3个树种中表现一致,都表现出逐渐增加的趋势;SOD活性和脯氨酸含量变化在3个树种上有所不同。卫矛叶内SOD活性显著升高,美国白蜡略有升高,沙枣除在300 mmol·L-1盐处理水平显著降低外,其他浓度下则变化不大。多重比较结果显示:沙枣和美国白蜡的脯氨酸含量基本上随盐浓度的增加而增加,卫矛脯氨酸含量在各浓度下变化不显著。
|
|
在盐胁迫下,植物根、茎、叶中的Na+含量均随盐浓度的升高而升高(图 2)。Na+在植株体内分布,根中含量最高,茎中含量最少。其原因可能是这3个树种主要通过在根部富集Na+来阻止盐分向植株地上部分运输。试验表明:卫矛对Na+富集最多,沙枣和美国白蜡根部对Na+的富集能力相对较弱(图 2A)。在500 mmol·L-1浓度下,沙枣和美国白蜡根中Na+含量与对照相比分别只增加了130.8%和96.5%,而卫矛则增加了248.4%。叶片在100 mmol·L-1盐浓度下Na+含量的增加不明显(图 2C);在500 mmol·L-1盐浓度下则增加明显,与对照相比,卫矛增加了978.0%,沙枣为96.05%,而美国白蜡为630.6%。
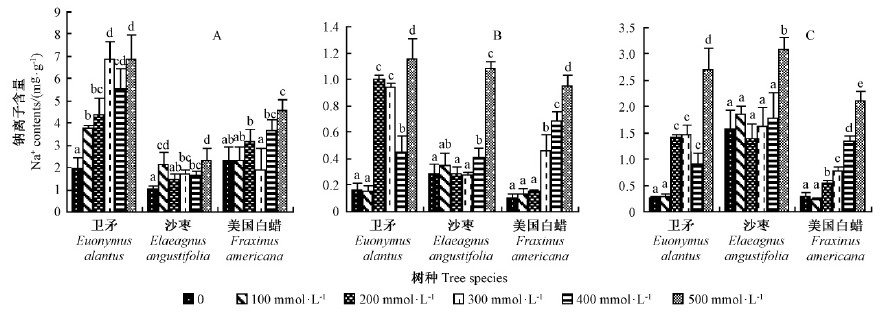 |
图 2 不同盐浓度胁迫对供试树种Na+含量的影响
Fig. 2 Effect of different concentrations salt stress on Na+ contents of experimental seedlings
A:根Root;B:茎Stem;C:叶Leaf.下同。The same below. |
随着盐胁迫的增强,K+含量在植物不同部位的变化有所不同(图 3)。卫矛根中K+含量除了在500 mmol·L-1盐浓度下略有升高外,表现为随盐浓度的增加而减少;沙枣和美国白蜡在400 mmol·L-1盐浓度下根中K+含量均有显著降低,说明Na+的增加对K+的吸收造成了影响(图 3A)。盐胁迫下,卫矛叶片中K+含量变化不明显。沙枣叶片中的K+含量随盐浓度的增加而降低,但是在500 mmol·L-1盐浓度下才有显著减少;美国白蜡则随盐浓度的增加而增加(图 3C)。随盐浓度增加,3个树种茎中的K+含量均没有显著性差异(图 3B)。
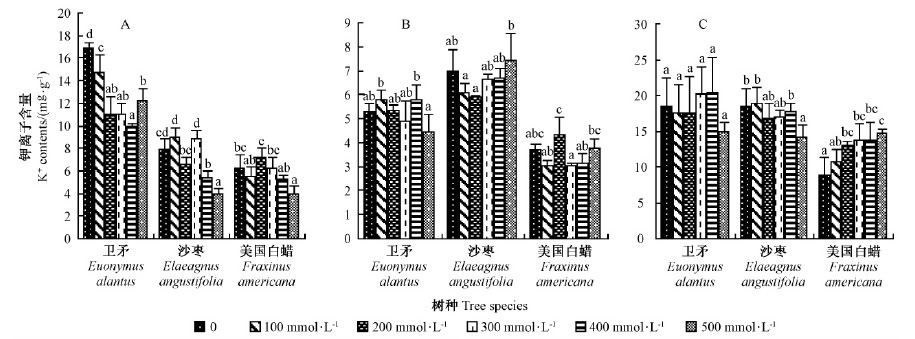 |
图 3 不同盐浓度胁迫对供试树种K+含量的影响
Fig. 3 Effect of different concentrations salt stress on K+ contents of experimental seedlings
|
从相关系数矩阵可看出,除茎、叶中的K+含量与其他指标相关性较小外,其他指标之间均存在极显著或显著相关(表 3),从而使它们所提供的信息发生了重叠。由于各指标在植物耐盐性中所起的作用有所不同,因此直接利用这些指标对植物幼苗进行耐盐性评价,会产生较大偏差。
|
|
对14个耐盐指标各树种不同盐浓度下的均值进行主成分分析,结果如表 4所示,第一、二、三主成分的累计贡献率达86.159%,已经对大多数数据信息给出了充分的概括,因此确定提取这3个主成分,这样把原来14个单项指标转换成了3个新的相互独立的综合指标,分别用C1,C2和C3表示。根据各综合指标的贡献率大小可以知道它们的相对重要性,同时根据14个指标在盐胁迫下平均值的标准化值及各综合指标的指标系数(表 4)求出每一树种的3个综合指标值(表 5)。
|
|
|
|
每一材料各综合指标的隶属函数值利用公式求得(张耿等,2007): μ(j)=(X-Xmin)/(Xmax-Xmin)。式中: X为各材料某一综合指标值,Xmax为某一综合指标值中的最大值;Xmin为该综合指标中的最小值。根据公式求出每一材料所有综合指标的隶属函数值(表 5)。
根据综合指标贡献率的大小(分别为0.398 03,0.280 83,0.182 73)用公式Wj=Pj/P,求得权重(张耿等,2007)。式中: Wj值表示第j个综合指标在所有综合指标中的权重;Pj表示各材料第j个综合指标的贡献率;P表示所有综合指标的贡献率总和。因此,求出3个综合指标的权重分别为0.462,0.326和0.212(表 5)。
2.5.4 综合评价利用公式D=Σ[μ(j)·Wj]求出各材料的综合耐盐能力大小(张耿等,2007)。式中: D值为各材料在盐胁迫下用综合评价指标所得的耐盐性综合评价值。根据D值对3个供试树种进行耐盐能力排序为:卫矛>沙枣>美国白蜡(表 5),这和盐害症状表现的结果相一致。
2.6 耐盐指标筛选采用灰色关联分析进行耐盐指标的筛选。按照灰色系统理论要求,将3个树种的耐盐综合评价值及14个指标视为一个整体,即灰色系统。其中,耐盐综合评价值为母序列Xo,相对株高生长量、生物量、叶绿素含量等为子序列Xi(i=1~14)。利用SPSS13.0对原始数值进行标准化处理,使其变成无量纲数值。利用公式Loi(k)=(Xmin+PXmax)/(Xki+PXmax)(其中: Xmin为|Xi-Xo|的最小值;Xmax为|Xi-Xo|的最大值;Xki为第k个树种i指标的|Xi-Xo|值;P=0.5)求出各树种下母序列Xo与各子序列Xi的关联系数。利用公式Roi=$\frac{1}{n}\sum\limits_{j = 1}^n {Loi\left({{k_j}} \right)} $求关联度(李禄军等,2006;秦光华等,2004)。结果表明株高相对生长量、膜透性、脯氨酸含量和根、茎、叶中的Na+,K+含量与植物耐盐性评价有较大的关联度(表 6)。
|
|
做到适地适树,对盐碱地的改良和开发利用是非常重要的。陶晶等(2007)研究发现在盐浓度达到0.8%~1.0%时,沙枣苗木高生长量仍能达到对照的80%以上。美国白蜡在江苏盐城沿海土壤含盐量0.3%~0.5%条件下,其造林成活率可达90%以上(董必慧,2006)。本研究显示卫矛、沙枣和美国白蜡的适宜生长土壤含盐量上限值分别为500 mmol·L-1(约1.3%)、400 mmol·L-1(约0.8%)和300 mmol·L-1(约0.5%)。利用综合评价值对3个树种的耐盐能力排序为:卫矛>沙枣>美国白蜡。这个结果与3个树种在盐胁迫下的受害症状表现所得到的结果相一致。
植物耐盐性是一个复杂的生理过程,不同的植物不同时期的耐盐性都有所不同,任何单一指标的测定与研究都不能有效准确地评价植物的耐盐性。因此,利用形态、生理和生化等指标对植物耐盐性进行综合评价是比较科学合理的。另一方面,指标过多不仅增加研究难度也会造成资源的浪费,找出那些起关键作用的指标,可以达到以较少指标准确评价植物耐盐性的目的。本文利用灰色关联分析对14指标进行筛选,筛选出相对株高生长量、膜透性、脯氨酸含量、根茎叶中的Na+和K+含量是对植物耐盐性评价有显著影响的指标。这些指标分别反应了植物在盐胁迫环境下生长情况、膜系统稳定性、渗透调节能力和对离子的选择吸收能力。膜透性的大小反映了植物叶片的受损程度,膜透性越大,叶片受损越严重,必然导致叶绿素含量降低。细胞膜油脂的过氧化反应水平决定了MDA含量变化(Tang et al.,2007)。SOD是膜系统的抗氧化酶,减轻膜系统的氧化损伤,其活性的增加是一个被动反应。Mohamed等(2004)也分析认为膜透性可以作为植物耐盐能力评价的一个重要指标。脯氨酸是植物在逆境环境条件下的一种重要渗透调节物质,有研究认为脯氨酸在植物体内不仅作为渗透调节剂调节渗透压,还起着改善植物微环境的作用,保证其它生化反应的正常进行(Md. Anamul et al.,2007)。Wided等(2007)的研究发现盐胁迫下脯氨酸在叶片中显著积累,并且可以作为一个耐盐评价指标。植物体内矿质元素的含量和分布情况对其耐盐能力有非常大的影响。Na+的在植物体内过度积累是造成植物盐害的主要原因。K+离子既是植物生长与发育所必需的营养元素,又在生理调节、物质构成中发挥着作用。K+在植物的生理活动中有着极其重要的作用,如平衡Na+,作为渗透调节剂等。Chen等(2011)的研究显示: Na+/K+的平衡对烟草耐盐能力的表现非常重要。盐胁迫还能诱导杨树(Populuseuphratica)一些Na+/K+相关基因表达,从而调节杨树体内的Na+/K+提高耐盐能力(Ding et al.,2010)。植物生理活动的改变最终在生长形态表现出来。因此,筛选出的这些指标综合了形态和生理生化指标,对评价这3个树种的耐盐能力是比较科学合理的。
植物对逆境环境的反应是很多综合因素影响的结果,土壤结构、植物生长阶段、遗传差异等因素都会对植物耐盐能力表现产生影响,因此,研究植物耐盐性,筛选耐盐评价指标并建立评价标准体系还需要不断深入探索。
| [1] |
董必慧. 2006.盐城沿海湿地美国白蜡树种引种造林试验.东北林业大学学报, 34(2): 22-23.( 1) 1)
|
| [2] |
郝建军, 康宗利, 于洋. 2007.植物生理学实验技术.北京:化学工业出版社.( 1) 1)
|
| [3] |
李合生, 孙群, 赵世杰, 等. 2000.植物生理生化实验原理和技术.北京:高等教育出版社.( 1) 1)
|
| [4] |
李禄军, 蒋志荣, 李正平, 等. 2006.3树种抗旱性的综合评价及其抗旱指标的选取.水土保持研究, 13(6): 253-255.( 1) 1)
|
| [5] |
李庆贱, 陈志强, 石瑞亭, 等. 2010.白榆家系苗期耐盐碱研究.北京林业大学学报, 32(5): 74-81.( 1) 1)
|
| [6] |
李源, 刘贵波, 高洪文, 等. 2010.紫花苜蓿种质耐盐性综合评价及盐胁迫下的生理反应.草业学报, 19(4): 79-86.( 1) 1)
|
| [7] |
马文月. 2004.植物抗盐性研究进展.农业与技术, 24(4): 95-99.( 1) 1)
|
| [8] |
倪细炉, 岳延峰, 田英, 等. 2010.4种盐生植物抗盐能力的综合评价.中国农学通报, 26(6): 138-141.( 1) 1)
|
| [9] |
秦光华, 姜岳忠, 李善文, 等. 2004.黑杨派新无性系苗期生长模型及灰色关联分析.北京林业大学学报, 26(2): 52-57.( 1) 1)
|
| [10] |
孙海菁, 王树凤, 陈益泰. 2009.盐胁迫对6个树种的生长及生理指标的影响.林业科学研究, 22(3): 315-324.( 1) 1)
|
| [11] |
陶晶, 陈士刚, 李青梅, 等. 2007.耐寒型抗盐碱树种银莓、沙枣引种及应用.防护林科技, (5): 94-96.( 1) 1)
|
| [12] |
王宝山, 赵可夫. 1995.小麦叶片中Na、K提取方法的比较.植物生理学通讯, 31(1): 50-52.( 1) 1)
|
| [13] |
於丙军, 罗庆云, 曹爱忠, 等. 2001.栽培大豆和野生大豆耐盐性及离子效应的比较.植物资源与环境学报, 10(1): 25-29.( 1) 1)
|
| [14] |
张耿, 高洪文, 王赞, 等. 2007.偃麦草属植物苗期耐盐性指标筛选及综合评价.草业学报, 16(4): 55-61.( 4) 4)
|
| [15] |
张华新, 宋丹, 刘正祥. 2008.盐胁迫下11个树种生理特性及其耐盐性研究.林业科学研究, 21(2): 168-175.( 1) 1)
|
| [16] |
中国科学院上海植物生理研究所. 1999.现代植物生理学试验指南.北京:科学出版社.( 1) 1)
|
| [17] |
Ganege D K K, 夏宜平, 朱祝军, 等. 2010.外源水杨酸对盐胁迫下非洲菊抗氧化酶活性和生理特性的影响.浙江大学学报:农业与生命科学版, 36(6): 591-601.( 1) 1)
|
| [18] |
Chen H T, He H, Yu D Y. 2011.Overexpression of a novel soybeangene modulating Na+/ and K+ transport enhances salt tolerance intransgenic tobacco plants. Physiologia Plantarum, 141(1):11-18.( 1) 1)
|
| [19] |
Ding M Q, Hou P C, Shen X, et al. 2010.Salt-induced expression ofgenes related to Na+/K+and ROS homeostasis in leaves of saltresistantand salt-sensitive poplar species. Plant Molecular Biology, 73(3): 251-269.( 1) 1)
|
| [20] |
Jagesh K T, Anilabh D M, Ravinder K, et al. 2010.Effect of salt stresson cucumber: Na+-K+ratio, osmolyte concentration, phenols andchlorophyll content. Acta Physiologiae Plantarum, 32(1):103-114.( 1) 1)
|
| [21] |
Lata K, Srivastav M, Dubey A K, et al. 2011.Effect of polyamines onseedlings of two mango(Mangifera indica L.)rootstocks under saltstress. Indian Journal of Plant Physiology, 16(3/4): 258-267.( 1) 1)
|
| [22] |
Md. Anamul H, Eiji O, Mst N A B, et al. 2007.Exogenous prolinemitigates the detrimental effects of salt stress more than exogenousbentaine by increasing antioxidant enzyme activities.Journal of plantphysiology, 164(5): 553-561.( 1) 1)
|
| [23] |
Mohamed M F, Karima H A S. 2004.Cellular basis of salinity tolerancein plants. Environmental and Experimental Botany, 52(2):113-122.( 1) 1)
|
| [24] |
Rania B S, Nabil Z, Walid B R, et al. 2010.Improved drought and saltstress tolerance in transgenic tobacco overexperessing a novel A20/AN1 zinc-finger“AlSAP”gene isolated from the halophyte grassAeluropus littoralis. Plant Molecular Biology, 72(1/2): 171-190.( 1) 1)
|
| [25] |
Tang D, Shi S, Li D, et al. 2007.Physiological and biochemicalresponses of Scytonema javanicum(cyanobacterium)to salt stress.Journal of Arid Environments, 71(3): 312-320.( 1) 1)
|
| [26] |
Wided M, Nader B A, Ahmed D, et al. 2007.Salt tolerance of theannual halophyte Cakile maritima as affected by the provenance andthe developmental stage. Acta Physiol Plant, 29(4): 375-384.( 1) 1)
|
 2013, Vol. 49
2013, Vol. 49

