文章信息
- 李铁军, 朴炫春, 廉家盛, 廉美兰
- Li Tiejun, Piao Xuanchun, Lian Jiasheng, Lian Meilan
- 利用生物反应器接触培养法增殖笃斯越橘丛生苗
- Proliferation of Adventitious Shoots of Vaccinium uliginosum Using Raft Bioreactors
- 林业科学, 2012, 48(11): 130-133.
- Scientia Silvae Sinicae, 2012, 48(11): 130-133.
-
文章历史
- 收稿日期:2012-02-23
- 修回日期:2012-09-28
-
作者相关文章
笃斯越橘(Vaccinium uliginosum)又称蓝浆果,属杜鹃花科(Ericaceae)越橘属(Vaccinium)(李亚东,2001),广泛分布于北半球。中国野生笃斯越橘资源主要分布在大兴安岭、小兴安岭地区(李亚东等,2001)。笃斯越橘果实具有营养保健作用(李亚东等,2004),包括消除眼睛疲劳、软化血管、增强人体免疫等功效,是近几年世界上发展十分迅速的集营养与保健于一身的果树,被国际粮农组织列为五大健康食品之一,具有广泛的市场前景。
笃斯越橘的繁殖方法较多,但种子育苗、绿枝扦插、硬枝扦插、根插、分株嫁接等繁殖方法存在繁殖速度慢、品种易退化等问题,且苗木生长势、果实品质较组培苗均有不足之处(Ahmed et al., 1996),因此生产上广泛应用组培苗进行栽培。植物组织培养一般利用固体培养基进行培养(马均等,2007),这种方法因培养基凝固剂的使用,成本较高,阻碍着组培苗产业化的应用进程。利用液体培养基进行培养是植物组培的另一种方法,此种方法因培养基处于流动状态,培养物可充分利用培养基中养分,同时培养物分泌的一些物质不是集中在培养物周围而是均匀地分散到培养基中,对培养物的生长有利(罗丽萍等,2001);此外,因不使用琼脂,还可降低组培成本。因此,改善培养工艺,建立组培新的技术体系,减少生产成本是实现商业生产的一种必然趋势。早在1959年Tulecke和Nickell(1959)首次将微生物培养用发酵工艺应用到高等植物的悬浮培养,而且从20 L玻璃瓶放大到30 L和134 L不锈钢发酵罐。自此之后生物反应器被广泛应用,不断普及,截止目前,已经在人参(Panax ginseng)(陈巍等,2005)、甘草(Glycyrrhiza uralensis)(向德军等,2001)、丹参(Salvia miltiorrhiza)(邱德有等,2004)等40多种植物材料中优化了毛状根培养系统。生物反应器不定根培养技术也得到迅速发展,目前其外植体系基本得到确立,韩国CBN Biotech有限公司已利用10 t大型反应器大量培养人参不定根,作为化妆品、保健品的原料,并有产品上市。生物反应器主要类型有搅拌式、气升式、鼓泡式和旋转式。其中气升式生物反应器是以气体为动力,靠导流装置的引导,形成气液固混合物的总体有序循环,具有混合效果好、结构简单、无运动部件、易清洗、不易染菌和传热传质效率高的特点(张明菊,2005)。本研究利用气升式生物反应器接触培养法进行笃斯越橘组培苗的大量增殖,探讨了影响反应器内笃斯越橘组培苗增殖的几种因素,旨在寻找适宜的反应器增殖培养条件,为笃斯越橘种苗的规模工厂化生产提供理论依据。
1 材料与方法 1.1 材料笃斯越橘‘美登’(V. uliginosum ‘Blomidon’)品种经过茎段培养得到的组培苗,在增殖培养基[MS+玉米素(ZT)2.0 mg·L-1+蔗糖40 g·L-1+琼脂7 g·L-1,pH 5.7]中培养60天后,将增殖的丛生组培苗切成单体植株,选用长势均一的苗,将其切成约1.5 cm长(带2片叶),作为反应器培养的外植体材料。
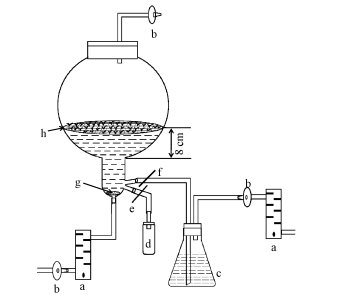
1.2 试验方法1) 生物反应器接触培养系统及培养基试验采用5 L球型气升式反应器接触培养系统(图 1),培养时在距离反应器球型底部8 cm处架支持网,每个反应器中注入2 L培养基,使培养基面与支持网持平;培养到一定阶段当培养基量减少时,打开图 1中开关f,补充培养基,保证接种于支持网上的外植体始终与培养基接触。所用的培养基为B5(Gamborg et al., 1968)培养基加入2 mg·L-1的ZT,40 g·L-1的蔗糖,将pH值调节为5.4。
|
图 1 反应器接触培养系统
Fig.1 The system of raft bioreactor
a:空气流量计;b:过滤器;c:贮液瓶;d:抽样瓶;e,f:开关;g:喷头;h:支持网。 a:Air flow meter;b:Filter;c:Medium reservoir;d:Sampling pot;e,f:Switch;g:Sparger;h:Supporter net. |
2) 试验处理 生物反应器内接种密度试验设置3个处理,每个反应器分别接种45,60和75个生长一致的外植体,通入空气(100 mL·min-1),在光强为30 μmol·m-2s-1的条件下培养;为了调查通气量对丛生芽增殖生长的影响,在反应器中接种60个外植体后,分别通入50,100和150 mL·min-1的空气,其他条件与接种密度试验相同;在探讨光强对增殖生长的影响时,在反应器内接种60个外植体,通入100 mL·min-1气体后,将反应器分别置于光强30,45和60 μmol·m-2s-1条件下培养。所有试验处理均接种3个反应器作为重复。
3) 反应器接触培养过程中培养基的动态变化为了探明反应器培养期间培养基pH、电导率(EC)和蔗糖的变化动态,在5 L反应器中接入60个外植体,通气量设置为100 mL·min-1,光强调节为45 μmol·m-2s-1,其他方法与试验1.2中“生物反应器接触培养系统及培养基”中的试验方法相同。为了取培养基样品,每5天在超净工作台内将反应器培养系统中开关(e)打开,取培养基约10 mL,置入-20 ℃冰箱中保存;取样至第60天后,将冷冻的培养基样品从冰箱取出,在室温下化冻,并测定样品的pH、EC及糖含量。
4) 培养基中pH、电导率及糖含量的测定 将培养基样品用孔径为0.44 μm的过滤器过滤,去掉杂质后用于分析测定。pH和电导率(EC)分别用酸度计(PHS-3C,上海精密科学仪器有限公司,上海)和电导率仪(DDS-307,上海精密科学仪器有限公司,上海)测定。糖含量参照李利军等(2003)的分光光度法测定,取0.5 mL稀释好的培养基样品溶液和5.0 mL磷钼黄溶液,用蒸馏水定容到10 mL,在水浴锅(100 ℃)中加热35 min后取出,用自来水冷却至室温,利用紫外可见分光光度计(UV1102,上海天美科学仪器有限公司,上海)在820 nm波长处测其吸光度值,由标准曲线线性方程计算培养基中糖含量。
5) 培养条件及数据分析 所有试验处理均接种3个反应器作为重复。培养温度为(25±2) ℃,每天用荧光灯光照16 h,培养60天后将反应器内增殖的丛生苗取出,随机取20个苗擦去表面的水分后称其质量并记录鲜质量;然后将其再放入55 ℃的烘干箱中,2天后待完全干燥,称干质量并记录。所得数据用SAS (Statistical Analysis System,Cary,NC,USA)软件处理,采用邓肯氏新复极差法进行分析比较(显著水平P<0.05)。
2 结果与分析 2.1 接种密度对丛生芽增殖生长的影响接种密度是反应器培养中重要的调控参数之一,反应器培养的最终目的是在一个反应器中得到大量而健壮的培养体。试验结果表明:接种量为60个时,每个外植体平均可分化38.6个小苗,显著多于45(分化23.7个)和75(分化30.1个)接种密度处理;从一个反应器中收获的总苗数来看,60和75两种接种密度处理获得的苗数多,超过2 000株,但两者中75接种密度处理得到的增殖苗瘦弱,鲜质量和干质量明显不如60接种密度。故在5 L反应器中加入2 L培养基进行笃斯越橘苗增殖培养时,接种量过多(70个)过少(40个)均不利于丛生芽的增殖生长,接种密度为60较为适宜。
|
|
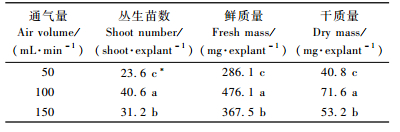
为了探究通气量对笃斯越橘丛生芽在反应器中增殖生长的影响,分别将通气量设置为50,100及150 mL·min-1,空气通入培养基培养60天后发现:通气量为100 mL·min-1时,每个外植体平均分化的苗数达到40.6个,显著高于通气量为50 mL·min-1(23.6个)和150 mL·min-1(31.2个)时的处理;且100 mL·min-1的通气量处理的反应器苗生长健壮,颜色鲜绿,其鲜质量(476.1 mg)和干质量(71.6 mg)值在3种通气量处理中也达到最高。因此,利用反应器进行笃斯越橘种苗扩繁时,在培养基中通入100 mL·min-1的空气为佳。
|
|
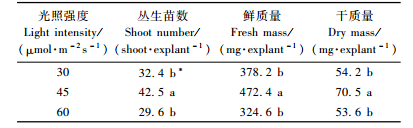
光照强度可激活或抑制某些酶的活性,是诱导植物器官分化的必要条件之一。将光照强度分别调节为30,45和60 μmol·m-2s-1后进行反应器培养,发现光照强度不仅影响苗的分化对其生物量的增加也有影响,光照强度越高,苗的颜色越深,但分化的苗数及苗的鲜质量和干质量的增加则需要一个适宜的光照强度。从表 3可以看出,光强在45 μmol·m-2s-1时,每个外植体不定芽分化数平均为42.5个,苗的鲜质量和干质量分别达到472.4 mg和70.5 mg,显著高于光照强度为30,60 μmol·m-2s-1的光强处理。故利用反应器进行笃斯越橘组培苗的增殖培养时,45 μmol·m-2s-1为较适宜的光照强度。
|
|
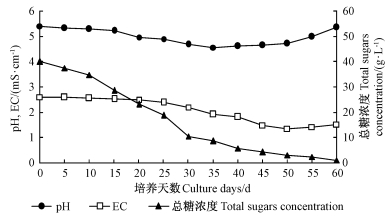
对反应器内笃斯越橘增殖培养过程中培养基的变化进行分析测定,从结果(图 2)可以看出:培养基中总糖浓度在培养0~10天缓慢下降,15~35天则呈现急剧下降的趋势,由15天的28.4 g·L-1下降到35天的8.5 g·L-1,35天后总糖含量很低,并随培养天数的增加而减少,培养结束时(50天)总糖含量仅为2.3 g·L-1;培养基中pH值在0~35天呈下降趋势,由原来的5.5一直降至4.56(35天),从第35天后开始略有上升的趋势,在培养末期60天时基本回升到5.36,这表明培养的外植体具有调节培养基pH的能力;与此同时,随着培养的进行,在0~25天,电导率值逐渐降低,25~50天时,电导率急剧下降,50天时则达到了最低1.35 mS·cm-1,50天以后电导率值出现上升的趋势,这可能是在培养后期,细胞衰亡导致细胞内无机离子释放的结果。
|
图 2 反应器笃斯越橘增殖培养过程中培养基中糖、pH及电导率(EC)的变化 Fig.2 Changes of total sugars concent, pH, and electric conductivity (EC) in culture medium during bioreactor culture of blueberry |
生物反应器培养过程中,接种密度是重要的调控参数之一,利用生物反应器进行植物扩繁的最终目的是得到最多量的健壮繁殖体,接种外植体不可过多或过少。已有研究表明,植物组织培养过程中外植体数/培养基量、外植体数/空气量和外植体数/容器容积等比值直接影响器官形成与发育(McClelland et al., 1990),在植物器官的培养过程中适宜接种密度依据植物种类、培养方式等而不同(Park et al., 2002)。依本研究结果,对笃斯越橘组培苗的增殖培养,5 L反应器中加入2 L培养基的条件下,接种60个外植体较为适宜。利用气升式生物反应器进行植物器官培养时,通入空气的多少是重要的参数指标;通气量与溶氧率有直接的关系,通气量少使培养体在液态培养基中因溶氧量不足器官分化及发育受到影响,通气量过多则因流体动力胁迫使植物生长受到抑制影响生物反应器培养效果(张春华等,2007)。本研究中笃斯越橘反应器增殖培养的适宜通气量为100 mL·min-1,这与玉兰花(Cymbidum niveo-maginatum)(金花等,2007)、人参(李慧娟等,2011)、辰星草(Limonium hybrid ‘Misty Blue’)(廉美兰等,2004)等植物器官反应器培养的结果相同。笃斯越橘组织培养过程中,光照强度影响组培苗增殖和生长,本研究中笃斯越橘生物反应器增殖培养适宜的光照强度为45 μmol·m-2s-1,这与郝明明等(2010)在笃斯越橘组培快繁试验中提出的适宜光照强度(40 μmol·m-2s-1)相近。说明笃斯越橘组培快繁,不论是生物反应器液体培养还是利用传统组培法进行固体培养,对光照强度的要求差异不大,大约为40~45 μmol·m-2s-1。
| [] | 陈巍, 高文远, 贾伟, 等. 2005. 人参属药用植物组织和细胞培养的研究进展. 中草药, 36(4): 616–620. |
| [] | 郝明明, 杜小春, 周文婷, 等. 2010. 蓝莓的快速繁殖. 安徽农业科学(22): 11759–11761. DOI:10.3969/j.issn.0517-6611.2010.22.034 |
| [] | 金花, 朴炫春, 廉美兰, 等. 2007. 利用简易生物反应器大量生产玉兰花根状茎及绿芽. 东北林业大学学报, 35(7): 44–45. |
| [] | 李慧娟, 朴炫春, 代月, 等. 2011. 人参不定根生物反应器培养及其动态学研究. 延边大学农学学报, 33(2): 94–98. |
| [] | 李利军, 孔红星, 何云, 等. 2003. 蔗汁中蔗糖含量的分光光度法测定. 分析测定学报, 22(4): 51–54. |
| [] | 李亚东. 2001. 越橘栽培与加工利用. 长春, 吉林科学技术出版社: 1-6. |
| [] | 李亚东, 姜惠铁, 张志东, 等. 2001. 中国笃斯越橘产业化发展的前景. 沈阳农业大学学报(3): 39–42. |
| [] | 李亚东, 吴林, 刘洪章, 等. 2004. 越橘果实中营养成分分析. 北方园艺(3): 22–23. |
| [] | 廉美兰, 朴炫春, 王颖, 等. 2004. 间歇浸没式生物反应器在辰星草培养苗扩繁中的应用. 园艺学报, 31(4): 532. |
| [] | 罗丽萍, 杨柏云, 章敏华, 等. 2001. 百合的组织培养. 中草药, 32(7): 640–642. |
| [] | 马均, 马明东. 2007. 曼地亚红豆杉的组织培养快繁技术. 林业科学, 43(7): 30–34. |
| [] | 邱德有, 宋经元, 马小军, 等. 2004. 丹参毛状根生物反应器大规模培养的研究. 分子植物育种, 2(5): 699–703. |
| [] | 向德军, 丁家宜, 刘涤. 2001. 甘草毛状根培养系统的建立及化学成分分析. 植物资源与环境学报, 10(1): 7–10. |
| [] | 张春华, 朴炫春, 廉美兰, 等. 2007. 生物反应器在满天星快繁中的应用. 植物学报(4): 526–531. |
| [] | 张明菊. 2005. 生物反应器产业概况. 黄冈职业技术学院学报, 7(3): 87–91. |
| [] | Ahmed El S, David K W, James J L, et al. 1996. Long term effects of propagation by tissue culture or softwood single-node cutting on growth habit, yield, and berry weight of 'Northblue' blueberry. Hortscience, 121(2): 339–342. |
| [] | Gamborg O L, Miller R A, Ojima K. 1968. Nutrient requirements of suspension cultures of soybean root cells. Experimental Cell Research, 50(1): 151–158. DOI:10.1016/0014-4827(68)90403-5 |
| [] | McClelland M T, Smith M A L. 1990. Vessel type, closure and explant orientation influence in vitro performance of five woody species. Hortscience, 25(7): 797–800. |
| [] | Park S Y, Murthy H N, Paek K Y. 2002. Mass multiplication ofprotocorm-like bodies using bioreactor system and subsequent plant regeneration in Phalaenopsis. Plant Cell, Tissue and Organ Culture, 63(1): 67–72. |
| [] | Tulecke W, Nickell L G. 1959. Production of large amounts of plant tissue by submerged culture. Science, 130(3379): 863–864. DOI:10.1126/science.130.3379.863 |
 2012, Vol. 48
2012, Vol. 48