文章信息
- 徐红, 徐勇, 勇强, 余世袁
- Xu Hong, Xu Yong, Yong Qiang, Yu Shiyuan
- 蒸汽爆破预处理对红柳木质组分及酶解性能的影响
- Woody Components and Enzymatic Hydrolysis Property of Tamarix ramosissima under Various Intensity of Steam Explosion
- 林业科学, 2012, 48(11): 92-97.
- Scientia Silvae Sinicae, 2012, 48(11): 92-97.
-
文章历史
- 收稿日期:2012-01-05
- 修回日期:2012-03-07
-
作者相关文章
红柳(Tamarix ramosissima)是高原上一种常见的典型植物,在我国西部地区拥有丰富的资源,仅每年平茬所产生的废弃种条就达到百万吨。作为一种可再生的植物纤维资源,红柳细胞壁中富含纤维素和半纤维素类糖组分,是一种潜在的生物炼制生物基化学品和燃料的优质原料,开展此类资源高效生物利用技术的研发,对于推动西部的国土绿化、生态建设、林业资源的高值利用和农业增收都具有重要意义(李世忠,2011)。目前,国内外有关红柳生物炼制技术和工艺的研究报道较少。
如同其他木质纤维原料,红柳的生物炼制必须经过原料的预处理,其中蒸汽爆破(以下简称为汽爆)可以有效破坏木质纤维素的大分子结构,暴露纤维素或半纤维素,增加后续酶水解反应的有效比表面积,具有速度快、操作简单和化学药品消耗少等优势,可用于木质纤维原料的预处理(Wyman et al., 2005)。原料组分和结构的差异可能会造成汽爆预处理的效果大相径庭,而反应强度系数作为一个工艺参数的综合指标可以较好地评价汽爆预处理效果(王堃等,2006;Hendriks et al., 2009)。本文以汽爆反应温度和保温时间拟合成反应强度系数lgR(Kabel et al., 2007),研究其对红柳的物理结构和化学组成的影响,并且通过纤维素酶水解性能进一步评价汽爆预处理效果,优化汽爆的工艺参数,为红柳生物炼制的相关研究提供理论指导。
1 材料与方法 1.1 原料及仪器原料来自甘肃永靖县,为3~5年生红柳的平茬枝条,直径15~30 mm,风干后剪切至5~6 cm段备用。主要组分为纤维素37.4%、木聚糖18.4%、木质素34.5%。试验所用的纤维素酶来自sigma-aldrich,其滤纸酶活力为每克110FPIU。
主要仪器有3.0 L全自动蒸汽爆破装置(实验室自制)、高效液相色谱(Agilent Technologies 1200 Series)、粉碎机(IKA A11 basic)、摇床(innovative 4000)、环境扫描电镜(Quanta 200)、阳极转靶X射线衍射仪(D/max 2500/PC)、电子天平(FA1004N)、紫外分光光度计(Ultrospec 2100 pro,Amersham Biosciences)、离心机(Thermo)。
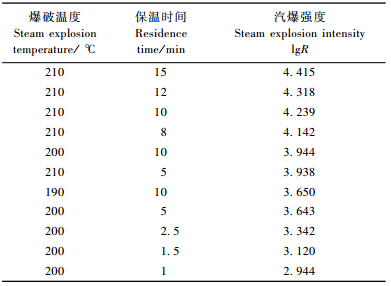
1.2 预处理及组分分析采用双平行试验(控制平行误差小于5.0%),取风干红柳100 g按表 1所示的强度系数lgR进行汽爆预处理,其中R= t·exp[(T-100)/14.75],式中:t为保温时间(min),T为爆破温度(℃)。汽爆后的红柳被称为汽爆料,再经过滤分离后可得到水溶物和固体渣。
|
|
采用双平行试验(控制平行试验误差小于5.0%)。采用50.0 g的反应体系,调节底物浓度5.0%(w/w),加入纤维素酶用量为每克纤维素20.0 FPIU,在pH 4.80、50 ℃条件下进行酶水解反应。定时取样0.5 mL经失活后进行高效液相色谱分析检测。
1.4 分析检测与计算参照NREL方法分析和测定各样品的纤维素、木聚糖、木质素、单糖和抑制物其他主要成分(Sluiter et al., 2008),采用Agilent 1200高效液相色谱仪以Bio-Rad HPX-87H色谱柱测定。扫描电镜观察,样品冷冻干燥,干燥后样品粘台, 真空喷金, 观察纤维形状,拍照。X射线衍射分析, 采用Cu靶。测定参数为:管电压40 kV, 管电流200 mA, Ds=1°, Fs=1°, Rs=0.3 mm, 扫描速度5(°)·min-1。固体渣的纤维素酶水解得率计算公式为:

|
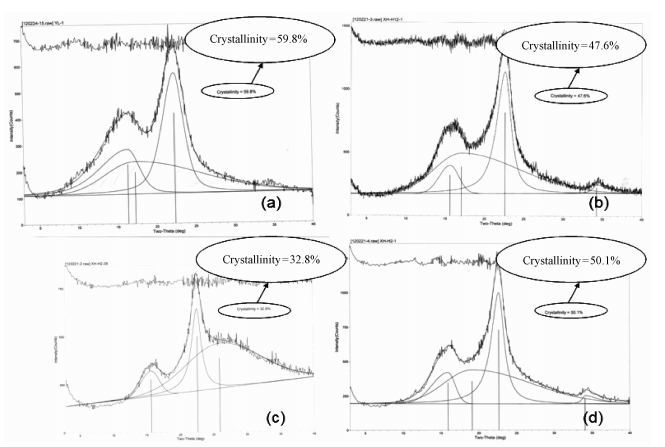
汽爆预处理可以有效改变木质纤维原料红柳的天然结构,并且随着汽爆预处理强度系数的提高,反应的激烈程度不断增加,导致汽爆红柳的颜色由褐色逐渐向黑色过渡,外形由块状向纤维状和泥浆状过渡。图 1中a~c为红柳原料和经不同强度系数汽爆预处理物料的扫描电镜图。对比它们木质纤维表面的2 400倍扫描电镜图像可见,天然红柳的木质纤维表面比较光滑,纤维之间排列规则、紧密,成球状或块状附着在纤维素表面,据报道称为木质素(图 1a);经过汽爆处理后,组织变得松散,空腔增大,纤维表面出现大量的裂纹和裂片,纤维束间发生分离,出现原纤化现象,这样就十分有利于提高纤维素大分子在后续酶水解过程中的反应速率和得率。比较图 1b和图 1c可以发现,随着汽爆预处理强度系数的提高,反应活化能进一步提高,木质纤维原料物理结构的破坏程度加剧,当强度系数lgR超过一定范围后,原料中的木质素又会发生熔融并且重新覆盖纤维素大分子;同时纤维素大分子的非结晶区也开始降解,导致可酶解的纤维素量减少,也会最终影响原料酶水解的得糖率;另外还会引起预处理设备的制造及运行成本的上升。从图 2中可以看出,原料红柳的相对结晶度为59.8%,而经过汽爆处理的物料相对结晶度显著降低,并且在一定范围内强度系数越大,相对结晶度越低,在lgR=4.239时其相对结晶度为32.8%,而lgR=4.415时其结晶度则为50.1%,这说明强度系数过大会造成重结晶现象的发生(谢芳等,2003),这与SEM检测结果一致。因此,寻找适度的汽爆预处理条件是红柳原料糖化和生物炼制的基础。

|
图 1 红柳经汽爆处理前后扫描电镜照片 Fig.1 SEM photos of native and steam-exploded Tamarix ramosissima 放大倍数为2 400 All of the magnification is 2 400。a.机械粉碎后的红柳Tamarix ramosissima after mechanical crushing; b. lgR=4.239汽爆后的红柳Tamarix ramosissima after SEP, lgR=4.239; c.lgR =4.415汽爆后的红柳Tamarix ramosissima after SEP, lgR=4.415. |
|
图 2 红柳原料和爆破后物料的X射线衍射 Fig.2 X-ray diffraction patterns of native and steam-exploded Tamarix ramosissima a.机械粉碎后的红柳Tamarix ramosissima after mechanical crushing; b.lgR=2.944汽爆后的红柳Tamarix ramosissima after SEP, lgR=2.944;c.lgR=4.239汽爆后的红柳Tamarix ramosissima after SEP, lgR=4.239;d.lgR =4.415汽爆后的红柳Tamarix ramosissima after SEP, lgR=4.415. |
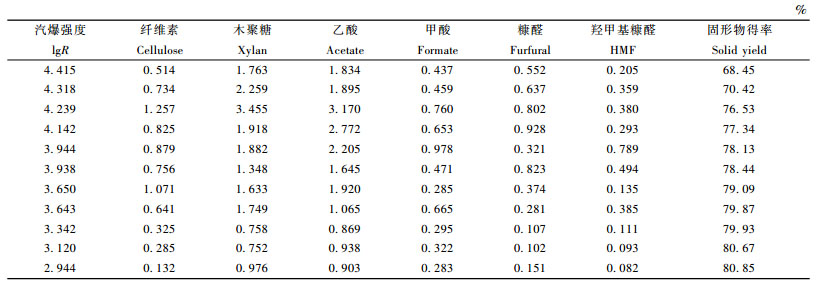
为了进一步表征汽爆对红柳原料各组分的影响,对各种汽爆强度系数下预处理得到的固体渣和溶出物同步进行化学分析和检测,结果分别如图 3和表 2所示。
|
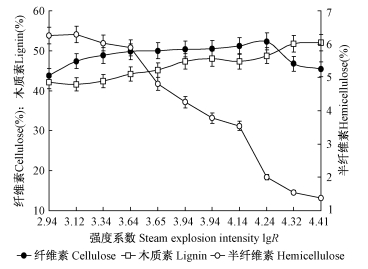
图 3 汽爆强度对固形物组分的影响 Fig.3 The solid components under various intensity of steam explosion |
|
|
由图 3可见,随着汽爆强度系数的上升,红柳中的木聚糖被不断水解和降解溶出,导致汽爆固体渣中木聚糖含量总体呈持续下降的趋势;当lgR≥3.643时,固体渣中残留的木聚糖的含量迅速减少;至反应强度系数超过4.415时,由于残留木聚糖的含量较低,并且它们主要是与纤维素和木质素组分紧密结合,汽爆强度对木聚糖的溶出的影响作用减弱。在试验范围内,红柳汽爆后固体渣中木聚糖的含量可降低至1.38%。这说明蒸汽爆破预处理对红柳木聚糖的溶出十分有效。
与木聚糖相比,纤维素和酸不溶木质素在汽爆过程中较为稳定。由于木聚糖的溶出致使固体渣中纤维素和木质素的含量随着汽爆强度的提高呈逐渐上升的趋势。在强度系数lgR ≤4.239时,汽爆后红柳渣的纤维素含量随着强度系数的提高总体上呈缓慢上升趋势,当强度系数为4.239时,物料的纤维素含量达到52.4%,超过此强度值则会引起固体渣中的纤维素含量迅速下降。结合表 2的分析结果可知,损失的纤维素部分并未生成葡萄糖,而是转变成其他的成分被损失。
表 2的物料分析结果表明,红柳在汽爆预处理过程中会产生众多的水溶性小分子,这主要来源于原料中各种大分子的水解和降解产物,如木糖、葡萄糖类单糖和木质素等,再经进一步降解衍生成多种复杂的小分子酸和呋喃类抑制物(Zaldivar et al., 2001; Palmqvist et al., 2000),如甲酸、乙酸、乙酰丙酸、5-羟甲基糠醛、糠醛(含量较少,表中未列出)和种类繁多的酚类等。其中,乙酸主要来自半纤维素乙酰基的降解、糠醛为木糖的降解所得、5-羟甲基糠醛和乙酰丙酸来自于葡萄糖的分解,糠醛和5-羟甲基糠醛的进一步分解可以生成甲酸,酚类则由木质素降解或缩聚而成(朱均均等,2009)。
从总体规律上来看,随着强度系数的提高,固形物的得率呈下降趋势,在lgR≤4.239范围内其固形物得率差别较小,维持在78%左右,当lgR>4.239时,其固形物得率较低,红柳中木聚糖和葡聚糖的水解溶出率呈上升的趋势,并且对木聚糖的影响效果明显强于纤维素。其中,纤维素水解溶出率的变化趋势较为稳定,而木聚糖的规律性波动明显,这与2种聚糖的组成和大分子结构有关。纤维素是组成和结构更为规则的线性大分子,而木聚糖是高度无定形、多侧链的复杂混合结构。在高温汽爆条件下,前者的水解反应活化能趋于一致,因而高热自水解反应相对均匀;而后者的反应活化能的差异较大,故反应不均匀,在不同的汽爆强度下呈现出一定程度的数据波动。
红柳汽爆物料的化学分析结果表明,汽爆用于红柳的预处理主要是对原料中木聚糖进行水解和降解作用,提高纤维素的有效含量,同时有效破坏红柳的木质天然结构,增大物料的比表面积(Yan et al., 2009; Lin et al., 2010),以利于后续的纤维素酶水解效率的提高。基于木聚糖水解溶出得率的考虑,在汽爆强度系数lgR=4.239(汽爆温度210 ℃,保温时间10 min)时,红柳中木聚糖水解溶出率最高,可达到3.46%,即占原料木聚糖的18.8%;对应的葡萄糖溶出率仅为1.26%,仅占原料纤维素的3.37%,即半纤维素的溶出是纤维素的6倍。由此可见,适宜的汽爆预处理可以有效地分离红柳中的木聚糖类半纤维素,有利于后续的纤维素酶水解。
2.3 汽爆强度对红柳纤维素酶水解性能的影响以上述不同汽爆强度条件下得到的汽爆固体渣为底物,控制底物浓度5.0%(w/w),以每克纤维素20.0 FPIU的纤维素酶用量分别水解24 h和48 h,酶解得率与汽爆强度、物料中纤维素含量的相互关系如图 4所示。
|
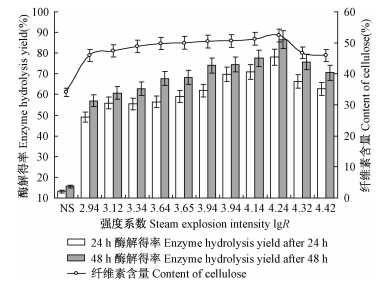
图 4 汽爆强度对红柳酶水解性能的影响 Fig.4 Effects of steam explosion strength on enzyme hydrolysis yield of Tamarix ramosissima 图中NS表示的是经过机械粉碎后过20~80目筛的红柳原料。The NS is Tamarix ramosissima of 20-80 mesh sieve after mechanical crushing. |
图 4表明,红柳经过适当的汽爆预处理,可以显著提高纤维素酶对物料的酶解效率。在lgR=0 ~ 4.239的范围内,汽爆物料的酶解得率随着汽爆强度的增加而增加;至lgR =4.239时,24 h和48 h的酶解得率均可达到最高值78.0%和86.6%;但是当lgR高于4.239以后,酶解得率又呈迅速下降的趋势。蒋建新等(2008)蒸汽爆破预处理沙柳(Salix psammophila)的酶解得率呈现相同的变化规律,即蒸汽爆破预处理可以有效地增加酶解得率,但当强度过大时,酶解得率反而下降。汽爆后沙柳在底物浓度为2.0%、酶用量每克纤维素20FPIU反应72 h后酶解得率仅为69.81%,明显低于汽爆后红柳的酶解得率。
综合2.1和2.2进行分析可知,汽爆红柳的纤维素酶水解得率上升与残余木质素的含量关系不明显,而与原料的天然木质纤维结构的破坏程度、尤其是木聚糖的溶出率呈正相关,同时受纤维素含量的影响(Horn et al., 2011)。过度的汽爆预处理反而会引起酶水解得率下降,主要原因是过高强度的汽爆一是造成部分纤维素的损失,尤其是非结晶区易于酶水解纤维素的流失,二是导致部分木质素重新熔融并包裹纤维素,二者的叠加效应致使在高汽爆强度条件下红柳汽爆固体渣的酶解得率下降。
高效、清洁预处理是木质纤维原料糖化及生物炼制的首要步骤,目前主要为化学法和蒸汽爆破法等。其中,化学法存在着化学品消耗和环境污染的压力,与之相比蒸汽爆破具有处理时间短、污染少和能耗低的优点,具有发展前途。汽爆红柳的酶解结果表明,汽爆用于红柳的糖化及生物炼制的预处理十分有效,汽爆强度系数是影响纤维素含量和酶水解性能的一个重要影响因素。在试验范围内,汽爆强度系数lgR =4.239(温度210 ℃,保温时间10 min)是最佳汽爆预处理工艺条件,汽爆渣的纤维素酶水解得率可达到86.6%。
3 结论汽爆预处理可以有效破坏红柳的天然结构,减少半纤维素和木素对纤维素的包裹作用,并且在一定范围内强度系数越大,破坏程度越大,当强度系数超过4.239(爆破温度210 ℃,保温时间10 min)时,会造成木质素会发生熔融重新包裹纤维素及重结晶现象,影响后续酶解得率。
汽爆预处理可以有效降解并溶出红柳中的木聚糖,进而提高纤维素的有效含量。随着汽爆强度系数的上升,汽爆物料中残留的木聚糖含量迅速下降,纤维素含量缓慢上升。当lgR=4.239时,纤维素含量达到52.4%,木聚糖含量降至最低达到2.01%。
汽爆红柳的纤维素酶水解得率上升与残余木质素的含量关系不明显,而与原料的天然木质纤维结构的破坏程度、尤其是木聚糖的溶出率呈正相关,同时受纤维素含量的影响。基于纤维素回收率、酶解得率和糖降解率,得到红柳的最佳汽爆工艺条件为爆破温度210 ℃,保温时间10 min(lgR=4.239)。在5.0%(w/w)底物浓度和酶用量每克纤维素20FPIU酶水解反应48 h,汽爆红柳的酶解得率可达到86.6%,比天然红柳的酶解得率15.5%提高近5.6倍。蒸汽爆破作为一种简单快速、化学药品和能耗低的预处理技术适宜于红柳的糖化和生物炼制。
| [] | 李世忠. 2011. 永靖县发展红柳资源的必要性与可行性探究. 吉林农业(4): 234. |
| [] | 蒋建新, 刘圣英, 马雅涛, 等. 2008. 蒸汽爆破预处理对沙柳组成及纤维结构性能影响研究. 现代化工, 28(2): 49–53. |
| [] | 王堃, 蒋建新, 宋先亮. 2006. 蒸汽爆破预处理木质纤维素及其生物转化研究进展. 生物质化学工程, 40(6): 37–42. |
| [] | 谢芳, 邵自强, 吕秉峰. 2003. 纤维素蒸汽闪爆改性前后的溶解性能及结构表征研究. 合成技术及应用, 18(2): 1–4. |
| [] | 朱均均, 勇强, 陈尚钘, 等. 2009. 玉米秸秆蒸汽爆破降解产物的分析. 林产化学与工业(29): 22–26. |
| [] | Hendriks A T, Zeeman G. 2009. Pretreatments to enhance the digestibility of lignocellulosic biomass. Biores Technol, 100(1): 10–18. DOI:10.1016/j.biortech.2008.05.027 |
| [] | Horn S J, Estevez M M, Nielsen H K, et al. 2011. Biogas production and saccharification of Salix pretreated at different steam explosion conditions. Bioresource Technology, 102(17): 7932–7936. DOI:10.1016/j.biortech.2011.06.042 |
| [] | Kabel M A, Bos G, Zeevalking J, et al. 2007. Effect of pretreatment severity on xylan solubility and enzymatic break down of the remaining cellulose from wheat straw. Bioresource Technology, 98(10): 2034–2042. DOI:10.1016/j.biortech.2006.08.006 |
| [] | Lin Z, Huang H, Zhang H, et al. 2010. Ball milling pretreatment of enhancing the efficiency of enzymatic hydrolysis. Biochemical and Biotechnology, 162(7): 1872–1880. DOI:10.1007/s12010-010-8965-5 |
| [] | Palmqvist E, Hahn-Hãgerdal B. 2000. Fermentation of lignocellulosic hydrolysates. Ⅱ: inhibitors and mechanisms of inhibition. Bioresource Technology, 74(1): 25–33. DOI:10.1016/S0960-8524(99)00161-3 |
| [] | Sluiter A, Hames B, Ruiz R, et al. 2008. Laboratory technical report. NREL/TP-510-42618. |
| [] | Wyman C E, Dale B E, Elander R T, et al. 2005. Coordinated development of leading biomass pretreatment technologies. Biores Technol, 96(18): 1959–1966. DOI:10.1016/j.biortech.2005.01.010 |
| [] | Yan L, Zhang H, Chen J, et al. 2009. Dilute sulfuric acid cycle spray flow-through pretreatment of corn stover for enhancement of sugar recovery. Bioresouce Technology, 100(5): 1803–1808. DOI:10.1016/j.biortech.2008.10.001 |
| [] | Zaldivar J, Nielsen J, Olsson L. 2001. Fuel ethanol production from lignocellulose: a challenge for metabolic engineering and process Integration. Appl Microb Biotech, 56(1/2): 17–34. |
 2012, Vol. 48
2012, Vol. 48