文章信息
- 雷明, 李昌晓, 陈伟, 魏虹
- Lei Ming, Li Changxiao, Chen Wei, Wei Hong
- 三峡水库岸坡系统不同用地类型对土壤酶活性和土壤化学性质的影响
- Effects of Different Land Use Patterns on Soil Enzymes Activities and Chemical Properties on Riverbank Slopes of the Three Gorges Reservoir
- 林业科学, 2012, 48(11): 15-22.
- Scientia Silvae Sinicae, 2012, 48(11): 15-22.
-
文章历史
- 收稿日期:2012-07-29
- 修回日期:2012-09-23
-
作者相关文章
三峡水库属反季节性调节水库,以年度为周期的人工水位调节,使本已脆弱的库岸生态系统的脆弱性进一步加剧。库区人口密集,人地矛盾十分突出,分布于水库岸坡的大量人类活动严重影响岸坡系统的生态健康,特别是在岸坡上的不合理农业耕作以及盲目性开展基础设施建设,导致库岸生态系统的服务功能明显下降(崔丽娟等,2011;吴义锋等,2011)。在三峡水库水位消涨范围的30 m落差带内,当消落区出露后仍然存在的大量农耕活动产生的影响尤为突出。三峡水库的库岸屏障带主要由大量岸坡系统构成。这些岸坡系统是陆生环境与水生环境之间的过渡带,是陆生系统物质能量进入水库水体的最后一道屏障,具有过滤和缓冲的重要作用,在维护三峡水库生态健康与生态安全方面具有极其特殊的地位(张建春等,2003)。因此,合理的岸坡土地利用方式尤为重要。然而对于具有重要生态功能的三峡库区岸坡系统的可持续利用问题却并未引起人们应有的足够重视。
不同的土地利用方式在反映人类利用土地各种活动目的的同时,也影响着土壤性质的变化(朱祖祥,1983)。改变土地利用方式,可以导致土壤生物化学循环的方向、变化速率以及物质再分配过程的改变,从而影响土壤的理化性质以及许多生态过程的发生(牛文元,1989;傅伯杰等,2001;1999;孔祥斌等,2003;高富等,2000),并最终体现在土壤化学性质的变化以及相应的土壤酶活性的改变。已有大量学者研究不同土地利用方式对土壤化学性质(常超等,2009;林杉等,2008;唐将等,2005;廖晓勇等,2005)或者对土壤酶活性(Klose et al., 2006;Maricel et al., 2005;Stege et al., 2009)单方面的影响,而很少研究不同土地利用方式下土壤酶活性与土壤化学性质之间的变化关系(徐雁等,2010),探讨土壤酶活性与土壤化学性质之间的互作机制,尤其还未见基于三峡库区岸坡系统的不同土地利用方式影响土壤酶活性与土壤化学性质的相关报道。本研究从三峡库区岸坡系统角度研究具有典型代表性的几种用地类型中的土壤酶活性与土壤化学性质之间的关联机制,为合理开发利用以及保护好三峡库区岸坡生态系统提供理论指导。由此假设:1)在三峡库区岸坡坡面尺度条件下,不同土地利用方式将直接影响土壤酶活性、土壤化学性质;2)在消落区进行农事耕作,将对土壤酶活性与土壤化学性质产生负面影响。
1 研究地点与研究方法 1.1 研究地区概况本研究区域位于三峡库区中段忠县境内的汝溪河流域,(107°53′56″—108°14′31″ E,30°22′37″—30°44′53″ N),境内为低山丘陵地貌,拥有典型的岸坡系统,海拔都在117 m以上,属亚热带东南季风区山地气候。温热寒凉,四季分明,雨量充沛,日照充足。≥ 10 ℃年积温5 787 ℃,年均温18.2 ℃,无霜期341天,日照时数1 327.5 h,日照率29%,年降雨量1 200 mm,相对湿度80%;三峡工程竣工后,三峡水库施行“冬蓄夏排”的反季节水位调度管理方式,每年10月汛末开始蓄水,10月底或11月初水库水位上升至最高水位175 m;5月水位又开始下降,6—9月水库水位维持在汛期最低水位145 m,从而形成垂直落差达30 m的三峡库区消落带;地带性森林植被为亚热带常绿阔叶林,原生植被破坏殆尽,现有植被以次生林和灌丛草被为主;土壤主要为发育于亚热带地区石灰性紫色砂页岩母质的紫色土,土层浅薄,土层厚度通常不到50 cm,水土流失较为严重。
1.2 样地设置及土壤样品采集与处理在实地踏查的基础上,于2010年12月在三峡库区忠县石宝镇境内的汝溪河流域坡度大致相同的岸坡上,选定库区具有典型代表性的样地作为研究区域。岸坡接受光照辐射强度大致相同,土壤预热条件基本一致。为使研究样地具有充分的代表性,尽可能考虑到岸坡上的各种不同用地方式,共设置了17个样地,包括3个林地类型、6个退耕地类型、2个耕地类型、4个草地类型、2个消落带类型。利用S型的布点方法(每个样地随机设3条S型样带,每条样带设5个取样点)保证样点的设置完全满足统计学随机性原则。由于人类的长期活动和库区蓄水的影响,致使现存的植被大都为次生植被和人工林,而天然林很少。原有的地带性亚热带常绿阔叶林大多都开垦为耕地和农田,后来部分陡坡耕地退耕还林,在一些土壤瘠薄、坡度较大的地方形成大面积的次生灌草丛,而在海拔175 m以下,受到蓄水的胁迫形成消落带。对样地经纬度、海拔、干扰情况进行记录,并对地被物进行描述(表 1)。每个样地取0~15 cm的表层土壤,5个样点采集1个土壤混合样品(Acosta-Martínez et al., 2007)。将土样带回试验室,风干、磨碎、过筛(孔径为0.25 mm和1 mm),然后保存在4 ℃冰箱中待测。在2周内完成土壤酶活性和土壤理化性质的测定。
|
|
土壤酶的测定参照林先贵(2010)的测定方法:过氧化氢酶采用高锰酸钾滴定法测定,结果以单位土质量消耗0.1 mol·L-1 KMnO4的体积(mL)表示;用3, 5-二硝基水杨酸比色法测定蔗糖酶活性,以24 h后1g土壤葡萄糖的μg数表示;脲酶采用苯酚钠比色法测定,其活性以3 h后每单位土质量产生的NH4+-N的μg数表示;用茚三铜比色法测定蛋白酶活性,以24 h后1 g土壤中氨基氮的微克数表示;采用磷酸苯二钠比色法测定磷酸酶活性,以单位土质量单位时间形成酚的质量(μg)表示。pH值以1:2.5土水比混合后用pH计测定,有机质采用重铬酸钾外加热法,全N采用凯氏定氮法测定,碱解-扩散法测定速效N,全P、速效P利用等离子发射光谱法测定。
1.4 统计分析运用统计软件SPSS(16.0)采用One-way ANOVA来分析不同用地类型对土壤酶活性与土壤化学性质的影响。差异显著性采用Tukey’s检验法来分析。采用Pearson相关系数法评价土壤酶活性与土壤化学性质之间的相关关系。
2 结果与分析 2.1 不同用地类型对土壤酶活性的影响不同土地利用类型显著影响土壤过氧化氢酶活性(F=7.740,P < 0.001图 2a)。各组的过氧化氢酶活性3.008~4.736 mL·g-1,受土地利用类型影响较大。林地中的过氧化氢酶活性显著低于草地(P < 0.01)、退耕地(P < 0.01)、消落带(P < 0.01)中的过氧化氢酶活性,依次降低35.64%,35.35%,36.49%。而草地、退耕地、耕地、消落带的过氧化氢酶活性相互之间差异并不显著(P > 0.05)。
不同土地利用类型显著影响土壤中的脲酶活性(F=13.215,P < 0.001,图 2b)。不同地类的脲酶活性在0.017 ~0.087 μg·g-1h-1之间。其中,退耕地土壤中的脲酶活性分别显著高于林地、草地与耕地(各组的P < 0.05),草地和消落带土壤中的脲酶活性均显著高于林地和耕地(各组的P < 0.05)。消落带与退耕地和草地中的土壤脲酶活性分别均无显著差异(各组的P > 0.05)。
不同土地利用类型也显著影响土壤中的蔗糖酶活性(F=11.534,P < 0.001,图 2c)。所测土壤中蔗糖酶活性在292.446~588.560 μg·g-1h-1之间。其中草地、退耕地土壤中的蔗糖酶活性分别均显著高于林地、耕地与消落带(各组的P < 0.05)。但草地、退耕地土壤之间的蔗糖酶活性差异却不显著;林地、耕地、消落带土壤之间的蔗糖酶活性差异也未达显著水平(P > 0.05)。
蛋白酶活性在不同土地利用类型土壤之间有一定的差异(F=3.381,P=0.030 < 0.05,图 2d)。不同地类的蛋白酶活性在3.431~4.596 μg·g-1h-1之间变化。退耕地土壤中的蛋白酶活性不但显著高于林地(P < 0.05),而且显著高于耕地(P < 0.05),其他用地类型之间差异不显著(P>0.05)。
不同土地利用类型还显著影响土壤中的碱性磷酸酶活性(F=36.130,P < 0.001,图 2e)。不同地类土壤中碱性磷酸酶活性在0.041~0.086 μg·g-1h-1之间。其中,草地、退耕地、耕地、消落带土壤中的碱性磷酸酶活性显著高于林地(各组的P < 0.05),依次高出52.33%,51.76%,46.75%和42.25%。除此之外,消落带土壤中的碱性磷酸酶活性显著低于草地(P < 0.05)、退耕地(P < 0.05),但与其他用地类型之间并未达到显著差异。
总体来说,在各种用地类型中,蔗糖酶的活性占优势地位,而脲酶的活性偏低。
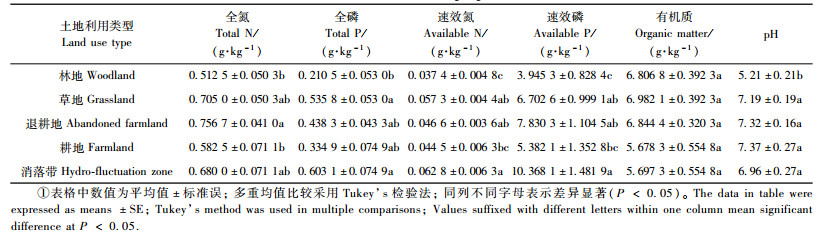
2.2 不同用地类型对土壤化学性质的影响不同用地类型对土壤的有机质含量没有显著影响(表 2),但却对全氮、速效氮、全磷、速效磷以及pH值均产生显著影响(P < 0.05)。林地土壤除了有机质与其余4个不同用地类型未达显著差异外,其全氮、速效氮、全磷、速效磷含量以及pH值均低于其他4种用地类型;与之形成鲜明对比,消落带土壤中的速效氮、速效磷以及全磷含量在所有用地类型中却居于最高。消落带土壤中的全氮含量分别高出林地和耕地33%与17%,速效氮含量分别高出林地和耕地68%与41%;同时,全磷含量分别高出林地和耕地186%与80%,速效磷含量分别高出林地和耕地163%与93%。退耕地中全氮含量居于最高,且显著高于林地和耕地土壤;草地中的有机质含量虽趋于最高,但与其余各组未达显著差异。
|
|
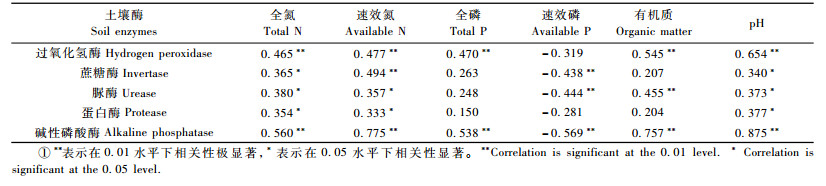
相关性分析表明:过氧化氢酶、碱性磷酸酶活性与全氮、速效氮、全磷、有机质含量以及pH值均分别呈极显著正相关(表 3)。过氧化氢酶活性与速效磷含量并未表现出显著相关性,而碱性磷酸酶活性与速效磷则表现出极显著的负相关;蔗糖酶、脲酶活性分别与全氮、速效氮含量以及pH值表现出显著正相关性,而与速效磷含量却表现出极显著负相关,与全磷含量未达显著相关性。研究还发现脲酶活性与土壤有机质含量呈极显著正相关性,蛋白酶活性与全氮、速效氮含量以及pH值也呈显著正相关。
|
|
土壤酶对维持土壤化学性质具有不可替代的作用。特定土壤酶活性的高低,不仅受到土壤化学性质的影响,还受到土壤所处环境条件的影响(张海峰等,2010)。由于土壤酶活性与土壤化学性质均系土壤的内在因素(Aon et al., 2001),因此人们通常认为二者之间存在着十分密切的相互关系(张宪武,1993;杨万勤等,2002)。在复杂的土壤环境里,重要的土壤酶如过氧化氢酶、脲酶、蔗糖酶、蛋白酶与碱性磷酸酶等,与土壤化学性质之间的关系可能还需要根据具体情况进行分析。
过氧化氢酶是土壤合成腐殖质和防止过氧化氢对生物毒害的重要氧化还原酶系(张海峰等,2010),其活性与土壤pH值存在直接关系(Kannan et al., 2008),其最适pH值7.0左右,过高或过低的pH值都会导致该酶不可逆而失活。林地的酸性土壤对过氧化氢酶产生直接抑制作用,使其过氧化氢酶在几种地类中的活性最低。土壤氮素、全磷含量与过氧化氢酶活性显著正相关(表 3),林地土层浅薄,土壤贫瘠,氮素、全磷含量很低(表 2),导致过氧化氢酶活性不高,这与张仕艳等(2010)的研究结果一致。有研究表明:土壤过氧化氢酶还与土壤有机质关系密切(曹帮华等,2008;陆梅等,2011),其活性能较好表征土壤腐殖化强度大小和有机质积累程度。本研究中,草地、退耕地、耕地、消落带的过氧化氢酶活性相互之间无显著差异,与这几种用地类型土壤有机质含量相互之间无显著性差异密切相关(表 2)。
脲酶直接参与土壤中含氮有机化合物的转化,其活性与土壤氮素、pH值直接相关(Trasar-Cepeda et al.,2008;刘广深等,2003),人们常用土壤的脲酶活性表征土壤的氮素状况。土壤中的脲酶含量过高,容易引起氨的挥发损失(孙艳艳等,2010)。研究结果表明:耕地中的脲酶含量偏低,与之相关的氮素、速效磷、有机质含量也不高,很可能是因为库区农民大都习惯于施用化肥而缺乏农家肥所致。库区频繁农事活动和特有的水文特征,将加剧土壤中有机质、氮素和速效磷的流失,这些营养元素的流失反过来又减少了酶促反应的底物(和文祥等,1997;樊军等,2002)。脲酶活性在林地中最低,与脲酶相关的氮素在林地中的含量也最低(表 2),极有可能是由于林地土壤的pH值偏离脲酶的最适范围(表 2),抑制了脲酶的活性。而退耕地中的脲酶含量却相对较高,这主要是因为以前的耕地土壤较为肥沃,退耕后种植柏木(Cupressus funebris),地面有丝茅(Imperata koenigii)等大量地被物,阻止雨水对土壤的冲刷,同时地表枯落物还能增加土壤营养元素的来源(许其功等,2007),使得作为脲酶重要底物之一的全氮含量在五大用地类型中居于最高(表 2)。还有可能退耕地人为干扰减少,地被物覆盖增加,土壤微环境改善,导致土壤的全氮含量显著高于耕地和具酸性土壤的林地(P<0.05),进而促进土壤脲酶活性增强。本研究发现消落带中的脲酶活性也分别显著高于林地和耕地(P<0.05),这可能是因为消落带土壤中的氮素含量分别高于林地和耕地,为脲酶提供了更加丰富的底物。本研究所在的消落带区域为耕地,施用大量氮肥、磷肥和杀虫剂,N元素的本底营养含量高,对脲酶活性具有一定促进作用。由此可见,笔者先前的第二项假设即在消落区进行农事耕作,将对土壤酶活性与土壤化学性质产生负面影响不成立。导致N元素的本底营养含量高的另一个因素可能是库区地表径流的侵蚀,使吸附大量速效氮、速效磷的物质进入水体沉积所致。
蔗糖酶是土壤中又一广泛存在的酶,其活性对土壤有机碳的矿化起决定作用,是土壤中碳循环的关键酶,该酶受其底物的诱导作用(Verònica et al., 2007;刘兰兰等,2009)。大量的植被需要从土壤吸收更多的碳素,从而刺激蔗糖酶活性的增强(Newman et al., 1993)。植物枯落物的蔗糖酶活性指数高于其他畜禽粪等,能提供更多蔗糖酶的酶促机制,可使蔗糖酶的活性显著提高(Savant et al., 1985)。由于草地大多为一年生草本,代谢较快,土壤中积累了大量枯落物;退耕地也产生大量枯落物,促使土壤微生物变得更为活跃,土壤呼吸强度加大,土壤酶活性增强(李东坡等,2005)。调查发现,林地由于村民常进入其中收集枯枝落叶等采集薪柴活动,使林地进入土壤的枯落物含量相对低于退耕地,因此,从草地、退耕地、林地、消落带到耕地,地表植被及土壤中枯落物含量呈递减趋势(表 1),蔗糖酶活性变化也具有相同趋势(图 2)。消落带中的土壤部分时间处于水淹胁迫,其土壤因缺氧而产生较低的氧化还原电位,将会直接抑制蔗糖酶的活性(刘恩科等,2008;Yan et al., 2003)。相关性分析表明,土壤中的氮素含量与蔗糖酶活性呈现显著正相关(P<0.05)(表 3)。林地土壤酸度抑制了蔗糖酶活性,以及采集薪柴等人为干扰,使氮素含量偏低,而速效磷含量与蔗糖酶活性呈显著的负相关(P<0.05)。试验时耕地中庄稼正处于生长期,被大量利用的速效磷造成蔗糖酶底物缺乏,一定程度上抑制了蔗糖酶活性。此外,耕地中严重的水土流失不但可能加剧速效磷含量的降低,也有可能造成消落带中土壤速效磷高于其他用地类型。
蛋白酶参与土壤中存在的氨基酸、蛋白质以及其他含氮有机化合物的转化,后者的水解产物是高等植物的氮源之一。土壤蛋白酶活性随剖面深度而减弱,并与土壤有机质含量、氮素及其他土壤性质有关。本试验研究主要在表土(0~15 cm)范围内进行,因此其蛋白酶活性在整个剖面最高(Selvaraj,2006;任万军,2011)。土壤施肥较多、植物残体及微生物分布较多的土壤,其养分含量高,有机质丰富,故蛋白酶活性高(张威等,2008)。本试验研究区的退耕地在退耕之前曾因农业耕种施用过大量肥料,地面上的植被枯落物也增加了土壤中有机质的来源(Gallo et al., 2005;Barth et al., 1978;夏汉平等,1997),使其土壤全氮含量在几个用地类型中最高(表 2),因此蛋白酶活性较高;而较低的速效氮含量可能是因为植被的大量利用所致。林地虽然土壤保水保肥性能较差,但其有机质含量却与另外4类用地类型没有显著差异(表 2),表明林地的有机质含量在一定程度上促进了蛋白酶的活性,以满足林地系统物质循环的需要。消落带虽然处于水淹不利环境,具丰富蛋白类有机质含量,使其蛋白酶处于较高活性,说明蛋白酶活性的高低不仅依赖于有机质的高低,还依赖于有机质的组成(刘存歧等,2007)。
磷酸酶都被认为是催化磷酸脂和磷酸酐水解的一组酶(Eivazi et al., 1977)。有机肥的加入能增强磷酸酶的活性,从而增加土壤中有效磷含量。在所有磷酸酶中,碱性磷酸酶是大部分土壤和枯落物中主要的磷酸酶(Criquet et al., 2004),但这些酶活性会受到土壤性质(主要是pH值)、地被物和土地管理状况的影响(Juma et al., 1977),也会影响与之相关的土壤化学性质。在本研究中草地、退耕地、耕地、消落带地被物量基本呈递减趋势,碱性磷酸酶活性也相应降低,而林地受土壤pH值、质地及人为的干扰,引起样地内碱性磷酸酶活性低,从而进一步导致磷素偏低。在消落带研究区,三峡蓄水以前是耕地,现出露后某些部分仍然被当地村民作为耕地继续种植,加之从岸坡上流失的土壤和养分进入水体,沉积于消落带土壤,致使消落带磷素含量远高于其他用地类型,使得其碱性磷酸酶活性显著高于林地。从而进一步证实笔者前面的第二项假设“在消落区进行农事耕作,将对土壤酶活性与土壤化学性质产生负面影响”不成立。本研究进一步发现碱性磷酸酶活性与氮素、全磷含量均表现出显著的正相关,这与刘存歧等(2007)的研究结果完全一致,出现这种现象主要是由于有机质会吸附大量的有机磷,进而增加碱性磷酸酶的活性。当速效磷降低到一定含量时,会刺激根系和微生物分泌产生磷酸酶(舒世燕等,2010)。与之相反,碱性磷酸酶活性与速效磷含量却表现出显著的负相关,这与董莉丽等(2008)在黄土丘陵区不同土地利用类型下的研究结果有所差异,出现这种差异,可能是因为本研究区水土流失以及较低土壤pH值所致,具体的原因还有待更深入的分析研究。
三峡水库岸坡不同用地类型下土壤酶活性受制于土壤环境的影响较大,土壤过氧化氢酶、脲酶、蔗糖酶、蛋白酶和碱性磷酸酶,与土壤氮素、pH值均分别呈显著的正相关性。三峡库区不同土地利用格局下土壤酶的变化机理与土壤化学性质之间的关系密切,为进一步探讨三峡库区退化土壤生态系统的修复和重建提供了一定的参考依据。由此证实笔者先前第一项假设“在三峡库区岸坡坡面尺度条件下,不同土地利用方式将直接影响土壤酶活性、土壤化学性质”成立。本研究发现,林地土壤的氮素、磷素含量在几种用地类型中最低,充分说明林地土壤养分含量相对较少。与其他几种岸坡用地类型相比,岸坡林地能够有效减少三峡库区的面源污染源,显著降低可能进入三峡库区水体的N,P含量。加大库区岸坡系统植树造林活动,保护好现有森林资源,意义重大。而消落带土壤中的速效氮、磷素含量在所有用地类型中却居于最高(表 2),这可能因为该区域一直是耕地,即使在三峡蓄水成库后仍被当地村民作为主要的农地进行耕作,并施用大量氮肥和磷肥,这也表明消落带的人为耕作可能是加剧水库水体N,P元素富营养化的重要来源之一。由此建设在三峡库区,需要进一步增加林地,同时限制消落带进行耕作等农事活动。
| [] | 曹帮华, 吴丽云. 2008. 滨海盐碱地刺槐白蜡混交林土壤酶与养分相关性研究. 水土保持学报, 22(1): 128–133. |
| [] | 常超, 谢宗强, 熊高明, 等. 2009. 三峡库区不同植被类型土壤养分特征. 生态学报, 29(11): 5978–5985. DOI:10.3321/j.issn:1000-0933.2009.11.028 |
| [] | 崔丽娟, 李伟, 赵欣胜, 等. 2011. 湿地岸坡恢复技术研究. 世界林业研究, 24(3): 16–21. |
| [] | 董莉丽, 郑粉莉. 2008. 黄土丘陵区不同土地利用类型下土壤酶活性和养分特征. 生态环境, 17(5): 2050–2058. |
| [] | 樊军, 郝明德. 2002. 旱地农田土壤脲酶与碱性磷酸酶动力学特征. 干旱地区农业研究, 20(1): 35–37. |
| [] | 傅伯杰, 陈利顶, 马克明. 1999. 黄土丘陵区小流域土地利用变化对生态环境的影响. 地理学报, 54(3): 241–246. |
| [] | 傅伯杰, 郭旭东, 陈利顶, 等. 2001. 土地利用变化与土壤养分的变化. 生态学报, 21(6): 927–931. |
| [] | 高富, 沙丽清, 许建初. 2000. 西庄河流域土地利用方式对土壤肥力影响的研究. 土壤与环境, 9(3): 223–226. |
| [] | 和文祥, 朱铭莪. 1997. 陕西土壤脲酶活性与土壤肥力关系分析. 土壤学报, 34(3): 393–398. |
| [] | 孔祥斌, 张凤荣, 齐伟, 等. 2003. 集约化农区土地利用变化对土壤养分的影响——以河北省曲周县为例. 地理学报, 58(3): 333–342. DOI:10.11821/xb200303002 |
| [] | 李东坡, 武志杰, 陈利军, 等. 2005. 长期定位培肥黑土土壤蔗糖酶活性动态变化及其影响因素. 中国生态农业学报, 13(2): 102–105. |
| [] | 廖晓勇, 陈治谏, 刘邵权, 等. 2005. 三峡库区小流域土地利用方式对土壤肥力的影响. 生态环境, 14(1): 99–101. |
| [] | 林杉, 冯明磊, 阮雷雷, 等. 2008. 三峡库区不同土地利用方式下土壤氧化亚氮排放及其影响因素. 应用生态学报, 19(6): 1269–1276. |
| [] | 林先贵. 2010. 土壤微生物研究原理与方法. 北京, 高等教育出版社: 243-265. |
| [] | 刘存歧, 陆健健, 李贺鹏. 2007. 长江口潮滩湿地土壤酶活性的陆向变化以及与环境因子的相关性. 生态学报, 27(9): 3663–3669. |
| [] | 刘恩科, 赵秉强, 李秀英. 2008. 长期施肥对土壤微生物量及土壤酶活性的影响. 植物生态学报, 32(1): 176–182. |
| [] | 刘广深, 徐冬梅, 许中坚, 等. 2003. 用通径分析法研究土壤水解酶活性与土壤性质的关系. 土壤学报, 40(5): 756–762. DOI:10.11766/trxb200111090518 |
| [] | 刘兰兰, 史春余, 梁太波, 等. 2009. 腐植酸肥料对生姜土壤微生物量和酶活性的影响. 生态学报, 29(11): 6136–6141. DOI:10.3321/j.issn:1000-0933.2009.11.047 |
| [] | 陆梅, 韩智亮. 2011. 滇池西岸森林公园4种针叶林土壤酶活性与养分关系研究. 安徽农业科学, 39(13): 7656–7660. DOI:10.3969/j.issn.0517-6611.2011.13.040 |
| [] | 牛文元. 1989. 生态环境脆弱带Ecotone的基础判定. 生态学报, 9(2): 97–105. |
| [] | 任万军, 黄云, 吴锦秀, 等. 2011. 免耕与秸秆高留茬还田对抛秧稻田土壤酶活性的影响. 应用生态学报, 22(11): 2913–2918. |
| [] | 舒世燕, 王克林, 张伟, 等. 2010. 喀斯特峰丛洼地植被不同演替阶段土壤磷酸酶活性. 生态学杂志, 29(9): 1722–1728. |
| [] | 孙艳艳, 蒋桂英, 刘建国, 等. 2010. 加工番茄连作对农田土壤酶活性及微生物区系的影响. 生态学报, 30(13): 3599–3607. |
| [] | 唐将, 李勇, 邓富银, 等. 2005. 三峡库区土壤营养元素分布特征研究. 土壤学报, 42(3): 473–478. DOI:10.11766/trxb200405280319 |
| [] | 吴义锋, 吕锡武. 2011. 岸坡特定生态系统对河渠微型生物群落的影响. 东南大学学报:自然科学版, 41(1): 150–154. |
| [] | 夏汉平, 余清发, 张德强. 1997. 鼎湖山3种不同林型下的土壤酸度和养分含量变化差异及其季节动态特性. 生态学报, 17(6): 645–653. |
| [] | 徐雁, 向成华, 李贤伟. 2010. 土壤酶的研究概况. 四川林业科技, 31(2): 14–20. |
| [] | 许其功, 席北斗, 沈珍瑶, 等. 2007. 耕作措施对三峡库区土壤侵蚀和养分流失的影响. 生态与农村环境学报, 23(3): 41–45. |
| [] | 杨万勤, 王开运. 2002. 土壤酶研究动态与展望. 应用与环境生物学报, 8(5): 564–570. |
| [] | 张海峰, 贡璐, 吕光辉. 2010. 塔里木河流域典型绿洲不同土地利用方式对土壤酶活性的影响. 新疆农业科学, 47(4): 770–773. DOI:10.6048/j.issn.1001-4330.2010.04.027 |
| [] | 张建春, 彭补拙. 2003. 河岸带研究及其退化生态系统的恢复与重建. 生态学报, 23(1): 56–63. |
| [] | 张仕艳, 原海红, 陆梅, 等. 2010. 滇西北不同利用类型土壤酶活性及其与理化性质与微生物的关系. 亚热带水土保持, 22(2): 13–16. |
| [] | 张威, 张明, 张旭东, 等. 2008. 土壤蛋白酶和芳香氨基酶的研究进展. 土壤通报, 39(6): 1468–1474. |
| [] | 张宪武. 1993. 土壤微生物研究. 沈阳, 沈阳出版社. |
| [] | 朱祖祥. 1983. 土壤学. 北京, 农业出版社: 276-279. |
| [] | Acosta-Martinez V, Cruz L, Sotomayor-Ramirez D, et al. 2007. Enzyme activities as affected by soil properties and land use in a tropical watershed. Applied Soil Ecology, 35(1): 35–45. DOI:10.1016/j.apsoil.2006.05.012 |
| [] | Acosta-Martínez V, Mikha M M, Vigil M F. 2007. Microbial communities and enzyme activities in soils under alternative crop rotations compared to wheat-fallow for the Central Great Plains. Applied Soil Ecology, 37(1): 41–52. |
| [] | Aon M A, Colaneri A C. 2001. Temporal and spatial evolution of enzymatic activities andphysico-chemical properties in an agricultural soil. Applied Soil Ecology, 18(3): 255–270. DOI:10.1016/S0929-1393(01)00161-5 |
| [] | Barth R C, Klemmedson J O. 1978. Shrub-induced spatial patterns of dry matter, nitrogen, and organic carbon. Soil Science Society of America Journal, 42(5): 804–809. DOI:10.2136/sssaj1978.03615995004200050031x |
| [] | Criquet S, Ferre E, Farnet A M, et al. 2004. Annual dynamics of phosphatase activities in an evergreen oak litter: influence of biotic and abiotic factors. Soil Biology and Biochemistry, 36(7): 1111–1118. DOI:10.1016/j.soilbio.2004.02.021 |
| [] | Eivazi F, Tabatabai M A. 1977. Phosphatases in soils. Soil Biology and Biochemistry, 9(3): 167–172. DOI:10.1016/0038-0717(77)90070-0 |
| [] | Gallo M E, Lauber C L, Cabniss S E. 2005. Soil organic matter and litter chemistry response to experimental N deposition in northern temperate deciduous forest ecosystems. Global Change Biology, 11(9): 1514–1521. DOI:10.1111/gcb.2005.11.issue-9 |
| [] | Juma N G, Tabatabai M A. 1977. Effects of trace elements on phosphatase activity in soils. Soil Science Society of America Journal, 41(2): 343–346. DOI:10.2136/sssaj1977.03615995004100020034x |
| [] | Kannan I, Wei S. 2008. Soil enzyme activities in two forage systems following application of different rates of swine lagoon effluent or ammonium nitrate. Applied Soil Ecology, 38(2): 128–136. DOI:10.1016/j.apsoil.2007.10.001 |
| [] | Klose S, Acosta-Martínez V, Ajwa H A. 2006. Microbial community composition and enzyme activities in a sandy loam soil after fumigation with methyl bromide or alternative biocides. Soil Biology and Biochemistry, 38(6): 1243–1254. DOI:10.1016/j.soilbio.2005.09.025 |
| [] | Maricel A, Roberto G, Wolfgang H, et al. 2005. Anatomical-physiological determination of surface bound phosphatase activity in ectomycorrhizae of Nothofagus oblique. Soil Biology and Biochemistry, 37(1): 125–132. DOI:10.1016/j.soilbio.2004.07.028 |
| [] | Newman S, Reddy K R. 1993. Alkaline phosphatase activity in the sediment-water column of a hypereutrophic lake. Journal of Environmental Quality, 22(4): 832–838. |
| [] | Stege P W, Messina G A, Sombra L L, et al. 2009. Micellar electrokinetic chromatography after precapillary enzyme assay for the determination of phosphatase activity in semiarid soil. Biochemical Engineering Journal, 46(2): 121–125. DOI:10.1016/j.bej.2009.04.018 |
| [] | Savant N K, James A F, Mcclellan G H. 1985. Effects of soil submergence on urea hydrolysis. Soil Science, 140(2): 81–88. DOI:10.1097/00010694-198508000-00001 |
| [] | Trasar-Cepeda C, Leiròs M C, Gil-Sotres F. 2008. Hydrolytic enzyme activities in agricultural and forest soils. Some implications for their use as indicators of soil quality. Soil Biology and Biochemistry, 40(9): 2146–2155. |
| [] | Venkatesan S, Senthurpandian V K. 2006. Comparison of enzyme activity with depth under tea plantations and forested sites in south India. . Geoderma, 137(1-2): 212–216. DOI:10.1016/j.geoderma.2006.08.011 |
| [] | Yan T M, Yang L Z, Campbell C D. 2003. Microbial biomass and metabolic quotient of soils under different land use in the Three Gorges Reservoir area. Geoderma, 115(1-2): 129–138. DOI:10.1016/S0016-7061(03)00082-X |
 2012, Vol. 48
2012, Vol. 48