文章信息
- 马宏, 李正红, 张艳丽, 王雁, 刘秀贤, 万友名
- Ma Hong, Li Zhenghong, Zhang Yanli, Wang Yan, Liu Xiuxian, Wan Youming
- 大花黄牡丹种子休眠的解除
- Release of Seed Dormancy of Paeonia ludlowii
- 林业科学, 2012, 48(9): 62-67.
- Scientia Silvae Sinicae, 2012, 48(9): 62-67.
-
文章历史
- 收稿日期:2011-08-30
- 修回日期:2012-01-04
-
作者相关文章
2. 中国林业科学研究院林业研究所 北京 100091
2. Research Institute of Forestry, CAF Beijing 100091
大花黄牡丹(Paeonia ludlowii)为芍药科芍药属牡丹组的多年生灌木,是我国西藏特有的重要药用及观赏植物(Hong,1997),被《中国物种红色名录》 (第一卷)列为极危物种(汪松等,2004)。种子繁殖是大花黄牡丹的唯一繁殖途径(成仿云等,1997; 邢震等,2007)。在自然条件下,结实植株仅20%左右,生根成活率仅10%左右,且幼苗死亡率极高,天然更新的巨大障碍是造成大花黄牡丹极危的重要因素之一(杨小林等,2006; 2007; 张蕾,2008; 赵仕虎等,2007; 周生军等,2009)。因此,对大花黄牡丹种子萌发特性进行研究具重要意义,而国内外对此研究极少。
牡丹组植物种子具休眠特性,包括上胚轴及下胚轴休眠,且上胚轴休眠更为突出(刘心民等,2005; 曾端香等,2000)。周仁超等(2002)对牡丹种子休眠解除的研究表明:不同种类种子休眠解除所需条件不同,如500 mg·L-1赤霉素(GA3)处理能显著加快紫斑牡丹(Paeonia rockii)生根速度,提高生根率,但200 mg·L-1以下GA3处理已生根种子却不能打破其上胚轴休眠; 相反,包括GA3在内的各种理化处理均不能使栽培牡丹(Paeonia suffruticosa)种子提早萌发,但以100 mg·L-1 GA3处理根长3 cm以上的生根种子却能打破上胚轴休眠(景新明等,1995); 对滇牡丹(Paeonia delavayi)的研究结果表明:以200 mg·L-1 GA3溶液浸泡24 h、挫伤种脐处种皮和50 ℃温水浸种3种处理方法对胚根的生长都有促进作用,GA3溶液浸泡也能打破上胚轴休眠(娄方芳等,2007)。
对大花黄牡丹种子萌发特性的研究仅见赵仕虎等(2007)的报道。该研究采用随采随播方式,于8月采种后以GA3、乙醇、机械破皮、沙藏处理后直接播种于大田,以不作处理为对照,种子于第2年3月开始出苗,所有处理从出苗开始至出苗结束历时16 ~ 25天,整个过程历时7个月左右,以GA3 500 mg·L-1处理后播种的效果最好,出苗率达91%,而对照出苗率也达77%。这与其他牡丹上胚轴有较长时间休眠有较大差异,且该研究未对播种后下胚轴萌生时间进行观察,也未对上胚轴休眠解除条件进行试验。
本文以自然风干3个月的大花黄牡丹饱满种子为材料,对其种子萌发特性及不同处理的休眠解除进行了系统研究,旨在为进一步揭示大花黄牡丹种子休眠机制提供更多理论依据,为大花黄牡丹的保护及规模化高效快捷育苗提供技术支撑。
1 材料与方法 1.1 材料大花黄牡丹种子2008年9月采自西藏灵芝县、米林县,采后晾干混装于布袋,室内保存,12月底寄达昆明时种子含水量11.2%。
1.2 方法 1.2.1 下胚轴休眠解除试验2008年12月25日种子经0.3%高锰酸钾消毒30 min后,清水冲洗,浸泡1周,待种子完全吸胀后再做各种处理。每处理均3重复,每重复100粒种子。
1) 常规播种:将种子直播于昆明市中国林业科学研究院资源昆虫研究所露地苗床,基质为红壤土、河沙、农家肥按1:1:1比例配制。基质随时保持湿润,冬季不采取加温措施。条播,播种深度5 cm,条距20 cm,粒距5 cm。3个小区,每小区100粒。
2) 温度对下胚轴休眠解除效应:设置5个温度处理,即5,10,15,20,25 ℃,置于人工气候箱中恒温培养。
3) 预处理对下胚轴休眠解除效应:共8个处理,即50 ℃温水(1)、乙烯利20 mg·L-1 (2)、乙烯利50 mg·L-1 (3)、乙烯利80 mg·L-1 (4)、GA3 200 mg·L-1 (5)、GA3 400 mg·L-1 (6)、GA3 600 mg·L-1 (7),以室温清水(8)为对照。以上处理浸泡时间均为24 h,处理后均置于15 ℃人工气候箱中恒温培养。
各处理种子均用高压灭菌的河沙进行层积,培养期间保持沙子湿润。播种20天后,每天观察发根情况,以胚根伸出种皮3 mm视为种子发根。对发根起始天数、发根历期、发根率、发根指数等进行调查及统计。
发根起始天数:指从播种到第1粒种子发根所需天数。
发根历期:发根高峰后连续15天不再有发根种子出现则终止调查,以第1粒种子发根至统计期间最后1粒种子发根所经历时间为发根历期。

|
式中:Gt:置床后t日的发根数; Dt:相应的发根日数。
1.2.2 上胚轴休眠解除试验种子经0.3%高锰酸钾消毒30 min,清水冲洗,浸泡1周后用经高压灭菌的河沙层积,放置于15 ℃人工气候箱中,保持沙子湿润,发根后用于发芽试验。发根种子经各种处理后,埋入泥炭土:珍珠岩(体积比2:1)的基质中置于15 ℃人工气候箱发芽,每个处理40粒生根种子,3次重复,统计各个处理的发芽率和发芽时间,以子叶出土5 mm视为种子发芽。设置以下处理。
1) 上胚轴休眠解除适宜处理时期:选择根长>3,2 ~ 3,1 ~ 2,<1 cm的种子用GA3 200 mg·L-1浸泡2 h,15 ℃人工气候箱发芽。
2) 温度对上胚轴休眠解除的影响:用GA3 200 mg·L-1浸泡根长>3 cm的种子2 h,于10,15,20,25 ℃的人工气候箱中发芽。
3) GA3对上胚轴休眠解除的影响:用50,100,200,300,400 mg·L-1的GA3浸泡根长>3 cm的种子2 h,以室温清水浸泡2 h为对照,处理后置于15 ℃人工气候箱发芽。
4) 低温处理对上胚轴休眠解除的影响:根长>3 cm的种子4 ℃处理20,30,40天,处理后置于15 ℃人工气候箱发芽,以不作任何处理直接于15 ℃人工气候箱发芽为对照。
统计与计算方法与发根试验相同。
1.3 试验数据的处理试验数据采用SPSS 16.0和Excel软件进行统计分析,处理间差异通过单因子方差(One Way ANOVA)检验其是否显著; 对差异显著者,进一步采用LSD和Duncan多重比较,字母法标记; 其中发芽率和生根率数据均进行反正弦转换,以转换后的值进行差异比较,在解释结果时则还原为试验实得数值(张力,2006)。
2 结果与分析 2.1 常规播种生根及萌发情况除播前浸泡外不作任何其他处理的常规播种情况下,大花黄牡丹种子生根及发芽时间极长,且极不整齐,不适于进行精准的统计分析,仅能总结其萌发的基本规律。种子于2009年1月1日播入花盆,2009年5月20日开始生根,即发根起始天数为140天; 10月15日开始出芽,即发芽起始时间为288天,从发根起始至发芽起始为148天。至2010年5月5日平均出芽率为35%,其后直到2010年7月均未再出芽,也即从播种至发芽结束历期490天,从发芽起始至发芽结束历期202天。在202天的发芽历期中,出苗极不规律,有时连续数天出苗,每天出苗1 ~ 3株,有时连续数天不出苗,随后又有苗萌生,无明显出苗高峰,且出芽期间仍有种子陆续生根。
该试验结果说明大花黄牡丹种子存在休眠特性,且表现为下胚轴和上胚轴休眠。
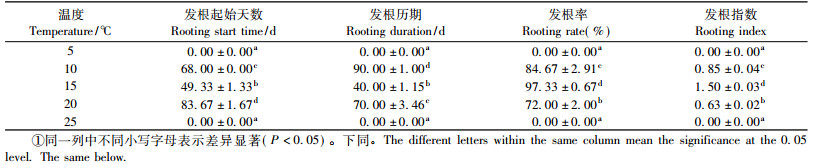
2.2 温度对下胚轴休眠解除效应统计结果(表 1)表明:5 ℃和25 ℃处理种子均未发根,10,15,20 ℃ 3种处理均有生根,且3种处理间的发根起始天数、发根历期、发根率、发根指数均存在显著差异,以15 ℃处理最为理想,该处理所需生根起始时间最短,为49天左右,发根历期也最短,仅需40天发根率即可达97.3%,发根指数达1.50,发根率及发根指数均显著高于其他处理。综合各指标评价,大花黄牡丹种子萌发以15 ℃为最适萌发温度,以此处理可较常规播种缩短发根起始时间91天。
|
|
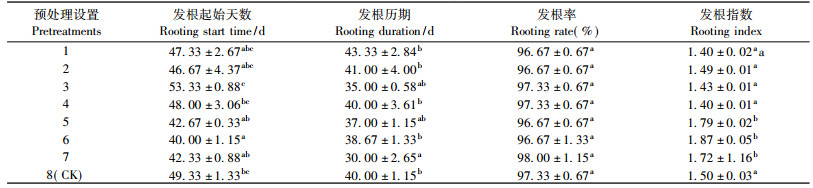
该试验设置的对照及不同预处理条件下,大花黄牡丹种子发根率均可达97%左右,相互间无显著差异(表 2)。但GA3 400 mg·L-1处理的生根起始时间为40天,较对照提早7天,发根历期为38.67天,较对照少10天,发根指数最高,达1.87,3个指标均显著优于对照。因此,采用GA3 400 mg·L-1对大花黄牡丹种子进行预处理,虽不能显著提高生根率,但生根更为整齐,建议生产上酌情使用。
|
|
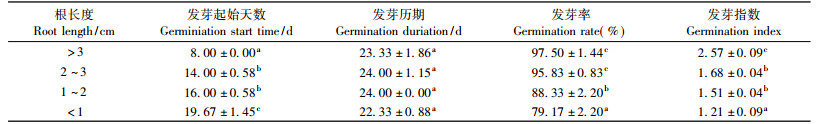
以GA3 200 mg·L-1处理不同根长的种子,以筛选适宜的解除上胚轴休眠的处理时期。结果(表 3)表明:根长<1 cm的种子所需起始发芽天数显著多于其他处理,发芽率、发芽指数则显著低于其他处理。而根长>3 cm的种子所需发芽起始时间显著少于其他处理,发芽率、发芽指数则显著高于其他处理。因此认为以根长达3 cm以上的种子进行上胚轴休眠解除处理最理想,从处理至发芽结束历期只需31天,出芽率可达97%左右。
|
|
温度对大花黄牡丹上胚轴休眠解除具有较大影响(表 4)。25 ℃处理种子发芽率为85.8%,显著低于其他处理,10 ℃处理所需发芽起始时间为21.33天,显著多于其他处理,发芽指数则显著低于25 ℃处理。15 ℃和20 ℃处理种子发芽起始天数、发芽率和发芽指数均无显著差异,发芽率分别为97.5%和95%,与10 ℃处理无显著差异。因此,15 ~ 20 ℃为大花黄牡丹上胚轴解除休眠的适宜温度。
|
|
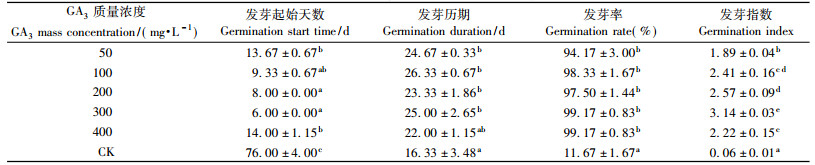
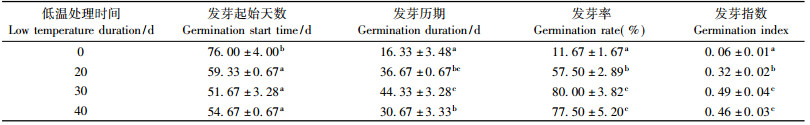
用不同质量浓度的GA3处理根长3 cm以上的种子,均能起到显著的上胚轴休眠解除效果(表 5)。清水浸泡的对照种子从处理到发芽起始需76天,从发芽起始至结束需16.33天,发芽指数0.06,发芽率仅为11.7%,未发芽的种子在试验结束时少部分种子整体腐烂,大部分种子胚根变褐。而不同质量浓度GA3处理的种子所需发芽起始天数均显著少于对照,发芽历期及发芽率相互间均无显著差异,发芽指数以300 mg·L-1处理最高。因此,用300 mg·L-1 GA3浸泡根长3 cm以上的种子2 h具有最好的上胚轴休眠解除效果。在此处理下,发芽起始时间仅需6天,发芽历期25天,发芽率高达99.2%,发芽指数达3.14。
|
|
4 ℃低温处理不同时间对大花黄牡丹上胚轴休眠解除也能起到显著效果(表 6),各处理种子发芽率均显著高于对照,其中以低温处理30天和40天效果最佳,发芽率可达77.5%和80%,两者之间无显著性差异。
|
|
1) 关于大花黄牡丹种子失活问题 休眠是植物种子对环境变化的适应特征,除受多基因调控外,还受植物激素和环境因子的影响(Finkelstein et al., 2008)。张蕾(2008)对大花黄牡丹种子活力检测后认为,大花黄牡丹种子自然风干8天时含水量降至11%,部分种子活力丧失,13天后种子含水量降至6.4%,种子全部丧失活力。龚洵等(1993)对黄牡丹的研究有类似结论,认为黄牡丹(Paeonia lutea)种子含水量为29.5%时胚的生命力开始下降,含水量为14.1%时,所有种子丧失活力。本研究所采用种子于2008年9月采收,于西藏灵芝县室内自然风干保存,于12月底送达昆明时种子含水量为11.2%。以上种子在适宜的处理下出芽率高达95%以上,不仅说明大花黄牡丹种子完全可于室内自然风干存放3个月以上,且可不必随采随播,也不必沙藏,为科学试验和生产实际提供了极大便利。
2) 关于大花黄牡丹下胚轴休眠问题 采用化学药剂处理(Oda et al., 2009)、温水浸种(Sadehgi et al., 2009)等方法或运用砂纸打磨(Sadehgi et al., 2009)、剖开种子(Ashley et al., 2009)等物理手段可有效打破部分种子由于种皮的理化限制而导致的休眠。景新明等(1995; 1999)研究结果表明:栽培牡丹种子在胚根显露前约有3个月的后熟期,去除种皮及各种理化处理均不能显著促进其萌发,而四川牡丹(Paeonia decomposita)、紫斑牡丹等4种野生牡丹,其种子萌发生根前需半年以上,但通过胚培养可使之减至2周。娄方芳等(2007)对黄牡丹种子萌发的研究结果显示:将新采收的成熟种子用GA3处理后在10 ℃下培养,15天后种子出现裂口,60天后生根率达26%,未作处理的对照生根率仅为2%,而GA3处理种子在15 ℃培养下20天后即有种子开始生根,2个月后生根率可达74%,但对照生根率也达50%,此结果表明黄牡丹的种子不论采用何种处理,仍需在适宜萌发温度下经2个月时间才能大量萌发。以上研究结果初步表明:牡丹属植物种子休眠为非物理休眠(胡小文等,2009),亦非化学休眠或综合休眠类型(方升佐等,2011; Cooke et al., 2002; Morris et al., 2000; Sari et al., 2006),而是由于胚未完成后熟作用而导致的生理休眠。由于牡丹种子萌发时先长胚根,再长胚芽,因此由生理后熟导致的休眠首先表现为下胚轴的休眠。
3) 关于大花黄牡丹上胚轴休眠解除 牡丹种子为典型的上胚轴休眠类型,对其休眠解除也有众多研究,多认为须在胚根生长至4 cm左右时用GA3或低温处理才能有效解除休眠(刘心民等,2005)。本文对大花黄牡丹上胚轴休眠解除的研究得出类似结果,以GA3 200 mg·L-1处理根长3 cm以上的种子效果最好,虽对根长1 cm以下的种子也有一定休眠解除效果,处理后40天左右出芽率可达79%,但起始发芽时间较3 cm的种子晚10天左右,而胚根由1 cm生长至3 cm也需要10天左右,因此认为GA3也要在胚根长至3 cm以上后才能充分发挥作用。虽然胚根长3 cm以上的种子经4 ℃低温层积20 ~ 40天也能有效解除上胚轴休眠,但其作用远不如GA3效果好。
关于大花黄牡丹下胚轴生长情况仅见张蕾(2008)的研究,但其研究未说明所用种子状况及萌发试验起始时间。本文所用为采后室内保存3个月的大花黄牡丹种子,但在最适于胚根生长的15 ℃恒温培养箱中培养仍需49天下胚轴才开始萌生,再需40天才完成发根; 而不同质量浓度的乙烯利、GA3及50 ℃浸种处理对生根率无显著影响,说明大花黄牡丹同样可能存在生理后熟作用,而这种作用在种子吸水后40天左右才能完成。由于尚无人研究过刚采收的大花黄牡丹种子于15 ℃下进行恒温培养的生根效果,因此,无从判断其种子生理后熟所需的确切时间。
3.2 结论综合考虑上胚轴及下胚轴休眠解除,大花黄牡丹种子理想的萌发程序和条件为:播种前室温清水浸泡7天,于15 ℃恒温培养; 待根生长至3 cm以上时,以300 mg·L-1 GA3浸泡2 h,置于15 ℃恒温培养。按此处理,从播种到种子发芽结束约需120天,较常规播种缩短370天以上,发芽率可达95%以上,较常规播种提高171.4%以上。
| [] | 成仿云, 李嘉珏, 陈德忠. 1997. 中国野生牡丹自然繁殖特性研究. 园艺学报, 24(2): 180–184. |
| [] | 尚旭岚, 徐锡增, 方升佐. 2011. 青钱柳种子休眠机制. 林业科学, 47(3): 68–74. DOI:10.11707/j.1001-7488.20110311 |
| [] | 胡小文, 武艳培, 王彦荣. 2009. 豆科植物种子物理休眠解除机制的研究进展. 西北植物学报, 29(2): 420–427. |
| [] | 龚洵, 武全安. 1993. 濒危植物黄牡丹受威胁因素初探. 植物引种驯化集刊(8): 141–146. |
| [] | 景新明, 郑光华, 洪德元. 1995. 栽培牡丹的种子萌发和贮藏特性. 植物生理学通讯, 31(4): 268–270. |
| [] | 景新明, 郑光华. 1999. 4种野生牡丹种子休眠和萌发特性及与其致濒的关系. 植物生理学报, 25(3): 214–221. |
| [] | 景新明, 郑光华. 1995. 野生紫斑牡丹和四川牡丹种子萌发特性及与其致濒的关系. 生物多样性, 3(2): 84–87. |
| [] | 刘心民, 程逸远, 张雾, 等. 2005. 牡丹种子萌发特性与播种繁殖技术研究进展. 河南林业科技, 12(4): 38–40. |
| [] | 娄方芳, 赵林森, 李宗艳. 2007. 昆明西山野生黄牡丹种子休眠与萌发特性初步研究. 西南林学院学报, 27(5): 34–37. |
| [] | 汪松, 解炎. 2004. 中国物种红色名录. 第1卷. 北京, 高等教育出版社. |
| [] | 邢震, 张启翔, 次仁. 2007. 西藏大花黄牡丹生境概况初步调查. 江苏农业科学(4): 250–253. |
| [] | 杨小林, 罗健, 鲍隆友. 2006. 濒危植物大花黄牡丹种群结构与分布格局. 西南林学院学报, 26(6): 6–9. |
| [] | 杨小林, 王秋菊, 兰小中, 等. 2007. 濒危植物大花黄牡丹(Paeonialudlowii)种群数量动态. 生态学报, 27(3). |
| [] | 曾端香, 尹伟伦, 赵孝庆, 等. 2000. 牡丹繁殖技术. 北京林业大学学报, 22(3): 90–95. |
| [] | 张蕾. 2008. 大花黄牡丹居群特征及种子生物学研究. 北京林大学硕士学位论文. http: //www. cnki. com. cn/Article/CJFDTOTAL-JSNY200704091. htm |
| [] | 张力. 2006. SPSS 13.0在生物统计中的应用. 厦门, 厦门大学出版社: 42-42. |
| [] | 赵仕虎, 秦临喜, 王琳, 等. 2007. 西藏大花黄牡丹繁殖方法初步研究. 中国现代中药, 9(11): 43–44. DOI:10.3969/j.issn.1673-4890.2007.11.015 |
| [] | 周仁超, 姚崇怀, 潘俊, 等. 2002. 紫斑牡丹种子休眠和萌发特性初步研究. 湖北农业科学(1): 59–60. |
| [] | 周生军, 鲍隆友. 2009. 濒危植物大花黄牡丹的野生资源现状与栽培研究. 中国林副特产(2): 92–94. |
| [] | Ashley J A, Preece J E. 2009. Seed cutting treatments stimulate germination and elucidate a dormancy gradient in dormant Fraxinus americana L. and Fraxinus pennsylvanica Marsh. Propagation of Ornamental Plants, 9(3): 122–128. |
| [] | Cooke J, Cooke B, Gifford D. 2002. Loblolly pine seed dormancy:constraints to germination. New Forests, 23(3): 239–256. DOI:10.1023/A:1020306816009 |
| [] | Finkelstein R, Reeves W, Arrizumi T, et al. 2008. Molecular aspects of seed dormancy. Annual Review of Plant Biology, 59: 387–415. DOI:10.1146/annurev.arplant.59.032607.092740 |
| [] | Hong D Y. 1997. Paeonia (Paeoniaceae) in Xizang (Tibet). Novon, 7(2): 156–161. DOI:10.2307/3392188 |
| [] | Oda A, Kenzo T, Fukuda K. 2009. Optimal germination condition by sulfuric acid pretreatment to improve seed germination of Sabina vulgaris Ant. Journal of Forest Research, 14(4): 251–256. DOI:10.1007/s10310-009-0129-5 |
| [] | Morris E C, Tieu A, Dixon K. 2000. Seed coat dormancy in two species of Grevillea (Proteaceae). Annals of Botany, 86(4): 771–775. DOI:10.1006/anbo.2000.1249 |
| [] | Sadeghi S, Ashrafi Z Y, Tabatabai M F, et al. 2009. Study methods of dormancy breaking and germination of common madder (Rubia tinctorum L.) seed in laboratory conditions. Botany Research International, 2(1): 7–10. |
| [] | Sari A O, Oguz B, Bilgic A. 2006. Breaking seed dormancy of laurel (Laurus nobilis). New Forests, 31(3): 403–408. DOI:10.1007/s11056-005-8678-8 |
 2012, Vol. 48
2012, Vol. 48