文章信息
- 张超, 高金锋, 李彦慧, 李玲
- Zhang Chao, Gao Jinfeng, Li Yanhui, Li Ling
- 低温对2种玉兰花色及相关酶活性的影响
- Effect of Low Temperature on Flower Color and Relevant Enzymes Activity of Two Magnolia Species
- 林业科学, 2012, 48(7): 56-60.
- Scientia Silvae Sinicae, 2012, 48(7): 56-60.
-
文章历史
- 收稿日期:2011-07-14
- 修回日期:2012-01-06
-
作者相关文章
2. 河北农业大学林学院 保定 071000
2. College of Forestry, Agriculture University of Hebei Baoding 071000)
木兰科(Magnoliaceae)木兰属(Magnolia)植物树形优美,花朵艳丽,紫玉兰(Magnolia liliflora)和二乔玉兰(M. ×soulangeana)更是营造我国北方早春园林景观的重要观花小乔木(傅大立等,2003)。我国北方早春晚霜低温一直是影响春花植物正常生长发育和观赏性的关键环境因素之一,李娜等(2010)研究发现:不同品种切花寒菊(Dendranthema morifolia)小花在低温胁迫后花瓣的酶活性降低、细胞膜透性增大,花粉的萌发力下降。田丹青等(2011)的研究认为,低温影响红掌叶片的形态和叶色的正常表达。花色是园林植物重要的观赏特性之一,也是鉴别早春玉兰种类最直接的依据。而关于木兰属植物的研究大多集中在种质资源评价(张庆宝等,2008)和园林应用(周兴文等,2011)上,关于低温对紫玉兰和二乔玉兰花色的影响,至今鲜见报道。在影响植物器官色泽表达方面,李崇晖等(2008)的研究表明:随着早春温度的不断上升,迎红杜鹃(Rhododendron mucronulatum)的花色苷含量降低,花色变淡。张洁等(2011)认为贴梗海棠(Chaenomeles speciosa)的花色与花色苷组分之间存在极显著的相关。本试验研究低温处理后2种玉兰的花色参数、色素含量及相关酶活性的变化,以期为低温对其花色表达的影响研究提供指导和借鉴,为提高其花色观赏价值提供基础数据。
1 材料与方法 1.1 试验材料:供试材料来源于河北农业大学西校区园林试验苗圃内4年生紫玉兰、二乔玉兰。试验苗圃面积为10 m×10 m,2种玉兰隔行种植,株行距为2 m将试验区对角线连接平均分成4个样本区,于2011年4月初在4个样本区分别采样,采样时于植株东、南、西、北4个方位随机采取长势一致,生长健康,无病虫害的紫玉兰和二乔玉兰盛花期花枝,每个样本区采样15个花枝进行低温处理。
1.2 试验方法 1.2.1 低温处理方法利用能够准确模拟自然降温过程的人工霜箱对试材进行低温处理,当霜箱冷却至0 ℃时,将花枝放入人工霜箱内,设置-1,-2,-3,-4,-5,-6 ℃ 6个温度,每个温度处理时间为1 h,每个温度处理2种玉兰各10个花枝,将低温处理后的花枝液氮处理放入-40 ℃超低温冰箱保存,以自然状态下未经低温处理的花瓣作为对照,每个温度处理试材取3次重复,取外层花瓣进行花色参数及相关指标的测定。
1.2.2 花色参数的测定采用日本产Minolta CR- 400型全自动色差计测定各处理外层花瓣中间部位花色参数L*,a*,b*,C*,其中L*表示亮度,a*表示红绿程度,b*表示蓝黄程度,C*表示彩度(Wang,2004)。
1.2.3 花色苷、类黄酮含量的测定称取各处理花瓣0.1 g,剪碎,加入5 mL 1%盐酸甲醇提取液,置于4 ℃冰箱中避光浸提24 h, 取上清液在最大吸收波长530,325 nm测吸光值。花色苷、类黄酮含量的计算参见李彦慧(2008)的方法。
1.2.4 PAL和CHI活性的测定取各处理花瓣0.2 g,加入5 mL pH7.0缓冲液(加入0.018 mol·L-1巯基乙醇,0.05 mol·L-1抗坏血酸以去除酚类物质对颜色的干扰)冰浴研磨,4 ℃,1 000 rpm离心20 min,上清液为PAL和CHI酶提取液。PAL酶活性测定反应体系:3 mL pH8.8硼酸缓冲液+1 mL苯丙氨酸+0.1 mL酶液,35 ℃恒温水浴反应1 h,6 mol·mL-1 HCl终止反应,于290 nm下测定吸光值,以每分钟每克鲜质量变化0.1个吸光度为1个酶活单位;CHI酶活性测定反应体系:2.7 mL牛血清蛋白+0.05 mL查尔酮+0.1 mL酶液,35 ℃恒温水浴反应30 min,于381 nm下测定吸光值, 以每分钟每克鲜质量变化0.1个吸光度为1个酶活单位。PAL和CHI活性的计算参照Lister等(1996)的方法。
1.2.5 数据处理采用Excel和DPS2006统计分析软件对数据进行统计处理及分析,试验结果均为3次重复平均值±标准误,采用Duncan新复极法进行多重比较。
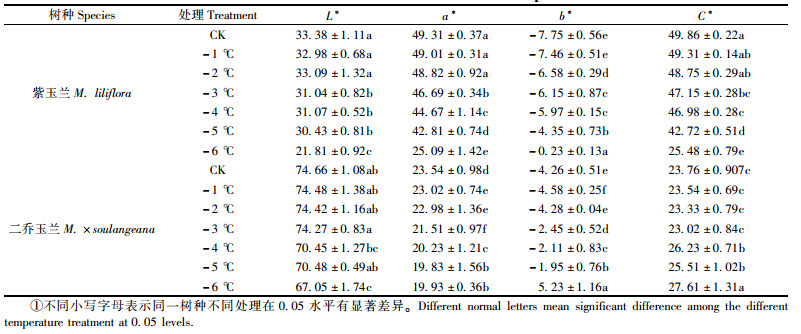
2 结果与分析 2.1 低温处理对花瓣色度值的影响低温处理后2种玉兰花瓣色度值的变化如表 1所示。随着处理温度的降低2种玉兰的L*值总体呈降低趋势,处理初期(-1~-2 ℃)变化缓慢,差异均不显著。紫玉兰在-3 ℃时显著降低,比对照降低了7.04%;二乔玉兰在-4 ℃时明显降低,比对照降低了5.64%。到-6 ℃时,2种玉兰的L*值达到最低,紫玉兰和二乔玉兰分别比相应对照降低34.66%和12.53%。
|
|
随着低温胁迫的加大,2种玉兰的a*值不断降低。紫玉兰在处理-3 ℃之前a*缓慢减小,-4 ℃之后显著降低,到-6 ℃时比对照降低了49.12%;二乔玉兰在处理-6 ℃之前各处理间的a*值达显著水平,且均显著低于对照。
2种玉兰的b*值随着处理温度的降低不断增大,二乔玉兰在-6 ℃时b*值由负值转变为正值,表明低温胁迫后,2种玉兰色泽由蓝色度减弱黄色度加强。
紫玉兰彩度参数C*随着处理温度的降低,呈现不断降低的趋势,处理温度-6 ℃时达到最低,比对照降低了48.89%;在-3 ℃之前,二乔玉兰的C*值随着温度的降低缓慢下降,-4~-6 ℃上升明显,分别比对照时增加10.41%, 7.37%和16.21%。
2.2 低温处理对花瓣花色苷和类黄酮含量的影响不同低温处理后,2种玉兰花色苷及类黄酮含量的变化如图 1所示。二乔玉兰在低温处理初期变化幅度缓慢,在-5 ℃时开始大幅度降低,比对照降低48.91%;紫玉兰在处理-2 ℃之前随着温度的降低而减小,之后变化缓慢,到-6 ℃时达到最低,比对照降低69.52%。

|
图 1 不同低温处理后花色苷及类黄酮含量的变化 Fig.1 The variation of anthocyanin and flavonoid content under different low temperature treatment □ —紫玉兰 Magnolia liliflora; ■二乔玉兰 M. × soulangeana 下同。The same below |
二乔玉兰类黄酮含量的变化随着处理温度的降低呈现不断下降的趋势(图 1B),-6 ℃时达到最低,比对照降低56.34%;低温处理初期,紫玉兰类黄酮含量变化幅度平缓,-5 ℃时开始下降,-6 ℃时比对照时低了74.32%。
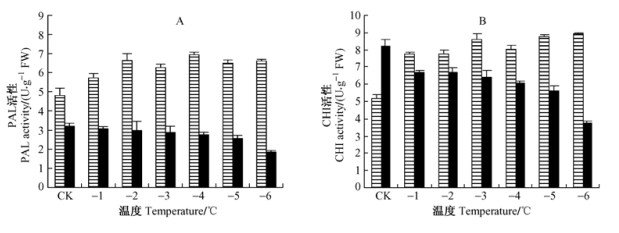
2.3 低温处理对花瓣PAL, CHI活性的影响2种玉兰PAL和CHI活性随着不同处理温度的变化如图 2所示。低温处理初期,紫玉兰的PAL和CHI酶活性随着温度的降低呈现上升趋势,PAL活性在处理-4 ℃时达到最大,比对照增加44.53%,之后变化平缓。CHI活性则在-3 ℃时达到峰值比对照增加了65.79%;二乔玉兰的PAL酶活性随着处理温度的降低缓慢下降,到-6 ℃时达到最低,PAL比对照降低41.93%。对照组CHI活性较高,-2~-5 ℃缓慢降低,到-6 ℃时比对照降低了53.83%。
|
图 2 不同低温处理后PAL和CHI活性的变化 Fig.2 The variation of PAL and CHI activity under different temperature treatment |
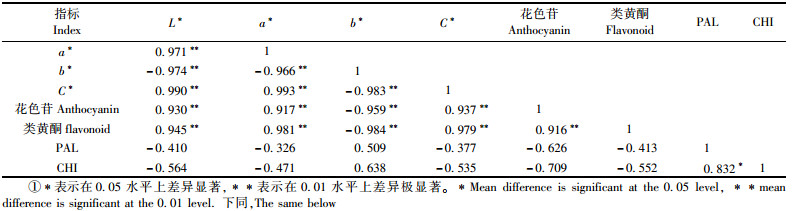
不同低温处理后2树种花瓣色度值、花色苷、类黄酮以及PAL和CHI活性指标间的相关关系(表 2),采用Pearson相关系数,双侧显著性检验。低温胁迫后,紫玉兰花色苷和类黄酮含量均与明亮度L*值,参数a*,C*值呈极显著正相关,与参数b*值呈极显著负相关,PAL和CHI活性的变化与花色苷和类黄酮含量的变化呈负相关关系,但不显著。
|
|
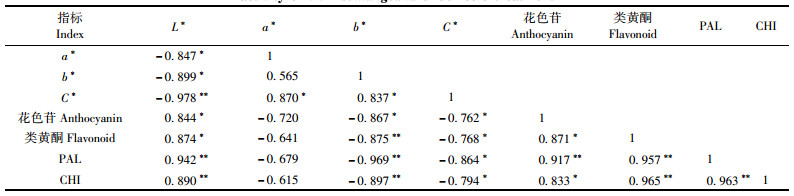
由表 3可知:二乔玉兰明亮度L*与花色苷和类黄酮呈极显著正相关关系,而与a*,b*,C*呈现负相关关系,表明明亮度越高,花色越不鲜艳。花色苷和类黄酮含量均与PAL和CHI酶活性呈显著或及显著正相关关系。
|
|
花色是衡量花卉植物观赏价值的主要标准之一, 影响植物花色的色素群主要有花色苷、类黄酮、类胡萝卜素和甜菜色素(傅荣昭等, 1995)。本试验中,低温导致2种玉兰花色苷和类黄酮含量的降低,相关酶活性的紊乱,对花色的正常表达产生了较大的影响。
胡晓立等(2010)和李云飞等(2009)的研究认为:土壤NaCl胁迫和干旱胁迫后,叶色的亮度值增加,红色度减退,彩度值变小。本试验研究发现:2种玉兰的亮度值L*随着低温胁迫的加大不断减小,花色亮度变暗;a*降低,由红色向绿色发生转变;紫玉兰b*值不断增大,二乔玉兰在处理-6 ℃时b*值由负值转变为正值,表明低温胁迫后,花色由蓝色度减弱黄色度加强;紫玉兰随着温度的降低彩度值不断减小,二乔玉兰则出现先减小后增大的趋势,表明低温导致花瓣彩色度减弱,而当温度过低时,花瓣变色彩度值增大。
色素是花瓣呈色的物质基础,植物通过改变花瓣中各种色素的种类、含量以及分布形成了多彩的花色。有研究表明,适当的低温有助于花色苷的合成(李兴国等,2003)。本试验结果表明:低温处理初期,二乔玉兰花色苷含量变化缓慢,到-5 ℃时陡然降低,比对照降低48.91%,表明适度的低温对二乔玉兰花色苷含量影响不大,温度过低导致其内部结构的破坏或者相关合成物质的减少,含量迅速降低;紫玉兰在低温处理初期,花色苷含量不断下降,-2~-5 ℃变化缓慢,-6 ℃又陡然下降,表明外来的突然降温会影响紫玉兰花色苷含量的合成,当适应了低温环境后变化不大,但低温胁迫继续加大会导致花色苷合成受阻,含量降低。
胡晓立等(2010)的研究认为:NaCl胁迫对类黄酮含量的影响主要是通过对其合成过程中的关键酶和类黄酮合成的前体物质的影响决定的。花色苷和类黄酮是次生代谢产物,其合成的起始酶是PAL酶,也是苯丙烷代谢的关键酶(高华君等,2006),CHI酶在总黄酮化合物的进一步转化中起到重要作用(Ju et al., 1995)。本试验研究发现:低温处理初期,二乔玉兰PAL和CHI活性缓慢降低,而此时花色苷和类黄酮含量变化也较为平缓,当温度继续下降,2种酶活性不断下降,花色苷和类黄酮的合成受阻,其含量也迅速下降,这与前人的研究结果一致。紫玉兰2种酶则随着温度的降低呈现先不断上升后变化缓慢的趋势,有研究证明PAL和CHI酶在植物的抗逆性研究中起重要作用(Engelsma,1974;Bufler et al., 1982),因此,这2种酶活性的提高可能主要是参与植物的抗逆生理,而没有或少部分参与到花色苷和类黄酮的合成,低温处理后这2种酶的活性不断上升,抵御外来低温对植物材料的伤害,而当温度继续降低时酶清除体内自由基能力减弱,活性不再增强,而花色苷和类黄酮的含量显著下降。
本试验研究结果表明:适度的低温(-1~ -4 ℃)对2种玉兰花色的表达影响不大,当处理温度继续降低(-5~-6 ℃)时,花色参数、色素含量以及相关酶活性发生显著变化,紫玉兰花色变暗,红度减退;二乔玉兰亮度降低,变色严重,影响了这2种玉兰的观赏价值。因此,做好早春玉兰的防寒保护工作,有助于2种玉兰花色的保护与维持。此外,如何提高低温胁迫条件下2种玉兰的观赏价值,有待进一步研究。
| [] | 傅大立, 李芳东, 赵天榜, 等. 2003. 玉兰属5树种生理指标的对比研究. 林业科学, 39(1): 44–49. DOI:10.11707/j.1001-7488.20030107 |
| [] | 傅荣昭, 马江生, 曹光诚, 等. 1995. 观赏植物色香形基因工程研究进展. 园艺学报, 22(4): 381–385. |
| [] | 高华君, 王少敏, 王江勇, 等. 2006. 套袋对苹果果皮花青苷合成及着色的影响. 果树学报, 23(5): 750–755. |
| [] | 胡晓立, 杨建民, 陈东亮, 等. 2010. NaCl胁迫对紫叶李叶片色泽的影响. 林业科学, 46(12): 64–69. DOI:10.11707/j.1001-7488.20101210 |
| [] | 李崇晖, 王亮生, 舒庆艳, 等. 2008. 迎红杜鹃花色素组成及花色在开花过程中的变化. 园艺学报, 35(7): 1023–1030. |
| [] | 李娜, 房伟民, 陈发棣, 等. 2010. 切花寒菊小花对低温胁迫的生理响应及其抗寒性分析. 西北植物学报, 30(4): 0645–0651. |
| [] | 李兴国, 于泽源. 2003. 花青苷的研究进展. 北方园艺(4): 6–8. |
| [] | 李彦慧. 2008. 李属彩叶植物耐SO2机制研究. 河北农业大学博士学位论文. |
| [] | 李云飞, 李彦慧, 王中华, 等. 2009. 土壤干旱胁迫对紫叶矮樱(Prunus cistenena cv.Pissardii)叶片呈色的影响. 生态学报, 29(6): 3678–3684. |
| [] | 田丹青, 葛亚英, 潘刚敏, 等. 2011. 低温胁迫对3个红掌品种叶片形态和生理特想的影响. 园艺学报, 38(6): 1173–1179. |
| [] | 张洁, 王亮生, 高锦明, 等. 2011. 贴梗海棠花青苷组成及其与花色的关系. 园艺学报, 38(3): 527–534. |
| [] | 张庆宝, 申亚梅, 范义荣, 等. 2008. 木兰属(Magnolia)观赏植物育种现状及育种策略. 江苏林业科技, 35(6): 46–52. |
| [] | 周兴文, 朱宇林. 2011. 紫玉兰的观赏特性及其在园林中的应用. .北方园艺(8): 93–95. |
| [] | Bufler G, Bangerth F. 1982. UV-induced peroxidase and phenylalanine ammonia-lyase activity and phaseollin accumulation in leaves of Phaseolus vulgaris L. in relation to ethylene. Plant Science Letters, 25(2): 227–237. DOI:10.1016/0304-4211(82)90181-X |
| [] | Engelsma G. 1974. On the mechanism of the changes in PhenylalanineAmmonia-lyase activity induced by ultraviolet and blue light in gherkin hypocotyls. Plant Physiology, 54(5): 702–705. DOI:10.1104/pp.54.5.702 |
| [] | Ju Z G, Liu C L, Yuan Y B. 1995. Relationship among phenylalanine ammonialyase activity, simple phenol concentration and anthocyanin accumulation in apple. Scientia Horticulture, 61: 215–226. DOI:10.1016/0304-4238(94)00739-3 |
| [] | Lister C E, Lancaster J E. 1996. Phenylalanine ammonialyase (PAL) activity and its relationship to anthocyanin and flavoniod levels in New Zealand-grown apple cultivars. Journal of the American Society for Horticulture Science, 12(2): 281–285. |
| [] | Wang L S, Hashimoto F, Shiraishi A, et al. 2004. Chemical taxonomy of the Xibei tree peony from China by floral pigmentation. Journal of Plant Research, 117(1): 47–55. DOI:10.1007/s10265-003-0130-6 |
 2012, Vol. 48
2012, Vol. 48