文章信息
- 刘小金, 徐大平, 杨曾奖, 张宁南, 杨丽莙, 邓和大, 张小云
- Liu Xiaojin, Xu Daping, Yang Zengjiang, Zhang Ningnan, Yang Lijun, Deng Heda, Zhang Xiaoyun
- 广东三地幼龄檀香生长和结香的早期评价*
- Evaluation of Growth and Heartwood Formation of Young Sandal Plantations in Guangdong Province, South China
- 林业科学, 2012, 48(5): 108-115.
- Scientia Silvae Sinicae, 2012, 48(5): 108-115.
-
文章历史
- 收稿日期:2011-02-21
- 修回日期:2011-03-25
-
作者相关文章
2. 龙珠岛檀香产业科技有限公司 高要 526113;
3. 广东省肇庆市林业局 肇庆 526040;
4. 雷州市珍稀树木实业有限公司 雷州 524200
2. Dragon Pearl Island Sandalwood Industrial Technology Corporation Ltd. Gaoyao 526113;
3. Forestry Bureau of Zhaoqing, Guangdong Province Zhaoqing 526040;
4. Leizhou Precious Tree Industrial Corporation Ltd. Leizhou 524200)
檀香(Santalum album),又名印度檀香、白旃檀、真檀等,为檀香科(Santalaceae)檀香属(Santalum)的一种根系半寄生常绿小乔木,原产于印度尼西亚的帝汶岛(Timor),后被引种到印度并且大面积天然繁殖(李应兰等, 1988;李应兰, 2003;Harbaugh et al., 2007)。檀香是一种集药用、香料、宗教、雕刻材料于一体的重要珍贵热带经济树种,其价值较高的部分主要是其具有芳香的心材和从心材中提取的檀香精油(Shri et al., 1972;Rai, 1990;李应兰, 2003)。
我国大陆最早于1962年引种檀香,并且取得成功,但由于受当时栽培技术及经济条件的制约,檀香人工林未能在我国形成规模性的种植(张宁南等, 2006)。近年来,随着栽培技术研究水平的提高,再加上国家林业局对发展种植珍贵树种的大力支持,檀香人工林大规模种植的各种技术障碍已经克服(Liu et al., 2009;刘小金等, 2010a;2010b;徐永荣等,2011),大规模种植的檀香人工林保存率均较高(梁称利等,2011)。据不完全估计,目前我国檀香人工林的种植面积已经超过700 hm2,并且还在逐年增加。
我国华南地区具有充足的水热资源,是檀香较为理想的适生地之一。自2004年起,广东、广西以及海南等地陆续开展了檀香人工林的大规模种植,规模较具代表性的为广东省肇庆市和湛江市。中国林业科学研究院热带林业研究所以科研合作的形式,在高要龙珠岛檀香产业科技有限公司、肇庆金龙珍贵树研究基地和雷州市珍稀树木实业有限公司等3家较专业的檀香种植单位建立试验基地,并对大规模种植的檀香生长情况做定期观测研究。笔者采用标准地的抽样研究方法,调查了上述3个试验基地内种植较早的同一批6年生檀香生长及心材形成(俗称“结香”)情况,通过分析其早期生长及心材形成状况,一方面可以深入了解檀香人工林规模化种植的具体情况(幼龄是否自然结香、精油含量及质量等),并对檀香作为珍贵树种在广东省规模化推广种植的前景做一初步评估,另一方面还可以为今后檀香优良品种的选育工作做准备。
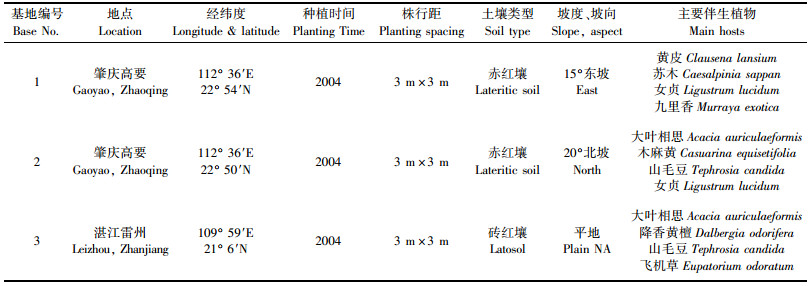
1 材料与方法 1.1 试验地概况试验地位于中国林业科学研究院热带林业研究所檀香试验的上述3个合作研究基地内,根据各基地内檀香的具体种植情况,选择种苗来源、种植时间和种植规格均一致且成片檀香人工林建立标准地,各标准地的种植情况见表 1。
|
|
2010年10月15—30日,在各标准地内(面积为400 m2,3个重复)实测檀香的树高、净树干高度、地径、胸径、冠幅(南北方向)等,再分别从各标准地内随机选择20株檀香用于分析心材形成情况。
1.2.1 心材取样方法檀香心材的取样根据Jones等(2007)的方法进行,略做修改。使用外径为10 mm、内径为4 mm的生长锥分别钻取檀香树干南北方向30和100 cm高度处的木材样品。已有研究表明,檀香树干30和100 cm高度处木材含油量及成分和整株檀香树的含油量及成分具有较强的相关性,可用于估算整株檀香树的精油产量(Jones et al., 2007)。
1.2.2 精油提取方法檀香精油的提取采用乙醚浸渍法(陈志霞等, 2001)。先将钻取的檀香木材样品去掉边材,用高速粉碎机把心材粉碎,过10目筛(李春花等, 2007),然后分成2份,分别称重,一份用乙醚进行震荡提取48 h,过滤后用减压浓缩仪将乙醚挥发掉,如此重复提取2次,最后对2次提取的檀香精油进行合并称量;另一份置于70 ℃恒温烘箱中烘干至恒重,用以测定含水量从而计算心材含油量。
1.2.3 精油成分分析方法采用美国Finnigan TRACE GC-2000-MSTM型气相色谱-质谱联用仪对提取的檀香精油进行成分测定。色谱条件:色谱柱Agilent DB-5(30 m×0.25 mm,0.25 μm);程序升温,起始柱温为45 ℃,保持5 min,再以3 ℃·min-1升至220 ℃,保持5 min;进样口温度为220℃;载气为氦气,流速为1.0 mL·min-1,不分流进样。质谱条件:离子源温度为200 ℃,离子化方式为EI源,电离电压为70 eV,质量扫描范围为35~335 amu。在上述试验条件下,得到檀香精油总离子流图和质谱数据。以总离子流图为依据,用仪器随机配置的微机处理器,采用面积归一化法计算出各峰面积的大小,确定各成分的相对含量;各峰的质谱数据,通过NIST和Willey标准质谱库,用电子计算机检索,再配合人工图谱解析和查阅已公开发表的有关檀香精油成分的质谱文献资料(余竞光等, 1988;1993;Verghese et al., 1990;Shellie et al., 2004;Kim et al., 2005;Jones et al., 2006;Ochi et al., 2006),从而确认檀香精油的化学成分。
1.2.4 统计分析方法采用SPSS(Version 13.0)通用分析软件包对3个试验基地内檀香的形态指标进行方差分析,均值的多重比较采用Duncan新复极差法(α=0.05)。
2 结果与分析 2.1 形态生长指标3个试验基地内檀香的形态生长指标方差分析结果见表 2。由表 2可知:3个基地内种植的同龄檀香,各种形态生长指标的差异达显著水平(P < 0.001)。除平均冠幅外,3号试验基地内6年生檀香的平均胸径、平均树高、平均地径、平均净树干高度均显著地高于1号和2号试验基地。从土壤的养分含量来比较,3号试验基地的土壤养分含量均比1号和2号试验基地要低(数据略),这很可能表明,种植地的气候条件比种植地的营养条件更有利于其生长。檀香是热带树种,原产地为印度尼西亚的帝汶岛(124°56′N,9°14′S),温度(热量)比较高,而3号试验基地位于广东湛江,纬度均比1号和2号试验基地均低,温度(热量)也比较高。一方面在同等时间内增加了积温、提高了生长量;另一方面,檀香在受到极端低温(-1℃)时会出现轻微的寒害而影响其顶梢生长(徐大平等,2008),而3号试验基地冬季最低温度基本不低于-1℃,1号和2号试验基地则偶尔会达到甚至低于该极端低温,相同的时间内增加了寒害胁迫的发生次数和持续时间,生长量就相应的减少了。3号试验基地内檀香的平均胸径生长量比2号试验基地增加30.66%,平均地径增粗22.54%;平均树高生长量比1号试验基地增加15.02%,平均净树干高度增加27.54%,平均冠幅增加15.52%。尽管1号和2号试验基地的地理位置较近,气候条件较为一致,但形态生长指标之间的差异仍然显著(表 2)。1号试验基地的平均胸径和平均地径均显著高于2号试验基地,而平均树高和平均冠幅则显著低于2号试验基地,平均净树干高度差异则不显著,出现这种差异的原因很可能和2个试验基地的经营管理方式(如修枝、寄主配置、除草、追肥方法及肥料配方等)有关,这也间接表明,采用合理的经营方式可以较显著地改变檀香的一些形态生长指标。
|
|
3个试验基地标准地内随机选择的檀香其心材形成情况见表 3。由表 3可知: 3个试验基地内的6年生幼龄檀香均陆续开始形成心材,尽管比例不多(15%~20%)。调查发现1号试验基地内有1株檀香其心材已经发展到100 cm高度处,精油含量为1.76%。幼龄檀香的精油含量比较低,在0.66%~1.76%之间。尽管3号试验基地内檀香的生长量较大(表 2),并且平均净树干高度也最高(檀香精油主要产自于主树干),但心材的量太少,用生长锥钻取的心材样品(质量小于0.2 g)暂无法提取精油。调查还发现,檀香心材主要有2种形态:477201220一种是颜色为浅黄色,质地坚硬,纹理细致均匀,手感明显比边材硬,与已有文献中关于檀香心材的描述较为一致,为自然状态下形成的正常心材(李应兰, 2003);另一种颜色比较黑,外观呈腐坏状态,质地软,很容易破碎,很可能是受到外界(如细菌、真菌、蛀干害虫等)环境的诱导或影响而形成的腐化心材(Jones et al., 2007),这种心材也可以提取檀香精油,但含量稍低。
|
|
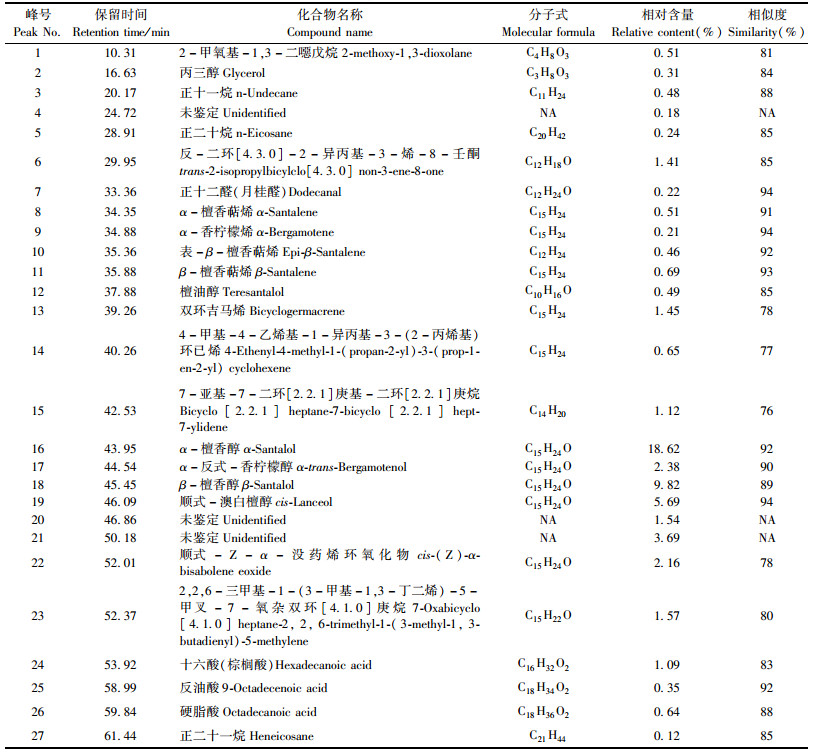
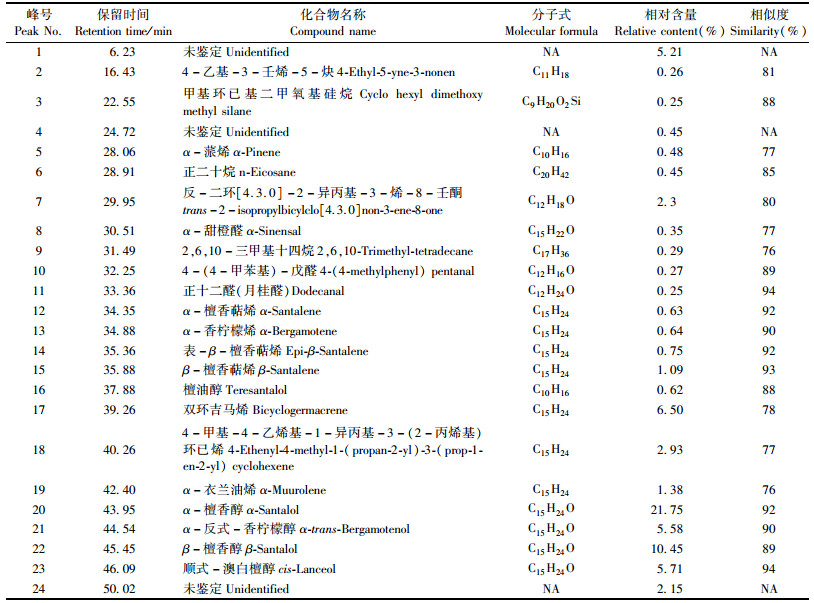
1号和2号试验基地内幼龄檀香心材中提取的檀香精油外观均呈淡黄色,较澄清,具有特征性的甜的木香,香气持久,密度稍小于水,与檀香木油的国际标准中性状一致(ISO, 2002),精油成分的总离子色谱图见图 1。由标准质谱数据库检索的各保留时间对应的化合物及相对含量见表 4, 5。1号试验基地提取的檀香精油中共分离出化合物27种(含3种未鉴定),占总峰面积的56.60%;2号试验基地的檀香精油中共分离出化合物24种(含3种未鉴定),占总峰面积的70.74%。从精油的成分组成上来看,α-檀香醇、β-檀香醇、表-β-檀香萜烯、α-檀香萜烯、β-檀香萜烯、α-反式-香柠檬醇、檀油醇等檀香精油的常见成分都有,但从各成分的相对含量来看,都比较低。由于檀香精油的质量主要取决于其总檀香醇含量大小,质量好的檀香精油其总檀香醇含量高达94%甚至更高(Shri et al., 1972;Verghese et al., 1990),而1号试验基地的檀香精油中总檀香醇含量为34.13%,2号试验基地总檀香醇含量为37.91%,离高质量的檀香精油还存在较大差距,这很可能是由于种植的时间还不够长。
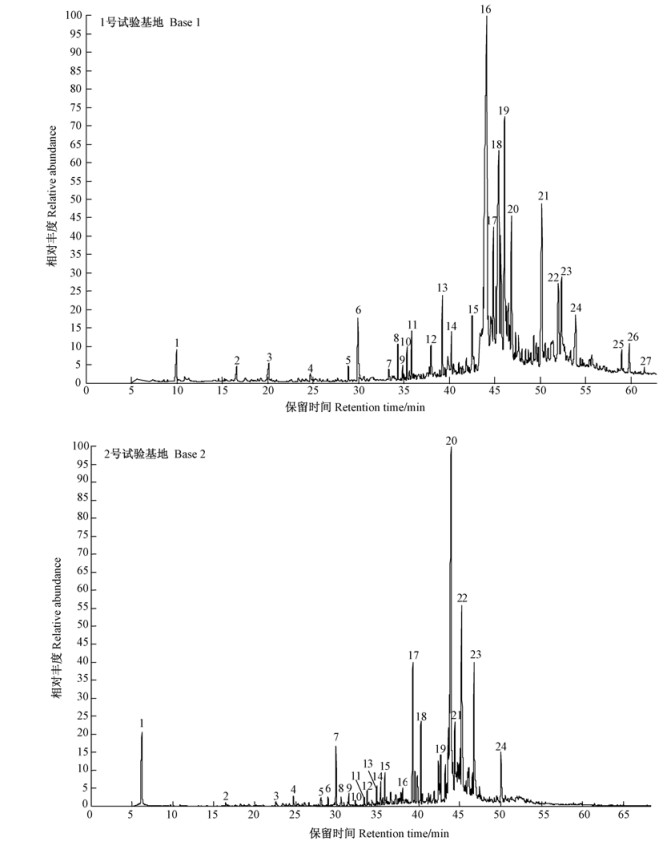
|
图 1 檀香精油成分的总离子流色谱 Fig.1 Total ion chromatogram of sandal essential oil |
|
|
|
|
檀香作为一种热带珍贵经济树种虽然已在我国引种成功,但作为人工林而开展大规模的种植却是从2004年前后才开始的。与早期推广试种的同龄檀香相比[平均树高4.97 m,平均胸径5.76 cm(李应兰, 2003)],目前规模种植的檀香人工林,其树高和胸径的平均生长量分别提高了13.68%和55.21%;3号试验基地内的6龄檀香,其平均胸径大小和早期种植在湛江地区的14龄檀香相当(平均胸径为8.73 cm),但树高略低(平均树高为6.33 m)(黄滨等, 1989)。这不仅表明了檀香可以在我国大规模种植,而且还可能说明采用专业种植、规模种植(集约经营)的方式更有利于檀香的生长,当然也可能和使用高效的栽培技术和采用良种壮苗有关。
3.2 幼龄檀香能自然结香印度早期的资料显示,檀香在10~13龄时才陆续开始形成具有芳香气味的心材,30龄左右为其最佳的商业采伐期(Rai, 1990),但是澳大利亚的一项调查发现,14龄的檀香人工林中,仍有25%的个体未形成心材(Brand et al., 2006);印度班加罗尔地区的一片20龄人工林,也有大约14%的个体仍没有形成心材(Arunkumar et al., 2011);而在我国广东湛江地区,有部分6龄檀香就开始自然结香了(广东省湛江南药试验场, 1983; 李应兰, 2003);在云南的西双版纳,有报道7龄檀香自然结香(周庆年等, 1982),这表明在不同的种植地区,檀香结香的时间差别较大。结合这次的调查结果,再次证实了檀香不仅能在我国南方地区生长良好,而且自然结香的时间也比较早,种植6年就陆续开始形成心材了。本研究还发现,尽管3号试验基地内檀香树高和胸径等形态生长指标均比1号和2号试验基地大,但自然结香的比例反而要小,这说明,对于檀香这一珍贵树种来讲,大的生长量并不意味着较早形成心材,可能与经营管理措施、种植地气候条件、生长状况以及外界环境的刺激或胁迫等有关(黄滨等, 1989)。
3.3 幼龄檀香提取的檀香精油和标准檀香油成分相似,但含量低从幼龄檀香心材中提取出的檀香精油,其主要成分和已报道的成龄檀香油相同。檀香木油的国际标准(ISO, 2002)中规定,同时满足α-檀香醇相对含量在41%~55%之间、β-檀香醇的相对含量在16%~24%之间的檀香木油才达到国际标准,而1号试验基地的檀香油中α-檀香醇含量为18.62%,β-檀香醇含量为9.82%,2号试验基地的檀香油中α-檀香醇含量为21.75%,β-檀香醇含量为10.45%,都没有达到檀香木油的国际标准。从精油含量来比较,檀香的精油含量一般为3%~9%(Rai, 1990),而2个试验基地幼龄檀香的精油含量都很低,平均只有1%左右甚至更低。檀香精油的各种有效成分,很可能在心材形成早期就存在了,后期只是一个随种植时间的增加其有效成分(主要是檀香醇类)逐渐积累或合成的过程。幼龄檀香精油中除了檀香醇类物质,还有一些饱和烃类、具环状结构的不饱和烃、醛类、不饱和酸类以及檀香醇和檀香烯的同分异构体等物质,这些物质很可能是合成檀香醇的部分或全部底物。随着种植时间的增加,在木质部内部次生代谢的调控下,再经过一系列的代谢途径,逐渐转化或合成为檀香醇类化合物,从而增加精油中檀香醇的含量。
3.4 檀香结香机制的研究急需开展檀香的商业价值主要在于其具芳香气味的心材,收获高质量的心材是种植檀香的最终目的,而心材的形成是一个受多方面调控的复杂生理生化过程。有研究认为,檀香心材的形成可能受到激素的调控(李应兰等, 1994;林奇艺等, 2000),从本文的研究结果来看,较快的形态生长量并不意味着形成高质量的心材,可能更受到后期经营管理的影响。因此,急需对心材形成机制进行系统研究。通过开展此项研究,一方面可以为檀香人工林种植后期的经营管理指明方向,使檀香人工林朝着大比例、高质量心材方向发展,大大提高经济效益;另一方面还可以为研究人工促进檀香心材形成的技术或种植方案做准备,最终实现缩短檀香人工林种植周期、提高心材产量和质量的目的。
| [] | 陈志霞, 林励. 2001. 不同提取方法对檀香挥发油含量及成分的影响. 广州中医药大学学报, 18(2): 174–177. |
| [] | 广东省湛江南药试验场. 1983. 湛江引种檀香树结香的观察. 中药材科技(5): 1–2. |
| [] | 黄滨, 冯明开, 陈舜让, 等. 1989. 檀香林分的生长分析. 中药材, 12(12): 7–11. DOI:10.3321/j.issn:1001-4454.1989.12.004 |
| [] | 李春花, 李春香, 李清, 等. 2007. 乳香、檀香混合挥发油的提取工艺研究. 中国药房, 18(12): 894–895. DOI:10.3969/j.issn.1001-0408.2007.12.006 |
| [] | 李应兰. 2003. 檀香引种研究. 北京, 科学出版社. |
| [] | 李应兰, 陈福莲. 1994. 人工促成檀香结香的研究. 热带亚热带植物学报, 2(3): 39–45. |
| [] | 李应兰, 陈福莲, 卜任, 等. 1988. 檀香的自然更新与直播造林技术. 广西植物, 8(4): 339–343. |
| [] | 梁称丽, 张宁南, 龙友深, 等. 2011. 不同种源檀香在广东低山区生长表现. 种子, 30(6): 1–5. |
| [] | 林奇艺, 蔡岳文, 袁亮, 等. 2000. 外界刺激檀香"结香"试验研究. 中药材, 23(7): 375–376. |
| [] | 刘小金, 徐大平, 张宁南, 等. 2010a. 赤霉素对檀香种子发芽及幼苗生长的影响. 种子, 29(8): 71–74. |
| [] | 刘小金, 徐大平, 张宁南, 等. 2010b. 苗期寄主配置对印度檀香幼苗生长影响的研究. 林业科学研究, 23(6): 924–927. |
| [] | 徐大平, 杨曾奖, 梁坤南, 等. 2008. 华南5个珍贵树种的低温寒害调查. 林业科学, 44(5): 1–2. DOI:10.11707/j.1001-7488.20080501 |
| [] | 徐永荣, 王鹏程, 纪和, 等. 2011. 寄主植物生长情况及配置距离对檀香幼林生长的影响. 湖北农业科学, 50(20): 4216–4220. DOI:10.3969/j.issn.0439-8114.2011.20.031 |
| [] | 余竞光, 丛浦珠, 林级田, 等. 1988. 国产檀香油化学成分和五个新化合物的初步结构研究. 药学学报, 23(11): 868–872. |
| [] | 余竞光, 丛浦珠, 林级田, 等. 1993. 国产檀香中α-反式香柠烯醇化学结构研究. 药学学报, 28(11): 840–844. |
| [] | 张宁南, 徐大平, 王卫文, 等. 2006. 檀香栽培现状与发展前景. 林业实用技术(10): 14–16. |
| [] | 周庆年, 刘文杰, 李惠敏, 等. 1982. 檀香树在西双版纳的结香情况和栽培技术. 热带农业科技(2): 48–50. |
| [] | Arunkumar A N, Srinivasa Y B, Joshi G, et al. 2011. Variability in and relation between tree growth, heartwood and oil content in sandalwood (Santalum album L.). Current Science, 100(6): 827–830. |
| [] | Brand J, Kimber P, Streatfield J. 2006. Preliminary analysis of Indian sandalwood (Santalum album L.)oil from a 14-year-old plantation at Kununurra, Western Australia. Sandalwood Research Newsletter, 21: 1–3. |
| [] | Harbaugh D, Baldwin B. 2007. Phylogeny and biogeography of the sandalwoods (Santalum, Santalaceae):repeated dispersals throughout the pacific. American Journal of Botany, 94(6): 1028–1040. DOI:10.3732/ajb.94.6.1028 |
| [] | ISO. 2002. Oil of sandalwood(Santalum album L.)Ⅱedition. 3518:2002 (E), 2002-03-01:Geneva, Switzwerland. |
| [] | Jones C G, Ghisalberti E L, Plummer J A, et al. 2006. Quantitative co-occurrence of sesquiterpenes; a tool for elucidating their biosynthesis in Indian sandalwood, santalum album. Phytochemistry, 67(22): 2463–2468. DOI:10.1016/j.phytochem.2006.09.013 |
| [] | Jones C G, Plummer J A. 2007. Non-destructive sampling of Indian sandalwood (Santalum album L.). for oil content and composition. Journal of essential oil research, 19(2): 157–164. DOI:10.1080/10412905.2007.9699250 |
| [] | Kim T H, Ito H, Hatano T, et al. 2005. Bisabolane-and santalane-type sesquiterpenoids from Santalum album of indian origin. Journal of Natural Products, 68(12): 1805–1808. DOI:10.1021/np050386x |
| [] | Liu X J, Xu D P, Xie Z S, et al. 2009. Effects of different culture media on the growth of Indian Sandalwood (Santalum album L.)seedlings in Zhanjiang, Guangdong, southern China. . Forestry Studies in China, 11(2): 132–138. DOI:10.1007/s11632-009-0023-4 |
| [] | Ochi T, Shibata H, Higuti T, et al. 2005. Anti-helicobacter pylori compounds from Santalum album. Journal of Natural Products, 68(6): 819–824. DOI:10.1021/np040188q |
| [] | Rai S N. 1990. Status and cultivation of sandalwood in India//Hamilton L, Conrad C E. Proceedings of the Symposium on Sandalwood in the Pacafic. 9-11, April. Honolulu, Hawaii. US Forestry Service General Technical Paper PSW-122: 66–71. |
| [] | Shellie R, Marriott P, Morrison P. 2004. Comprehensive two-dimensional gas chromatography with flame ionization and time-of-flight mass spectrometry detection:qualitative and quantitative analysis of West Australian sandalwood oil. Journal of Chromatographic Science, 42(8): 417–422. DOI:10.1093/chromsci/42.8.417 |
| [] | Shri B, Sastri M. 1972. The wealth of India. CSIR publication, New delhi, 9: 208–224. |
| [] | Verghese J, Sunny T P, Balakrishnan K V. 1990. (+)-a-santalol and (-)-p-santalol(Z) concentration, a new quality determinant of East Indian sandalwood oil. Flavour and Fragrance Journal, 5(4): 223–226. DOI:10.1002/(ISSN)1099-1026 |
 2012, Vol. 48
2012, Vol. 48