文章信息
- 刘晋仙, 陶建平, 王玉平, 何泽, 乌玉娜, 郭庆学
- Liu Jinxian, Tao Jianping, Wang Yuping, He Ze, Wu Yuna, Guo Qingxue
- 海南霸王岭山地原始林与伐后林中木质藤本与支持木的多样性及相互关系
- Species diversity and tree-liana relationship in the tropical montane primary forest and post logged forest of Bawangling, Hainan Island, China
- 林业科学, 2012, 48(5): 15-19.
- Scientia Silvae Sinicae, 2012, 48(5): 15-19.
-
文章历史
- 收稿日期:2011-10-31
- 修回日期:2012-03-24
-
作者相关文章
在热带森林中木质藤本的物种丰富度通常占木本植物物种丰富度的25%左右,最高可达44%(Schnitzer et al., 2002),木质藤本对热带森林生物多样性和生态系统功能有重要贡献,是热带森林的重要组成部分。在森林中树木是木质藤本最主要的支撑物,它们二者间的相互作用在很大程度上决定了木质藤本对森林的影响程度(Malizia et al., 2006)。木质藤本会直接或间接地影响森林中树木的生长和更新(陈亚军等, 2007)。而森林类型、演替状态、干扰因素以及木质藤本的攀援方式和个体大小均会直接影响木质藤本对支持木的选择(Dewalt et al., 2000;Laurance et al., 2001;Pérez-Salicrup, 2001;颜立红等, 2007;赵科等, 2010),同时森林冠层郁闭度、树木高度和树木胸径会影响木质藤本在森林中的多度与分布(Yuan et al., 2009)。木质藤本对支持木的利用能力决定了它们的分布策略和对森林群落作用的大小(蔡永立等, 2005)。
目前国内外对干扰林(Reddy et al., 2003;Rice et al., 2004)和原始林(Putz et al., 1987;Appanah et al., 1993;袁春明等, 2010)中藤本植物群落的分布、多样性以及与支持木之间的关系已做了较多研究。对海南霸王岭热带山地原始雨林(赵科等, 2010)和低地干扰林(Ding et al., 2009;乌玉娜等, 2010;2011) 中木质藤本的多样性和结构特征展开了相应研究,山地雨林不同林型中树木群落结构特征也有相关报道(臧润国等, 1999;2001;杨彦承等, 2008)。但缺乏霸王岭山地雨林择伐林中树木与木质藤本的群落结构、多样性以及它们之间相关性的报道。研究表明,采伐干扰会增加热带森林中木质藤本的多度和生物量(Parren et al., 2005;Asner et al.,2006;González-Teuber et al.,2008;Schnitzer et al., 2004;2010;2011),从而会改变森林的结构和动态。本研究选择霸王岭山地原始林和恢复31年的伐后林, 开展群落调查,对比分析2种林地的群落结构特征、物种组成差异以及木质藤本与支持木的关系,以进一步了解择伐干扰对群落结构及群落物种多样性的影响,为合理保护和经营山地雨林提供理论依据。
1 研究区概况霸王岭国家级自然保护区位于海南岛西南部山区(109°03′—109°17′ E, 18°57′—19°11′ N), 总面积约299 800 hm2。该地区属热带季风气候, 干湿季明显。年平均气温23.6 ℃, 年均降水量1 500~2 000 mm,但分布不均, 5—11月为雨季, 12月至翌年4月为旱季。该地区地形复杂,以山地为主, 海拔100~1 654 m,林区内土壤以砖红壤为主, 随海拔增加, 逐渐过渡为山地红壤、山地黄壤和山地草甸土(刘万德等, 2010)。本研究调查的具体地点是长臂猿保护区对面山脊(海拔850~1 000 m,坡度5~10°)的山地原始林和伐后林,土壤为山地黄壤。
2 研究方法野外调查于2009年1—4月进行。在霸王岭山地雨林区内选择原始林和自然恢复31年的伐后林(经采育择伐,强度为30% ~ 45%)作为调查样地。在2林地内分别设置10 m×100 m的样带各2条,每条样带再分为10 m×10 m样地,共设样地40块。记录各样地内胸径≥1 cm的树木的物种名称、胸径、高度以及所攀附木质藤本的物种名称和胸径。采用上限排外法将木质藤本的胸径分为5个等级: < 0.5 cm、0.5~1 cm、1~2 cm、2~5 cm和≥5 cm,将树木胸径分为6个等级:1 ~3 cm、3~5 cm、5~10 cm、10~20 cm、20~40 cm和≥40 cm,树木高度分为5个等级:1.5~3 m、3~5 m、5~10 m、10~20 m和≥20 m。采用单因素方差(One-way ANOVA)分析树木和木质藤本的丰富度、多度以及相同径级内树木和藤本的密度在2林型间的差异。树木附藤率、每藤支持木数以及每木附藤数在2林型间的差异采用Mann-Whitney U检验。支持木胸径、高度与平均每木藤本数间的关系采用相关性和回归分析。显著性水平设定为P < 0.05,所有分析采用SPSS 18.0统计分析软件完成。
3 结果与分析 3.1 树木及木质藤本的物种丰富度和多度原始林样地中DBH≥1 cm的树木共1 722株,隶属于46科,78属,120种。多度最高的前5科依次是樟科(Lauraceae)(15.5%)、茜草科(Rubiaceae)(8.1%)、壳斗科(Fagaceae)(7.3%)、山矾科(Symplocaceae)(6.5%)和桃金娘科(Myrtaceae)(4.9%)。所攀附的木质藤本共有714株,隶属于23科,31属,38种;多度最高的前5种依次是匍匐九节(Psychotria serpens)(21.7%)、夜花藤(Hypserpa nitida)(17.7%)、杜仲藤(Parabarium micranthum)(11.5%)、菝葜(Smilax china)(6.4%)和华南蒟(Piper austrosinense)(6.4%)。
伐后林样地中DBH≥1cm的树木共2 710株,隶属于49科,82属,133种。多度最高的前5科依次是樟科(12.5%)、壳斗科(9.2%)、山矾科(7.5%)、桃金娘科(6.7%)和茜草科(5.8%)。所攀附的木质藤本共有772株,隶属于25科,27属,33种;多度最高的前5种依次是夜花藤(22.7%)、杜仲藤(13.8%)、匍匐九节(12.1%)、细枝菝葜(Smilax amaurophlebia)(11.2%)和菝葜(6.8%)。
树木丰富度(F=5.144,P < 0.05) 和多度(F=18.983,P < 0.01) 在2林型间差异显著,均是伐后林高于原始林。藤本的丰富度(P = 0.659) 和多度(P = 0.615) 在2林型间差异不显著。3 cm ≤ DBH<20 cm的树木密度以及0.5 cm ≤ DBH < 2 cm的木质藤本密度均表现为伐后林大于原始林,只有DBH ≥ 5 cm木质藤本的密度表现为原始林大于伐后林(表 1)。
|
|
原始林样地共有树木1 722株,其中有720株被木质藤本攀附,平均附藤率是41%±2.73%;伐后林样地共有树木2 710株,其中899株被木质藤本攀附,平均附藤率是34%±1.21%。原始林树木平均附藤率显著高于伐后林(P < 0.05)。
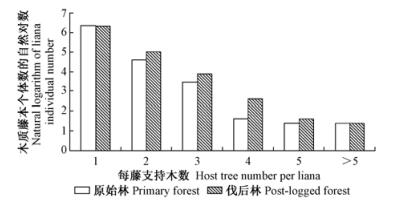
3.2.2 每藤支持木数及每木附藤数原始林样地中每株木质藤本平均攀附1.04 ± 0.042株支持木;伐后林样地中每株木质藤本平均攀附1.19 ± 0.038株支持木。大多数木质藤本只攀附1株支持木,攀附5株以上支持木的木质藤本相对较少,这种趋势在2种林型中表现一致(图 1)。
|
图 1 每藤支持木数分布频率 Fig.1 Distribution frequency of host tree number per liana |
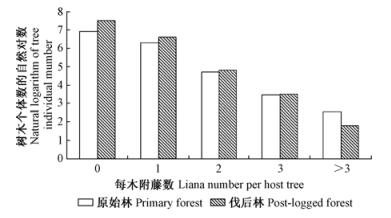
原始林样地附藤树木共有720株,其上攀附木质藤本714株,平均每株支持木攀附木质藤本0.986 ± 0.035株;伐后林样地附藤树木共有899株,其上攀附木质藤本773株,平均每株支持木攀附木质藤本0.857 ± 0.029株。绝大多数支持木只被1株木质藤本攀附,被3株以上木质藤本攀附的支持木数量较少(图 2)。
|
图 2 每木附藤数分布频率 Fig.2 Distribution frequency of liana number per host tree |
原始林样地中平均每木藤本数与支持木胸径之间呈显著的三次函数关系(y=-1.08×10-5x3+1.01×103x2-2.84×10-4x+0.503, R2=0.38,P < 0.000 1);伐后林样地中平均每木藤本数与支持木胸径之间呈显著的幂函数关系(y=1.69×10-1x0.515,R2=0.49,P < 0.000 1)(图 3)。

|
图 3 树木胸径与平均每木藤本数的关系 Fig.3 Correlation between tree DBH and mean number of lianas per tree |
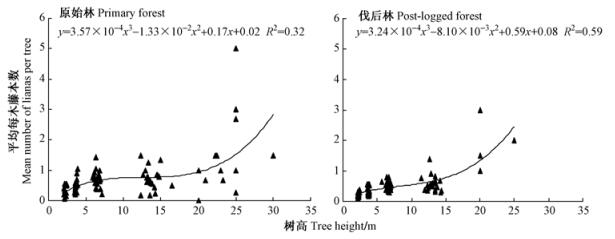
在原始林与伐后林样地中,平均每木藤本数与支持木高度之间存在显著的正相关性,均表现为三次函数关系:原始林为y=3.57×10-4x3-1.33×10-2x2+0.17x+0.02, R2=0.32,P < 0.001;伐后林为y=3.24×10-4x3-8.10×10-3x2+0.59x+0.08, R2=0.59,P < 0.001。2林型内都是随着树木高度的增加攀附的藤本数逐渐增多,伐后林增加的幅度大于原始林(图 4)。
|
图 4 树木高度与平均每木藤本数的关系 Fig.4 Correlation between tree height and mean number of lianas per tree |
本研究表明伐后林中树木的丰富度和多度均高于原始林。采伐作业保留的伐桩萌生了较多的幼株,同时伐后林经过低中度择伐后,林冠层郁闭度变化较小, 林内光照强度较低, 温度变化缓和, 湿度较高, 这些环境条件的综合作用促进了幼株生长。再者,采伐后产生的林隙为新生树种的定居提供了条件,促进了物种多样性增加(Ding et al., 2008),因此伐后林中树木的多度和丰富度高于原始林。而木质藤本的丰富度和多度在2种林型中没有显著变化,这与Dewalt等(2000)对巴拿马中部低地森林和Yuan等(2009)对哀牢山湿地常绿阔叶林中藤本的调查结果并不一致。中等径级树木和木质藤本的多度均表现为伐后林高于原始林,而≥5 cm径级木质藤本的多度表现为原始林高于伐后林(表 1)。择伐干扰后改变了周围的微环境,冠层郁闭度相对降低,促进了森林底层植被的生长(Cannon et al., 1998),因此,伐后林经过30多年的恢复后,原来萌生的幼苗胸径大多已经处在5~20 cm,原来处在中等径级内的树木已经生长为冠层的高大乔木。而大径级木质藤本数量的减少与高大乔木的采伐有关,一般高大的树木容易被大径级的木质藤本攀附(van der Heijden et al., 2008;袁春明等, 2010),在采伐大乔木的同时其上攀附的大径级的木质藤本也遭到破坏。
2林型中树木胸径与平均每木藤本数之间存在显著的相关性,原始林中随着支持木胸径的增加攀附的藤本数先增多后减少,伐后林中随着支持木胸径的增加攀附的藤本数先增多后趋于稳定(图 3)。在热带雨林中,一般大径级支持木枝下高较大,不利于小径级木质藤本攀附,且其上已经攀附的木质藤本会随着枝条或树皮一起脱落,这可能是造成大径级支持木附藤率降低的原因,但还待进一步证实。在2林型间,支持木胸径与附藤率相关性的变化趋势不同,可能与2林型中不同攀援方式的木质藤本的组成比例不同。干扰会直接影响木质藤本不同攀援方式的相对比例(Dewalt et al., 2000),颜立红等(2007)也研究发现藤本与支持木胸径之间的相关性因攀援方式的不同而不同。支持木高度与平均每木藤本数之间存在显著的正相关性(图 4)。为了竞争光资源,大多数木质藤本都努力到达森林冠层(Putz et al., 1987),只有攀附高大的支持木才会提高到达冠层的机率,因此树木越高攀附的藤本数越多。随着树木高度增加平均每木藤本数的增加量表现为伐后林大于原始林。赵科等(2010)对霸王岭热带山地雨林木质藤本垂直结构的研究表明,根攀类木质藤本随高度增加会逐渐增多。在本研究中,主茎缠绕是原始林样地木质藤本的主要攀援方式,而伐后林样地木质藤本的主要攀援方式有主茎缠绕和根攀2种,因此伐后林中每木藤本数随着树木高度增加而增大。
| [] | 蔡永立, 宋永昌. 2005. 浙江天童常绿阔叶林藤本植物的适应生态学研究Ⅱ. 攀援能力和单株攀援效率.植物生态学报, 29(3): 386–393. |
| [] | 陈亚军, 陈军文, 蔡志全. 2007. 木质藤本及其在热带森林中的生态学功能. 植物学通报, 24(2): 240–249. |
| [] | 刘万德, 臧润国, 丁易, 等. 2010. 海南岛霸王岭热带季雨林树木的死亡率. 植物生态学报, 34(8): 946–956. |
| [] | 乌玉娜, 陶建平, 奚为民, 等. 2011. 海南霸王岭天然次生林边缘效应下木质藤本与树木的关系. 生态学报, 31(11): 3054–3059. |
| [] | 乌玉娜, 陶建平, 赵科, 等. 2010. 海南霸王岭天然次生林边缘效应下木质藤本的变化. 林业科学, 46(5): 1–6. DOI:10.11707/j.1001-7488.20100501 |
| [] | 颜立红, 祁承经, 刘小雄, 等. 2007. 湖南藤本植物胸径与其支柱木胸径的相关性. 生态学报, 27(10): 4317–4324. DOI:10.3321/j.issn:1000-0933.2007.10.043 |
| [] | 杨彦承, 张炜银, 林瑞昌, 等. 2008. 海南霸王岭陆均松类热带山地雨林伐后林结构与物种多样性研究. 林业科学研究, 21(1): 37–43. |
| [] | 袁春明, 刘文耀, 杨国平, 等. 2010. 哀牢山湿性常绿阔叶林木质藤本植物的物种多样性及其与支柱木的关系. 林业科学, 46(1): 15–22. DOI:10.11707/j.1001-7488.20100103 |
| [] | 臧润国, 杨彦承, 蒋有绪. 2001. 海南岛霸王岭热带山地雨林群落结构及树种多样性特征的研究. 植物生态学报, 25(3): 270–275. |
| [] | 臧润国, 余世孝, 刘静艳, 等. 1999. 海南霸王岭热带山地雨林林隙更新规律的研究. 生态学报, 19(2): 151–158. |
| [] | 赵科, 陶建平, 郝建辉, 等. 2010. 海南霸王岭热带雨林木质藤本垂直结构特征. 生态学报, 30(12): 3173–3181. |
| [] | Appanah S, Gentry A H, Lafrankie J V. 1993. Liana diversity and species richness of Malaysian rain forests. Journal of Tropical Forest Science, 6(2): 116–123. |
| [] | Asner G P, Broadbent E N, Oliveira P J C, et al. 2006. Condition and fate of logged forests in the Brazilian Amazon. The Nation Academy Sciences of the USA, 103(34): 12947–12950. DOI:10.1073/pnas.0604093103 |
| [] | Cannon C H, Peart D R, Leighton M. 1998. Tree species diversity in commercially logged Bornean rain forest. Science, 281: 1366–1368. DOI:10.1126/science.281.5381.1366 |
| [] | Dewalt S J, Schnitzer S A, Denslow J S. 2000. Density and diversity of lianas along a chronosequence in a central Panamanian lowland forest. Journal of Tropical Ecology, 16(1): 1–19. DOI:10.1017/S0266467400001231 |
| [] | Ding Y, Tao J P, Zhang W Y, et al. 2008. Gap regimes and gap phase regeneration in a tropical Montane rain forest of Hainan Island, South China. Journal of Natural Resources, 23(6): 1022–1034. |
| [] | Ding Y, Zang R G. 2009. Effects of logging on the diversity of lianas in a lowland tropical rain forest in Hainan island, South China. Biotropica, 41(5): 618–624. DOI:10.1111/j.1744-7429.2009.00515.x |
| [] | González-Teuber M, Gianoli E. 2008. Damage and shade enhance climbing and promote associational resistance in a climbing plant. Journal of Ecology, 96(1): 122–126. |
| [] | Laurance W F, Pérez-Salicrup D R, Delamônica P, et al. 2001. Rain forest fragmentation and the structure of Amazonian liana communities. Ecology, 82(1): 105–116. DOI:10.1890/0012-9658(2001)082[0105:RFFATS]2.0.CO;2 |
| [] | Malizia A, Grau H R. 2006. Liana-host tree associations in a subtropical montane forest of north-western Argentina. Journal of Tropical Ecology, 22(3): 331–339. DOI:10.1017/S026646740600318X |
| [] | Parren M P E, Doumbia F. 2005. Logging and lianas in West Africa∥Bongers F, Parren M P E, Traoré D. Forest climbing plants of West Africa:diversity, ecology and management.Wallingford:CABI Publishing, 183-201. |
| [] | Pérez-Salicrup D R. 2001. Effect of liana cutting on tree regeneration in a liana forest in Amazonian Bolivia. Ecology, 82(2): 389–396. DOI:10.1890/0012-9658(2001)082[0389:EOLCOT]2.0.CO;2 |
| [] | Putz F E, Chai P. 1987. Ecological studies of lianas in Lambir National Park, Sarawak, Malaysia. Journal of Ecology, 75(2): 523–531. DOI:10.2307/2260431 |
| [] | Reddy M S, Parthasarathy N. 2003. Liana diversity and distribution in four tropical dry evergreen forests on the Coromandel coast of south India. Biodivers Conserv, 12(8): 1609–1627. DOI:10.1023/A:1023620901624 |
| [] | Rice K, Brokaw N, Thompson J. 2004. Liana abundance in a Puerto Rican forest. Forest Ecology and Management, 190(1): 33–41. DOI:10.1016/j.foreco.2003.10.004 |
| [] | Schnitzer S A, Bongers F. 2002. The ecology of lianas and their role in forests. Trends in Ecology and Evolution, 17(5): 223–230. DOI:10.1016/S0169-5347(02)02491-6 |
| [] | Schnitzer S A, Bongers F. 2011. Increasing liana abundance and biomass in tropical forests:emerging patterns and putative mechanisms. Ecology Letters, 14(4): 397–406. DOI:10.1111/ele.2011.14.issue-4 |
| [] | Schnitzer S A, Carson W P. 2010. Lianas suppress tree regeneration and diversity in treefall gaps. Ecology Letters, 13(7): 849–857. DOI:10.1111/ele.2010.13.issue-7 |
| [] | Schnitzer S A, Parren M P E, Bongers F. 2004. Recruitment of lianas into logging gaps and the effects of pre-harvest climber cutting in a lowland forest in Cameroon. Forest Ecology and Management, 190(1): 87–98. DOI:10.1016/j.foreco.2003.10.008 |
| [] | van der Heijden G M F, Phillips O L. 2008. What controls liana success in Neotropical forests? Global Ecology and Biogeography. Global Ecology and Biogeography, 17(3): 372–383. DOI:10.1111/geb.2008.17.issue-3 |
| [] | Yuan C M, Liu W Y, Tang C Q, et al. 2009. Species composition, diversity, and abundance of lianas in different secondary and primary forests in a subtropical mountainous area, SW China. Ecological Research, 24(6): 1361–1370. DOI:10.1007/s11284-009-0620-7 |
 2012, Vol. 48
2012, Vol. 48


