文章信息
- 谢涛, 王焕龙, 张儒
- Xie Tao, Wang Huanlong, Zhang Ru
- 几种小红栲变性淀粉的结构特性
- Structural Properties of Several Castanopsis carlesi Modified Starches
- 林业科学, 2011, 47(9): 185-188.
- Scientia Silvae Sinicae, 2011, 47(9): 185-188.
-
文章历史
- 收稿日期:2009-12-03
- 修回日期:2010-01-24
-
作者相关文章
目前世界上变性淀粉的年产量已经达到500万t左右,如美国为200万t以上,欧洲为90万t,日本在30万t以上; 而我国在2000年变性淀粉的产量为35万t,仅为世界产量的7%,根本无法满足国内109万t以上的市场需求而每年都要从国外进口(付陈梅等,2003)。小红栲(Castanopsis carlesi)又名米槠,为壳斗科栲属常绿乔木,分布于我国长江以南各地,资源丰富,其种子是我国最大的野生木本粮食资源橡实的一种。小红栲种仁味甜可食,淀粉含量达60.5% (谢碧霞等,2002)。目前,国内外有关小红栲淀粉的相关研究报道很少。谢涛等(2002; 2003)研究表明:小红栲淀粉颗粒的形状比较规则,具有明显的偏光黑十字,其晶体结构属于C型。小红栲淀粉的直链淀粉含量为22.83%,糊化温度为65.5 ~ 69.5 ℃。小红栲淀粉糊具有酶解率较高、透明度低、凝沉稳定性较强、冻融稳定性较好的特性; 在pH 6.0 ~ 8.0范围内小红栲淀粉糊的黏度较高,温度和转速对糊黏度有一定影响,浓度对糊黏度有显著影响。钟秋平等(2008a; 2008b)研究发现:加压处理对小红栲淀粉凝胶体口感有显著影响,淀粉加工过程中,通过控制高压处理的含水率、压力和保压时间,可得到所需特性的淀粉。高压处理不会改变小红栲淀粉的晶体类型,但对晶相结晶度有极显著的影响。高压处理时淀粉含水率越高,其结晶度越低; 压力增加,其结晶度降低。本文将进一步对小红栲多孔淀粉、交联淀粉和交联多孔等变性淀粉的结构特性进行研究,以期为小红栲淀粉的深度开发奠定理论基础。
1 材料与方法 1.1 样品制备1) 交联淀粉的制备(谢涛等,2008) 准确称取适量小红栲淀粉(采自湖南衡山,自制成淀粉,纯度达绝干物质的96.5%)和NaCl (AR),加入蒸馏水摇匀成悬液,以0.1 mol·L- 1 NaOH(AR)调至所需pH值,加入一定量的三氯氧磷(Sigma公司,分析纯)作为交联剂搅拌均匀,水浴恒温反应到规定时间后,以0.1 mol·L- 1稀HCl溶液将pH值调至6.5,并迅速抽滤,再经洗涤、抽滤后于55 ℃烘干到恒重。
2) 交联多孔淀粉的制备(谢涛等,2008) 移取5 mL耐高温α -淀粉酶(Sigma公司,活力15 000 U·mL- 1)以pH值为6.0的柠檬酸(AR) -磷酸氢二钠(AR)缓冲液稀释20倍,再准确称取糖化酶(Sigma公司,活力100 000 U·g- 1) 1.0 g以pH值为6.0柠檬酸-磷酸氢二钠缓冲液稀释100倍。上述2种单酶液再按3: 4(v/v)混合均匀即得复合酶溶液。准确称取干燥的交联淀粉,按体积比3 : 2加入蒸馏水和一定pH值的柠檬酸-磷酸氢二钠缓冲液,摇匀后于50 ℃下保温10 min,再按438 U·g- 1淀粉加入预热的酶液,恒温反应14 h后,以1.2 mol·L- 1 HCl溶液调至pH值为3灭酶2 min,抽滤、洗涤并将pH值调为中性,于55 ℃烘干至恒重。
3) 多孔淀粉的制备 以小红栲原淀粉为原料,采用小红栲交联多孔淀粉制备的酶解工艺制得多孔淀粉。
1.2 检测方法采用扫描电子显微镜,按谢涛等(2003)的方法进行形态结构测定。采用傅里叶变换红外仪,按按谢涛等(2008)的方法进行红外光谱测定。采用pH滴定法(黄立新等,2000)进行交联度测定。采用X -射线衍射仪,按谢涛等(2003)的方法进行X -射线衍射分析。采用软件Origin7.5进行分析和计算,以曲线拟合分峰法求得小红栲原淀粉及其变性淀粉的绝对结晶度XC、微晶尺寸L及微晶面间距d。其中,结晶度由式(1) XC = IC / (IC + Ia)、微晶尺寸由式(2) L = kλ / (βcosθ)及微晶面间距由式(3) d = λ / (2sinθ)计算而得。式(1) ~ (3)中: IC和Ia分别是结晶区和无定型区的累积衍射强度; k = 0.89; λ为入射线波长,λ = 1.54 Å; β为衍射峰半高宽; θ为衍射角度。
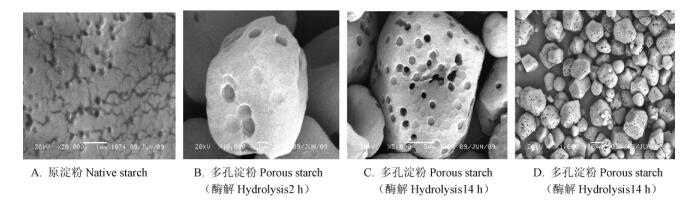
2 结果与讨论 2.1 多孔淀粉的形态结构图 1是小红栲原淀粉与多孔淀粉的扫描电镜图。小红栲原淀粉颗粒表面分布很多裂纹和凹坑(图 1A),α -淀粉酶和糖化酶对颗粒表面的裂纹并不产生酶解作用,其酶解作用只发生在颗粒表面的凹坑处,且沿着凹坑逐渐往颗粒中心酶解(图 1B)。这种现象与已有的研究报道(Fannon et al., 1992; Zhao et al., 1996; Manelius et al., 2000)相符,表明淀粉颗粒表面凹坑的多少在一定程度上能够影响颗粒表面微孔生成的数目,凹坑处可能存在有利于淀粉酶水解的淀粉链结构。随着淀粉酶水解时间延长,在淀粉颗粒表面出现的微孔越来越多、越来越大且越来越深,最终可以导致淀粉颗粒破裂解体。当淀粉酶水解时间适宜时,可以制备得到具有较理想结构的多孔淀粉,颗粒表面比较均匀地布满孔径1 μm左右的孔洞,在颗粒内部形成空腔结构,能够提供一个较大的储藏空间,很好地吸附目的物质(图 1C,D)。另外,即使在同一张SEM图片中,不同淀粉颗粒表面的微孔数目、大小和深度也存在不同程度的差异(图 1C)。
|
图 1 小红栲原淀粉与多孔淀粉的扫描电镜图 Figure 1 SEM of native and microporous C. carlesi starches |
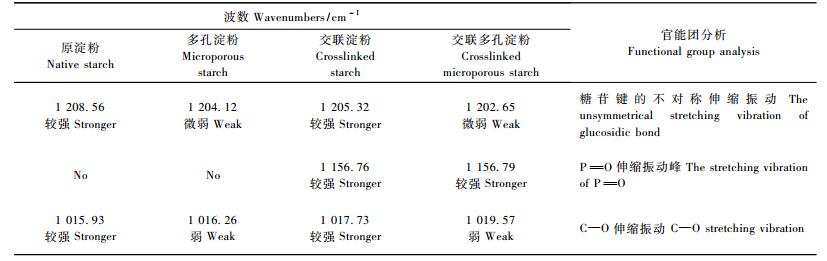
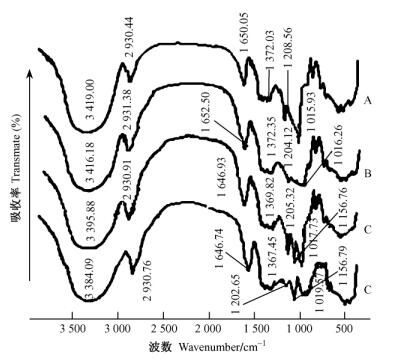
小红栲原淀粉、多孔淀粉、交联淀粉和交联多孔淀粉的红外吸收光谱见图 2和表 1。由图 2和表 1可知:与原淀粉(图 2A)比,多孔淀粉(图 2B)和交联多孔淀粉(图 2D)在1 208.45 cm- 1处的开链醚键(或糖苷键) C—O—C伸缩振动峰和1 015.93 cm- 1处的C—O伸缩振动峰的强度显著降低,说明酶解反应发生在淀粉链的糖苷键上,这与α -淀粉酶和糖化酶的作用特点是一致的; 而交联淀粉(图 2C)和交联多孔淀粉(图 2D)在1 152.68 cm- 1处则出现较强的P =O伸缩振动峰,说明三氯氧磷与淀粉粒上的—OH发生了酯化交联反应。采用pH滴定法进一步测得小红栲交联淀粉和交联多孔淀粉的交联度分别为13.8和16.2。
|
图 2 小红栲原淀粉(A)、多孔淀粉(B)、交联淀粉(C)和交联多孔淀粉(D)的红外光谱 Figure 2 FTIR spectra of native (A), microporous (B), crosslinked (C) and crosslinked microporous (D) C. carlesi starches |
|
|
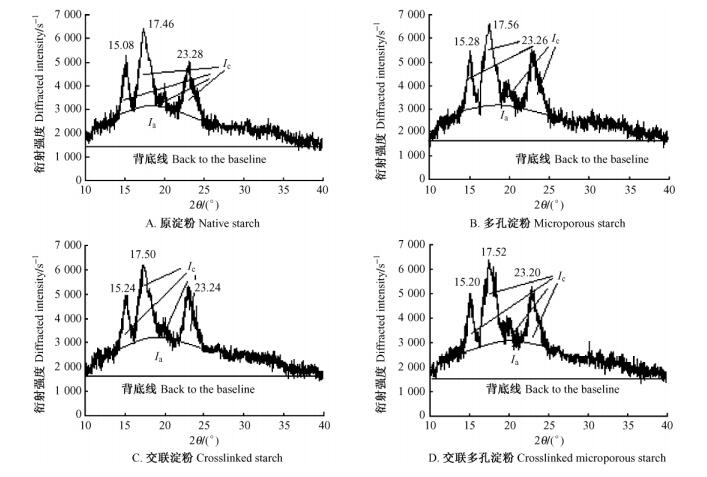
小红栲原淀粉及其变性淀粉的X -射线衍射图如图 3所示。从图 3中可看出:小红栲原淀粉及其变性淀粉的X -射线衍射图谱由尖峰衍射特征和弥散衍射特征2部分组成,是典型多晶体系的衍射曲线,在15.08°,17.36°,19.50°和23.28°附近对应的衍射峰强度依次为较强、强、极弱和较强,介于A型和B型之间,因此属C型晶体。在X -射线衍射图上出现的3个强结晶衍射峰,布拉格角在15.08°,17.36°和23.28°附近,对应于(1ī0),(110)和(200)晶面,说明小红栲原淀粉及其变性淀粉结构均由结晶结构和无定型结构组成。
|
图 3 小红栲原淀粉(A)、多孔淀粉(B)、交联淀粉(C)和交联多孔淀粉(D)的X -射线衍射图谱 Figure 3 X-ray diffractions of native (A), microporous (B), crosslinked (C) and crosslinked microporous (D) C. carlesi starches |
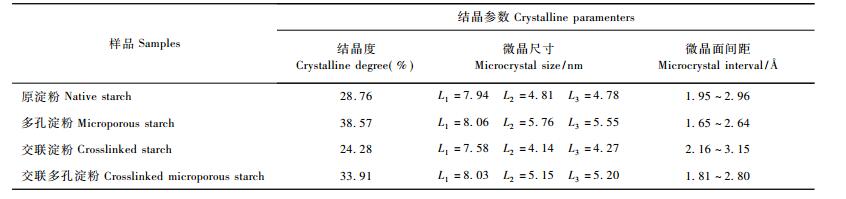
由图 3求得小红栲原淀粉及其变性淀粉的绝对结晶度XC、微晶尺寸L及微晶面间距d(表 2)。从表 2可知:交联淀粉、原淀粉、交联多孔淀粉和多孔淀粉的结晶度、微晶尺寸依次增加,而微晶间距依次缩小。这主要是因为:一方面,与原淀粉(或多孔淀粉)相比,交联反应会对淀粉颗粒的结晶区造成不同程度的破坏,从而导致交联淀粉(或交联多孔淀粉)的结晶度降低,且微晶尺寸相应变小; 而另一方面,原淀粉(或交联淀粉)在复合淀粉酶的协同作用下,随着无定型区不断被水解,结晶区比例明显增加,同时微晶粒间的距离缩短,并形成新的氢键,从而导致多孔淀粉(或交联多孔淀粉)的微晶尺寸增大。
|
|
复合淀粉酶制备多孔淀粉的基本原理是:淀粉颗粒表面的凹坑处是酶作用的部位,表面孔洞由浅入深,直达颗粒中心,最终在颗粒内部形成空洞结构,其上较均匀地分布着孔径1 μm左右的孔洞。
FTIR红外光谱证明:交联、酶解反应分别发生在淀粉颗粒的羟基和开链醚键(或糖苷键)上。
广角X -射线衍射分析表明:小红栲原淀粉及其变性淀粉的X -射线衍射图谱均由尖峰衍射特征和弥散衍射特征2部分组成,属C型晶体。交联淀粉、原淀粉、交联多孔淀粉和多孔淀粉的结晶度、微晶尺寸依次增加,而微晶间距依次缩小。
付陈梅, 阚建全, 陈宗道. 2003. 微孔淀粉研究进展[J]. 粮食与油脂, 18(1): 9-11. |
黄立新, 周俊侠, 张力田. 2000. 酯化交联淀粉反应及性质的研究(Ⅰ)———反应历程[J]. 食品与发酵工业, 26(5): 5-8. |
谢碧霞, 谢涛. 2002. 我国橡实淀粉资源开发利用的研究[J]. 中南林学院学报, 22(3): 22-25. |
谢涛, 谢碧霞. 2002. 小红栲淀粉糊特性的研究[J]. 食品工业科技, 23(11): 43-46. |
谢涛, 谢碧霞. 2003. 小红栲淀粉颗粒特性的研究[J]. 食品科学, 23(1): 23-26. |
谢涛, 李英. 2008. 交联微孔甘薯淀粉理化特性研究[J]. 食品科学, 29(12): 153-155. DOI:10.3321/j.issn:1002-6630.2008.12.030 |
钟秋平, 谢碧霞, 李清平, 等. 2008a. 高压处理对橡实淀粉黏度特性影响的研究[J]. 中国粮油学报, 23(3): 31-35. |
钟秋平, 谢碧霞, 王森, 等. 2008b. 高压处理对橡实淀粉晶体特性的影响规律[J]. 农业工程学报, 24(6): 45-48. |
Fannon J E, Hauber R J, Bemiller J N. 1992. Surface pores of starch granules[J]. Cereal Chemistry, 69(3): 284-287. |
Manelius R, Nurrin K, Bertoft E. 2000. Enzymatic and acidic hydrolysis of cationized waxy maize starch granules[J]. Cereal Chemistry, 77(3): 345-352. DOI:10.1094/CCHEM.2000.77.3.345 |
Zhao J G, Madson M A. 1996. Cavities in porous corn starch provide a large storage space[J]. Cereal Chemistry, 73(3): 379-380. |
 2011, Vol. 47
2011, Vol. 47