文章信息
- 高振华, 顾继友
- Gao Zhenhua, Gu Jiyou
- 利用苯酚液化大豆粉制备耐水性木材胶黏剂
- Water Resistant Wood Adhesives Prepared with Phenolated Soy Flours
- 林业科学, 2011, 47(9): 129-134.
- Scientia Silvae Sinicae, 2011, 47(9): 129-134.
-
文章历史
- 收稿日期:2009-12-09
- 修回日期:2010-05-26
-
作者相关文章
近来,由于不可再生的化石资源日益消耗,人们对丰富、可再生的生物质资源利用越来越关注,以获得生物能源和石油化工原料的替代物,实现人类的可持续发展。大豆在世界各国广泛种植,是获取豆油与植物蛋白的重要作物之一。据联合国粮农组织(FAO)统计,2008年世界大豆产量超过2.4亿t。然而,大豆榨油后的豆粕主要用于动物饲料,仅有少量用于非食品领域(如胶黏剂、涂料、纤维、泡沫、塑料等)。胶黏剂是人造板的血液,目前主要是合成树脂胶黏剂。我国2008年人造板产量已超过9 409.95万m3,居世界第一。在不可再生的化石资源日益消耗的形势下,利用可再生的生物质原料制备高品质人造板用胶黏剂将是未来人造板的发展趋势。
大豆蛋白胶作为一种生物质基胶黏剂,在1950年左右曾是人造板用主要胶黏剂之一。然而传统大豆蛋白胶耐水性差、胶接强度较低等不足,随后被合成高分子胶黏剂完全替代。由于石油资源的不断消耗以及人类可持续发展的需要,大豆蛋白胶现已重新受到关注。
大豆蛋白约由52% 11S,35% 7S,8% 2S和5%15S的球蛋白组成,除了2S球蛋白相对分子质量在8 000~20 000之间,其他球蛋白的相对分子质量均在150 000~600 000之间(Kumar et al., 2002)。因此要有效利用大豆蛋白制备胶黏剂,首先要解决高分子质量溶解问题,否则胶黏剂的固含量都不会太高,例如在国内近年授权的关于大豆蛋白胶黏剂的大多数发明专利中(钱湘群等,2009; 王伟宏等,2008; 2009),胶黏剂的大豆蛋白或者大豆粉的含量都在10%~18%之间。
另外,传统大豆蛋白胶黏剂胶接强度低的主要原因是大豆蛋白的三级结构呈紧密的球形结构,使得大豆蛋白中许多极性和非极性基团都包裹于球形结构之内,对木材等极性基团的吸附作用减弱(Sun et al., 1999; van der Leeden et al., 2000)。为此,人们通常对大豆蛋白进行变性处理,使大豆蛋白分子部分伸展,改善胶接强度,例如采用碱性试剂(如氢氧化钠等)、酶(如谷氨酰胺转氨酶)、酰化试剂(如乙酸酐)、尿素、盐酸胍、十二烷基磺酸钠等(张天昊等,2008a; Zhang et al., 2007),对大豆蛋白进行变性、水解和酰化改性,或者将大豆蛋白或者改性大豆蛋白与酚醛树脂(庞久寅等,2008; Kuo et al., 2001; Hse et al., 2001)、聚乙烯醇、聚乙酸乙烯酯(赵科等,2000)、Kymene® 557H(一种纸张增强剂)(Li et al., 2004)等合成高分子共混改性,使大豆蛋白胶在胶接强度、耐水性等性能得到了一定改善。但这些变性处理仅仅使大豆蛋白部分的二、三级结构伸展,所以改善效果都不甚理想。
生物质的苯酚液化以苯酚为液化剂,在酸性催化剂和较高温度下将不熔不溶的生物质材料转化为可熔可溶产物。苯酚液化技术可将资源丰富、可再生的生物质原料转化成制备高品质胶黏剂、泡沫等生物质高分子材料的原料,从而替代部分石油化工产品并节约石油。纤维素、木材、树皮、玉米淀粉、废纸、单宁等生物质原料通过苯酚液化,已先后制成了高品质胶黏剂(Yuan et al., 2009)。有学者高附加值利用豆渣,采用苯酚液化技术实现了豆渣的液化(张天昊等,2008b),以实现利用豆渣液化物生产木材胶粘剂的构思,但未见利用豆渣液化物制备胶黏剂的研究报道; 对于利用豆粉苯酚液化物制备耐水性大豆蛋白胶黏剂等相关研究,迄今为止也未见到文献报道。本文的研究构思就是通过苯酚高温液化,将不易溶解的大分子大豆球形蛋白降解转化为可熔可溶的产物,其间能够破坏大豆蛋白的球形结构而使球形分子伸展,从而解决大豆蛋白溶解性差、对木材吸附作用差的这2个瓶颈问题; 再将液化产物与甲醛反应,可制备低游离甲醛释放的耐水性木材胶黏剂。
1 材料与方法 1.1 材料豆粉,购于哈高科大豆食品有限责任公司,其主要组分为:蛋白质含量56.2%、水分4.7%、脂肪1.5%、碳水化合物31.9%、灰分5.7%,豆粉未经其他处理,直接使用; 其他试验药品,如苯酚、98%浓硫酸、85%磷酸、氢氧化钠、37.2%甲醛溶液均为分析纯; 制备胶合板用桦木单板(1.5 mm厚)购于哈尔滨胶合板厂,压板前将单板锯割成420 mm×420 mm的幅面。
1.2 豆粉的苯酚液化将600 g苯酚和30 g催化剂(硫酸和磷酸混合液)加入四口瓶中,在搅拌下升温到130 ℃; 然后逐渐加入适量的豆粉(200,250或300 g),当所有豆粉加完,在130~150 ℃搅拌下保持90 min; 随后冷却到70 ℃,并加入反应物总质量5%的NaOH溶液(浓度50%)和30%的水,继续搅拌60 min。冷却即得苯酚液化豆粉(PLS),产物为无明显沉淀、黑色液体。
1.3 苯酚液化豆粉-甲醛(PLS-F)胶黏剂合成将苯酚液化豆粉和甲醛溶液投入反应釜中,加热到65 ℃并保持80 min; 然后升温到90 ℃继续反应30 min; 加入碱和第1批水在80~85 ℃反应到一定黏度,加入第2批水继续反应直到目标黏度。各PLS-F胶的氢氧化钠与苯酚液化豆粉的质量比为0.26,甲醛与苯酚液化豆粉的质量比为0.60。同时,合成一种纯酚醛树脂胶黏剂作为参比,其氢氧化钠/苯酚质量比为0.29,甲醛与苯酚质量比为0.67(F/P摩尔比2.1)。
1.4 苯酚液化豆粉的液化率取10 g左右(W1,精确到0.000 1 g)液化产物,用100 mL丙酮/水(质量比1/1) 复合溶剂溶解,然后用秤重了的G4玻璃纤维滤纸(W2)过滤,滤纸残留物用复合溶剂涤洗3遍,最后将滤纸和过滤残留物在(103±2)℃烘箱中烘至恒重,称量(W3)。苯酚液化豆粉的液化率=(W3 -W2)/(a×W1)×100%,式中a为W1克液化产物中的豆粉含量,由豆粉苯酚液化时的投料计算得到。
1.5 苯酚液化豆粉的游离酚含量和苯酚结合酚含量将各苯酚液化豆粉配置成浓度0.5%的水溶液(pH为10~10.5),采用HPLC法在Agilent 1100高效液相色谱仪上测定游离酚含量。色谱柱: Zorbax column(Eclipse XDB-C8,ID=4.6 mm,length=150 mm,Agilent); 紫外检测器,波长288 nm; 流动相:甲醇/水(体积比1/2),流速1.0 mL·min-1。一系列已知浓度的苯酚溶液(0.1%,0.2%,0.3%,0.4%和0.5%,pH为10~10.5) 在相同条件下做标准曲线。
苯酚液化豆粉中的结合酚含量为液化产物中实际投料苯酚总含量与试验测得的游离酚含量的差值。
1.6 红外光谱分析将各苯酚液化产物在-35 ℃、真空度85 Pa下冷冻干燥至恒重,采用KBr压片法在Nicolet MagnaIR560 FTIR光谱仪上进行红外分析; 同时,相同条件对纯豆粉也进行红外分析。
1.7 GPC法测定相对分子质量及分布各苯酚液化豆粉产物以及制备得到的胶黏剂在Agilent 1100 HPLC上采用GPC法测定相对分子质量及分布。色谱柱: 79911 GP-104 PL gel(相对分子质量4 000~400 000) 串联79911 GP-103 PL gel(相对分子质量1 000~40 000);样品:浓度0.5%水溶液; 流动相为水,流速1 mL·min-1; 示差检测器; 以单分散聚乙二醇为相对分子质量标样(标样相对分子质量106,194,400,620,1 010,1 900,4 020,6 450,11 840和22 450)。
1.8 苯酚液化豆粉-甲醛胶黏剂的物理性能按照国家标准GB/T 14074—2006测定各胶黏剂的黏度、pH值、固体含量、游离甲醛含量(盐酸羟胺法)。
1.9 苯酚液化豆粉-甲醛胶黏剂的胶接性能和游离甲醛释放量各苯酚液化豆粉-甲醛胶黏剂和纯酚醛树脂胶的胶接性能和游离甲醛释放量通过压制3层桦木胶合板的方法进行评价。胶合板的制备工艺如下:施胶量360 g·m-2(双面施胶); 预压压力0.8 MPa,预压25 min; 热压温度140 ℃,热压压力1.2 MPa,热压时间4 min。
胶黏剂的耐久性由胶合板的28 h煮-烘-煮湿强度表征,按照国家标准GB/T 9846.1—2004进行测定; 胶黏剂的游离甲醛释放量按照国家标准GB 18580—2004进行测定
2 结果与讨论 2.1 苯酚液化豆粉(PSF)的特性大豆粉作为胶黏剂原料,主要是利用豆粉中的大豆蛋白组分。大豆蛋白是一种紧密的球形结构,其多数极性基团被包裹在球形颗粒内,所以将大豆蛋白直接用作胶黏剂,仅有少数球形结构表面基团与基材(被胶接物)发生吸附作用(van der Leeden et al., 2000),这是大豆蛋白胶黏剂胶接强度低的本质原因。因此,苯酚液化豆粉的一个主要目的就是通过苯酚的高温液化作用,破坏大豆蛋白球形大分子内的氢键和化学键(二硫键),使紧密球形结构展开,释放其内部极性基团,而提高胶接强度。
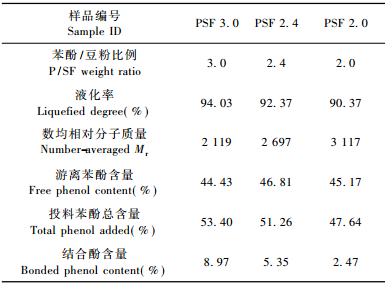
通过高温条件(130~150 ℃)和酸性催化剂存在下的苯酚液化,不易溶解的大分子质量大豆蛋白大分子首先发生降解,转化为易溶解的分子质量较小的产物。大豆蛋白中约90%的球蛋白相对分子质量在150 000~600 000之间(Kumar et al., 2002)。表 1中采用GPC测量得到液化大豆蛋白的数均相对分子质量在2 119~3 117之间,远低于液化前的150 000~600 000,由此使液化大豆蛋白极易溶于水和丙酮等溶剂中,表现为液化率高,即苯酚液化后90.37%的豆粉都易溶于丙酮中或者水中。图 1为不同苯酚/豆粉比例下豆粉液化产物GPC图,可更直观地查看豆粉液化产物中的相对分子质量大小及分布: GPC图主要由11个GPC峰(a,b,c,…,j,k)组成,对应相对分子质量分别为7 250,4 530,2 950,2 220,1 855,1 112,766,516,355,257和91;另外GPC图也表明,由于豆粉成分复杂,加之高温苯酚液化反应复杂,其液化产物组分十分复杂,除相对分子质量为91的k峰表示游离苯酚外,其他相对分子质量分级的化学组成和结构尚无法确认。但由GPC可肯定,苯酚液化使大豆蛋白相对分子质量急剧降低,液化产物各组分的相对分子质量在250~7 250之间,远低于液化处理前大豆蛋白的相对分子质量。
|
|
|
图 1 不同苯酚/豆粉比例下液化豆粉的GPC图 Figure 1 GPC spectra of phenolated soy flours with various phenol/soy flour ratios |
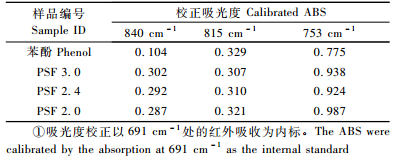
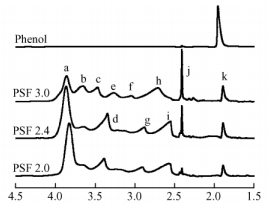
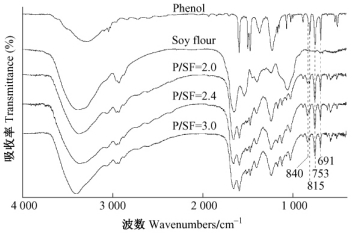
在苯酚液化过程中,一方面是豆粉中的各组分在高温和酸的作用下降解成分子质量很低的液化产物,另一方面苯酚又会与豆粉的低分子质量液化产物发生反应,形成结合酚结构。有学者在相似液化条件下应用苯酚液化纤维素、木材等生物质材料研究中就确定,苯酚能够与生物质液化产物反应而结合,从而增加液化产物的反应活性点(Zhang,2003; Hui,2007)。表 1中各液化产物的结合酚含量也证实液化过程中苯酚和豆粉液化产物发生反应; 对于液化产物的FTIR分析进一步证实了这一点,Zhang(2003)结合NMR确认FTIR谱在840和753 cm-1附近分别表示苯酚的1,4-取代苯环和1,2-取代苯环的吸收峰; 在豆粉苯酚液化产物的FTIR中,在840和753 cm-1处的确存在吸收峰,由于各豆粉液化产物中存有游离苯酚,苯酚在附近(815和691 cm-1)也存在红外吸收而干扰分析,为此各红外谱峰以691 cm-1处(游离苯酚中单取代苯环)吸收峰为内标进行校正,消除FTIR测试样品厚度及游离苯酚对吸光度影响,然后校正的吸收峰与游离苯酚相应位置的FTIR吸光度进行对比,结果如表 2所示,即在840和753 cm-1处分别表示苯酚的1,4-取代苯环和1,2-取代苯环的吸收强度都有了明显的增强,说明结合苯酚通过对位或邻位加成到液化豆粉上,形成4-取代苯酚支链和2-取代苯酚支链; 另外由图 2的FTIR可直观看到,液化产物在840 cm-1的吸收强度增量明显高于753 cm-1处的,由此说明结合苯酚主要通过对位取代连接到液化豆粉上,形成4-取代苯酚支链,这是由于1,4-取代苯环反应的空间位阻(与羟基对位)小于1,2-取代苯环的位阻(与羟基邻位)。通过苯酚和豆粉液化产物的反应,在液化豆粉中引入耐水性的苯环(通过结合苯酚引入),所以苯酚液化豆粉产物可直接与甲醛等交联剂反应,形成体型结构,从而可提高胶黏剂的耐久性和胶接强度。
|
|
|
图 2 苯酚液化豆粉、豆粉及苯酚的FTIR图 Figure 2 FTIR spectra of phenolated soy flour, soy flour and phenol |
由图 1的GPC图还可看出,苯酚/豆粉比例分别为3.0,2.4和2.0时,液化产物中大分子质量组分(a峰)的面积逐渐增加(分别为11.5%,19.8%和29.9%),而小分子质量组分中的j峰明显降低(分别为23.58%,10.7%和6.8%); 数均分子质量逐渐增加(分别为2 119,2 697和3 117)。这说明:随着苯酚/豆粉比例增加,液化体系中苯酚浓度(表 1的投料苯酚含量)越高,在液化过程中能和豆粉发生反应的作用点越多,使豆粉降解的更充分,最终产物的分子质量就越低。由此,通过液化反应在豆粉中接枝上的苯酚结构就越多,也即结合酚含量越低,如表 1所示。
2.2 苯酚液化豆粉-甲醛(PSFF)胶黏剂的特性通过苯酚高温液化,大豆蛋白大分子转化成分子质量较小的产物,因此,该处理不仅使其球形二级结构展开,释放被包裹和结合的极性基团,提高大豆蛋白与极性基材的吸附作用,从而增加胶接强度; 同时,大豆蛋白大分子链中肽键降解时,还产生更多能够与甲醛反应的活性基团(主要是氨基),加之结合酚的引入进一步增加与甲醛的反应点。因此大豆粉经过苯酚液化后,虽然分子质量降低,但通过甲醛的缩聚反应能够被重先分子组装,形成耐水性的体型大分子物质。所以,采用合适的合成反应工艺,苯酚液化豆粉能够制备成高品质的大豆胶黏剂。
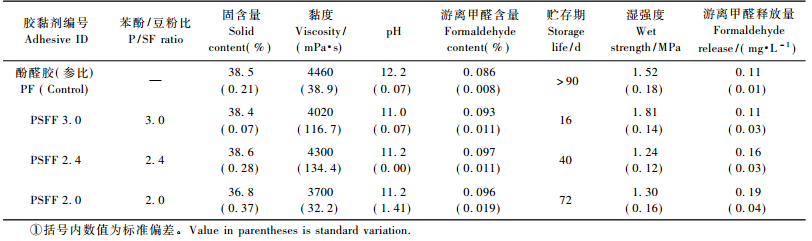
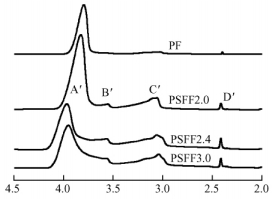
不同苯酚/豆粉比例下所制备得到的苯酚液化豆粉-甲醛胶黏剂的主要特性如表 3所示。各种PSFF胶黏剂的固含量和游离甲醛含量与参比酚醛树脂相近; PSFF胶的pH值和黏度则比酚醛树脂胶稍小; 但是豆粉胶的贮存期在16~72天之间,比酚醛树脂胶要小很多,并且随着苯酚/豆粉比例的降低而逐渐增长,这主要是苯酚液化豆粉中结合酚含量随着苯酚/豆粉比例降低而逐渐降低(如表 1所示),结合苯酚的反应活性点比大豆蛋白的多,因此与甲醛反应过程中,结合酚含量高的液化产物生成的胶黏剂分子的分子质量要高。图 3各种胶黏剂的GPC图证实了这一点:胶黏剂PSFF 2.0(苯酚/豆粉比例=2.0) 的主峰(峰A')分子质量为6 761,比参比酚醛树脂胶的(6 166) 提高了9.6%,而胶黏剂PSFF 2.4和PSFF3.0的主峰分子质量相当(约为9 260),比酚醛树脂胶的提高了50.2%。GPC图同时也表明,由于苯酚液化豆粉产物的成分十分复杂,所制得的各种PSFF胶黏剂中组分多(如图 3的GPC峰B',C'和D'所示,对应分子质量分别为3 420,1 050和255)、含有较多的小分子质量组分(D'峰)。
|
|
|
图 3 苯酚液化豆粉-甲醛胶黏剂及酚醛树脂胶的GPC图 Figure 3 GPC spectra of phenolated soy flours-formaldehyde (PSFF) adhesives and phenol-formaldehyde (PF) adhesive |
所制备PSFF胶的胶接性能和游离甲醛释放量通过压制3层桦木胶合板进行评价,如表 3所示。表中的湿强度是胶合板试件连续经过4 h水煮、20 h(60 ℃)烘干、4 h水煮处理后,在湿态下测量得到的拉伸剪切强度,因此湿强度不仅表征胶黏剂的胶接强度,同时也表征了胶黏剂的胶接耐久性。胶黏剂PSFF 3.0的湿剪切强度为1.8 MPa,比参比酚醛树脂胶的(1.5 MPa)提高了20%;胶黏剂PSFF 2.4和PSFF 2.0的湿剪切强度相当(1.2~1.3 MPa),比酚醛树脂胶的低了约15%,但都比国家标准GB 9846.1—2004所要求的耐候级胶合板要求的(1.0 MPa)高25%左右。各种PSFF胶黏剂制得胶合板的游离甲醛释放量在0.11~0.19 mg·L-1之间,虽然胶黏剂PSFF 2.4和PSFF 2.0的甲醛释放量比参比酚醛树脂的略高些,但都远低于国家标准GB18580-2004要求的E0级(0.5 mg·L-1)板材要求。由此可见,通过苯酚高温液化处理,可将本身不耐水的大豆粉制备成低游离甲醛释放的、胶接性能满足国家标准要求的胶黏剂,并可由于制备耐候级胶合板。
3 结论经过苯酚高温液化,90%以上的大豆粉转化成相对分子质量在250~7 250之间的、易于溶解的活性产物,部分苯酚以1,4-取代和1,2-取代方式与豆粉反应形成结合酚; 随着苯酚/豆粉比例的增加,豆粉的液化率和液化产物中的结合酚含量逐渐增加,但数均分子质量逐渐降低。大豆粉在苯酚存在下的液化降解中,不仅破坏大豆蛋白球形大分子内的氢键和化学键,使紧密球形结构展开而释放其球形蛋白内的极性基团,还出现肽链的断裂以及肽链和苯酚的反应(形成结合酚),使液化豆粉中与甲醛反应的活性基团数量增加。通过与甲醛的缩聚反应,将苯酚液化豆粉制备成了低游离甲醛释放的、胶接性能满足国家标准要求的胶黏剂,可用于耐候级胶合板的制备。
庞久寅, 董丽娜, 张士成. 2008. 大豆蛋白复合胶黏剂的研究进展[J]. 生物质化学工程, 42(3): 41-44. |
钱湘群, 盛奎川, 席雷, 等. 2009. 一种改性大豆蛋白胶粘剂的刨花板制备方法. 中国发明专利, 专利号ZL 200710164451. 9.
|
王伟宏, 张显权, 庞磊, 等. 2009. 单宁酸改性豆粉胶粘剂及其制备方法. 中国发明专利, 专利号ZL200710072642. 2.
|
王伟宏, 张显权. 2008. 低碱量豆粉胶黏剂. 中国发明专利, 专利号ZL200610010370. 9.
|
张天昊, 张求慧, 赵广杰. 2008a. 大豆基生物质胶粘剂研究进展[J]. 中国胶粘剂, 17(3): 51-55. |
张天昊, 张求慧, 赵广杰, 等. 2008b. 大豆豆渣苯酚液化物制备工艺的研究[J]. 大豆科学胶粘剂, 27(3): 501-504. |
赵科, 郝许峰, 刘大壮. 2000. 大豆分离蛋白复合胶粘剂研制[J]. 郑州大学学报:自然科学版, 21(1): 15-18. |
Hse C Y, Fu F, Bryant B S. 2001. Development of formaldehyde-based wood adhesives with co-reacted phenol/soybean flour. In: Wood adhesives 2000. Proc. No. 7252, Forest Products Society, Madison, WI, USA, 13-19.
|
Hui P. 2007. Wood liquefaction in the presence of phenol with a weak acid catalyst and its potential for novolac type wood adhesives[J]. Ph D Dissertation, Louisiana State University, USA. |
Kumar R, Choudhary V, Mishra S, et al. 2002. Adhesives and plastics based on soy protein products[J]. Industrial Crops and Products, 16(3): 155-172. DOI:10.1016/S0926-6690(02)00007-9 |
Kuo M L, Stokke D D. 2001. Soybean-based adhesives for composite products. In: Wood adhesives 2000. Proc. No. 7252, Forest Products Society, Madison, WI, USA, 163-166.
|
Li K C, Peshkova S, Geng X L. 2004. Investigation of Soy ProteinKymene® Adhesive Systems for Wood Composites[J]. Journal of the American Oil Chemists' Society, 81: 487-491. DOI:10.1007/s11746-004-0928-1 |
Sun X, Ke B. 1999. Shear strength and water resistance of modified soy protein adhesives[J]. Journal of the American Oil Chemists' Society, 76(8): 977-980. DOI:10.1007/s11746-999-0115-2 |
van der Leeden M, Rutten A, Frens G. 2000. How to develop globular proteins into adhesives[J]. Journal of Biotechnology, 79: 211-221. DOI:10.1016/S0168-1656(00)00238-8 |
Yuan J L, Gao Z H, Wang X M. 2009. Phenolated larch-bark formaldehyde adhesive with various amounts of sodium hydroxide[J]. Resin and Pigment Technology, 39(5): 290-297. |
Zhang Y C. 2003. Analysis of liquefaction behavior of cellulose in phenol and bound phenol in liquefied product[J]. Ph D Dissertation, University of Tokyo, Japan. |
Zhang Z, Hua Y. 2007. Urea-modified soy globulin proteins(7S and 11S): effect of wettability and secondary structure on adhesion[J]. Journal of the American Oil Chemists' Society, 84(7): 853-857. |
 2011, Vol. 47
2011, Vol. 47