文章信息
- 周珊, 虞方伯, 郭明, 单胜道, 邸玉翠, 徐少娟, 李松华, 郑圣丰
- Zhou Shan, Yu Fangbo, Guo Ming, Shan Shengdao, Di Yucui, Xu Shaojuan, Li Songhua, Zheng Shengfeng
- 竹炭固定化紫外诱变假单胞菌处理间甲酚废水的研究
- Removal of m-Cresol Wastewater by Immobilizing UV Mutated Pseudomonas sp.on Bamboo-Carbon
- 林业科学, 2011, 47(9): 114-118.
- Scientia Silvae Sinicae, 2011, 47(9): 114-118.
-
文章历史
- 收稿日期:2009-12-22
- 修回日期:2010-09-19
-
作者相关文章
间甲酚是生产杀虫剂、树脂、增塑剂和香料合成的中间体。间甲酚是一种原型质毒物,毒作用于所有生物活体。其可通过与皮肤、黏膜的接触不经肝脏解毒直接进入血液循环,导致细胞破坏,也可通过口腔侵入人体造成细胞损伤。含酚废水的处理主要有物理法、化学法和生物法。生物法具有经济、安全、无二次污染等特点,在应用方面更显优势(Olariu et al., 2002; Fialová et al., 2004;Bergauer et al., 2005; Atagana,2004)。固定化微生物技术作为一种新兴生物处理技术,是将微生物固定在载体上使其高度密集并保持其生物活性。该技术具有反应效率高、稳定性强、易于固液分离等优点,固定化微生物技术已成为国内外生物科学、环境科学及其相关学科的研究重点,并在有毒、难降解污染物的治理中得以应用(Li et al., 2005)。
前期研究中(周珊等,2008),以竹炭为载体,以假单胞菌为苯酚降解菌,采用载体结合法将假单胞菌吸附固定在竹炭上,用竹炭固定化假单胞菌处理苯酚水样。研究表明:竹炭固定化假单胞菌可保持较高的降解活性,能有效地耐受有机负荷,在竹炭吸附和生物降解的协同作用下能有效降解水样中苯酚。竹炭固定化假单胞菌对苯酚的降解相对于游离假单胞菌,不需污泥回流,固液易于分离,污泥量少,对高浓度苯酚的降解率更高、处理量更大(周珊等,2008)。但用竹炭固定化假单胞菌处理间甲酚废水时,由于较高浓度间甲酚会抑制假单胞菌的生长,处理效率较低,且生物膜易脱落。本研究先采用紫外光对假单胞菌进行诱变,然后以竹炭为载体,制备竹炭固定化紫外诱变假单胞菌,用其处理间甲酚水样。研究竹炭固定化紫外诱变假单胞菌的投加量、pH等因素对间甲酚去除的影响; 研究进水浓度随反应时间的变化关系,分析竹炭固定化紫外诱变假单胞菌去除间甲酚的反应动力学。
1 材料与方法 1.1 主要材料氯化钙、硫酸亚铁、硫酸镁、氢氧化钠、氯化铵、磷酸氢二钾、酵母浸膏、间甲酚等。上述试剂均为分析纯,由上海化学试剂厂提供。
竹炭由浙江临安姚氏炭业有限公司提供。竹炭研磨、筛选分级后用去离子水淋洗数次,洗净,在恒温干燥箱中烘干至恒重,储存备用。假单胞菌种由安信达环保科技(宁波)有限公司提供。
1.2 主要仪器设备752型紫外可见分光光度计(上海光谱仪器有限公司),AR2140电子分析天平(梅特勒-托利多仪器上海有限公司),DGG-9070B型电热恒温鼓风干燥箱(国华电器有限公司),78HW-3型恒温磁力搅拌器(杭州仪表电机有限公司),PHS-3C型数字式酸度计(上海科学仪器厂),THZ-82恒温振荡器(上海博迅实业有限公司),QM-BP行星球磨机(杭州仪表电机有限公司),SW-CJ-HBU洁净工作台(苏州安泰空气技术有限公司),HZQ-QX全温振荡器(中国哈尔滨市东联电子技术开发有限公司),PSX智能型恒温恒湿培养箱(宁波莱福科技有限公司),KYKY-1000B型电镜(中国科学院仪器厂),生物反应器(自制)。
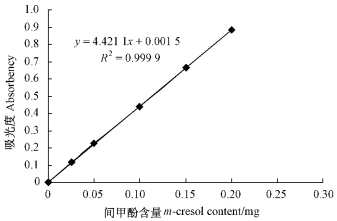
1.3 检测方法PHS-3C型数字式酸度计进行pH测定。间甲酚测定采用紫外分光光度法。测定条件:波长275 nm,1 cm石英比色皿。间甲酚标准溶液吸光度A和间甲酚含量的标准曲线见图 1。
|
图 1 间甲酚标准曲线 Figure 1 The standard curve of m-cresol |
无菌条件下,将假单胞菌接种到琼脂斜面培养基上,将接种好的斜面培养基放置在恒温恒湿培养箱中,30 ℃下培养24 h。然后将接种斜面上的菌种,挑取一环接入250 mL装有20 mL液体培养基的三角瓶中。30 ℃下摇床(170 r·min-1)培养16 h后,离心,用生理盐水离心洗涤2次后加生理盐水至总体积20 mL,再分别取5 mL菌液到7个直径6 cm的灭菌培养皿中,将培养皿置于磁力搅拌器上,用紫外灯(15 W,灯距28 cm)分别照射0,10,30,60,90,120和150 s,然后将菌液在黑暗条件下培养12 h。
液体培养基: NH4Cl 500 mg·L-1,K2HPO4 400 mg·L-1,CaCl2 · 2H2O 500 mg·L-1,MgSO4 50 mg·L-1,FeSO4·7H2O 10 mg·L-1,Yeast Extract 200 mg·L-1。液体培养基加入融化琼脂,制备斜面培养基。
1.4.2 细菌生长曲线的测定筛选单个菌落接种于50 mL预先配置好的液体培养基中,30 ℃下振荡(170 r·min-1)培养24 h,然后取菌液,将其按照体积1: 100的接种量分别接种于3瓶50 mL预先配置好的液体培养基上,在相同条件下振荡培养,并分别于培养2,4,6,8,10,12,14,16,18,20,22,24,26,28,30 h后取菌体培养悬液10 mL,以未接种的原液体培养基校正752型紫外可见分光光度计的零点,在波长600 nm处测定菌液的OD600值。以菌液的吸光度值(OD600)为纵坐标,以培养时间作为横坐标,绘制假单胞菌的生长曲线(钱存柔等,2003)。
1.4.3 假单胞菌的驯化分别将紫外诱变后菌液、未经诱变假单胞菌液灭菌后接入装有5 L上述液体培养基的反应器中,在常温下曝气培养,曝气量控制在0.2 Nm3·h-1左右(曝气量太大或太小都会影响微生物的正常生长)。当反应器底部出现污泥时,开始投加间甲酚进行驯化。第一次间甲酚的投加浓度为10 mg·L-1,然后间甲酚投加浓度逐步递增至200 mg·L-1。
1.4.4 竹炭固定化菌的制备以5 mm的竹炭(比表面积S为365 m2·g-1,孔比容积Vp为0.34 mL·g-1)为载体,分别将未经诱变假单胞菌和紫外诱变假单胞菌吸附固定在竹炭上,制得竹炭固定化假单胞菌和竹炭固定化紫外诱变假单胞菌。具体制备方法见参考周珊等(2008)。
1.4.5 竹炭固定化诱变假单胞菌对间甲酚的降解室温下,用竹炭固定化紫外诱变假单胞菌处理100 mL初始浓度为100 mg·L-1的间甲酚模拟水样,考察固定化诱变菌的投加量(15,20,25 g)、pH(约2,4,6,8,10) 对间甲酚去除的影响。
室温下,分别用20 g竹炭固定化紫外诱变假单胞菌处理不同初始浓度的间甲酚模拟水样100 mL,定时取样,进行竹炭固定化紫外诱变假单胞菌去除间甲酚的动力学研究。
2 结果与分析 2.1 紫外光照射时间的影响取经紫外光照射一定时间后的菌液0.5 mL,加盐水稀释后,采用平板稀释计数法测定不同稀释度下的平均菌落数,再根据平板稀释计数法规则选取最合理的平均菌落数值乘以稀释倍数得假单胞菌总数(陈声明等,2007; 张胜华,2005)。
从表 1中可知: 0~90 s时菌落总数随着紫外灯照射时间的增长而减少,90~120 s时菌落总数趋于稳定,150 s时菌落总数又开始减少。因此,本试验范围内假单胞菌紫外诱变的最佳照射时间为120 s。
|
|
用紫外光照射假单胞菌120 s,然后分别测定紫外诱变菌株和未经过诱变菌株的生长曲线。
诱变菌株达到稳定生长期只要20 h,比未经诱变菌株的稳定生长期快了6 h(图 2)。这表明:菌株经紫外诱变后,菌株生长繁殖的速度有了一定的提高,有效缩短了菌株的生长周期。DNA具有强烈吸收紫外光的能力,尤其是核酸链上的碱基对,其中嘧啶比嘌呤更敏感。小剂量紫外线可引起DNA突变,缩短育种时间(张胜华,2005)。

|
图 2 假单胞菌诱变前后生长曲线 Figure 2 Growth curves before and after mutagenesis of Pseudomonas sp. |
将假单胞菌株用紫外诱变120 s后,进行驯化,驯化期内间甲酚投加浓度逐步递增至200 mg·L-1,然后制得竹炭固定化紫外诱变假单胞菌。相同条件下,将未经诱变假单胞菌驯化后制得竹炭固定化假单胞菌。图 3为竹炭固定化紫外诱变假单胞菌与竹炭固定化假单胞菌的扫描电镜图。从电镜照片不难看出,假单胞菌体能够耐受浓度小于200 mg·L-1的间甲酚,并在载体竹炭表面定殖、成膜。未经紫外诱变假单胞菌株在竹炭表面形成的菌胶团量明显少于诱变菌(图 3a,b),未经紫外诱变假单胞菌株在竹炭的内部孔隙仅形成一层薄薄的生物膜; 而诱变菌在竹炭的内部孔隙,细胞间有胞外聚合物搭桥相连,细胞紧密地聚合成絮凝状,形成明显菌胶团,诱变菌在竹炭上所成的生物量明显较未经诱变菌对照增加(图 3c,d)。可以初步判定紫外诱变处理使得原始菌株耐受间甲酚的能力得以强化。理论上讲,菌体着生于载体表面或其间,形成生物膜或絮状体会产生更高的基因转移可能性,而这可能导致具有更高降解效率的“结合”菌株产生(Bossier et al., 1996)。此外,越来越多的研究表明菌体密度对实现某些生理功能至关重要,如质粒的结合、转移等。在菌体密度超过一定的阀值后,诸如群体感应(quorum sensing,QS)一类的生理活动才能进行(Fugua et al., 1994)。

|
图 3 扫描电镜照片(× 1 000) Figure 3 SEM(× 1 000) a.固定紫外诱变假单胞菌后竹炭表面Bamboo-carbon surface after immobilizing mutant Pseudomonas sp.; b.固定假单胞菌后竹炭表面Bamboo-carbon surface after immobilizing Pseudomonas sp.; c.固定紫外诱变假单胞菌后竹炭内部孔隙Inner pore of bamboo-carbon after immobilizing mutant Pseudomonas sp.; d.固定假单胞菌后竹炭内部孔隙Inner pore of bamboo-carbon after immobilizing Pseudomonas sp. |
室温下,分别向100 mL初始浓度为100 mg·L-1的间甲酚模拟水样中添加不同量的竹炭固定化紫外诱变假单胞菌,不调节水样pH值。考察竹炭固定化紫外诱变假单胞菌的投加量对间甲酚去除效果的影响。
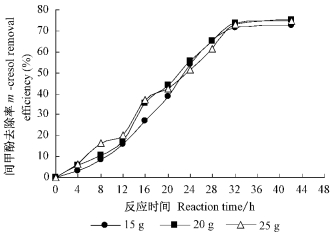
竹炭固定化紫外诱变假单胞菌的投加量影响到间甲酚的去除。当竹炭固定化紫外诱变假单胞菌的投加量增至25 g时,反应20 h后,间甲酚的去除率反而低于投加量为20 g时的(图 4)。可见竹炭固定化紫外诱变假单胞菌的投加量过大,会导致反应到一定时间后,残余的间甲酚作为竹炭固定化紫外诱变假单胞菌的碳源量不足,相对过剩的微生物对营养的吸收利用产生了竞争,大量细胞会处于贫营养状态,细胞活性降低,从而降低了降解效率。本试验,竹炭固定化紫外诱变假单胞菌的最适宜投加量为20 g,后续试验均采用该投加量。
|
图 4 竹炭固定化紫外诱变假单胞菌的投加量对间甲酚去除的影响 Figure 4 Effect of amount of bamboo-carbon immobilized UV mutated Pseudomonas sp. on m-cresol removal |
调节水样至不同pH值,考察水样pH值对竹炭固定化紫外诱变假单胞菌对间甲酚去除的影响。由图 5可以看出: pH值对间甲酚的去除有明显影响。pH值在4~6时,竹炭固定化紫外诱变假单胞菌对间甲酚的去除效果较好,pH大于或小于该范围,间甲酚去除率明显降低。这是因为微生物生长过程中机体内以酶促反应为主,pH值对酶促反应速率有显著影响。酶促反应存在的最适pH值范围,pH值高于或低于适宜范围时,酶和底物分子结合的有关基团解离状态会发生改变,使酶的活性明显降低,微生物代谢活力下降,影响到对有机物的降解能力(陈声明等,2007; 张胜华,2005)。

|
图 5 pH对间甲酚去除的影响 Figure 5 Effect of pH on m-cresol removal |
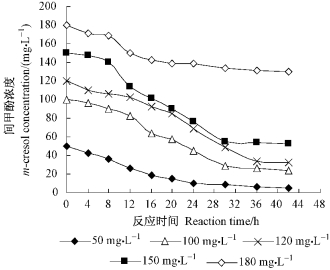
室温下,分别用20 g竹炭固定化紫外诱变假单胞菌处理不同初始浓度的间甲酚模拟水样100 mL。本试验范围内,间甲酚去除率随间甲酚浓度的增大而减小。间甲酚初始浓度为50 mg·L-1时,间甲酚去除率最高,42 h后去除率可达90.9%,而初始浓度为180 mg·L-1的水样42 h后去除率仅为49.7%。当间甲酚浓度≤150 mg·L-1时,间甲酚去除量随间甲酚浓度增大而增大,42 h后最高可达9.70 mg,间甲酚浓度>150 mg·L-1时则迅速降至4.97 mg(图 6)。
|
图 6 不同初始浓度间甲酚的去除 Figure 6 m-Cresol removal by solutions of different initial concentrations |
从表 2可以看出:竹炭固定化紫外诱变假单胞菌对间甲酚的去除能较好地符合零级反应方程。当间甲酚浓度≤150 mg·L-1时,间甲酚去除速率k0随间甲酚浓度的增大而增加,间甲酚浓度>150 mg·L-1,速率常数k0明显降低。说明过高的底物浓度在一定程度上抑制了诱变假单胞菌对间甲酚的降解。
|
|
本试验范围内,紫外诱变可以提高假单胞菌株的生长繁殖速度。假单胞菌的最佳诱变时间为紫外照射120 s。紫外诱变假单胞菌可在竹炭表面及内部孔隙形成菌团,紫外诱变处理使得原始菌株耐受间甲酚的能力得以强化。水样pH值和竹炭固定化紫外诱变假单胞菌的投加量影响到间甲酚的去除效果。100 mL初始浓度为100 mg·L-1的间甲酚水样中竹炭固定化紫外诱变假单胞菌的投加量为20 g时最佳。pH值在4~6时,竹炭固定化紫外诱变假单胞菌对间甲酚的去除效果较好,pH大于或小于该范围,间甲酚去除率明显降低。竹炭固定化紫外诱变假单胞菌对间甲酚的去除能较好地符合零级反应方程,间甲酚浓度大于150 mg·L-1时,诱变假单胞菌对间甲酚的降解受到抑制。
陈声明, 张立欣. 2007. 微生物学研究技术[M]. 北京: 科学出版社.
|
钱存柔, 黄仪秀. 2003. 微生物实验教程[M]. 2版. 北京: 北京大学出版社.
|
张胜华. 2005. 水处理微生物学[M]. 北京: 化学化工出版社.
|
周珊, 胡泽友, 喻景权. 2008. 竹炭固定化假单胞菌处理含酚废水的研究[J]. 高校化工学报, 22(5): 889-894. |
Atagana H I. 2004. Biodegradation of phenol, o-cresol, m-cresol and p-cresol by indigenous soil fungi in soil contaminated with creosote[J]. World Journal of Microbiology and Biotechnology, 20(8): 851-856. DOI:10.1007/s11274-004-9010-z |
Bergauer P, Fonteyne P A, Nolard N, et al. 2005. Biodegradation of phenol and phenol-related compounds by psychrophilic and cold-tolerant alpine yeasts[J]. Chemosphere, 59(7): 909-918. DOI:10.1016/j.chemosphere.2004.11.011 |
Bossier P, Verstraete W. 1996. Triggers for microbial aggregation in activated sludge[J]. Applied Microbiology and Biotechnology, 45(1/2): 1-6. |
Fialová A, Boschke E, Bley T. 2004. Rapid monitoring of the biodegradation of phenol-like compounds by the yeast Candida maltosa using BOD measurements[J]. International Biodeterioration and Biodegradation, 54(1): 69-76. DOI:10.1016/j.ibiod.2004.02.004 |
Fugua W C, Winans S C, Greenberg E P. 1994. Quorum sensing in bacteria: the luxR-luxI family of cell density-responsive transcriptional regulators[J]. Journal of Bacteriol, 176(2): 269-275. DOI:10.1128/jb.176.2.269-275.1994 |
Li P J, Wang X, Stagnitti F, et al. 2005. Degradation of phenan-threne and pyrene in slurry reactors with immobilized bacteria Zoogloea sp[J]. Environmental Engineering Science, 22(3): 390-399. DOI:10.1089/ees.2005.22.390 |
Olariu R I, Klotz B, Barnes I, et al. 2002. FT-IR study of the ringretaining products from the reaction of OH radicals with phenol, o-, m-, and p-cresol[J]. Atmos Environ, 36(22): 3685-3697. DOI:10.1016/S1352-2310(02)00202-9 |
Salmond G P C, Bycroft B W, Stewart G S A B, et al. 1995. The bacterial "enigma" cracking the code of cell-cell communication[J]. Molecular Microbiology, 16(4): 615-624. DOI:10.1111/mmi.1995.16.issue-4 |
 2011, Vol. 47
2011, Vol. 47


