文章信息
- 谭健晖
- Tan Jianhui
- 贮藏温度和时间对马尾松花粉保护酶活性及萌发率的影响
- Effects of Storage Temperature and Storage Time on Germination Rate and Protective Enzymes Activity of Pinus massoniana Pollen
- 林业科学, 2011, 47(9): 28-32.
- Scientia Silvae Sinicae, 2011, 47(9): 28-32.
-
文章历史
- 收稿日期:2011-05-10
- 修回日期:2011-07-20
-
作者相关文章
马尾松(Pinus massoniana)是我国南方重要的用材及产脂树种,在林桨纸一体化及松脂产业化建设中占有举足轻重的地位。1980—1987年广西营建了200 hm2以生长为改良目标的马尾松初级种子园,为推动马尾松良种化的进程发挥了重要的作用。20多年来,为解决种子园产量低和大小年等问题,笔者开展了树体管理、抚育施肥和人工辅助授粉等研究。随着高世代选育工作的推进,每年需要开展大量的杂交授粉工作,而花期不遇和花粉污染是杂交授粉工作的制约因素,通过花粉贮藏可以解决这2个问题。因此,如何对花粉进行有效贮藏成为杂交育种(制种)和人工辅助授粉中亟待解决的问题。前人关于花粉的研究多集中在不同贮藏条件与萌发率的关系(高爱新等,2009; Parton et al., 2002; 徐进等,1998; 孙爱芹等,2010; Yin et al., 2005; 王钦丽等,2005),只在少数花粉或花粉制剂研究中涉及有花粉生活力方面的报道(颜伟玉等,2005; 张红城等,2005)。有研究表明:花粉进入成熟期,内部发生一系列的生理代谢反应,活力逐渐下降,而花粉中的保护酶类能够清除氧自由基,延缓衰老,因此,保护酶活性的高低能够直接反映花粉的活力(邢世岩等,1998; 赵文飞等,2004)。笔者研究贮藏温度和贮藏时间对马尾松花粉保护酶活性和萌发率的影响,旨在从花粉的酶活性方面对花粉贮藏期间生理生化反应进行探索,为马尾松花粉的贮藏提供科学依据。
1 材料与方法 1.1 试验材料花粉采自南宁市林业科学研究所马尾松嫁接种子园23年生母树,参试号为桂MRC265。于2009年2月6—8日采集成熟待花枝,保湿带回进行水培,1 ~ 2天换水1次。每天将待开花蕾采下放在硫酸纸上,花粉散开后过40 ~ 60目筛放入装有1/3 ~ 1/2硅胶的密封容器内干燥,硅胶变色即更换,至硅胶不变色且花粉不沾瓶壁时花粉的含水量达到贮藏要求。将干燥好的花粉装入棕色瓶内用棉花封口,立刻放入装有硅胶的密封容器内保存,花粉量不超过容器体积的2/3,密封容器内的硅胶变色要及时进行更换。
1.2 试验方法 1.2.1 花粉萌发率测定采用液体培养基法,培养基为: 5%蔗糖+ 0.5% H3BO3 + 0.03% CaCl2,pH 5.6。培养条件: 28 ℃,暗培养24 ~ 36 h。取3个视野,每视野约100粒花粉,花粉管伸长的长度大于花粉粒直径时为具生活力花粉,具生活力花粉/总花粉数=萌发率。
1.2.2 花粉贮藏本试验分室温,4,-10和-20 ℃ 4种贮藏温度; 0,72,144,216,286和358天6种贮藏时间。将处理好的花粉分成4份,每份6瓶,共24瓶,分别放在室内避光处(室温)、冰箱冷藏室(4 ℃)、冰箱冷冻室(-10 ℃)和冰柜(-20 ℃)内。达到设定贮藏时间时从4种温度下各取出1瓶花粉,取出少量用于测定花粉萌发率,余下花粉密封后放在-80 ℃超低温保存,待试完毕统一测定酶活性。
1.2.3 花粉酶活性测验酶液的提取:称取花粉1.000 g,加入10 mL 0.05 mol·L-1磷酸缓冲液(pH7.8),冰浴研磨15 ~ 25 s,于10 000 rpm冷冻离心15 min,将悬浮液用一次性医用针筒吸出,过滤膜后即为粗酶提取液(李合生等,2000)。
SOD活性测定:取0.05 mL的酶液加入试管中,以蒸馏水作对照,做2支对照管,分别加入磷酸缓冲液1.5 mL,130 mmol·L-1的甲硫氨酸溶液0.3 mL,750 μmol·L-1的氮蓝四唑溶液0.3 mL、100 μmol·L-1的EDTA -Na2溶液0.3 mL、20 μmol·L-1核黄素溶液0.3 mL和蒸馏水0.25 mL。混匀后将1支对照管置于暗处,其他各管于4 000 Lx日光灯下反应20 min,以不照光的对照管作为空白,分别测定560 nm波长下的吸光值,SOD酶活性单位用U·g-1表示。
POD活性测定:反应液为100 mL 0.1 mol·L-1磷酸缓冲液(pH6.0) + 1 mL 30% H2O2+0.05 mL愈创木酚,测定时取酶液0.05 mL加3 mL反应液,混合后摇匀,立即在UN -1206分光度计下测定OD407值,每5 s读数1次,共读2 min,取反应呈线性部分的数值计算每分钟内的OD值的变化,酶活性单位用mg·g-1 min-1表示。
CAT活性测定:反应液为2 mL0.1 mol·L-1磷酸缓冲液(pH7.8) + 1 mL 0.08% H2O2,酶液0.2 mL,以磷酸缓冲液作为空白,用石英比色皿,每15 s测1次OD240值,共测3 min。CAT酶活性单位用mg·g-1 min-1表示。
以上指标的测定均重复3次,对异常数据进行剔除。
1.3 数据处理分别对不同贮藏温度和不同贮藏时间的花粉萌发率、POD活性、SOD活性、CAT活性进行双因素方差分析(SPSS软件)。
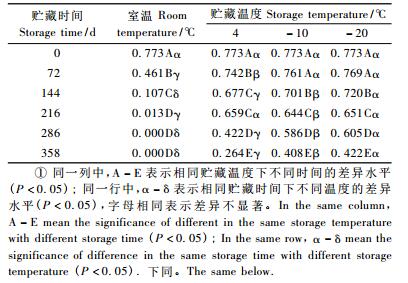
2 结果与分析 2.1 贮藏条件对花粉萌发率的影响不同贮藏条件下,马尾松的花粉萌发率及方差分析的结果见表 1。贮藏温度和贮藏时间均对花粉萌发率产生影响,其中影响最大的是贮藏温度,其次为贮藏时间。花粉萌发率下降最快的时期分别为室温时72 ~ 144天,4 ℃下216 ~ 286天、-10和-20 ℃下286 ~ 358天,最佳贮藏时间取花粉萌发率快速下降期的上限值,分别为室温72天,4 ℃下216天,-10和-20 ℃下286天,由于-10和-20 ℃ 2种温度下贮藏358天的萌发率的下降率小于50%,在生产实践中有较大的应用价值。
|
|
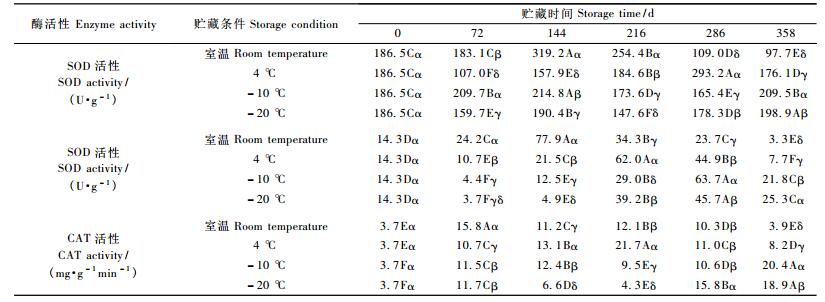
不同贮藏条件下,马尾松花粉的SOD活性及方差分析的结果见表 2。不同贮藏时间和贮藏温度均对SOD活性产生影响,其中室温和-4 ℃2种温度在不同的贮藏时间下SOD呈下降-升高-下降的变化趋势,高低起伏变化大,最高峰值分别出现在144和286天,最高峰值比最小值分别大226.6%和174.0%; -10和-20 ℃ 2种温度在不同的贮藏时间下SOD起伏变化不大,总体呈上升的趋势,最高峰值均出现在358天,最高峰值比最小值分别大26.7%和34.7% (图 1)。
|
|

|
图 1 贮藏条件对花粉SOD活性的影响 Figure 1 Effects of storage time and temperature on pollen's SOD activity  |
不同贮藏条件下,马尾松花粉的POD活性及方差分析的结果见表 2。不同贮藏时间和贮藏温度均对POD活性产生影响,其中室温和4 ℃ 2种温度在不同的贮藏时间下POD呈升高-下降的变化趋势,最高峰值分别出现在144和216天,最高峰值比最小值分别大2 466.7%和516.0%; -10和-20 ℃ 2种温度在不同的贮藏时间下POD呈下降-升高-下降的变化趋势,最高峰值均出现在358天,最高峰值比最小值分别大1 602.7%和1 116.2% (图 2)。

|
图 2 贮藏温度和时间对POD活性的影响 Figure 2 Effects of storage time and temperature on pollen's POD activity |
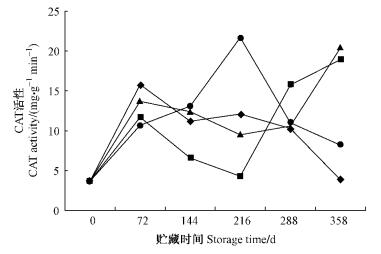
不同贮藏条件下,马尾松花粉的CAT活性及方差分析的结果见表 2。不同贮藏时间和贮藏温度均对CAT活性产生影响,其中室温和4 ℃ 2种温度在不同的贮藏时间下CAT呈升高-下降的变化趋势,最高峰值分别出现在72和216天,最高峰值比最小值分别大327.0%和486.5%; -10和-20 ℃ 2种温度在不同的贮藏时间下CAT呈升高-下降-升高的变化趋势,最高峰值均出现在358天,-10 ℃的CAT活性总体比-20 ℃高,最高峰值比最小值分别大45.1%和411.9% (图 3)。
|
图 3 贮藏温度和时间对CAT活性的影响 Figure 3 Effects of storage time and temper on pollen's CAT activity |
不同贮藏温度和贮藏时间对马尾松花粉萌发率的影响不同,随着贮藏时间的延长,花粉萌发率下降最快的时期分别为室温下72 ~ 144天,4 ℃下216 ~286天,-10和-20 ℃下286 ~ 358天,在这些时期3种酶活性分别出现最高峰值(图 1-3)。不同的贮藏温度下,358天时的萌发率降至最低值,此时3种保护酶活性在室温和4 ℃ 2种温度下降至最低值,-10和-20 ℃下2种温度下除POD外出现缓慢升高趋势。
3 结论与讨论马尾松花粉贮藏对松属间的杂交育种(制种)和马尾松种子园的辅助授粉具有重要意义。使贮藏后的花粉保持较高的萌发率和较强的活力是评价花粉贮藏成败的2个指标(孙霞等,1997; 赵文飞等,2004)。若以萌发率下降率低于50%和3种保护酶活性较强为前提,在本试验条件下,马尾松花粉的最佳贮藏时间为:室温下72天,4 ℃下216天,-10和-20 ℃下358天,此时的花粉保持较高的萌发率和较强的抗氧化抗衰老能力。采用-10和-20 ℃下冷冻贮藏花粉,贮藏时间达1年且CAT和SOD 2种酶的活性表现出不断升高趋势,说明花粉活性强,生命力旺盛,对活性氧的清除能力高,仍能通过自身的协调作用来抑制花粉的衰老和失活。正常年份中松属中的加勒比松(Pinus caribaea)、湿地松(Pinus elliotii)和马尾松的花期分别出现在12月—次年1月,1—2月和3月,花期相差较大,在进行种间(内)控制授粉时常需要将花期不遇的花粉贮藏至来年使用,贮藏期为1年甚至多年,-10和-20 ℃下358天时的花粉萌发率和花粉活性均较高,贮藏时间仍有延长的空间,因此研究-10和-20 ℃下的花粉长期保存有重要意义。
自由基学说认为植物体内活性氧的产生和清除处于一种动态的平衡状态,而一旦平衡被打破,就会出现逆境胁迫(Kanazaw et al., 2000; 林植芳等,1984; 谭健晖,2007; 谭健晖等,2007)。在花粉贮藏预处理中,为减少花粉的呼吸和代谢作用,需将花粉的含水率降至6% ~ 8%,这一过程首先造成水分散失,随着贮藏时间的延长,花粉细胞不断失水,水分胁迫加重,同时,活性氧代谢失调不断累积,细胞不断衰老,出现氧化胁迫。在水份、低温和氧化3重胁迫下,抗氧化保护酶体系(SOD,POD和CAT)协同作用,清除活性氧自由基,维持细胞膜稳定,防止细胞膜脂氧化,这是细胞自身的一种保护机制。在花粉贮藏72 ~ 144天和216 ~ 286天期间此阶段室温和4 ℃ 2种温度下CAT,SOD和POD萌发率大幅下降,直线升高,先后达到最高峰值,表现出较高的活性,3种保护酶在达到最高峰值后均出现下降并降至最低值; -10和-20 ℃ 2种贮藏温度下POD的变化趋势与室温和4 ℃相似,于萌发率大幅下降前的286天直线升高达到最高峰值后下降,CAT和SOD酶虽也在萌发率大幅下降期内酶活性升高至最高峰值,但没有出现下降的趋势,且这2种酶出现双峰变化模式,峰值分别出现在72和358天,双峰模式是否更有利于花粉的长期贮藏有待更进一步的研究。本试验表明:随着贮藏时间的延长,在花粉萌发率下降最快期间,抗氧化保护酶直线升高出现最高峰值,活性增强,变化活跃,协同作用以抵抗胁迫。3种酶活性出现最高峰值前后花粉萌发率出现大幅度下降,可以推测当酶促抗氧化体系的活性不足以抵御逆境的胁迫,或者说无法维持其自身平衡时在宏观上直接表现出了马尾松花粉萌发率下降。
在马尾松花粉贮藏过程中,随着胁迫的加剧,花粉内部的生理代谢活动与花粉的衰老或失活等多种因子密切相关,室温和4 ℃ 2种贮藏温度下3种酶的变化趋势基本相似,只是出现最高峰值的时间不同,CAT出现最高峰值的时间比SOD和POD早72天,由此推测,在马尾松花粉贮藏过程中,在花粉萌发率开始大幅下降前期已启动CAT酶,协调体内的平衡以获得较强的抗胁迫能力,但单一CAT酶的抗氧化能力有限,随着胁迫的加剧,SOD和POD酶先后启动,活性直线升高,在萌发率大幅下降后到达最高峰值,CAT为零上高温胁迫敏感型保护酶,SOD和POD为零上高温胁迫非敏感型酶,随着花粉贮藏时间的延长,3者在抗氧化过程中协同作用,共同维持花粉的活力。-10和-20 ℃ 2种贮藏温度下3种保护酶的作用不同,POD出现最高峰值的时间比SOD和CAT早72天,也就是说,POD是零下低温胁迫的敏感型保护酶,在花粉萌发率开始大幅下降前期已启动POD,启动早活性高且起伏大,出现最高峰值后活性直线下降,此时直观上表现出萌发率大幅下降,是否已出现极限值而导致POD失活,有待进一步研究,而SOD和CAT虽然在零下低温胁迫中启动较迟,但变化平缓并呈现缓慢升高的趋势,说明这2种酶活性强,持续时间长,在逆境胁迫加剧的情况下仍具有维持细胞膜平衡,清除活性氧自由基的作用。
高爱新, 秦国峰, 欧阳彤, 等. 2009. 马尾松花粉萌发性状和不同林分马尾松花粉生活力的初步研究[J]. 福建林业科技, 36(3): 103-106. |
李合生, 孙群, 赵世杰, 等. 2000. 植物生理生化实验原理和技术[M]. 北京: 高等教育出版社.
|
林植芳, 李双顺, 林桂珠. 1984. 水稻叶片的衰老与超氧物歧化酶活性及脂质过氧化作用的关系[J]. 植物学报, 26(6): 605-615. |
孙爱芹, 常伟光, 韩斌, 等. 2010. 不同枣品种花粉生活力及贮藏方法研究[J]. 中国农学通报, 26(1): 166-168. |
孙霞, 邢世岩, 路冬. 1997. 银杏花粉生活力研究[J]. 果树科学, 15(1): 58-64. |
谭健晖. 2007. 采穗母株年龄效应对巨尾桉抗氧化生理的影响[J]. 林业科学, 43(4): 43-50. |
谭健晖, 王以红, 蔡玲, 等. 2007. 无性繁殖衰退过程中的生理变化[J]. 北京林业大学学报, 29(3): 15-22. |
王钦丽, 卢龙斗, 吴小琴, 等. 2002. 花粉的保存及其生活力测定[J]. 植物学通报, 19(3): 365-373. |
邢世岩, 有祥亮, 李可贵, 等. 1998. 银杏雄株开花生物学特性的研究[J]. 林业科学, 34(3): 51-58. |
徐进, 陈天华, 王章荣, 等. 1998. 不同贮藏方法及光照对马尾松花粉活力的影响[J]. 南京林业大学学报, 22(3): 728-731. |
颜伟玉, 吴小波, 邹阳, 等. 2005. 蜜蜂花粉中同工酶的研究[J]. 江西农业大学学报, 27(5): 772-774. |
张红城, 程蒙, 董捷. 2009. 六种蜂花粉中酶活性的研究[J]. 食品科学, 30(21): 229-230. DOI:10.3321/j.issn:1002-6630.2009.21.054 |
赵文飞, 邢世岩, 姜永旭. 2004. 贮藏时间对银杏花粉保护酶活性和萌发率的影响[J]. 武汉植物学研究, 22(3): 259-263. |
Kanazaw S, Sano S, Koshiba T, et al. 2000. Changes in antioxidative in cucumber cotyledons during naturalsence: comparison with those during dark induced senescence[J]. Plant Physiol, 109: 211-216. DOI:10.1034/j.1399-3054.2000.100214.x |
Parton E, Vervaeke I, Delen R, et al. 2002. Viability and storage of bromeliad pollen[J]. Euphytica, 125: 1552-1661. |
Yin J L, Zhao H E. 2005. Summary of influential Factors on pollen viability and its preservation methods[J]. Chinese Agricultural Science Bulletin, 21(4): 110-114. |
 2011, Vol. 47
2011, Vol. 47