文章信息
- 黄承玲, 陈训, 高贵龙
- Huang Chengling, Chen Xun, Gao Guilong
- 3种高山杜鹃对持续干旱的生理响应及抗旱性评价
- Physiological Response of Seedlings of Three Azalea Species of Drought Stress and Evaluation of Drought Resistance
- 林业科学, 2011, 47(6): 46-55.
- Scientia Silvae Sinicae, 2011, 47(6): 46-55.
-
文章历史
- 收稿日期:2010-12-06
- 修回日期:2011-03-03
-
作者相关文章
2. 贵州省植物园 贵阳 550004;
3. 贵州科学院 贵阳 550001
2. Guizhou Botanical Garden Guiyang 550004;
3. Guizhou Academy of Sciences Guiyang 550001
杜鹃属(Rhododendron)植物种类繁多,全世界约有1000余种,中国西南是杜鹃的主要分布中心,仅云、贵、川3省就占全国种类的65%以上。近年来,贵州省杜鹃花资源调查工作不断深入,贵州分布的已知杜鹃花种类增至111种(杨成华等,2006),主要生长在中部及西部海拔600~2400m的混交林、疏林或灌木丛中(陈训等,2003)。而位于贵州省西北部的百里杜鹃保护区共有杜鹃属植物33种,占全省杜鹃属植物的35%左右。在2009年9月至2010年3月西南大部分地区降水量不足200mm,干旱持续达230天,导致保护区杜鹃花的开花数量仅是往年的三分之一,一些从外地引入的高山杜鹃幼苗枯死,严重影响杜鹃资源的保护。目前,对高山杜鹃抗旱生理生化研究较少。有学者研究土壤水分胁迫对杜鹃叶片形态、光合特性日变化、光温响应、叶片脂类过氧化、抗氧化系统和水分利用效率的影响,对少数种类进行抗旱性评价(张长芹等,2002; 周广等,2010; 柯世省等,2007a; 柯世省等,2007b;柯世省等,2007c;柯世省等,2007d;柯世省等,2008)。本文立足于贵州丰富的野生杜鹃资源,选取3种高山杜鹃为材料,采用盆栽控水法对其抗旱性生理进行研究,并对其抗旱能力进行评价,以期为高山杜鹃的保护、抗旱育种提供理论依据。
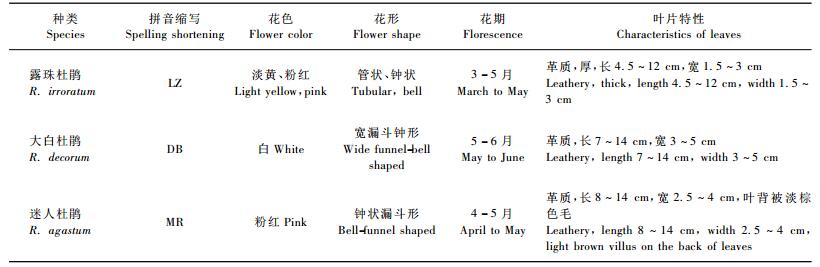
1 材料与方法 1.1 试验材料选取在百里杜鹃保护区广泛分布的3种高山杜鹃为研究对象,其花与叶片特性见表 1(陈训等,2003)。采用3年生杜鹃实生幼苗作为试验材料。高山杜鹃幼苗取自百里杜鹃保护区的育苗大棚,苗木管理和生长正常。
|
|
2010年4月将长势一致的3年生实生幼苗移植于普通塑料花盆内(上口径×下口径×高=300mm×200mm×250mm),每盆1株,每种高山杜鹃种植140盆,盆土为普通园土,每盆装盛土量一致,常规管理。2个月后在温室内采用盆栽控水法进行水分胁迫处理,并保持与室外通风。每种杜鹃设对照(CK)和自然干旱处理,为了避免试验过程中植株死亡影响取样,故每种处理准备植株70盆:对照是给苗木浇清水至饱和,以后每5天正常浇透水; 干旱处理为先给苗木浇清水至饱和,以后50天内不再浇水,第51天开始复水即浇水至饱和。分别在0,10,20,30,40,50,60天上午8:00左右采样,由于高山杜鹃3年生幼苗叶片数较少,每棵植株上部叶片一般为3~4片,每次采样时随机采取3盆植株所有的上部叶片以保证材料充足和一致,每次采样设3次重复,采样后的植株不再重复采样。叶片去除叶柄后袋封存编号,置入冰桶中带回实验室,立即剪碎混合均匀后对样品进行理化指标测试,其中第60天为复水后数据。试验期间观察记录其叶片形态变化。
1.3 测定方法质膜透性采用相对电导率法(王均明等,1999),酶活性及丙二醛(MDA)含量采用南京建成生物有限公司的试剂盒测定。可溶性蛋白质、游离脯氨酸和可溶性糖的测定参照高俊风(2006)的方法。超氧化物歧化酶(SOD)活性测定是以其抑制氮蓝四唑(NBT)光反应50%为1个单位酶活性,SOD单位为U·mg-1; 过氧化物酶(POD)活性用愈创木酚法测定,以每分钟OD470增加0.1为1个单位酶活性,POD单位为U·mg-1。MDA用硫代巴比妥酸(TBA)反应法测定。可溶性蛋白质用考马斯亮蓝法测定。游离脯氨酸测定采用酸性茚三酮比色法,可溶性糖用蒽酮比色法来测定。
1.4 数据分析采用隶属函数法对3种高山杜鹃抗旱能力进行综合评定(庄丽等,2005)。采用灰色关联分析法,计算各指标与抗旱隶属函数均值的关联系数,然后分别求出各指标与抗旱隶属函数均值的关联度,并按关联度大小排列出关联序(吴晓丽等,2008),关联度越大,表示指标与抗旱性关系越紧密。
隶属函数的基本计算方法为:R(Xj)=(Xj-Xmin)/(Xmax-Xmin),如果指标与抗旱性呈负相关,则:R(Xj)=1-(Xj-Xmin)/(Xmax-Xmin)。式中Xj为指标测定值,Xmin,Xmax为所有参试材料某一指标的最小值和最大值。将抗旱隶属函数值进行累加,并求其平均值。
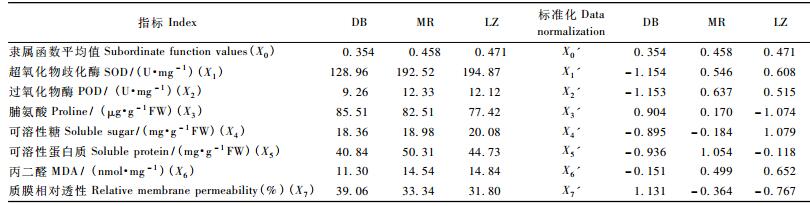
灰色关联分析的方法:1)建立灰色系统:将各种高山杜鹃抗旱指标的平均隶属函数值作为参考数据列(母序列),记为X0; 以各个抗旱指标的平均数为比较数列(子序列),记为X1,X2,X3…X7,分别表示SOD,POD……质膜相对透性。2)比较数据列的无量纲化:按下列公式进行标准化处理:Xi'(k)=(Xi(k)-Xi)/Si,式中,Xi(k)为原始数据; Xi'(k)为原始数据无量纲处理后的结果; Xi和Si分别为同一指标平均值和标准差。3)计算关联系数和关联度。关联系数,计算公式如下:
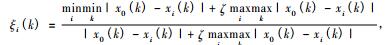
|
(1) |
式中,i为某个指标; ξi(k)为比较数列Xi对参考数列X0在第k点的关联系数; ζ为分辨系数,0<ζ<1。一般采取折中的办法,取ζ=0.5。使用比较数列Xi对参考数列X0的关联系数求出各指标对高山杜鹃抗旱性的关联度,计算公式为:
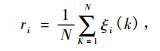
|
(2) |
式中,ri为比较数列Xi与参考数列X0的关联度,i=1,2,……,7。对试验数据用SPSS进行方差分析,差异显著性运用Duncan's检验法进行多重比较。所有数据用Excel和Origin软件进行处理并作图,在图中标出标准差。
2 结果与分析 2.1 持续干旱对叶片外部形态的影响逆境条件下植物外部形态有明显变化,受到直接影响的是叶片。如干旱使新叶生长缓慢,叶片数量减少,表皮细胞变小,叶面积明显缩小,从而影响叶片的光合能力(黄华等,2008; 徐飞等,2010)。因此叶片受损程度是评价植物抗逆能力的直观和直接的一个指标。根据观察记录,3种高山杜鹃在对照处理的情况下叶片正常生长,叶色亮绿。干旱处理时,3种杜鹃叶片受到不同程度的损伤。主要表现为新叶(上部叶片)反卷,下垂,叶尖枯黄; 老叶褐化,变黄,自然脱落。受损程度随着胁迫时间的延长而加深,经观察,大白杜鹃在干旱胁迫20天时叶片受损不明显,但到20天之后表现出明显的受损症状; 迷人杜鹃和露珠杜鹃则在胁迫30天之后才开始出现受损症状。
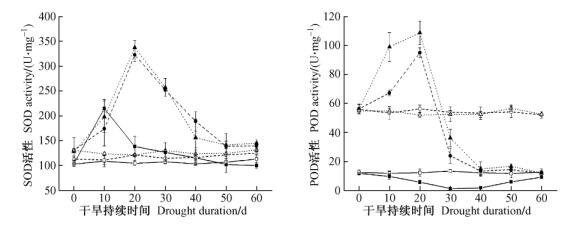
2.2 持续干旱对保护酶活性的影响从图 1可以看出:对照处理的幼苗SOD活性变化不明显,与对照相比,3种高山杜鹃在干旱胁迫时叶片SOD活性都呈先升后降的变化趋势,但达到峰值的时间不同。大白杜鹃在干旱持续10天时达到最大值215.11U·mg-1,随后叶片SOD活性呈下降趋势,到20天以后降幅变缓。而迷人杜鹃和露珠杜鹃在干旱持续20天时达最大值(迷人杜鹃为322.65U·mg-1,露珠杜鹃为337.26U·mg-1),持续干旱40天时叶片SOD活性快速下降,随后到50天时缓慢下降。当遭遇持续干旱时,叶片中活性氧不断产生,高山杜鹃叶片的SOD迅速响应,大白杜鹃SOD活性先达到顶峰,但SOD活性一直低于迷人杜鹃和露珠杜鹃; 复水后,3种高山杜鹃的SOD活性都有所上升,但大白杜鹃叶片SOD活性低于干旱前的水平,而迷人杜鹃和露珠杜鹃叶片SOD活性恢复到干旱前的水平,表明持续干旱对大白杜鹃的伤害程度较深。干旱胁迫时大白杜鹃幼苗与其他2种杜鹃幼苗叶片中SOD活性有显著差异(P<0.05),迷人杜鹃和露珠杜鹃幼苗叶片SOD活性无显著差异(P>0.05)。
|
图 1 持续干旱对高山杜鹃叶片保护酶活性的影响 Figure 1 Effect of drought on defense enzymes activities of azalea seedlings |
对照和处理的大白杜鹃叶片POD活性始终低于其他2种杜鹃,并且干旱时的变化趋势也与其他2种杜鹃不同。随着干旱的持续,迷人杜鹃和露珠杜鹃叶片POD活性呈先升后降的趋势。在干旱初期POD活性快速升高,到干旱20天时达到最大值(迷人杜鹃为95.12U·mg-1,露珠杜鹃为108.8U·mg-1);随后POD活性开始降低,在干旱30天时POD活性低于对照并迅速下降,到40天时活性最低(迷人杜鹃为13.55U·mg-1,露珠杜鹃为15.0U·mg-1); 复水后,叶片POD活性没有恢复上升。大白杜鹃叶片POD活性在初期呈下降趋势,在干旱10天时叶片POD活性比对照低,持续干旱30天时活性最低,为1.42U·mg-1,到持续干旱40天后POD活性缓慢升高,复水后又稍有下降,但都低于对照。干旱胁迫时大白杜鹃幼苗与其他2种杜鹃幼苗叶片中POD活性有极显著差异(P<0.01),迷人杜鹃和露珠杜鹃幼苗叶片POD活性没有显著差异。
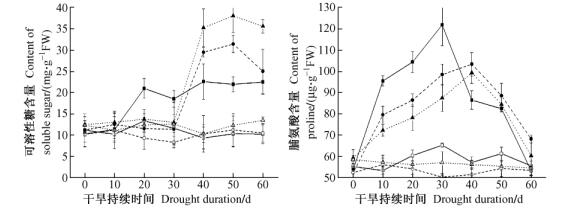
2.3 持续干旱对渗透调节物质含量的影响如图 2A所示:与对照相比,持续干旱条件下高山杜鹃幼苗叶片的可溶性糖含量明显增加。大白杜鹃叶片的可溶性糖在持续干旱前20天迅速上升,在持续干旱20天时含量比其他2种杜鹃高,随后变化趋势较为平缓,复水后含量也没有明显变化。迷人杜鹃和露珠杜鹃叶片可溶性糖含量的变化趋势相似,在持续干旱的前30天可溶性糖含量缓慢上升,随后迅速增加且明显高于大白杜鹃。在干旱50天时达到高峰,迷人杜鹃为31.5mg·g-1FW,露珠杜鹃为38.1mg·g-1FW,之后有下降趋势,复水后含量仍呈缓慢下降。大白杜鹃在持续干旱的情况下可溶性糖的响应比其他2种杜鹃较为迅速,在干旱初期便迅速增加以适应干旱胁迫; 迷人杜鹃与露珠杜鹃则在持续干旱30天后才迅速积累可溶性糖以抵御干旱的伤害,而且积累可溶性糖的能力明显高于大白杜鹃。干旱胁迫时大白杜鹃幼苗与露珠杜鹃幼苗叶片中可溶性糖含量有极显著差异(P<0.01),迷人杜鹃与其他2种杜鹃幼苗叶片可溶性糖含量差异不显著(P>0.05)。
|
图 2 持续干旱对高山杜鹃叶片渗透调节物质含量的影响 Figure 2 Effect of drought on osmoses regulatory molecules of azalea seedlings |
如图 2B所示:与对照相比,在干旱胁迫时3种杜鹃叶片中脯氨酸含量都有明显的积累过程,3种杜鹃叶片脯氨酸含量都呈单峰曲线。大白杜鹃在持续干旱30天时达到高峰121.92μg·g-1FW,随后呈下降趋势。迷人杜鹃和露珠杜鹃叶片脯氨酸含量在持续干旱40天时达到峰值,分别为103.47和99.45μg·g-1FW,含量低于大白杜鹃的峰值,随后脯氨酸含量呈下降趋势,但下降的趋势较大白杜鹃的缓慢,而且含量比大白杜鹃高。复水后3种杜鹃叶片脯氨酸含量都减少。脯氨酸的积累能缓解干旱带来的伤害,但这种缓解能力有限,在脯氨酸含量达到峰值后都呈下降趋势。干旱胁迫时大白杜鹃幼苗与其他2种杜鹃幼苗叶片中脯氨酸含量有显著差异(P<0.05),迷人杜鹃和露珠杜鹃幼苗叶片脯氨酸含量没有显著差异。可见,大白杜鹃叶片的脯氨酸对干旱的响应比其他2种杜鹃迅速。
2.4 持续干旱对可溶性蛋白质含量的影响由图 3可知:与对照相比,大白杜鹃叶片可溶性蛋白质含量的变化呈单峰曲线,在干旱初期含量呈上升趋势,可溶性蛋白质含量高于对照,到干旱20天时,到达最大值56.32mg·g-1FW,随后可溶性蛋白质的含量呈下降趋势,含量低于对照,复水后仍然下降。迷人杜鹃和露珠杜鹃叶片可溶性蛋白质含量在干旱初期迅速下降,比对照含量低,在干旱20天时达到最小值(迷人杜鹃为26.6mg·g-1FW,露珠杜鹃为19.36mg·g-1FW),随后可溶性蛋白质含量持续上升,在干旱40天时达到最大值(迷人杜鹃为71.67mg·g-1FW,露珠杜鹃为69.84mg·g-1FW),之后可溶性蛋白质又开始下降,但含量高于对照。干旱胁迫时大白杜鹃幼苗与其他2种杜鹃幼苗叶片中可溶性蛋白质含量有极显著差异(P<0.01),迷人杜鹃和露珠杜鹃幼苗叶片的可溶性蛋白质含量有显著差异(P<0.05)。

|
图 3 持续干旱对高山杜鹃叶片可溶性蛋白质含量的影响 Figure 3 Effect of drought on soluble protein content of azalea seedlings |
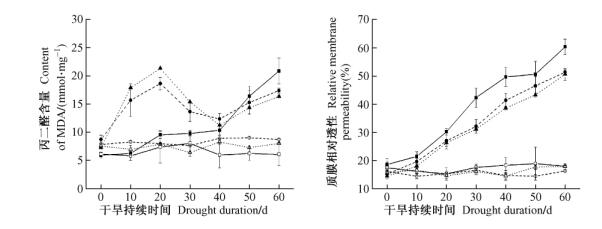
由图 4可知:与对照相比,3种高山杜鹃在持续干旱时叶片中MDA含量有明显变化,表明干旱造成高山杜鹃叶片不同程度的膜脂质过氧化,但各种杜鹃变化趋势不同。大白杜鹃叶片中MDA呈持续上升趋势,而迷人杜鹃和露珠杜鹃叶片MDA含量呈现先升高后降低再升高的变化趋势,在干旱初期20天迅速升高达到峰值,分别为18.63和21.36nmol·mg-1,随后含量开始下降,到40天后又出现回升。可能是因为这2种杜鹃对干旱有适应过程,当保护酶系统产生防御作用时,MDA含量下降。干旱胁迫时大白杜鹃幼苗与其他2种杜鹃幼苗叶片MDA含量有极显著差异(P<0.01),迷人杜鹃和露珠杜鹃幼苗叶片MDA含量没有显著差异。
|
图 4 持续干旱对高山杜鹃叶片丙二醛含量和质膜相对透性的影响 Figure 4 Effect of drought on MDA and relative membrane permeability of azalea seedlings |
在高山杜鹃幼苗受到干旱胁迫时,叶片的质膜相对透性随着胁迫时间的延长而增大,其中大白杜鹃叶片的质膜透性始终高于其他2种杜鹃,表明大白杜鹃叶片受到逆境伤害时脂膜过氧化程度高于其他2种杜鹃。干旱胁迫时大白杜鹃幼苗与迷人杜鹃幼苗叶片的质膜相对透性差异显著(P<0.05),与露珠杜鹃叶片的质膜相对透性差异极显著(P<0.01),迷人杜鹃和露珠杜鹃幼苗叶片的质膜相对透性差异不显著。
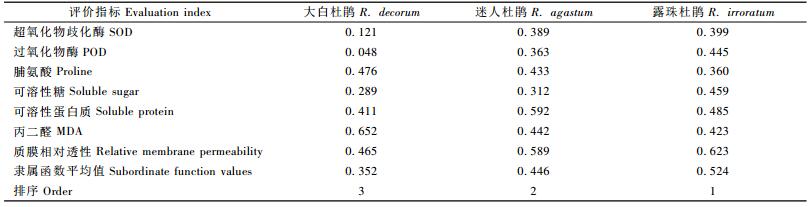
2.6 高山杜鹃抗旱性的综合评价植物的抗旱性是一个复合性状,利用模糊数学的隶属函数法对高山杜鹃的抗旱性进行综合评价,用每种高山杜鹃各项指标隶属度的平均值作为树种抗旱能力综合鉴定标准,该值越大,抗旱性越强。结果如表 2所示:大白杜鹃、迷人杜鹃和露珠杜鹃的隶属函数平均值分别为0.352,0.446和0.524,抗旱能力从大到小的顺序为:露珠杜鹃>迷人杜鹃>大白杜鹃。
|
|
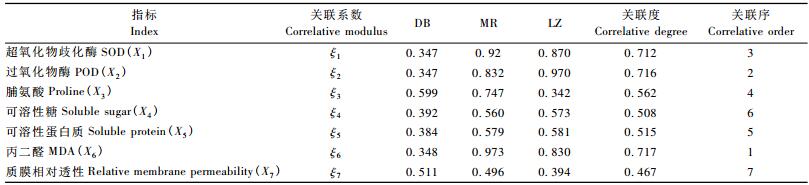
灰色关联分析是灰色系统理论的一种新的分析方法,它是用关联度大小来描述事物之间、因素之间关联程度的一种定量化的方法。根据灰色系统理论,关联度表示各指标与抗旱系数的密切程度,关联度越大说明该指标与抗旱系数的关系越密切。3种高山杜鹃抗旱指标的平均值及标准化处理后的结果见表 3,通过表 3的结果可以计算出抗旱指标与抗旱性的关联度,并排列出关联序(表 4)。基于灰色关联分析理论,关联度越大,表明参考数列与比较数列的关系愈紧密,反之,关系较远。关联度大小可表明某一项指标对干旱的敏感程度。从表 4可以看出:3种高山杜鹃的抗旱性与7个生理指标的关联度从大到小分别为:0.717,0.716,0.712,0.562,0.515,0.508,0.467。由此可知:MDA,POD和SOD与抗旱性的关联度较大; 其次为脯氨酸、可溶性蛋白质和可溶性糖含量; 而叶片的质膜相对透性对高山杜鹃抗旱性的影响最小。通过关联分析,说明干旱胁迫下保护酶类的活性大小与丙二醛含量是衡量高山杜鹃抗旱性的首要指标; 脯氨酸是水合能力很强的氨基酸,干旱胁迫下其含量的增加有助细胞持水和生物大分子结构的稳定,可溶性糖和蛋白质的积累能增大细胞液浓度,因此渗透调节物质是衡量高山杜鹃抗旱性的辅助指标。
|
|
|
|
植物体在生命过程中不断地产生有害的活性氧,而植物体内清除活性氧的防卫系统使其产生与清除维持动态平衡。SOD,POD,CAT是生物体内清除自由基的重要保护酶。多数研究认为,干旱伤害程度与这3种酶活力的提高呈负相关(Dhindsa et al.,1981;Chowdhury et al.,1985),即水分胁迫时SOD,POD,CAT的活性与抗氧化能力呈正相关(王建华等,1989)。本研究的结果也表明:除了露珠杜鹃叶片POD活性外,高山杜鹃叶片中SOD和POD活性随着干旱的持续呈先升后降的趋势。与柯世省等(2007c)对云锦杜鹃(R.fortunei)、时忠杰等(2007)对板栗(Castanea mollissina)、姜英淑等(2009)对欧李(Cerasus humilis)、王新建等(2008)对豫楸1号(Catalpa bungei cl.‘Yu-1’)不同砧木嫁接苗的研究结果一致。POD的作用具有双重性,一方面POD可在逆境或衰老初期表达,清除H2O2,表现为保护效应,另一方面POD也可在逆境或衰老后期表达,参与活性氧的生成、叶绿素的降解(赵丽英等,2005),而大白杜鹃叶片中的POD活性的变化趋势证明了这种双重性的存在,大白杜鹃叶片POD活性在持续干旱后期上升,加重叶片细胞的质膜过氧化程度。
大白杜鹃叶片可溶性蛋白质含量的变化趋势与其他2种杜鹃不同,可能与可溶性蛋白质的渗透调节功能有关,高含量的可溶性蛋白质可使细胞维持较低的渗透势,抵抗水分胁迫带来的伤害(Xiong et al.,2002)。本研究表明,随干旱时间的延长,大白杜鹃叶片的可溶性蛋白质含量呈先增加后降低的趋势,这与康俊梅等(2005)在苜蓿(Medicago sativa)上的研究结果一致,说明在胁迫处理初期植物体内的不溶性蛋白质变为可溶性蛋白质以增强渗透调节能力,而在胁迫处理后期干旱胁迫超过植物所能忍耐的阈值,植物体内的合成代谢受阻,蛋白质降解。在持续干旱情况下,迷人杜鹃和露珠杜鹃在干旱初期代谢受影响,从而影响蛋白质合成,含量降低,而当干旱持续时,可溶性蛋白质含量迅速增加,防止脱水,当超过耐受阈值时,含量下降。
脯氨酸和可溶性糖是重要和有效的有机渗透调节物质。当植物遭受渗透和水分胁迫时,脯氨酸和可溶性糖的积累是普遍现象。水分胁迫下,植物体内多种生理反应被诱导和加速,植物细胞通过脯氨酸和可溶性糖的积累进行渗透调节,从而阻止细胞膜解离,增强细胞保水能力,稳定细胞结构,防止细胞脱水(吴强盛等,2003)。柯世省等(2007c)对云锦杜鹃、徐娟等(2001)对兴安杜鹃(R.dauricum)、徐莲珍等(2008)对刺槐(Robinia pseudoacacia)的研究都表明:随着水分胁迫程度加深叶片中脯氨酸和可溶性糖含量增加。本研究结果表明,随着干旱的持续,高山杜鹃幼苗叶片中可溶性糖含量不断积累,与上述文献的结论相同,而脯氨酸则随着干旱持续呈上升后下降,与徐莲珍等(2008)对元宝枫(Acertruncatum)和侧柏(Platycladus orientalis)、喻晓丽等(2007)对火炬树(Rhus typhina)的研究结果一致。
逆境伤害时脂膜过氧化导致MDA积累,使蛋白质和核酸变性,导致膜流动性降低,膜透性增强,因此MDA和质膜相对透性是植物遭受逆境伤害的常用指标。持续干旱时,3种高山杜鹃叶片MDA含量随着时间延长呈先升后降再升的变化趋势,这与喻晓丽等(2007)对火炬树的研究结果一致。但大白杜鹃在胁迫前期MDA含量低于其他2种杜鹃,可能原因是前期大白杜鹃酶保护防御系统先启动,而迷人杜鹃和露珠杜鹃则有适应过程,在胁迫中期酶防御系统启动后,MDA含量出现下降趋势,当过氧化程度加深后,防御系统失去作用,MDA开始上升。而持续干旱使3种高山杜鹃幼苗质膜相对透性明显增强,这与许多抗旱性研究结果一致(王新建等,2008; 柯世省,2007c)。
通过对各理生理指标隶属度的平均值对3种高山杜鹃抗旱能力综合评价,结果表明露珠杜鹃的抗旱性最强,大白杜鹃的抗旱性最弱,迷人杜鹃抗旱能力居中,这与张长芹等(2002)的结果相似。
陈训, 巫华美. 2003. 中国贵州杜鹃花[M]. 贵阳: 贵州科技出版社.
|
高俊风. 2006. 植物生理学实验指导[M]. 北京: 高等教育出版社.
|
黄华, 梁宗锁, 韩蕊莲. 2008. 持续干旱胁迫对女贞形态与生长的影响[J]. 林业科学, 44(8): 145-149. DOI:10.11707/j.1001-7488.20080827 |
姜英淑, 陈书明, 王秋玉, 等. 2009. 干旱胁迫对2个欧李种源生理特征的影响[J]. 林业科学, 45(6): 6-10. DOI:10.11707/j.1001-7488.20090602 |
康俊梅, 杨青川, 樊奋成. 2005. 干旱对苜蓿叶片可溶性蛋白的影响[J]. 草地学报, 13(3): 199-202. DOI:10.11733/j.issn.1007-0435.2005.03.006 |
柯世省, 杨敏文. 2007a. 水分胁迫对云锦杜鹃光合特性日变化的影响[J]. 福建林业科技, 34(3): 10-14. |
柯世省, 杨敏文. 2007b. 水分胁迫对云锦杜鹃光合生理和光温响应的影响[J]. 园艺学报, 34(4): 959-964. |
柯世省, 杨敏文. 2007c. 水分胁迫对云锦杜鹃抗氧化系统和脂类过氧化的影响[J]. 园艺学报, 34(5): 1217-1222. |
柯世省. 2007d. 土壤干旱胁迫对云锦杜鹃水分利用效率的影响[J]. 河南师范大学学报:自然科学版, 35(2): 150-153. |
柯世省. 2008. 土壤干旱下云锦杜鹃光合作用的限制形式[J]. 云南农业大学学报, 23(3): 387-391. |
时忠杰, 杜阿朋, 胡哲森, 等. 2007. 水分胁迫对板栗幼苗叶片活性氧代谢的影响[J]. 林业科学研究, 20(5): 683-687. |
王建华, 刘鸿先, 徐同. 1989. 超氧物歧化酶(SOD)在植物逆境和衰老生理中的作用[J]. 植物生理学通讯, 25(1): 1-5. |
王均明, 孟丽, 孙金花, 等. 1999. 林木抗旱性与其根次生构造关系的研究[J]. 中国水土保持, (6): 20-22. |
王新建, 何威, 杨淑红, 等. 2008. 豫楸1号4种砧木嫁接苗对干旱胁迫的生理响应[J]. 林业科学, 44(5): 31-37. DOI:10.11707/j.1001-7488.20080508 |
吴强盛, 夏仁学, 张琼华. 2003. 果树对水分胁迫反应研究进展[J]. 亚热带植物科学, 32(2): 72-76. |
吴晓丽, 韩清芳, 贾志宽. 2008. 不同紫花苜蓿几个抗旱指标的灰色关联分析[J]. 干旱地区农业研究, 23(3): 100-103. |
徐飞, 郭卫华, 徐伟红, 等. 2010. 刺槐幼苗形态、生物量分配和光合特性对水分胁迫的响应[J]. 北京林业大学学报, 32(1): 24-30. |
徐娟, 曹玉峰, 刘焕婷. 2010. 不同水分胁迫对兴安杜鹃、迎红杜鹃生理指标的影响[J]. 中国新技术新产品, (7): 228-229. |
徐莲珍, 蔡靖, 姜在民, 等. 2008. 水分胁迫对3种苗木叶片渗透调节物质与保护酶活性的影响[J]. 西北林学院学报, 23(2): 12-14. |
杨成华, 李贵远, 邓伦秀, 等. 2006. 贵州百里杜鹃保护区的杜鹃属植物种类及其观赏特性研究[J]. 西部林业科学, 35(4): 14-18. |
喻晓丽, 邸雪颖, 宋丽萍. 2007. 水分胁迫对火炬树幼苗生长和生理特性的影响[J]. 林业科学, 43(11): 58-62. |
张长芹, 罗吉风, 苏玉芬. 2002. 六种杜鹃花的耐旱适应性研究[J]. 广西植物, 22(2): 174-176. |
赵丽英, 邓西平, 山仑. 2005. 活性氧清除系统对干旱胁迫的响应机制[J]. 西北植物学报, 25(2): 413-418. |
周广, 孙宝腾, 张乐华, 等. 2010. 井冈山杜鹃叶片抗氧化系统对高温胁迫的响应[J]. 西北植物学报, 30(6): 1149-1156. |
庄丽, 陈亚宁, 陈明, 等. 2005. 模糊隶属法在塔里木河荒漠植物抗旱性评价中的应用[J]. 干旱区地理, 28(3): 367-372. |
Chowdhury R S, Choudhuri M A. 1985. Hydrogen peroxide metabolism as an index of water stress tolerance in jute[J]. Physiologia Plantarum, 65(4): 476-480. DOI:10.1111/ppl.1985.65.issue-4 |
Dhindsa R S, Matowe W. 1981. Drought tolerance in two mosses:correlated with enzymatic defence against lipid peroxidation[J]. Journal of Experimental Botany, 32(1): 79-91. DOI:10.1093/jxb/32.1.79 |
Xiong L M, Schumaker K S, Zhu J K. 2002. Cell signaling during cold,drought,and salt stress[J]. Plant Cell, 14: 165-183. DOI:10.1105/tpc.010278 |
 2011, Vol. 47
2011, Vol. 47