文章信息
- 陈羽, 姜清彬, 仲崇禄, 张勇, 陈珍
- Chen Yu, Jiang Qingbin, Zhong Chonglu, Zhang Yong, Chen Zhen
- 接种AM菌对麻楝不同种源苗期的生长效应
- Effects of Arbuscular Mycorrhizal Fungi on Seedling Growth of Chukrasia tabularis
- 林业科学, 2011, 47(5): 76-81.
- Scientia Silvae Sinicae, 2011, 47(5): 76-81.
-
文章历史
- 收稿日期:2010-09-14
- 修回日期:2010-12-24
-
作者相关文章
麻楝(Chukrasia tabularis)是楝科(Meliaceae)麻楝属(Chukrasia)植物,成熟树木高达40 m,胸径达1.2 m,天然分布于1°—25° N,73°—120° E,包括印度、东南亚及澳洲西北部等地区(Ho et al., 1995; Chen,1995; Kalinganire et al., 2002)。麻楝是具有高价值多用途的树种,适宜做风景树、绿荫树和行道树; 也是国际性珍贵速生用材树种(Kalinganire et al., 2000; 潘澜等,2010),其木材用途广泛,是用于胶合板材、名贵高档家具、房屋建筑、室内装修、音箱、钢琴壳、雕刻、仪器箱盒等的高档木材。麻楝也是药用植物(Nagalakshmi et al., 2001; 周静等,2004; Kaur et al., 2008)。近年来,随着人们对珍贵用材需求的不断增加及麻楝天然林资源的减少,麻楝木材价格也不断上升,国际市场上麻楝锯材的价格高达每立方米1 000美元1)。因此,世界其他非天然分布地区也广泛开展引种研究和栽培试验,对麻楝属树种的研究和利用也得到进一步重视(Mabberley et al., 1995; 仲崇禄等,2001; Kalinganire et al., 2002; 罗志明等,2007)。我国在20世纪70年代就对麻楝进行了研究,但由于种种原因,进展缓慢。从2000年开始才逐渐有对麻楝研究的报道,包括麻楝引种和造林施肥等试验1) (仲崇禄等,2001; 罗志明等,2007; 潘澜等,2010)。
1) 李儒法. 2007.麻楝地理种源引种试验.北京:中国林业科学研究院,1-14.
众所周知,菌根(mycorrhizal)对树木的引种成功和生长起着关键作用,这已被许多事实所证明(郭秀珍等,1989; 弓明钦等,1997; 郑来友,2010)。麻楝属丛枝菌根(AM菌根)营养型树种(弓明钦等,1997),Shi等(2006)对我国海南楝科28种植物的共生菌根调查发现有5个属33种AM菌,仅与麻楝共生的AM菌根类型就达12种之多,可见菌根与麻楝的生长关系密切。因此,在开展麻楝引种和造林研究的同时,也要对麻楝相应的共生菌根进行研究,这不仅是课题研究的需要,也是为今后长期开展麻楝研究建立基础。为此,笔者开展了3个AM菌株对接种5个种源的海南麻楝苗期生长效应的研究,旨在为麻楝引种选择优良AM菌提供技术支撑。
1 材料与方法 1.1 试验材料 1.1.1 供试苗木供试苗木为5个种源的麻楝实生苗,苗龄45天,麻楝种源资料见表 1。将麻楝种子经1 g·L-1的HgCl2溶液振荡消毒1 min,用无菌水反复冲洗多次后晾干,温室中播种于经高温高压灭菌(103 kPa,121℃,60 min)的混合基质(黄心土、砂、泥炭、蛭石比例为1.5 :2 :1.5 :1)中,种子出芽前每天早晚2次淋水,出芽后改为每天傍晚浇水1次,当幼苗长出2对真叶,挑选苗高等长势一致的幼苗进行移栽并接种。
|
|
供试菌种为3个AM菌株(表 2)。AM菌种在灭菌的混合基质(砂、泥炭、蛭石比例为2:1.5:1)中利用三叶草(Triflium repens)进行生物繁殖,4个月后去其茎叶,将根系剪碎与培养基质混合,晾干后备用。
|
|
试验采用完全随机化设计,5个种源的麻楝幼苗分别接种3个AM菌株,另设置对照,共20个处理,每处理接种10株幼苗,重复3次。试验总苗数为600株。试验所需苗木的播种、移植、接种、苗木管理均在温室内完成,自然光照,每天傍晚浇水1次。
1.2.2 幼苗接种幼苗移植与接种AM菌同时进行。将播种盆中45天苗龄的幼苗,选择苗高等长势一致的幼苗进行移栽,栽培容器为250 mL容量的一次性塑料吸水杯,高9 cm,口径7 cm,杯底直径4.5 cm,每杯移栽一株幼苗,幼苗移栽前放入2 /3体积的灭菌基质,然后加入5 g AM菌剂,再用灭菌基质覆盖装至杯口,植入供试幼苗,浇水定根。
1.2.3 试验数据观测幼苗移植接种后每隔1个月进行苗高生长量测定(分别以H1,H2,H3,H4,H5表示)。6个月后收获试验苗,测定指标如下:苗高(H6)、地径(GD)、叶片数(LN)、叶干质量(LDM)、茎干质量(SDM)、根干质量(RDM)、总干质量(TDM)。通过显微镜观测根样,统计菌根感染情况。
1.2.4 矿质营养元素分析6个月后收获试验苗,摘取每株苗木从上往下数第3个侧枝靠近尖端的5片叶子,将每个处理每个重复的10株进行采样,混合,70 ℃烘干后,研磨成粉,取样进行矿质营养元素(N,P和K)含量的测定。全N的测定采用凯氏法,全P的测定采用钼锑抗比色法,植株全K的测定采用火焰光度计法(张志良,1990; 陈应龙等,1999)。
1.3 数据分析试验数据苗高、地茎、叶片数、叶干质量、茎干质量、根干质量和总干质量,运用SAS 8.1软件进行方差分析和Ducan多重比较分析。按如下公式计算菌根感染率、菌根感染率分级、菌根感染强度和菌根依赖性MD(弓明钦等,1997),菌根感染率在方差分析前利用Excel 2003软件进行平方根反正弦转换。
菌根感染率(%) = (菌根感染的根段数/检查的菌根根段总数)× 100。
菌根感染分级标准按受感染的营养根占观察总根数的比例确定:1级(0 ~ 5%); 2级(6% ~ 25%); 3级(26% ~ 50%); 4级(51% ~ 75%); 5级(76% ~ 100%)。
菌根依赖性MD =接种植株平均干质量/对照株平均干质量)× 100,(MD>300%为强依赖性,MD>200%为中等依赖性,MD<200%为弱依赖性或没有依赖性)。
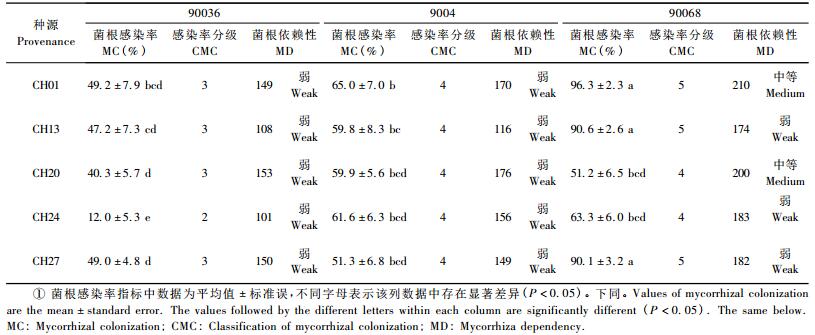
2 结果与分析 2.1 麻楝幼苗接种AM菌的菌根合成情况接种6个月后,3个AM菌株都可以与5个种源麻楝幼苗形成侵染(表 3); 其中90068菌株×种源CH01,CH13和CH27菌根感染率分别为96.3%,90.6%和90.1%,与其他处理有显著差异,感染率分级均为5级。而90036菌株×种源CH24菌根感染率最低(12.0%),感染率分级为2级。从菌根依赖性指标看,仅90068菌株×种源CH01和CH20为中等,其他各处理均为弱。综合比较,3个菌株与5个种源麻楝幼苗的菌根合成情况,菌株90068×种源CH01接种效果显著优于其他组合。
|
|
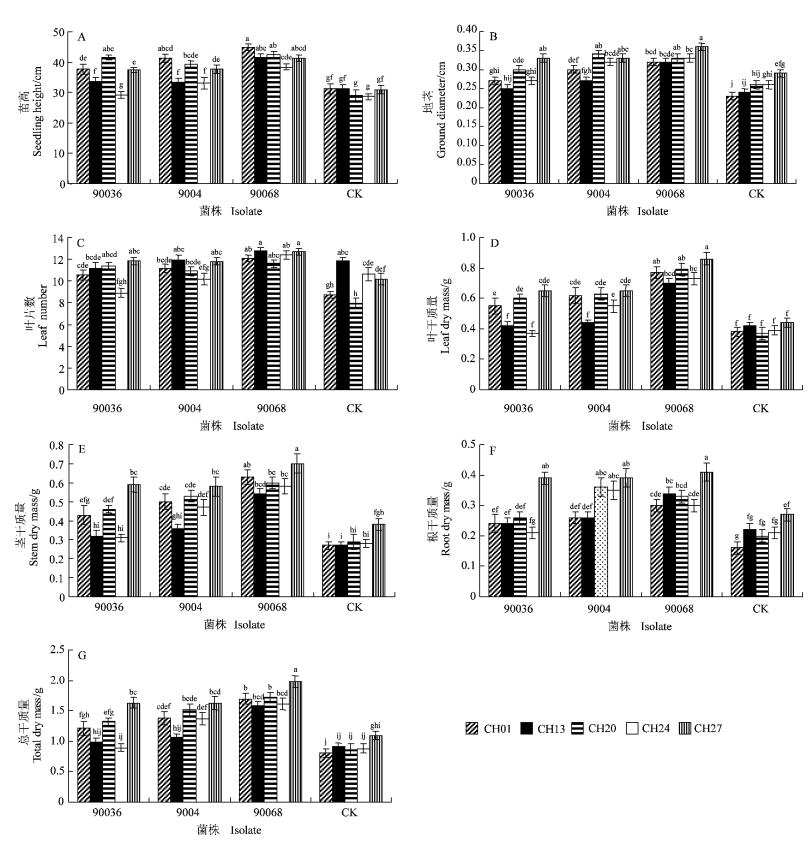
对接种6个月的幼苗进行生物量测定,结果显示(图 1) :组合90036菌株×种源CH20,9004菌株×种源CH01,90068菌株×种源CH01,CH13,CH20和CH24与其他组合在苗高上表现差异显著,所有处理中90068菌株×种源CH01苗高均值最大(44.83 cm); 地茎指标中90068菌株×种源CH27均值最大(0.36 cm),同组合90036菌株×种源CH27,9004菌株×种源CH20、CH27,90068菌株×种源CH20与其他处理有显著差异; 90068菌株×种源CH13 (12.77枚),CH27 (12.73枚)在叶片数指标中表现显著; 在叶干质量指标上,90068菌株×种源CH01,CH20和CH27组合与其他处理有显著差异; 90068菌株×种源CH01和CH27在茎干质量指标上表现为与其他处理有显著差异; 从根干质量指标来看,组合90036菌株×种源CH27,9004菌株×种源CH20,CH24,CH27,90068菌株×种源CH27与其他组合差异显著,所有处理中90068菌株×种源CH27根干质量均值最大(0.41 g); 此外,对总干质量指标而言,仅90068菌株×种源CH27组合与其他各处理存在显著差异,达到1.98 g。综合各指标,90068菌株×种源CH27接种后幼苗生长效应优于其他组合。
|
图 1 5个种源麻楝幼苗接种AM菌的效果 Figure 1 Effect of inoculation with AM fungi on seedlings of 5 provenances C. tabularis 不同字母表示存在显著差异(P < 0.05)。 Values followed by the different letters are significantly different (P < 0.05). |
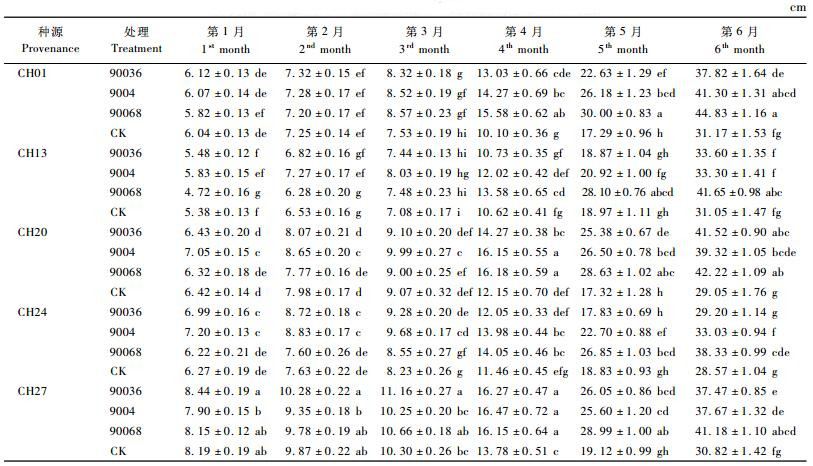
连续6个月调查麻楝幼苗苗高,分析接种AM菌后麻楝苗期苗高增长情况,结果见表 4。在接种后的前3个月,种源CH27能够与菌株90036,90068以及对照表现出显著差异。而并非所有接种AM菌的种源都显著高于对照; 到第4个月,除种源CH13,CH24之外,其他种源接种AM菌苗高都显著高于对照,接种AM菌对麻楝幼苗苗高增长作用开始显现。到第5个月和第6个月,接种90068菌株对5个种源的麻楝幼苗苗高增长明显增强。可见,接种AM菌能够促进麻楝幼苗的生长,对5个种源的麻楝幼苗的苗高增长,接种90068菌株生长促进作用较明显,并且作用表现在接种5个月之后。
|
|
接种AM菌6个月后,测定麻楝幼苗在单位质量内(g·kg-1)氮磷钾3种矿质元素的含量,结果见表 5。在氮、钾元素水平上,接种3个AM菌株对5个种源麻楝幼苗均与对照无显著差异; 而对矿质元素磷的吸收,接种90068菌株与其他菌株(包括对照)均表现显著差异,其中90068菌株×种源CH13接种处理矿质元素吸收含量最高(2.594 g·kg-1)。由此可见,接种90068菌株有利于5个种源麻楝幼苗对磷元素的吸收和积累; 其他菌株对磷元素吸收促进作用不显著。对于氮和钾2种矿质元素,表现为接种AM菌对麻楝幼苗吸收和积累不明显。
|
|
对5个种源麻楝幼苗进行人工接种AM菌试验,证明麻楝幼苗接种AM菌可以形成丛枝菌根; 并且不同种源材料均可表现出明显的接种效果,从而证实麻楝确实是一种内生菌根树种,反映了Smith等(1997)和Shi等(2006)报道的类似结果。但是麻楝是否也有外生菌根,目前尚未发现报道。试验发现对麻楝幼苗实施AM菌的人工接种后可以提高菌根感染率,对苗木高、地径、叶片数等生物量有促进作用; 不同种源的麻楝幼苗对AM菌表现出一定程度的菌根依赖性,进一步证明AM菌的人工接种对麻楝幼苗生长的重要性。
不同AM菌种对不同种源麻楝幼苗接种的效果不一致,说明不是所有AM菌接种都与宿主植物形成较佳的共生体,依据“适树适菌”的原则,在推广应用前必须对菌种进行必要的筛选,选出最佳宿主植物与AM菌的共生组合。本研究结果表明,在5个种源麻楝幼苗接种的3个AM菌株当中,菌株90068无论在菌根侵染性、生物量和矿质元素的吸收等方面,都表现最佳。其中菌株90068×种源CH01接种后的菌根合成情况效果最好; 菌株90068×种源CH27在生物量方面作用最优; 菌株90068×种源CH01在幼苗苗高增长促进作用最明显,表现为5至6个月之后; 其次矿质元素吸收方面,菌株90068×种源CH13对磷元素的吸收明显高于其他接种处理。而菌株90036与菌株9004在接种后幼苗测定的各项指标中表现各有优劣。其中菌根合成、生物量和苗高增长方面,菌株9004优于菌株90036;而对于矿质元素的吸收,菌株90036要优于菌株9004。由此可见,不同种源麻楝幼苗接种不同AM菌种后的生长指标与不同种源麻楝幼苗对不同AM菌依赖性测定的结果,两者之间有时结论并非一致,这可能是因为麻楝幼苗对不同菌种的反应不同,有些菌种促进地下根系发育的作用大于对地上部分的作用,从而导致总生物量的增加(弓明钦等,1997)。但就总的结果而言,供试的90068菌株表现最好。
接种菌根菌能显著提高植物矿质营养元素的总含量,有利于促进根系对矿质元素的吸收(Mosse,1957; 陈应龙等,1999; 周志春等,2009)。本研究对麻楝接种AM菌能够促进对氮磷钾3种矿质元素的总吸收量。但是从单位质量内分析发现,仅对磷的吸收有明显的提高,对氮钾元素促进吸收作用并不明显,这与弓明钦等(1997)和刘润进等(2000)报道的接种菌根菌对矿质营养元素吸收作用类似,他们认为菌根根系单位质量吸收磷显著高于对照,而对氮钾元素是否提高则要看是何种宿主植物。
本研究结果表明,人工接种AM菌对麻楝幼苗培育和生长有较好的促进作用。接种不同AM菌种和对不同种源麻楝幼苗苗期生长作用也有一定的差别,接种后形成的菌根能够促进麻楝幼苗根系对土壤中重要营养元素磷的吸收,这为改善麻楝苗木根系微生物组成和土壤环境提供了新的有效途径。此外,对接种AM菌进行菌根化造林试验的效果也值得研究,后期会有相关报道。
陈应龙, 弓明钦, 王凤珍, 等. 1999. 混合接种Glomus与Pisolithus菌株对尾叶桉矿质营养吸收的影响[J]. 林业科学研究, 12(3): 262-267. |
弓明钦, 陈应龙, 仲崇禄. 1997. 菌根研究及应用[M]. 北京: 中国林业出版社: 171-177.
|
弓明钦, 王凤珍, 陈羽, 等. 2002. 柚木菌根及其对苗期生长影响的研究[J]. 林业科学研究, 15(5): 515-520. |
郭秀珍, 毕国昌. 1989. 林木菌根及应用技术[M]. 北京: 中国林业出版社: 31-39.
|
黄少伟, 谢维辉. 2001. 实用SAS编程与林业试验数据分析[M]. 广州: 华南理工大学出版社.
|
刘润进, 李晓林. 2000. 丛枝菌根及其应用[M]. 北京: 科学出版社: 98-99.
|
罗志明, 李儒法. 2007. 麻楝地理种源苗期试验研究[J]. 热带林业, 35(3): 28-30. |
潘澜, 薛立, 刘斌, 等. 2010. 稀土对麻楝幼苗抗寒性的影响[J]. 植物生理学通讯, 46(8): 773-778. |
张志良. 1990. 植物生理学实验手册[M]. 上海: 华东师范大学出版社.
|
郑来友. 2010. 菌根化育苗造林技术---促进植被恢复的一项有效措施[J]. 林业实用技术, (5): 58-60. |
仲崇禄, 洪长福, 白嘉雨, 等. 2001. 麻楝属树种种源苗期试验及其在我国发展潜力[J]. 广东林业科技, 17(4): 26-31. |
周静, 周波, 谭穗懿, 等. 2004. 麻楝叶挥发油成分的GC-MS分析[J]. 中药材, 27(11): 815-817. DOI:10.3321/j.issn:1001-4454.2004.11.011 |
周志春, 陈连庆, 黄秀凤. 2009. 马褂木菌根真菌筛选和菌根化育苗效果研究[J]. 林业科学研究, 22(2): 196-199. |
Chen B Y. 1995. Geographical distribution of Chinese Meliaceae[J]. J Trop Subtrop Bot, 3(3): 12-22. |
Ho K S, Noshiro S. 1995. Chukrasia A. H. L. Juss//Lemmens R H M J, Soerianegara I, Wong W C. Plant Resources of South-East Asia, No. 5 (2): Timber Trees: Minor Commercial Timbers. Backhuys Publishers: Leiden, 127-130.
|
Kalinganire A, Pinyopusarerk K. 2000. Chukrasia: Biology, Cultivation and Utilisation. ACIAR Technical Reports No. 49. CSIRO: Canberra, 35. https://link.springer.com/article/10.1007/s00468-014-1092-0
|
Kaur R, Arora S, Singh B. 2008. Antioxidant activity of the phenol rich fractions of leaves of Chukrasia tabularis A[J]. Juss. Bioresource Technology, 99(16): 7692-7698. DOI:10.1016/j.biortech.2008.01.070 |
Mabberley D J, Pannell C M. 1995. Meliaceae//Dassanayake M D, Fosberg F R, Clayton W D. A Reviesed Handbook to the Flora of Ceylon. Vol. Ⅸ: Published for the Smithsonian Institution and the National Science Fondation, Washington, D. C. Amerind Publishing Co Pvt Ltd: New Delhi, 229-300.
|
Mosse B. 1957. Growth and chemical composition of mycorrhizal and non-mycorrhizal apples[J]. Nature (London), 179: 992-994. |
Nagalakshmi M A H, Thangadurai D, Muralidara Rao D, et al. 2001. Phytochemical and antimicrobial study of Chukrasia tabularis leaves[J]. Fitoterapia, 72(1): 62-64. DOI:10.1016/S0367-326X(00)00245-8 |
Shi Z Y, Chen Y L, Feng G, et al. 2006. Arbuscular mycorrhizal fungi associated with the Meliaceae on Hainan Island, China[J]. Mycorrhiza, 16(2): 81-87. DOI:10.1007/s00572-005-0017-6 |
Smith F A, Smith S E. 1997. Structural diversity in (vesicular)-arbuscular mycorrhizal symbioses[J]. New Phytol, 137(3): 373-388. DOI:10.1046/j.1469-8137.1997.00848.x |
 2011, Vol. 47
2011, Vol. 47