文章信息
- 金浩, 唐丽荣, 曾巧玲, 郑新宇, 林冠烽, 黄彪
- Jin Hao, Tang Lirong, Zeng Qiaoling, Zheng Xinyu, Lin Guanfeng, Huang Biao
- 炭陶除氟吸附材料的研制
- Research on Carbon/Pottery Adsorption Composite for Removing Fluoride
- 林业科学, 2011, 47(4): 147-151.
- Scientia Silvae Sinicae, 2011, 47(4): 147-151.
-
文章历史
- 收稿日期:2009-04-30
- 修回日期:2009-07-13
-
作者相关文章
2. 漳州职业技术学院建筑工程系 漳州 363000;
3. 福建省林业科学研究院 福州 350012
2. Department of Architectural Engineering, Zhangzhou Institute of Technology Zhangzhou 363000;
3. Fujian Academy of Forestry Fuzhou 350012
氟是人体必须的微量元素,维持饮用水中氟浓度在0.5~1 mg·L-1之间对人的骨骼生长发育和预防龋齿是有益的(詹予忠等,2007)。根据世界卫生组织(WHO)的规定,人体能够接受的最高的氟化物含量为1.5 mg·L-1(WHO,1993)。如果长期饮用氟浓度高于1.5 mg·L-1的水,则会引起氟斑牙、氟骨病等(Esin et al., 2008; Mitali et al., 2006)。我国高氟水分布范围广,涉及约有27个省、市、自治区,根据全国调查报道我国约有7亿以上的人饮用含氟量超标的水,严重威胁着人体健康(马玉新,2004)。
常用的除去水中氟的方法主要有沉淀法和吸附法两大类(Srimurali et al., 1998)。钙盐沉淀法是一种简单廉价的除氟方法,但受氟化钙溶解度的影响,该方法不能达到饮用水标准,主要用于含氟较高的工业水处理(徐金兰等,2003)。此外,黏土由于含有铝盐、硅酸盐, 从而具有混凝效能, 可以与氟离子产生沉淀,从而达到去除氟的目的(江霜英等,2003)。吸附法具有出水稳定、工艺流程简单等优点,特别适合于较低浓度含氟水的处理(Ramanaiah et al., 2007; Maurice et al., 2004)。坦桑尼亚将明矾/石灰预吸附、骨炭再吸附2种吸附剂相结合,取得了很好的效果(Mjengera et al., 2003)。竹炭对氟离子有很高的选择吸附能力, 但因价格昂贵, 应用受到限制(张启伟等,2005)。近年来,国内外学者对天然矿物的除氟研究较多,比如含镧、铈、锆等稀土元素的除氟吸附剂。Kamble等(2007)研究了载镧聚合物除氟剂; David等(2002)研究了将锆负载于鳌合树脂上的除氟性能。这些除氟剂通常有较大的吸附容量,但价格较昂贵。为降低成本、提高吸附性能,采用竹屑、骨粉及膨润土三者复合,经高温炭化、活化制得炭陶除氟吸附材料。本文对除氟吸附材料的性能影响因素进行了研究。
1 材料与方法 1.1 试验材料及仪器材料:竹屑,粒径为40~80目,来自福建建瓯。钙基膨润土, 由福建省第九建筑工程公司提供。猪骨头,经碱预处理后,粉碎、过筛(60~80目)。氟化钠,优级纯,来自上海化学试剂公司。
仪器:KDPS-70型炭化炉,CIC-100型离子色谱仪,美国Thermo electro公司Nicolet 380型傅里叶红外光谱仪,JSM-5310LV型扫描电子显微镜。
1.2 试验方法将竹屑、膨润土以及骨粉按照一定的比例混合,加入少量水,经成型挤条机及造粒机,得到的直径约为0.3 cm的圆形颗粒。然后以3~20 ℃·min-1的升温速率升到5个不同的温度(500,550,600,650,700 ℃),并保温0~4 h。最后,将制得的炭陶颗粒粉碎至80~120目,水洗,烘干,用自封袋保存。以上试验重复3次。
1.3 除氟性能的测试(国家环境保护总局,2002)称取0.1 g吸附剂于锥形瓶中,加入初始氟离子浓度为5 mg·L-1、pH 7.12的氟化钠溶液50 mL,盖上瓶塞封口,放入温度为30 ℃、转速为160 r·min-1的恒温水浴中进行振荡吸附3 h。将吸附后的体系过滤,用离子色谱(型号:CIC-100)法测定滤液中氟离子浓度。以上试验重复3次。色谱条件为色谱柱, NT-SA-4A阴离子交换柱(250 mm×4.6 mm); 淋洗液为2.4 mmol·L-1 Na2CO3+1.8 mmol·L-1 NaHCO3; 流速为1.5 mL·min-1; 进样体积为20 μL。
平衡吸附容量及除氟率按下式计算:
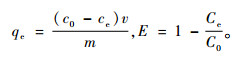
|
式中:qe为吸附平衡时单位质量吸附剂对吸附质的吸附量(mg·g-1); E为除氟率(%); C0为溶液中初始时氟离子浓度(mg·L-1); Ce为溶液中平衡时氟离子浓度(mg·L-1); v为溶液体积(L); m为吸附剂质量(g)。
1.4 炭陶样品的表征扫描电子显微镜(SEM):将炭陶样品研磨成细粉状,烘至绝干,之后用真空镀金,于JSM-5310LV型扫描电子显微镜下观察。
傅里叶转换红外光谱仪(FTIR):将炭陶样品研磨至200目(0.071 mm)。在500 mg KBr中加入1 mg的炭化物,混匀,取200 mg压片、干燥, 在美国Thermo electro公司Nicolet 380型傅里叶红外光谱仪上进行测试。
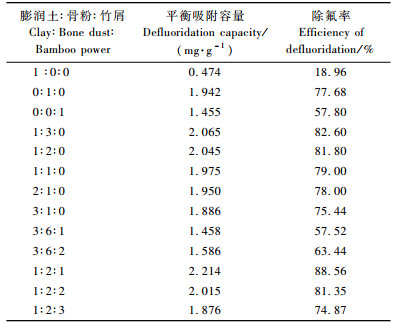
2 结果与分析 2.1 原料配比的影响研究讨论膨润土、骨粉及竹屑三者以不同比例混合后,以5 ℃·min-1的升温速率升温到600 ℃,并且保温1 h所制备炭陶除氟吸附材料的吸附性能。由表 1可知:单独处理的膨润土、骨粉、竹屑除氟吸附材料的平衡容量分别为0.474,1.942和1.455 mg·g-1,骨炭对氟离子的平衡吸附容量最大,处理的膨润土最小,随着除氟吸附材料中膨润土含量的增加,除氟吸附材料的平衡吸附容量及除氟率均下降。膨润土对氟离子的平衡吸附容量仅为0.474 mg·g-1,而骨炭对氟离子的平衡吸附容量为1.942 mg·g-1,这说明在除氟过程中,骨炭起的作用更大,所以骨炭在除氟吸附材料中的含量至关重要,随着骨炭含量的增加,其除氟效果越好。当膨润土与骨粉的比值为1:2时,除氟吸附材料的平衡吸附容量比膨润土与骨粉的比值为1:1时的平衡吸附容量增加得较多,当两者的比例增加到1:3时,其平衡吸附容量增加得并不多。另外,骨粉的增加会增加材料的成本,因此膨润土与骨粉的比例为1:2时较宜。
|
|
由表 1还可知:随着竹屑的加入,所制得的炭陶除氟吸附材料的平衡吸附容量在1.458~2.214 mg·g-1之间,均比竹炭(1.455 mg·g-1)及膨润土(0.474 mg·g-1)高。这说明膨润土与竹屑及骨粉混捏形成混合体,热处理后,竹质原料转化成竹质炭化物,体积缩小,与包裹其的陶土(膨润土受热形成)之间形成孔隙(主要为大孔),同时竹质原料及骨粉经过炭化、活化形成了活性炭和骨炭,这样活性炭、骨炭及陶土各自自身的孔隙以及三者之间在制备过程中形成的孔隙就构成了复合吸附材料中丰富的大孔、中孔、微孔体系,增大了复合材料的比表面积。另一方面,在热处理过程中膨润土中铁离子等物质进一步作用,改善了复合材料的表面化学性质,提高了复合材料的化学吸附能力,这样体系中产生物理吸附与化学吸附的协同效应,达到了增大炭陶材料吸附能力的目的(黄彪等,2007)。
另外,从表 1还可知:随着竹屑含量的增加,所制得的炭陶除氟吸附材料的平衡吸附容量出现先增加后减少的趋势。这是由于竹屑经炭化、活化得到的竹炭对氟离子也具有较好的吸附效果,其平衡吸附容量为1.455 mg·g-1。随着竹屑的增加,炭陶除氟吸附材料的平衡吸附容量也增加, 当三者的比例为1:2:1时达到较高值。但竹屑含量过多,当炭陶样品总量不变时,骨粉就减少,而骨炭在除氟吸附材料中的含量至关重要,骨粉减少导致炭陶除氟吸附材料的平衡吸附容量的减少量比竹屑增加导致炭陶除氟吸附材料的平衡吸附容量的增加量要大,所以炭陶除氟吸附材料的平衡吸附容量出现减少的趋势。
综上所述,三者(膨润土、骨粉及竹屑)的比例为1:2:1时,制备得到的炭陶除氟吸附材料的吸附效果最佳。此时,平衡吸附容量为2.214 mg·g-1,除氟率为88.56%。
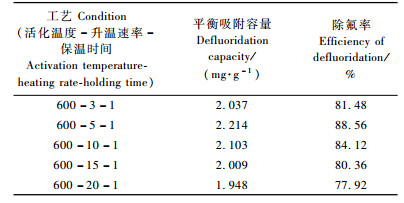
2.2 升温速率的影响以3,5,10,15,20 ℃·min-1的升温速率升温到600 ℃,并保温1 h,制备炭陶除氟吸附材料,其中膨润土、骨粉及竹屑的比例为1:2:1。由表 2可知:随着升温速率的增加,炭陶除氟材料的平衡吸附容量及除氟率均出现先增加后减小的趋势。升温速率太慢,在各温度段停留时间较长,炭陶中的骨炭及竹炭的部分微孔烧失成中孔或大孔,吸附性能减弱,除氟能力下降; 升温速率过快,炭陶中的骨炭及竹炭活化不够充分,除氟效果也不好。鉴于此,升温速率选择5 ℃·min-1为宜。此时,炭陶除氟吸附材料的平衡吸附容量及除氟率分别为2.214 mg·g-1和88.56%。
|
|
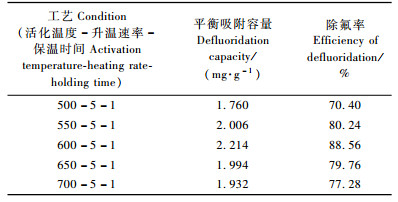
以5 ℃·min-1的升温速率升温到500,550,600,650,700 ℃,并保温1 h,制备炭陶除氟吸附材料,其中膨润土、骨粉及竹屑的比例为1:2:1。由表 3可知:随着温度的上升,炭陶除氟吸附材料的吸附容量及除氟率均出现先增大后减少的趋势。活化温度过低,堵塞在骨炭及竹炭孔结构中的杂质不易分解,影响两者孔隙结构的提高,导致除氟效果不佳。温度过高,骨炭表面烧失严重,基本上变成白色,导致表面致密,严重影响了炭陶的除氟性能。因此,选活化温度为600 ℃比较适宜。
|
|
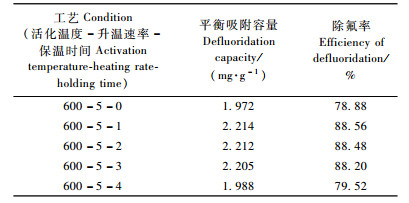
以5 ℃·min-1的升温速率升温到600 ℃,并保温0,1,2,3,4 h,制备炭陶除氟吸附材料,其中膨润土、骨粉及竹屑的比例为1:2:1。由表 4可知:炭陶除氟吸附材料的吸附容量及除氟率均随着保温时间的延长总体上呈现先升后降的趋势。保温时间较短,活化不够充分,影响了炭陶中骨炭及竹炭孔隙结构的形成,因而炭陶除氟吸附材料的吸附效果较低。保温时间过长,炭陶复合材料中固相之间的反应程度增加,导致骨炭、竹炭及黏土表面官能团发生变化,形成了一些不利于除氟的结构,严重影响了炭陶除氟吸附材料对氟的吸附。通过以上分析,选保温时间为1 h为宜。
|
|
采用日本JSM-5310LV型扫描电子显微镜观察炭陶除氟吸附材料的表面微观形貌。图 1, 2和3分别示出了在升温速率为5 ℃·min-1、温度为600 ℃、保温时间为1 h的工艺条件下,制得的竹炭、骨炭及炭陶除氟吸附材料的SEM图。

|
图 1 竹炭的SEM观察 Figure 1 The observation of SEM on bamboo char |

|
图 2 骨炭的SEM观察 Figure 2 The observation of SEM on bone char |

|
图 3 炭陶的SEM观察 Figure 3 The observation of SEM on carbon/pottery composite |
由图 1,2和3可知:膨润土、骨粉及竹屑经催化活化后能较好地有机结合在一起,形成炭陶复合吸附材料。膨润土及骨粉在活化焙烧后存在大量的孔隙结构,因此其并没有对竹炭的孔隙结构起到堵塞作用,并且还能在一定程度上为氟离子进入竹炭的孔隙结构中提供良好的通道作用。另外,骨炭由于本身具有大量的孔隙结构,对氟离子也具有一定的吸附作用,使得炭陶除氟吸附材料的比表面积更大,孔隙结构更加发达,对氟离子的吸附性能有所提高。
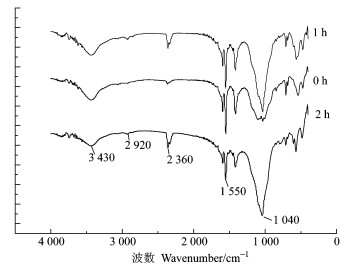
2.6 傅里叶转换红外光谱仪扫描分析采用Thermo electro公司Nicolet 380型傅里叶转换红外光谱仪进行扫描,对炭陶除氟吸附材料的表面官能团进行剖析。图 4示出了升温速率为5 ℃·min-1、600 ℃下分别保温0,1和2 h的炭陶除氟吸附材料的红外光谱图。表 5示出了炭陶红外光谱吸收带的位置和吸收峰强度(吴平霄,2004)。
|
图 4 不同保温时间炭陶的红外光谱 Figure 4 The FTIR of carbon/pottery composite with different holding time |
|
|
由图 4及表 5可知:在不同的保温条件下,除了在2 360 cm-1处骨炭中P—OH伸缩振动或黏土中Si—OH伸缩振动的吸收强度以及在1 040 cm-1处黏土中Si—O伸缩振动或活性炭中C—O弯曲振动的吸收强度及峰宽不同外,其他各个吸收峰对应的波数和吸收强度基本相同。一般认为,骨粉在高温下能形成大量的磷酸磷灰石和羟基磷灰石的分子结构,具有较多的P—OH基团,所以在2 360 cm-1处,随着保温时间的延长,其峰的吸收强度增加。当活化时间达到一定程度后,形成的P—OH基团趋于稳定,所以在保温时间为1和2 h时,其峰的吸收强度基本相同。保温时间为0时,由于活化时间过短,活化不够充分,竹炭中形成的C—O键较少,故在1 040 cm-1处吸收峰较宽,吸收强度弱。随着活化时间的延长,活化更加充分,形成的C—O键较多,吸收峰变窄,吸收强度增加。
3 结论1) 制备炭陶除氟吸附材料的工艺中,升温速率、活化温度及保温时间均对其平衡吸附容量产生了一定的影响。
2) 最佳产品的平衡吸附容量为2.214 mg·g-1,除氟率为88.56%。
3) 由竹炭、骨炭及炭陶的SEM可知:黏土、骨粉及竹屑在活化焙烧的过程中,能较好地有机结合在一起形成复合材料。该材料具有较发达的孔隙结构,对氟离子有一定的除去作用。由FTIR可知:活化温度越高,越有利于骨炭中P—OH键或黏土中的Si—OH键的形成,这对加大材料的除氟效果起到了积极作用。
4) 采用竹屑、骨粉及膨润土制备的炭陶除氟吸附材料,具有较高的吸附容量,成本较低,除氟工艺简单等特点,是一种比较理想的除氟剂。
国家环境保护总局. 2002. 水与废水分析监测方法[M]. 4版.北京: 中国环境科学出版社.
|
黄彪, 林冠烽, 陈学榕, 等. 2007. 新型炭陶复合吸附材料制备方法[J]. 中国国家发明专利: 200710008525.X. |
江霜英, 高廷耀. 2003. 粘土对水中氟离子吸附去除机理的研究[J]. 化工环保, 23(4): 204-208. |
马玉新. 2004. 膨润土系列除氟剂的制备及其除氟性能的研究[J]. 中国海洋大学硕士学位论文. |
吴平霄. 2004. 黏土矿物材料与环境修复[M]. 北京: 化学工业出版社.
|
徐金兰, 王玉泉, 王志盈, 等. 2003. 石灰沉淀-混凝沉淀处理含氟废水的实验[J]. 水处理技术, 29(5): 282-285. |
张启伟, 王桂仙. 2005. 竹炭对饮用水中氟离子的吸附条件研究[J]. 广东微量元素科学, 12(3): 63-66. |
詹予忠, 李玲玲, 李浩, 等. 2007. 制备条件对硅胶负载氧化锆吸附除氟的影响[J]. 环境科学与管理, 32(5): 83-85. |
David A, Pacheco T, Sunamani K, et al. 2002. Adsorption of fluoride ion on the zirconium(Ⅳ) complexes of the chelating resins functionalized with amine-N-acetate ligands[J]. Separation Science and Technology, 37(4): 877-894. DOI:10.1081/SS-120002221 |
Esin A, Esengul K, Lutfi O. 2008. Plasma modification of the anion-exchange membrane and its influence on fluoride removal from water[J]. Separation Purification Technology, 6(1): 455-460. |
Kamble S P, Jagtap S, Labhsetwar N K, et al. 2007. Defluori-dation of drinkingwater usingchitin, chitosan and lanthanum-modified chitosan[J]. Chemical Engineering Journal, 129(1/3): 173-180. |
Maurice S O, Yoshihiro K, Ochieng A, et al. 2004. Adsorption equilibrium modeling and solution chemistry dependence of fluoride removal from water by trivalent-cation-exchanged zeolite F-9[J]. Journal of Colloid and Interface Science, 27(9): 341-350. |
Mitali S, Aparna B, Partha P P, et al. 2006. Use of laterite for the removal of fluoride from contaminated drinking water[J]. Journal of Colloid and Interface Science, 30(2): 432-441. |
Mjengera H, Mkongo G. 2003. Appropriate deflouridation technology for use in flourotic areas in Tanzani[J]. Physics and Chemistry of the Earth, 28(20/27): 1097-1104. |
Ramanaiah S V, Venkata M S, Sarma P N. 2007. Adsorptive removal of fluoride from aqueous phaseusing waste fungus (Pleurotus ostreatus 1804)biosorb ent: Kinetics evaluation[J]. Ecological engineering, 31(2): 47-56. |
Srimurali M, Pragathi A, Karthikeyan J. 1998. A study on removal of fluorides from drinking water by adsorption onto low-cost materials[J]. Environmental Pollution, 99(2): 285-289. DOI:10.1016/S0269-7491(97)00129-2 |
World Health Organization(WHO).1993.Guidelines for drinking water quality.World Health Organization(WHO), Geneva.
|
 2011, Vol. 47
2011, Vol. 47