文章信息
- 陈亚琪, 康海权, 陈秋平, 沈建福
- Chen Yaqi, Kang Haiquan, Chen Qiuping, Shen Jianfu
- 油茶蒲提取物的抗氧化活性
- Antioxidant Activity of Extracts from the Fruit Shell of Camellia oleifera
- 林业科学, 2011, 47(3): 20-24.
- Scientia Silvae Sinicae, 2011, 47(3): 20-24.
-
文章历史
- 收稿日期:2009-10-08
- 修回日期:2009-12-19
-
作者相关文章
油茶(Camellia oleifera)属于山茶科(Theaceae)、山茶属(Camellia)植物,是我国特有的木本油料树种,有几千年的栽培历史。目前全国油茶林约为400万hm2,主要分布在湖南、江西、广西、浙江、福建、安徽和贵州等南方省、自治区(马力,2007)。据中药大辞典记载,茶油、油茶籽、油茶叶、茶籽饼、茶子木花以及油茶根皮等都具有一定的生物活性。中国药典将茶油收载入药,而目前对油茶蒲活性成分和生理功能的研究较少。油茶蒲即油茶果最外层,是油茶加工的副产物,含有大量的木质素、多缩戊糖、蛋白质和皂素等化学成分,可以用来生产栲胶、糠醛、木糖醇、活性炭等(马力,2007; 贺桂先等,2007),但多以废弃物焚烧处理。林生深等(1997)首次报道采用丙酮-水体系提取油茶蒲中的抗氧化剂,发现其抗氧化成分主要为没食子酸和儿茶素类,并采用POV法对其抗氧化性进行研究。陈跃龙等(2008)建立油茶蒲中多酚的富集工艺,采用60%丙酮-水提取、乙酸乙酯萃取、流经D101型大孔吸附树脂、用30%乙醇洗脱,多酚的含量可达45%。本研究以油茶蒲粗提物为原料,采用乙酸乙酯和正丁醇对其进行分级萃取,比较各相的总酚含量及抗氧化活性,并对两者间的相关性进行分析,从而为油茶蒲提取物在抗氧化方面的应用奠定基础。
1 材料与方法 1.1 试验材料油茶蒲:品种为普通白花油茶,取自浙江省常山县芳村镇。
1.2 试剂与仪器1,1-二苯基-2-苦基苯肼(DPPH,1,1-Diphenyl-2-picrylhydrazyl),2,2-吖嗪双(3-乙基-7-苯并噻唑啉磺酸)二铵盐[ABTS,2,2,-Azino-bis (3-ethylbenzothiazoline-6-sulfonic acid) diammonium salt) ],三吡啶三吖嗪(TPTZ,2,4,6-Tri(2-pyridyl)-s-triazine),水溶性维生素E (Trolox,6-Hydroxy-2,5,7,8-tetrame hylchroman-2-carboxylic acid)购自Sigma公司; FolinCiocalteu试剂购于北京鼎国生物技术有限责任公司; 全血体系总抗氧化能力(T-AOC法)测定试剂盒购于南京建成生物工程研究所; 其余试剂均为国产分析纯。
TU-1810紫外可见分光光度计(北京普析通用仪器有限责任公司); RE-52AAA旋转蒸发器(上海嘉鹏科技有限公司); SHB-ⅢA循环水式多用真空泵(上海豫康科教仪器设备有限公司); HH-4数显恒温水浴锅(国华电器有限公司); BS124S万分之一天平(Sartorius公司)。
1.3 试验方法 1.3.1 油茶蒲粗提物的制备油茶蒲经挑选后热风干燥,用50%的乙醇溶液,以料液比1:5热回流提取2次,喷雾干燥,即得到油茶蒲粗提物。
1.3.2 油茶蒲粗提物的分级萃取称取一定量的油茶蒲粗提物,用水配制成悬浮液。依次用等体积的乙酸乙酯和正丁醇分别萃取2次。将乙酸乙酯相、正丁醇相及水相旋转蒸发至干粉,称重并计算获得率。
1.3.3 油茶蒲粗提物及分级萃取各相总酚含量的测定总酚含量的测定采用Folin-Ciocalteau法(Singleton et al., 1965; 张海晖等,2008)。在10 mL容量瓶中分别加入0,0.1,0.2,0.3,0.4,0.5,0.6 mL 0.1mg·mL-1的没食子酸标准溶液,加入1.0 mL Folin-Ciocalteu试剂,加入2 mL 15%的Na2CO3溶液,用蒸馏水定容至10 mL,充分混合后,室温放置2 h,于760 nm波长下测定吸光值A760,得到线性回归方程y=14.174x+0.047 4 (其中x为没食子酸含量mg,y为吸光度),R2=0.998 2。将油茶蒲粗提物及分级萃取各相配制成1 mg·mL-1的待测液; 取0.1 mL的待测液,按上述步骤测定A760,根据标准曲线计算总酚含量。
1.3.4 油茶蒲粗提物及分级萃取各相抗氧化活性的测定DPPH法(Yuan et al., 2008) :将油茶蒲粗提物及分级萃取各相配制成不同的浓度梯度(25.0,20.0,15.0,10.0,5.0和2.5 μg·mL-1),各取1.0 mL上述浓度的样品溶液于试管中,再加入3.0 mL质量浓度为0.04 g·L-1的DPPH·溶液,混合均匀,避光反应30 min后,在517 nm处测吸光值为Ai,根据不同浓度样品溶液对DPPH·的清除率作图。
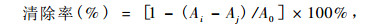
|
其中:A0为未加样品时的吸光值,Ai为加入样品后的吸光值,Aj为样品溶液的吸光值。
TEAC法Re等(1999)的方法上稍作修改,用去离子水将ABTS溶解,使其浓度为7 mmol·L-1,加入K2S2O8,使其浓度为2.45 mmol·L-1,将该溶液在室温下置于暗处过夜(12~16 h)。将生成的ABTS·+溶液用磷酸缓冲液(PBS)稀释,使其在30 ℃,734 nm波长下的吸光度为0.70 ± 0.02,即得到ABTS·+工作液。将油茶蒲粗提物及分级萃取各相配制成不同的浓度梯度(16.0,14.0,12.0,10.0,8.0,6.0,4.0和2.0 μg·mL-1),在试管中加入1.0 mL的样品溶液,再加入3.0 ml的ABTS·+工作液,混合,30 ℃静置6 min,在734 nm处测吸光值为Ai。根据不同浓度样品溶液对ABTS·+的清除率作图。

|
其中:A0未加样品时的吸光值; Ai为加入样品后溶液的吸光值; Aj为样品溶液的吸光值。
FRAP法在Benzie等(1996)的方法上稍作修改,将油茶蒲粗提物及分级萃取各相配制成不同的浓度梯度(30.0,25.0,20.0,15.0,10.0和5.0 μg·mL-1),取1.0 mL样品溶液加入到3.0 mL工作液(10 mmoL· L-1 TPTZ,20 mmol· L-1 FeCl3,0.3 moL·L-1醋酸缓冲液以1:1:10的比例混合,预热至37 ℃备用)中,摇匀后于37 ℃水浴中静置10 min,593 nm波长处测定其吸光值。另以0.02,0.04,0.06,0.08,0.10,0.12和0.14 mmol·L-1 FeSO4的标准溶液代替待测样品作标准曲线,样品的抗氧化活性以达到同样吸光度值所需的FeSO4毫摩尔数表示。
T-AOC法:使用T-AOC测定试剂盒,按照说明进行操作。
2 结果与分析 2.1 油茶蒲粗提物及分级萃取各相的总酚含量乙酸乙酯相、正丁醇相及水相的获得率分别为7.8%,25.3%和61.3%。油茶蒲粗提物及分级萃取各相的总酚含量如图 1所示,由高到低为:乙酸乙酯相>正丁醇相>粗提物>水相。

|
图 1 油茶蒲粗提取及分级萃取各相的总酚含量 Figure 1 The polyphenol contents in crude extract and its three fractions of the fruit shell of C. oleifera |
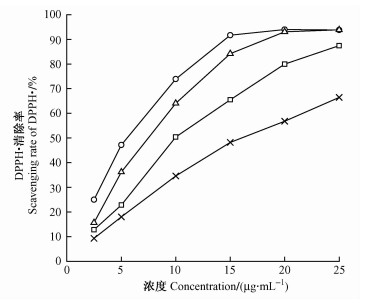
DPPH·是一种很稳定的以氮为中心的自由基,它的稳定性主要来自共振稳定作用及3个苯环的空间障碍,而使夹在其中间氮原子上的不成对电子不能发挥其应有的电子成对作用(刘丽香等,2008)。DPPH·乙醇溶液呈紫色。自由基清除剂可与其单电子配对,将溶液还原为浅黄色。该法被广泛应用于评价植物提取物的体外抗氧化活性。由图 2可知:油茶蒲粗提物及分级萃取各相的DPPH自由基清除能力有显著差异,清除能力由高到低依次为乙酸乙酯相、正丁醇相、粗提物和水相。粗提物及分级萃取各相的IC50 (清除率达50%所需的浓度)分别为4.9,6.3,9.1和15.7 μg·mL-1,分别为阳性对照Vc的1.3,1.7,2.4和4.1倍。
|
图 2 油茶蒲粗提物及分级萃取各相对DPPH·的清除作用 Figure 2 Scavenging rate of DPPH· in crude extract and its three fractions of the fruit shell of C. oleifera
 粗提物 Crude extract 粗提物 Crude extract  乙酸乙酷相 Ethyl acetate fraction 乙酸乙酷相 Ethyl acetate fraction  正丁醇相 Butanol fraction 正丁醇相 Butanol fraction  水相 Water fraction 水相 Water fraction 下同。 The same below. |
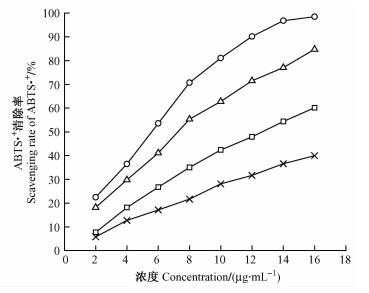
ABTS·+也是一种较为稳定的自由基,呈蓝绿色。当有自由基清除剂存在时,ABTS·+的单电子被配对生成无色的ABTS,从而使溶液的颜色变浅。由图 3可知:油茶蒲粗提物及分级萃取各相的ABTS·+自由基清除能力差异显著。清除能力由高到低依次为乙酸乙酯相、正丁醇相、粗提物和水相。粗提物及分级萃取各相的IC50 (清除率达50%所需的浓度)分别为4.5,6.5,12.4和18.2 μg·mL-1,分别为阳性对照Vc的0.8,1.2,2.3和3.3倍。
|
图 3 油茶蒲粗提物及分级萃取各相对ABTS·+的清除作用 Figure 3 Scavenging rate of ABTS·+ in crude extract and its three fractions of the fruit shell of C. oleifera |
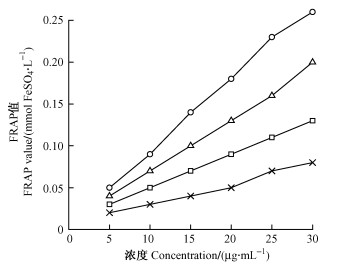
在较低的pH条件下,TPTZ-Fe3+可被样品中的还原物质还原为TPTZ-Fe2+,呈现出明显的蓝色,在593 nm下吸收值最大。根据吸光度的大小计算试样抗氧化活性的强弱,测定结果用FRAP值(FeSO4当量)表示,数值越大,抗氧化能力越强。由图 4可知:油茶蒲粗提物及分级萃取各相的FRAP值有显著差异。清除能力由高到低依次为乙酸乙酯相、正丁醇相、粗提物和水相。在10 μg·mL-1的浓度下,FeSO4当量分别0.09,0.07,0.05和0.03 mmol·L-1,相同浓度下,阳性对照Vc的FeSO4当量为0.13 mmol·L-1。
|
图 4 FRAP法测定的油茶蒲粗提物及分级萃取各相的FRAP值 Figure 4 FRAP value in crude extract and its three fractions of the fruit shell of C. oleifera |
该方法是利用抗氧化物质能使Fe3+还原成Fe2+,后者可与菲琳类物质形成稳定的络合物的性质,从而可以通过比色法测定受试样品在全血体系中抗氧化能力的强弱。以全血总抗氧化能力(TAC)表示,数值越大,抗氧化能力越强。由图 5可知:在样品浓度为0.5 mg·mL-1时,油茶蒲粗提物及分级萃取各相全血体系总抗氧化能力由高到低依次为乙酸乙酯相、正丁醇相、粗提物和水相。其TAC值分别为39.62,19.03,16.95和9.66 U·mL-1。相同浓度下,阳性对照Vc的TAC值为134.31 U·mL-1。

|
图 5 油茶蒲粗提物及分级萃取各相的全血体系总抗氧化能力 Figure 5 T-AOC in crude extract and its three fractions of the fruit shell of C. oleifera |
如图 6所示:总酚含量与抗氧化活性间存在着一定的正相关性,总酚含量越高,提取物的抗氧化活性越强。其中FRAP法的测定结果与总酚含量间的相关系数达到0.988 0。其他方法的相关系数也达到0.8以上。可以推测多酚类物质可能是油茶蒲提取物抗氧化的主要成分。

|
图 6 油茶蒲粗提物及分级萃取各相总酚含量与其抗氧化能力的相关性曲线 Figure 6 The correlation between content of polyphenol and the antioxidant activity in crude extract and its three fractions of the fruit shell of C. oleifera |
1) 本文使用4种不同的体外抗氧化体系,比较了油茶蒲粗提物及分级萃取各相的体外抗氧化活性,4种方法测定的结果一致,表明各抗氧化体系的测定结果间存在一定的相关性和可靠性。
2) 油茶蒲粗提物及分级萃取各相抗氧化能力强弱依次为:乙酸乙酯相>正丁醇相>粗提物>水相,其中乙酸乙酯相在清除DPPH·,ABTS·+等能力方面具有很强的抗氧化活性,其清除效果与Vc相当。该结果表明:具有极性梯度的液-液萃取方法可以使油茶蒲提取物中的抗氧化成分按极性有效分离,且抗氧化成分主要集中在极性较弱的乙酸乙酯相中,而极性较强的水相抗氧化活性很弱。
3) 多酚类化合物作为一类具有多元酚结构的植物次生代谢产物,在食品、医药和化妆品等领域应用广泛,具有抗氧化和抗心血管疾病、抑菌消炎和抗病毒、抗癌、抗老化和防晒等多种生物活性(赵扬帆等,2006)。抗氧化性是其最重要的一种生物活性,这与多酚类化合物的结构有密切的联系。其酚羟基结构(邻苯二酚或邻苯三酚)中的邻位酚羟基很容易被氧化成醌类结构,消耗环境中的氧,同时对活性氧等自由基具有很强的捕捉能力,反应如下:PH(多酚)+ROO·(脂质自由基) → P·+ROOH (张力平等,2005)。目前,许多研究均表明植物提取物和食品中的多酚含量与其抗氧化性密切相关。张泽生等(2009)对山竹(Yushania)果皮中的抗氧化物质进行研究,正丁醇相表现出较强的抗氧化活性,且该相中的总酚含量也较其他相高。王志远等(2007)对8种水果的抗氧化活性与多酚含量进行测定,结果表明两者之间存在正相关性。此外,研究表明不同品种黄酒(陈金娥等,2008)、蜂蜜(曹炜等,2005)、桑葚(Celtis sinesis) (李升锋等,2008)、黑大豆种皮(徐金瑞等,2006)等的抗氧化活性均与其多酚的含量呈正相关性。因此,对油茶蒲中的多酚类物质进行分离和鉴定,了解其抗氧化的有效成分,从而为以油茶蒲为原料的药物和功能性食品的开发提供理论基础,很具有实际意义。
曹炜, 陈卫军, 宋纪蓉. 2005. 不同种类蜂蜜总酚酸含量测定和抗氧化作用的研究[J]. 食品科学, 26(1): 48-51. |
陈金娥, 高虹. 2008. 不同品种黄酒中多酚含量及抗氧化性研究[J]. 酿酒科技, 4: 37-41. |
陈跃龙, 唐玲, 李红冰, 等. 2008. 油茶果皮多元酚富集工艺研究[J]. 时珍国医国药, 19(6): 1369-1370. |
贺桂先, 李林松, 徐林初, 等. 2007. 油茶的生长特性及其功能价值[J]. 江西林业科技, 4: 39-42. DOI:10.3969/j.issn.1006-2505.2007.04.013 |
李升锋, 徐玉娟, 廖森泰, 等. 2008. 不同品种桑椹抗氧化能力及其与Vc、花色苷和总酚含量的关系[J]. 食品研究与开发, 29(4): 31-34. |
林生深, 张晋, 张红, 等. 1997. 从油茶果壳中提取天然抗氧化剂的研究[J]. 广东工业大学学报, 14(2): 43-48. |
刘丽香, 梁兴飞, 孙怡, 等. 2008. 苦丁茶提取物多酚含量与抗氧化活性的测定[J]. 茶叶科学, 28(4): 289-293. |
马力. 2007. 油茶籽的综合开发利用[J]. 中国食品添加剂, 3: 126-129. DOI:10.3969/j.issn.1006-2513.2007.01.029 |
王志远, 李清彪, 杨翠娴, 等. 2007. 八种水果中的多酚含量及其抗氧化性[J]. 天然产物研究与开发, 19: 1040-1043. DOI:10.3969/j.issn.1001-6880.2007.06.030 |
徐金瑞, 张名位, 刘兴华, 等. 2006. 黑大豆种皮抗氧化能力及其与总酚和花色苷含量的关系[J]. 中国农业科学, 39(8): 1545-1552. |
张海晖, 段玉清, 倪燕, 等. 2008. 谷物中多酚类化合物提取方法及抗氧化效果研究[J]. 中国粮油学报, 23(6): 107-111. |
张力平, 孙长霞, 李俊清, 等. 2005. 植物多酚的研究现状及发展前景[J]. 林业科学, 41(6): 157-162. DOI:10.11707/j.1001-7488.20050627 |
张泽生, 赵璐, 牟浩, 等. 2009. 山竹果皮中抗氧化活性物质的提取分离[J]. 食品研究与开发, 30(6): 11-14. |
赵扬帆, 郑宝东. 2006. 植物多酚类物质及其功能学研究进展[J]. 福建轻纺, 11: 107-110. DOI:10.3969/j.issn.1007-550X.2006.11.028 |
Benzie I F, Strain J J. 1996. The ferric reducing ability of plasma (FRAP) as a measure of "antioxidant power": the FRAP assay[J]. Journal of Analytical Biochemistry, 239(1): 70-76. DOI:10.1006/abio.1996.0292 |
Re R, Pellegrini N, Proteggente A, et al. 1999. Antioxidant activity applying an improved ABTS radical cation decolorization assay[J]. Free Radical Biology and Medicine, 26(9/10): 1231-1237. |
Singleton, V L, Rossi, J A. 1965. Colorimetry of total phenolics with phosphomolybdic-phosphotungstic acid reagent American Journal of Enology and Viticulture, 16(3):144-158.
|
Yuan J F, Zhang Z Q, Fan Z C, et al. 2008. Antioxidant effects and cytotoxicity of three purified polysaccharides from Ligusticum chuanxiong Hort[J]. Carbohydrate Polymers, 74: 822-827. DOI:10.1016/j.carbpol.2008.04.040 |
 2011, Vol. 47
2011, Vol. 47

