文章信息
- 李仁洪, 胡庭兴, 涂利华, 刘闯, 雒守华, 向元彬, 戴洪忠, 谢财永
- Li Renhong, Hu Tingxing, Tu Lihua, Liu Chuang, Luo Shouhua, Xiang Yuanbing, Dai Hongzhong, Xie Caiyong
- 华西雨屏区慈竹林凋落叶分解过程养分释放对模拟氮沉降的响应
- Nutrient Release in Decomposition of Leaf Litter in Neosinocalamus affinis Stands in Response to Simulated Nitrogen Deposition in Rainy Area of Western China
- 林业科学, 2010, 46(8): 8-14.
- Scientia Silvae Sinicae, 2010, 46(8): 8-14.
-
文章历史
- 收稿日期:2009-09-06
- 修回日期:2010-02-17
-
作者相关文章
2. 四川省林业调查规划院 成都 610081;
3. 四川省林木种苗站 成都 610081
2. Sichuan Forestry Inventory and Plan Institute Chengdu 610081;
3. Sichuan Forest Tree Seeds and Seedlings Service Chengdu 610081
近几十年来,由于矿物燃料燃烧、含氮(N)化肥的生产和使用、人口增长和畜牧业发展等原因,人类向大气中排放的含氮化合物越来越多,大气氮沉降成比例增加(Vitousek et al., 1997; 莫江明等, 2004),而且这种趋势在未来数十年内还将持续下去(Galloway et al., 2004)。目前中国已成为继欧洲、美国之后的全球第三大氮沉降集中区(Zheng et al., 2002)。氮沉降的增加已造成河口、海口和江湖等水域氮富集和陆地生态系统氮超负荷,并引起一系列严重的生态问题,如影响森林植物生长、组成和多样性等,最终导致森林衰退(李德军等,2003)。凋落物分解及其养分释放是森林生态系统物质循环和能量流动的关键性过程,在高量并持续增加的全球氮沉降背景下,研究该过程对氮沉降的响应具有重要的理论和现实意义。氮沉降影响了森林凋落物中的营养元素和次生物质含量,并且影响着凋落物分解的化学过程,因此影响着凋落物的分解(莫江明等,2004)。有研究认为氮沉降对凋落物分解具有促进(Kuperman et al., 1999; 项文化等,2005; 樊后保等,2008)、抑制(Magill et al., 2000; 宋学贵等,2007)和无影响(Hobbie et al., 2004)3种作用,进而影响凋落物的养分释放。目前,氮沉降相关研究主要集中在针阔叶林生态系统,而氮沉降对竹林生态系统凋落物养分释放影响的研究尚未见报道。
慈竹(Neosinocalamus affinis)在我国竹林中占有很大的比重,也是近年退耕还林工程经营的主要竹种之一,在长江中上游生态屏障建设及区域经济发展中具有重要作用。华西雨屏区由于其特殊的地理位置和气候条件,年氮湿沉降量达到了82.4~147.5 kg·hm-2(涂利华等,2009; 李仁洪等,2009),超出该地区的临界负荷值,并有逐渐增加的趋势。本文研究了华西雨屏区慈竹林凋落叶养分释放对氮沉降的响应,以期为评估未来大气氮沉降增加对该区域竹林生态系统物质循环的影响提供参考,并为竹林生态系统可持续发展和科学管理提供基础数据。
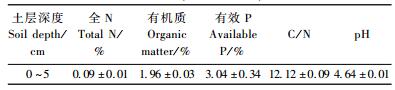
1 材料与方法 1.1 试验地概况试验地位于四川省雅安市青衣江流域二级阶地后缘老板山中部的四川农业大学林业试验站内(30°08′ N,103°00′ E),海拔660 m。该地属中亚热带湿润气候,年均气温16.1 ℃,≥10 ℃积温5 231 ℃,年均无霜期298天,年均日照时数1 019.9 h,全年太阳辐射总量为3 640.13 MJ·cm-2。该区处于“华西雨屏”的中心地带,是四川省多雨中心区之一, 年均降雨量1 772.2 mm,云雾多,相对湿度大。土壤系白垩纪灌口组紫色砂页岩风化的坡堆积物形成的紫色土,土层厚度>40 cm。本研究在施氮处理前取慈竹林土壤混合样,测定其土壤初始化学性质(表 1)。
|
|
试验地慈竹林栽植于1989年11月,面积1.5 hm2,平均密度为750丛·hm-2,平均胸径5.9 cm,平均高13.2 m。竹林郁闭度>95%,林下几乎无植被,凋落物层厚1~3 cm。2007年12月林地内现存凋落物蓄积量为13 747.5 kg·hm-2,叶、枝和箨分别占59.00%,36.76%和4.24%。
1.2 研究方法 1.2.1 试验设计2007年11月,在慈竹林中建立12个3 m×3 m样方,每个样方之间距离>3 m,以防止相互干扰; 参照国内外野外模拟氮沉降梯度(莫江明等,2004; 樊后保等,2008; 宋学贵等,2007; Magill et al., 2000)和本研究区的氮沉降现状,将12个样方分属4个处理组,分别为对照(CK,0 kg·hm-2 a-1)、低氮(LN,50 kg·hm-2 a-1)、中氮(MN,150 kg·hm-2 a-1)、高氮(HN,300 kg·hm-2 a-1)(不包括大气氮沉降量),每处理3个重复。在2007年5—6月凋落高峰期收集凋落叶,风干,称取10.0 g装入25 cm×25 cm尼龙网分解袋中(上、下表面孔径均为1 mm×1 mm)。2007年12月1日,将凋落叶分解袋放置于12个样方土壤表面,让凋落叶自然分解。每月月初和月中将NH4NO3溶解于1 L自来水中,用喷壶均匀地喷施于各样方中,增加的年降水量相当于2.67 mm; 对照样方则喷施等量的水。除施氮处理外,各样方的其他处理均保持一致。
1.2.2 样品收集及测定凋落叶分解袋于2008年1,3,5,7,9和11月底取样,对应的分解时间分别为2,4,6,8,10和12个月。每次每样方随机取样2袋,除去根系、土壤等杂质,在65 ℃下烘至恒量,磨碎,过2 mm筛,供养分含量测定。参照中华人民共和国林业行业标准(1999),用5 mL H2SO4-HClO4(10:1)消煮约0.5 g凋落叶,消煮后用蒸馏水将消煮液全部洗入100 mL容量瓶中,定容,作为测定全N,全P,全K,Ca,Mg的消煮待测液。靛酚蓝比色法测定全N; 钼锑抗比色法测定全P; 原子吸收光谱法测定全K,Ca,Mg; 外加热重铬酸钾容量法测定全C。
1.2.3 数据处理养分残留率(R) = (Ct ×Mt) / (C0 ×M0) ×100%,式中Ct为t时刻凋落叶养分含量(g·kg-1 ),Mt为t时刻凋落叶干质量(kg),C0为初始养分含量(g·kg-1),M0为初始干质量(kg)。用改进的Olson负指数衰减模型y=ae-kt对凋落叶养分残留率进行拟合,y为养分残留率(%),a为拟合参数,k为分解系数(kg·kg-1 a-1),t为时间(a)。利用SPSS 13.0软件进行One-way ANOVA分析,用LSD法进行多重比较,以确定各处理凋落叶分解过程中养分含量、养分残留率间的差异显著性。
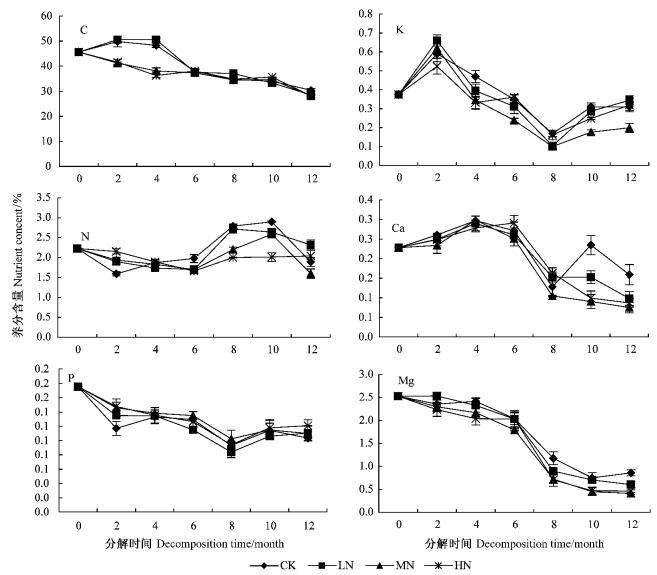
2 结果与分析 2.1 慈竹凋落叶养分含量对氮沉降的响应由图 1可知,分解初期,CK,LN处理C元素含量上升,随后下降,而MN,HN处理则一直单调下降,总体来看各处理C元素含量呈下降趋势。各处理其他元素含量变化趋势如下: N元素经历下降—上升—下降变化过程; P元素变化情况比较复杂,但总体上呈下降趋势; K元素变化表现为上升—下降—上升; Ca元素初期小幅上升,随后下降; Mg元素变化则为单调下降,后期趋于平缓。
|
图 1 凋落叶分解过程中养分含量变化动态 Figure 1 Dynamics of nutrient concents in the leaf decomposition process |
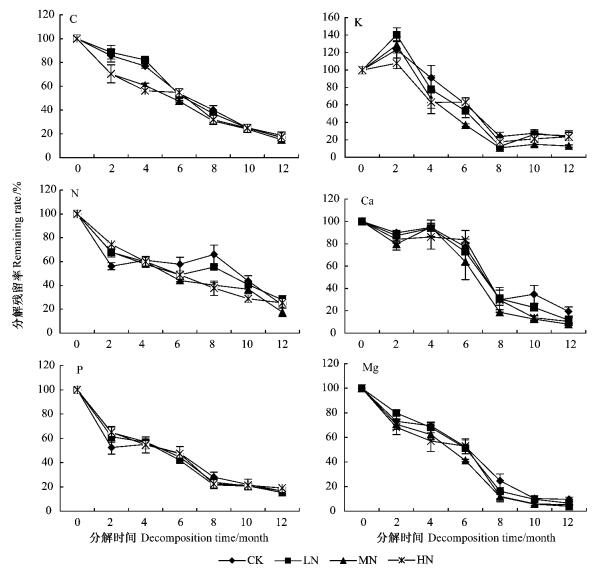
经过对凋落叶分解12个月的测定,由图 2可以看出,各处理C,P,Mg元素均直接释放,其中分解前4个月MN,HN处理C元素释放速率较大,这主要是由于MN,HN处理高量氮加速了凋落叶的快速分解。N,K,Ca各处理释放模式如下:除CK处理在分解4个月, 8个月时,LN在分解8个月时N元素富集外,各处理其他时期均释放; K元素在分解前2个月有1个明显富集过程,3~8个月释放,8个月后趋于平稳; Ca元素除3~4个月少量富集外,一直处于释放过程。
|
图 2 凋落叶分解过程中养分残留率变化动态 Figure 2 Dynamics of remaining nutrient rate in the decomposing process of leaf litter |
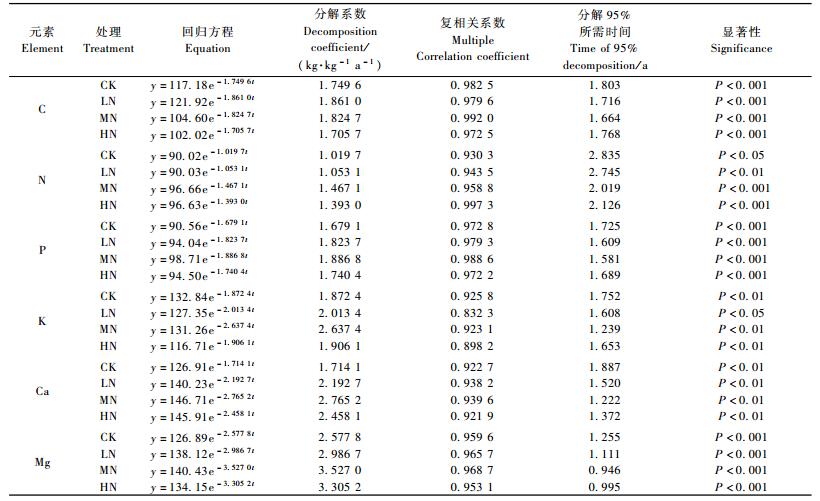
为了进一步探讨氮沉降与凋落叶分解过程中各养分元素残留率之间的关系,利用Olson提出的指数衰减模型,对不同处理的养分元素残留率(y)与时间(t)进行拟合,得出的Olson指数衰减数学模型的相关系数均达到显著水平(表 2),说明拟合效果良好。从表 2可以看出,C元素年分解系数LN处理最大,HN处理最小,N,P,K,Ca和Mg元素年分解系数均是MN处理最大。一般以95%凋落物被分解所需的时间来表示凋落物的周转期(胡肄慧等,1986),把凋落物所含养分元素残留量被分解95%所需时间也作为1个周转期(樊后保等,2008),LN,MN,HN处理养分元素的周转期均比CK短,其中C,N,P,K,Ca和Mg元素MN处理周转期分别比对应CK短0.139,0.816,0.144,0.513,0.665和0.309 a; 氮沉降对N元素的影响程度最大,LN,MN和HN处理周转期分别比CK(2.835 a)缩短0.090,0.816和0.709 a。由此可见,氮沉降促进了凋落叶C,N,P,K,Ca,Mg元素的释放,其中MN处理促进作用最强。
|
|
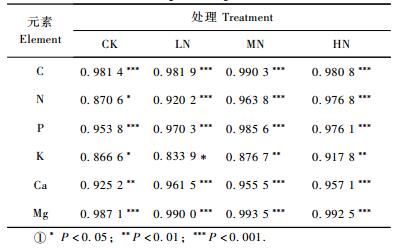
结合氮沉降对凋落物干物质分解影响的研究,经过统计发现,C,N,P,K,Ca和Mg元素残留率与干物质残留率存在较大的相关性,相关系数均达到显著水平(表 3)。从元素释放动态模型来看,C,N,P,K,Ca和Mg元素具有元素释放与干物质分解双重释放格局。
|
|
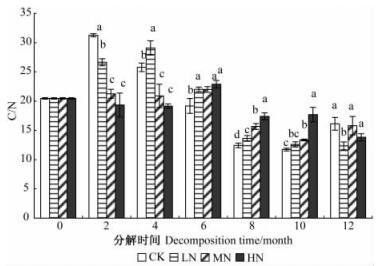
试验期内各处理凋落叶C/N在12~31之间变动,总体上,各处理变化趋势都是先升高后降低(图 3)。分解2个月时,CK显著高于N处理,而6个月,8个月,10个月时CK低于N处理; 总体来看,分解前2个月N处理降低凋落叶C/N值,而2个月后提高其C/N比值。
|
图 3 凋落叶分解过程中C/N的变化动态 Figure 3 Dynamics of C/N ratios in the decomposing process of leaf litter |
相关研究表明,毛竹(Phyllostachys edulis)林凋落叶N,P的含量随分解呈增加趋势,而K,Ca,Mg的含量则趋于减小,N,P在凋落叶分解初期为累积阶段,而后才释放归还,K,Ca,Mg在整个分解过程中均为释放; 滨海沙地吊丝单(Dendrocalamopsis vario-striata)林和麻竹(Dendrocalamus altiflorus)山地笋用林凋落叶N,P元素含量呈现出升-降-升的变化规律,而K在前期流失强烈,中期平缓,后期略有回升(曹群根等,1997; 张梅等,2008; 邱尔发等,2005)。与其他竹林类型相比,慈竹凋落叶N,P,K含量变化和释放模式具有自身特点。这主要与凋落物的类型、分解阶段和养分本身特性有关。凋落物质量决定着分解过程中的养分释放动态,初始养分和木质素含量分别决定着分解初期和后期的养分释放速率(郭剑芬等,2006; 李志安等,2004)。Berg等(1981)认为各种凋落物N含量在0.3%~1.4%范围内时将出现N固定,而N含量在0.6%~2.8%范围则表现为N的释放。在本研究中,慈竹凋落叶初始N含量较高(2.2%),在凋落叶分解初期,因降雨淋溶而释放; 随后N元素富集是由于适宜的湿度和温度有利于微生物的生长和繁殖,增加凋落叶N含量,N元素富集到一定程度后又开始释放。与N元素相同,初始K含量也可以解释凋落叶分解过程中K元素动态。在凋落叶分解初期富集,凋落叶初始K含量(0.38%)低,不能满足凋落叶分解微生物生长和繁殖,而向附近土壤获取K元素,凋落叶分解后期K含量的升高,主要是由于降雨淋溶等原因造成。P元素动态同时受控于物理、生物和化学因素, 但以生物因素的影响较强(Laskowski et al., 1995)。
本研究结果显示,养分元素释放动态模型具有元素释放与干物质分解双重释放格局。这与其他学者的研究结论一致,说明了各养分元素的释放与干物质的分解密不可分(赵谷风等,2006; 樊后保等,2008)。在慈竹凋落叶分解初期,由于Ca元素释放速率低于干物质分解速率,从而导致Ca含量的升高,而Ca的释放模式仍表现为直接释放。C,Mg元素的释放过程也与干物质分解紧密相联,都表现为直接释放。
3.2 慈竹凋落叶分解过程中主要养分元素的释放对氮沉降的响应以往研究表明,氮沉降对森林凋落物养分释放的影响有促进、延缓、无作用等不同的表现形式,不同的氮沉降量对养分释放的作用具有一定的差异性,如樊后保等(2008)对杉木(Cunninghamia lanceolata)人工林研究表明,N1(60 kg·hm-2 a-1),N2(120 kg·hm-2 a-1)处理表现出对杉木叶凋落物C,N元素释放的促进作用,而N3(240 kg·hm-2 a-1)处理表现出抑制C,N元素释放。本文与其研究结果相似,氮沉降促进了慈竹凋落叶C,N,P,K,Ca,Mg元素的释放,其中MN处理促进作用最强,这主要是由于凋落叶养分释放与干物质分解密切相关。慈竹凋落叶干物质分解过程表明,氮沉降促进凋落叶干物质的分解,其中MN处理对其促进作用最大。宋学贵等(2007)对川西南常绿阔叶林研究也表明,氮沉降抑制凋落物干物质的分解,从而抑制C,N,P,K元素的释放。O′Connell(1994)的研究结果表明氮沉降抑制了凋落物分解,其N残留量显著高于对照。这更一步印证凋落物养分释放与凋落物干物质分解密切相关。有研究发现,往生态系统输入N的量有一临界值,超过该临界值将会引起分解者微生物的作用向低效率转变,从而延缓凋落物的分解(Aber et al., 1998; Berg, 2000; Micks et al., 2004)。也有研究证实适度的氮沉降对凋落物分解有促进作用,但高氮沉降会对凋落物分解产生不利影响(Kuperman, 1999; Anderson et al., 1999)。这也可以解释本文中氮沉降促进凋落叶养分元素的释放,且MN处理促进作用最强的现象。
本研究中,氮沉降对凋落叶N元素释放的影响程度最大,LN,MN,HN处理的N周转期分别比CK(2.835 a)缩短0.090,0.816和0.709 a。一方面,外加N在一定程度上增加凋落物可利用的N素,促进微生物的生长和繁殖,从而加快凋落物分解速度(Mo et al., 2003); 另一方面,外加N增大了凋落物中含N有机化合物的矿化和硝化速率,降低凋落物中的含量(方运霆等,2004)。由于两方面的共同影响,从而改变慈竹凋落叶N元素的释放模式。
3.3 慈竹凋落叶分解过程中氮沉降对C/N的影响目前,一些研究表明氮沉降增加会改变森林凋落物的C/N,进而影响其分解的速率。如Månsson等(2003)研究发现,氮沉降明显降低了橡树(Quercus robur)凋落物的C/N; 项文化等(2005)的研究也得出类似结论。樊后保等(2008)研究表明,氮沉降处理降低了杉木凋落叶C/N比。本研究与其有一定的差异性,在凋落叶分解过程中各处理C/N在12~31之间变动,变化趋势为先升高后降低,总体上,分解前2个月氮沉降降低了凋落叶C/N值,而2个月后提高其C/N比值。究其原因是,在凋落叶分解初期氮沉降促进了C元素的快速释放,降低了C/N比值; 2个月后,氮沉降对N元素释放促进作用最大,N元素释放速率高于C元素释放速率,从而氮沉降增加了C/N比值。在一定范围内,N沉降能满足微生物对其分解的凋落叶C/N的要求,有利于微生物的生长和繁殖,促进凋落叶分解和养分释放。
综上所述,本研究表明在大气氮沉降持续增加的情况下,慈竹林凋落叶分解和养分释放受到促进作用,氮沉降有利于林地养分的循环,改善土壤的肥力状况。然而竹林生态系统凋落物通常包括凋落叶、凋落箨和凋落枝,虽然N沉降促进慈竹林凋落叶的养分释放,而对其凋落枝、凋落箨和根系等的影响方向和程度如何,还需做进一步的研究。
曹群根, 傅懋毅, 李正才. 1997. 毛竹林凋落叶分解失重及养分累积归还模式[J]. 林业科学研究, 10(3): 303-308. |
樊后保, 刘文飞, 徐雷. 2008. 氮沉降下杉木(Cunninghamia lanceolata)人工林凋落叶分解过程中C、N元素动态变化[J]. 生态学报, 28(6): 2543-2553. |
方运霆, 莫江明, PerG, 等. 2004. 森林土壤氮素转换及其对氮沉降的响应[J]. 生态学报, 24(7): 1523-1531. |
郭剑芬, 杨玉盛, 陈光水, 等. 2006. 森林凋落物分解研究进展[J]. 林业科学, 42(4): 93-100. |
胡肄慧, 陈灵芝, 孔繁志, 等. 1986. 两种中国特有树种的枯叶分解速率[J]. 植物生态学与地植物学学报, 10(1): 35-43. |
李德军, 莫江明, 方运霆, 等. 2003. 氮沉降对森林植物的影响[J]. 生态学报, 23(9): 1891-1900. |
李仁洪, 胡庭兴, 涂利华, 等. 2009. 模拟氮沉降对华西雨屏区慈竹林凋落物分解的影响[J]. 应用生态学报, 20(11): 2588-2593. |
李志安, 邹碧, 丁永祯, 等. 2004. 森林凋落物分解重要影响因子及其研究进展[J]. 生态学杂志, 23(6): 77-83. |
莫江明, 薛碌花, 方运霆. 2004. 鼎湖山主要森林植物凋落物分解及其对N沉降的响应[J]. 生态学报, 24(7): 1413-1420. |
邱尔发, 陈卓梅, 郑郁善, 等. 2005. 麻竹山地笋用林凋落物发生、分解及养分归还动态[J]. 应用生态学报, 16(5): 811-814. |
宋学贵, 胡庭兴, 鲜骏仁, 等. 2007. 川西南常绿阔叶林凋落物分解及养分释放对模拟氮沉降的响应[J]. 应用生态学报, 18(10): 2167-2172. |
涂利华, 胡庭兴, 黄立华, 等. 2009. 华西雨屏区苦竹林土壤呼吸对模拟氮沉降的响应[J]. 植物生态学报, 33(4): 728-738. |
项文化, 闫文德, 田大伦, 等. 2005. 外加氮源及与林下植物叶混合对杉木林针叶分解和养分释放的影响[J]. 林业科学, 41(6): 1-6. DOI:10.11707/j.1001-7488.20050601 |
张梅, 郑郁善. 2008. 滨海沙地吊丝单竹林凋落物分解及养分动态研究[J]. 西南林学院学报, 28(3): 4-7. |
张东来, 毛子军, 张玲, 等. 2006. 森林凋落物分解过程中酶活性研究进展[J]. 林业科学, 42(1): 105-109. |
赵谷风, 蔡延奔, 罗嫒媛, 等. 2006. 青冈常绿阔叶林凋落物分解过程中营养元素动态[J]. 生态学报, 26(10): 3286-3295. DOI:10.3321/j.issn:1000-0933.2006.10.018 |
Aber J D, McDowell W, Nadelhoffer K J, et al. 1998. Nitrogen saturation in northern forest ecosystems, hypotheses revisited[J]. Bioscience, 48: 921-934. DOI:10.2307/1313296 |
Anderson J M, Hetherington S L. 1999. Temperature, nitrogen availability and mixture effects on the decomposition of heather (Calluna vulgaris (L.) Hull) and bracken (Pteridium aquilinum (L.) Kuhn) litters[J]. Functional Ecology, 13: 116-124. DOI:10.1046/j.1365-2435.1999.00014.x |
Berg B, Staaf H. 1981. Leaching, accumulation and release of nitrogen in decomposing forest litter[J]. Ecological Bulletins, 33: 163-178. |
Berg B. 2000. Litter decomposition and organic matter turnover in northern forest soils[J]. Forest Ecology and Management, 133: 13-22. DOI:10.1016/S0378-1127(99)00294-7 |
Galloway J N, Dentener F J, Capone D G, et al. 2004. Nitrogen cycles: past, present, and future[J]. Biogeochemistry, 70(2): 153-226. DOI:10.1007/s10533-004-0370-0 |
Hobbie S E, Gough L. 2004. Litter decomposition in moist acidic and non-acidic tundra with different glacial histories[J]. Oecolosia, 140: 113-124. DOI:10.1007/s00442-004-1556-9 |
Kuperman R G. 1999. Litter decomposition and nutrient dynamics in oak-hickory forests along a historic gradient of nitrogen and sulfur deposition[J]. Soil Biology & Biochemistry, 31: 237-244. |
Laskowski R, Niklinska M, Maryanski M. 1995. The dynamics of chemical elements in forest litter[J]. Ecology, 76(5): 1393-1406. DOI:10.2307/1938143 |
Magill A H, Aber J D. 2000. Dissolved organic carbon and nitrogen relationships in forest litter as affected by nitrogen deposition[J]. Soil Biolog & Biochemistry, 32: 603-613. |
Månsson K F, Falkengren G U. 2003. The effect of nitrogen deposition on nitrification, carbon and nitrogen mineralisation and litter C:N ratios in oak(Quercus robur L.)forests[J]. Forest Ecology and Management, 179: 455-467. DOI:10.1016/S0378-1127(02)00535-2 |
Micks P, Downs M R, Magill A H, et al. 2004. Decomposing litter as a sink for 15N-enriched additions to an oak forest and a red pine plantation[J]. Forest Ecology and Management, 196: 71-87. DOI:10.1016/j.foreco.2004.03.013 |
Mo J M, Brown S, Peng S L, et al. 2003. Nitrogen availability in disturbed, rehabilitated and mature forests of tropical China[J]. Forest Ecology and Management, 175(3): 573-583. |
O′Connell A M. 1994. Decomposition and nutrient content of litter in a fertilized eucalypt forest[J]. Biology and Fertility of Soils, 17(2): 159-166. DOI:10.1007/BF00337749 |
Vitousek P M, Aber J D, Howarth R W, et al. 1997. Human alteration of the global nitrogen cycle: Sources and consequences[J]. Ecological Applications, 7(3): 737-750. |
Zheng X H, Fu C B, Xu X K, et al. 2002. The Asian nitrogen cycle case study[J]. Ambio, 31(2): 79-87. DOI:10.1579/0044-7447-31.2.79 |
 2010, Vol. 46
2010, Vol. 46