文章信息
- 曾今尧, 刘丙万, 郑咏梅, 江雷
- Zeng Jinyao, Liu Bingwan, Zheng Yongmei, Jiang Lei
- 美国白蛾及其他5种灯蛾鳞片超微结构的比较
- A Comparison among the Ultrastructures and Characteristics of Wing Scales of the Fall Webworm and Other 5 Tiger Moth Species (Lepidoptera: Arctiidae)
- 林业科学, 2010, 46(6): 97-101.
- Scientia Silvae Sinicae, 2010, 46(6): 97-101.
-
文章历史
- 收稿日期:2008-10-14
- 修回日期:2009-09-16
-
作者相关文章
2. 中国科学院化学研究所 北京 100080
2. Institute of Chemistry, Chinese Academy of Science Beijing 100080
鳞片位于蛾类体表,对其生存和繁衍具有至关重要的作用。鳞片可以吸收或者反射光能,协助调节体温,也是蛾类能在寒冷夜晚活动的原因之一(Kingsolver et al., 1983;Kristensen,1984;Vukusic et al., 2003);鳞片所产生的颜色与花纹还可以起到警戒色、保护色或者吸引异性的作用(Mallet et al., 1987;Burghardt et al., 2000;Brakefield et al., 2000);鳞片还有防湿去污的功能,保证翅膀的干燥与清洁(Grodnitsky,1999;Zheng et al., 2007)。目前对蛾类鳞片的研究涉及范围较广,如翅的长度与鳞片长度之间的关系,鳞片结构色与色素色的形成机制,鳞片结构与发育过程及鳞片的进化等等(Greenstein,1972;Nardi et al., 1986;Ghiradella,1989; 1991;Vukusic et al., 1999;Simonsen,2001;Simonsen et al., 2003)。鳞片的形态特征还可以准确地反映种、属间的差异,用于动物的分类、鉴定、进化及亲缘关系等研究(房岩等,2007)。对蛾类鳞片超微观结构与形态的研究始于19世纪50年代,如Greenstein详细描述了大蚕蛾(Hyalophora cecropia)鳞片发育过程中鳞片形成细胞和孔洞形成细胞的超微观结构;Nardi等观察了烟草天蛾(Manduca sexta)鳞片空间图案的形成过程,Simonsen等阐述了颚蛾科(Agathiphagidae)鳞片的进化过程。在我国,对鳞片的研究起步较晚,仅有对蛱蝶科部分种类鳞片的超微结构研究,尚未对蛾类鳞片超微结构的详细研究(房岩等,2007)。
隶属于灯蛾科(Aretiidae)的美国白蛾(Hyphantria cunea)是一种世界性的检疫害虫。由于美国白蛾繁殖迅速、适应性强、传播途径广、幼虫食性杂等特点,自20世纪70年代末传入我国后已造成很大危害,直接影响我国农林业经济的发展(季荣等,2003;杨忠岐等,2007)。仅2004年的发生面积就高达11.7万hm2,年经济损失50多亿元,减少林木生长量1 700万m3(赵铁珍等,2006)。近年来在美国白蛾生物学特征及化学、生物防治方面的研究已经取得了重大成果(魏建荣等,2003;Che et al., 2005;Gomi,2006)。但迄今为止,尚未有过关于美国白蛾鳞片特征的报道,更缺乏美国白蛾与其他灯蛾间鳞片差异的系统性对比研究。包括美国白蛾在内的很多灯蛾在美国和加拿大都是当地蝙蝠的主要捕食对象(Fullard et al., 1997;2003),但在我国尚未有利用蝙蝠防御美国白蛾的研究。蛾类鳞片的形态结构也是科研工作者研究蝙蝠与蛾类捕食关系的依据之一,对蝙蝠粪便残渣的分析可以确定蝙蝠所食蛾类的种类(唐占辉等,2005;韦力等,2006)。本研究在扫描电镜下研究了美国白蛾及其他5种常见灯蛾体表鳞片的超微观结构与形态,并进行了比较,探讨了美国白蛾等灯蛾鳞片形态结构和生理机能的关系,灯蛾科不同种属间鳞片超微形态特征的差异及在分类学上的意义,为包括美国白蛾在内的灯蛾在行为学、分类学、进化、与蝙蝠的捕食关系以及今后利用蝙蝠对美国白蛾进行生物防治的研究提供了重要依据。
1 材料与方法 1.1 标本采集2006年2月至8月分别于福建省(117.01°N,25.12°E)采集异粉蝶灯蛾(Nyctemera adversata)5只和人纹污灯蛾(Spilarctia subcarnea)6只,北京房山(39.43°N,115.59°E)采集黄臀黑污灯蛾(Epatolmis caesarea)5只、净雪灯蛾(Spilosoma album)10只和黑须污灯蛾(Spilarctia casigneta)10只。美国白蛾标本5只来自中国科学院动物研究所农业虫害鼠害综合治理研究国家重点实验室。
1.2 样品制备与电镜观察采用常规扫描电镜标本制作方法。选取美国白蛾及其他5种灯蛾展翅标本前翅非翅脉处,覆盖有鳞片的部分,按照翅膀正面和背面,鳞片正面和背面分别用导电胶固定在扫描电镜样品台上,E-102型离子溅射仪镀金。在场发射扫描电子显微镜下观察(JEOL JSM-6700F)(Zheng et al., 2007)。
1.3 鳞片结构的测量与统计扫描电镜下得到美国白蛾及其他5种灯蛾前翅鳞片的图片,选取每种蛾类每种鳞片10片完整且平坦的进行扫描,用Adobe Photoshop7.0软件测量鳞片的基本形态及鳞片表面脊之间的距离。鳞片长度是从鳞片根部至端部最长处的长度,鳞片宽度是鳞片最宽处的宽度。脊间距是鳞片正面隆起的纵脊之间的距离。所有测量数据借助Excel和SPSS软件进行方差分析(One-way ANOVA)和LSD多重比较,所得结果以平均值±标准误(Mean±SE)表示(Yao et al., 2007)。
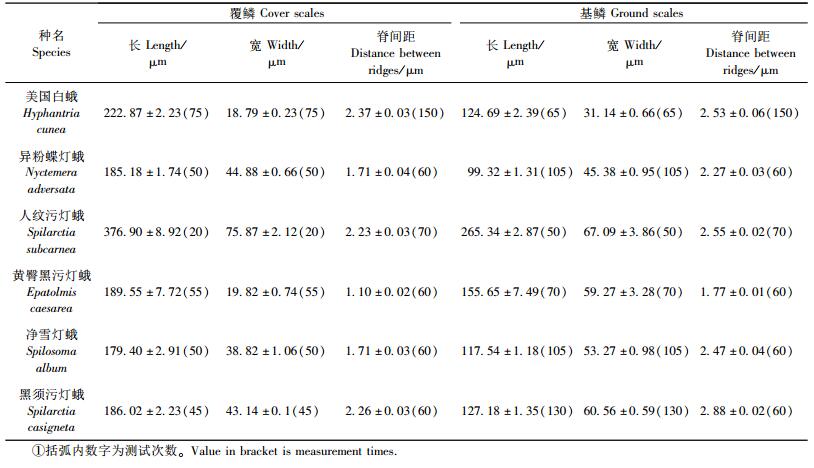
2 结果 2.1 鳞片的排列方式与形态美国白蛾及另外5种灯蛾鳞片的排列方向都是从翅基部到翅端部,明显分为2层:覆鳞(cover scales,sc)与基鳞(ground scales,gs)(钟敏等, 2003),并有规律地隔行排列成覆瓦状(图版Ⅰ)。鳞片基部都有小柄镶嵌在翅膜的鳞片囊内。6种灯蛾的覆鳞都成长条形,端部圆滑或微有缺刻,无锯齿状,覆盖在基鳞之上。基鳞为长卵形,端部成不规则锯齿状,排列在2排覆鳞之间。由于覆鳞长而窄于基鳞,所以覆盖并不完全,只覆盖在基鳞中脉部分,基鳞边缘部分仍然可见。2种鳞片根部都有一个鳞片柄插入翅膀上的凹槽中,表面都有连接于鳞片根部与端部的向外突出成脊状的平行弧形脉(图版Ⅱ)。所测种类中,人纹污灯蛾的覆鳞和基鳞均最长(376.9 μm±8.92 μm;265.34 μm±2.87 μm)最宽(75.87 μm±2.12 μm;67.09 μm±3.86 μm);净雪灯蛾的覆鳞最短(179.4 μm±2.91 μm);异粉蝶灯蛾的基鳞最短(99.32 μm±1.31 μm);美国白蛾的覆鳞和基鳞均最窄(18.79 μm±0.23 μm;31.14 μm±0.66 μm)。

|
图版Ⅰ Plate Ⅰ 1.美国白蛾前翅鳞片的排列方式(× 350); 2.美国白蛾基鳞与覆鳞的形态特征(× 600); 3.基鳞上层(面向空气的一面)的超微观结构; 4.覆鳞上层(面向空气的一面)的超微观结构。完整鳞片: 3a(× 950),4a(× 600);鳞片部分放大(× 5 000): 3b,4b;鳞片内部超微观结构(× 12 000): 3c,4c。 1. Arrangement of forewing scales in Hyphantria cunea (× 350); 2. Forms of cover scales and ground scales in Hyphantria cunea (× 600); 3. Ultrastructure of upper side (face to air side) of ground scales; 4. Ultrastructure of upper side (face to air side) of cover scales. The whole scales: 3a (× 950), 4a(× 600); a piece of a scale(× 5 000) : 3b, 4b; the ultrastructure of inner scale (× 12 000) : 3c, 4c. |
|
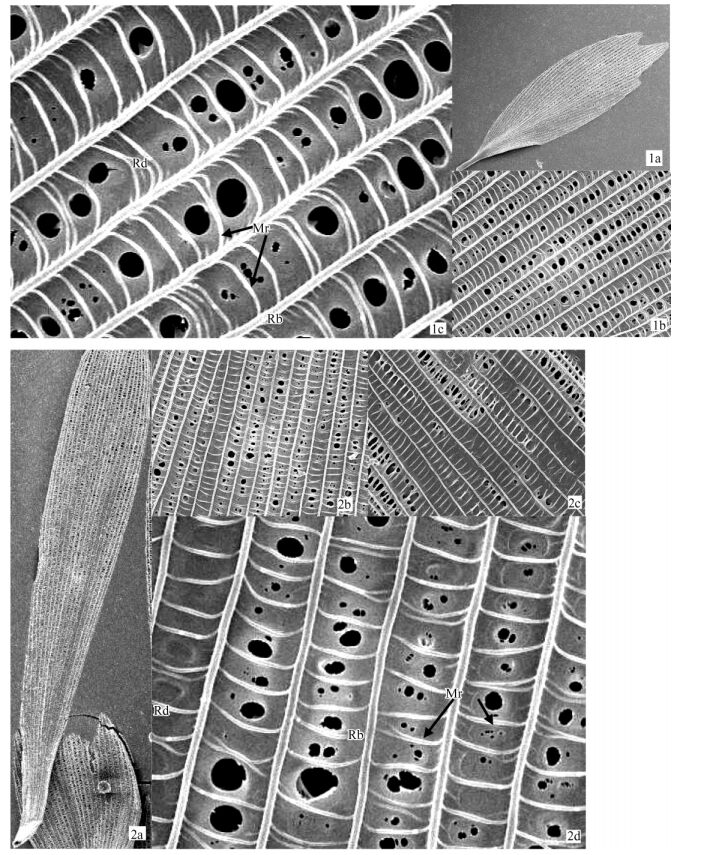
图版Ⅱ Plate Ⅱ 1.基鳞下层(面向翅膀的一面)的超微观结构; 2.覆鳞下层(面向翅膀的一面)的超微观结构。完整鳞片: 1a(× 750),2a(× 400);鳞片部分放大(× 5 000) : 1b,2b-c; 鳞片内部超微观结构(× 12 000) : 1c,2d。 1. Ultrastructure of under side (face to wing side) of ground scales; 2. Ultrastructure of under side (face to wing side) of cover scales. The whole scales: 1a(× 750), 2a(× 400); a piece of a scale (× 5 000) : 1b, 2b-c; the ultrastructure of inner scale (× 12 000) : 1c, 2d. cs:覆鳞Cover scales; gs:基鳞Ground scale; Rd:脊Ridges; Rb:梁Ribs; Mr:小梁Microribs; T:柱Trabeculae; L:脊板Lamellae. |
|
|
在高倍扫描电子显微镜下,可以清楚看见6种灯蛾每个鳞片都有上下2层,中间有一定的厚度充满空气,而成扁囊状。
鳞片上层,即面向外界的一面,结构比较复杂,由纵向的向外突出的脊(ridges,Rd)和横向的有一定间隔的横梁(ribs,Rb)构成网格状。每根脊都是由很多脊板(lamellae,L)从根部向端部沿着脊的方向倾斜一定的角度覆盖而成,并向外隆起高于梁的位置,在低倍显微镜下就只看见鳞片表面弧形平行的脊。与脊板垂直的是小梁(microribs,Mr)。圆柱形小梁平行排列连接鳞片上层的脊板与下层的脊,2根小梁之间成凹槽状。在有横梁存在的地方,小梁通过横梁与横梁另一边的小梁连接。由脊和横梁围城的网格内是中空的,通过网格可以看见鳞片下层。网格还使中间的空气层与外界相通。通过有的网格还可以在横梁的下方看见与横梁垂直并连接鳞片上下2层的柱(trabeculae,T)。所测结果中,美国白蛾覆鳞的脊间距最大(2.37 μm±0.03 μm);黄臀黑污灯蛾覆鳞和基鳞的脊间距均最小(1.1 μm±0.02 μm;1.77 μm±0.01 μm);黑须污灯蛾基鳞的脊间距最大(2.88 μm±0.02 μm)。
鳞片下层,即面向翅膀的一面,结构比较简单而平坦成板状。也有纵向的脊连接鳞片根部与端部,但不向外突出,也不由脊板组成。由脊和横梁围城的网格被表皮组织填充,有的网格填充不完全成不规则的孔洞状。小梁与脊垂直,并在有横梁的地方通过横梁与横梁另一边的小梁连接。
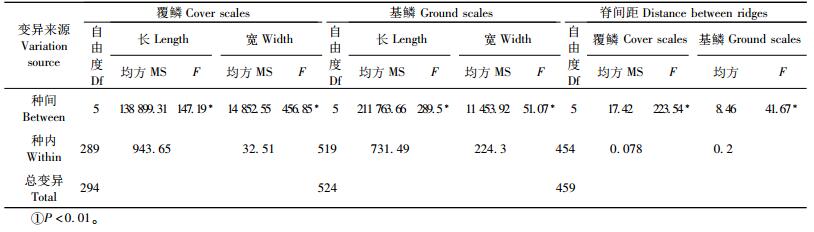
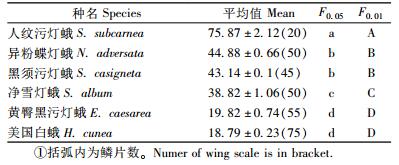
2.3 覆鳞与基鳞的形态特征的差异显著性检验对6种灯蛾的覆鳞和基鳞的长度、宽度和脊间距6个指标进行种属间差异显著性检验,结果表明6个指标在种属间均达极显著差异(P < 0.01) (表 2)。以F值最大的覆鳞的宽度作多重比较(表 3)。由此可见,美国白蛾除了与黄臀黑污灯蛾差异不显著以外,与其他4种灯蛾均差异极显著。可以推测,其他5个指标也有种间差异不显著。
|
|
|
|
根据鳞片的表面形态可以把鳞片分为:融合型鳞片(fused scale)与镂空型鳞片(hollow scale)(Simonsen,2001)。融合型鳞片是指鳞片上下层均被表皮填充,不成网格状,以前也称为原始型鳞片(primitive-type scale)。有研究已经表明融合型鳞片是在镂空型鳞片的基础上进一步融合而成,所以并不原始(Ghiradella,1998)。如异蛾科(Heterobathmiidae)和毛顶蛾科(Eriocraniidae)很多种类的覆鳞,颚蛾科(Agathiphagidae)、异蛾科(Heterobathmiidae)、毛顶蛾科(Eriocraniidae)、长角蛾科(Adelidae)、日蛾科(Heliozelidae)和丝兰蛾科(Prodoxidae)很多种类的基鳞,小翅蛾科(Micropterigidae)很多种类的覆鳞和基鳞都是融合型鳞片(Simonsen,2001)。镂空型鳞片是指鳞片上下2层有1层是中空网格状,网格与鳞片内部相通,又叫正常型鳞片(normal-type scale)。绝大多数鳞翅目昆虫的鳞片属于此类型。而根据翅膀上鳞片的排列方式和表面形态可以把鳞片分为4种类型:单层鳞片覆盖型(single-layer scale covering)、一型双层鳞片(type-1 bilayer scale covering)、二型双层鳞片(type-2 bilayer scale covering)和三型双层鳞片(type-3 bilayer scale covering)。单层鳞片覆盖型是指翅膀上只有一种形态的鳞片覆盖,如蝙蝠蛾科(Hepialidae)的Dicranoses属和Oiketicus属的个别种类;一型双层鳞片是指一层大而融合型鳞片覆盖一层小而融合型鳞片,很多较原始的蛾类鳞片都属于此类型;二型双层鳞片是指一层大而镂空型鳞片覆盖一层小而镂空型鳞片,如蝙蝠蛾科的Gazoryctra属,Ogygiosis属,Prototheora属和Callipielus属的个别种类及其他绝大多数蛾类鳞片都属于此类型;三型双层鳞片是指一层镂空型鳞片覆盖一层融合型鳞片,如颚蛾科(Agathiphagidae)和扇鳞蛾科(Mnesarchaeidae)绝大多数种类的鳞片(Simonsen,2001)。笔者的研究结果证实,美国白蛾及另外5种灯蛾的鳞片排列是一层窄而长的鳞片覆盖一层短而宽的鳞片,且都属于镂空型鳞片,即美国白蛾及其他5种灯蛾的鳞片类型属于二型双层鳞片。
种属间比较表明,美国白蛾覆鳞的形态大小更接近于黄臀黑污灯蛾(P>0.05),说明它们的亲缘关系可能更近,而与另外4种灯蛾覆鳞差异很大;基鳞的形态大小都很容易与其他5种灯蛾区分开。美国白蛾覆鳞的脊间距显著大于其他5种灯蛾,而基鳞的脊间距与人纹污灯蛾(P>0.05)和净雪灯蛾(P>0.05)的差距不大。单一指标不能很好的将美国白蛾的鳞片与其他5种灯蛾区分,必须综合覆鳞和基鳞的形态大小及脊间距这6个参量,才可以将美国白蛾的鳞片与其他5种灯蛾的鳞片区分。蛾类翅膀表面鳞片的超微结构为科以下单位(属、种)分类鉴定中的重要依据,虽然不宜单独用于种的鉴定,但对于区分不同种仍具有重要参考价值。
食虫蝙蝠是美国白蛾的自然天敌之一。美国白蛾在美国和加拿大都是当地食虫蝙蝠,如大棕蝠(Eptesicus fuscus)、花尾蝠(Euderma maculatum)等的主要捕食对象(Fullard et al., 1997;2003)。食虫蝙蝠捕食昆虫后,往往消化并不完全,因此可以根据蝙蝠粪便中昆虫的残体或鳞片的种类判断和分析蝙蝠的食性。蛾类鳞片的形态特征虽然不宜单独用于种的鉴定,但在蝙蝠食性分析中结合其他昆虫残体,行为生态学数据对灯蛾种的确定具有一定指导意义,也能为我国今后蝙蝠与美国白蛾的捕食关系研究及利用蝙蝠防治美国白蛾的研究提供参考和例证。蛾类鳞片脊间距的大小往往决定了蛾类利用一定波长的光能调节体温的能力,这也决定了蛾类在夜晚活动的能力和时间范围,从而为进一步寻找并确定相对应美国白蛾的蝙蝠天敌的种类提供了依据(Rydell et al., 2000)。从以鳞片形态为基础,利用蝙蝠粪便残渣分析所捕灯蛾种类,到最终确定在我国究竟哪种或哪类蝙蝠将成为美国白蛾自然天敌的研究道路上,还需要大量其他灯蛾鳞片形态的相关数据及进一步的行为生态学研究。
房岩, 王同庆, 孙刚, 等. 2007. 蛱蝶翅鳞片的超微结构观察[J]. 昆虫学报, 50(3): 313-317. |
季荣, 谢宝瑜, 李欣海, 等. 2003. 外来入侵种——美国白蛾的研究进展[J]. 昆虫知识, 40(1): 13-18. |
唐占辉, 盛连喜, 曹敏, 等. 2005. 西双版纳地区犬蝠和棕果蝠食性的初步研究[J]. 兽类学报, 25(4): 367-372. |
韦力, 周善义, 张礼标, 等. 2006. 三种共栖蝙蝠的回声定位信号特征及其夏季食性的比较[J]. 动物学研究, 27(3): 235-241. |
魏建荣, 杨忠岐, 苏智. 2003. 利用生命表评价白蛾周氏啮小蜂对美国白蛾的控制作用[J]. 昆虫学报, 46(3): 318-324. |
杨忠岐, 张永安. 2007. 重大外来入侵害虫——美国白蛾生物防治技术研究[J]. 昆虫知识, 44(4): 465-471. |
赵铁珍, 高岚, 柯水发. 2006. 2004年全国美国白蛾疫区的非经济损失评估[J]. 林业经济问题, 26(4): 321-326. |
钟敏, 沈佐锐. 2003. 鳞翅目昆虫鳞片的结构发育与眼斑的形成[J]. 昆虫知识, 40(5): 410-415. |
Brakefield P M, Liebert T G. 2000. Evolutionary dynamics of declining melanism in the peppered moth in the Netherlands[J]. Biol Sci, 267(1456): 1953-1957. DOI:10.1098/rspb.2000.1235 |
Burghardt F, Knüttel H, Becker M. 2000. Flavonoid wing pigments increase attractiveness of female common blue (Polyommatus icarus) butterflies to mate-searching males[J]. Naturwissenschaften, 87: 304-307. DOI:10.1007/s001140050726 |
Che C, Zhang Z N. 2005. A facile synthetic method for (3Z, 6Z, 9S, 10R)-9, 10-epoxy-3, 6-heneicosadiene, sex pheromone component of Hyphantria cunea (Drug)[J]. Chin Chem Lett, 16(4): 468-470. |
Fullard J H, Dawson J W. 1997. The echolocation calls of the spotted bat Euderma maculatum are relatively inaudible to moths[J]. J Exp Biol, 200: 129-137. |
Fullard J H, Dawson J W, Jacobs D S. 2003. Auditory encoding during the last moment of a moth's life[J]. J Exp Biol, 206: 281-294. DOI:10.1242/jeb.00085 |
Ghiradella H. 1991. Light and color on the wing: structural colors in butterflies and moths[J]. Appl Opt, 30(24): 3492-3500. DOI:10.1364/AO.30.003492 |
Ghiradella H. 1998. Hair, Bristles and Scales// Harrison F W, Locke M. Microscopical Anatomy of Invertebrates 11A (Insecta). New York: Wiley-Liss, 257-287.
|
Ghiradella H. 1989. Structure and development of iridescent butterfly scales: lattices and laminae[J]. J Morphol, 202: 69-88. DOI:10.1002/(ISSN)1097-4687 |
Gomi T. 2006. Sexual difference in the effect of temperature on the larval development in Hyphantria cunea (Drury) (Lepidoptera: Arctiidae)[J]. Appl Entomol Zool, 41(2): 303-307. DOI:10.1303/aez.2006.303 |
Greenstein M E. 1972. The ultrastructure of developing wings in the giant silk moth, Hyalophora cecropia. Ⅱ[J]. Scale forming and socket forming cells. J Morphol, 136: 23-52. |
Grodnitsky D L. 1999. Form and Function of Insect Wings[M]. Baltimore and London: The Johns Hopkins University Press.
|
Kingsolver J G, Watt W B. 1983. Thermoregulatory strategies in Colias butterflies: thermal stress and the limits to adaptation in thermally varying environments[J]. Am Nat, 121: 32-55. DOI:10.1086/284038 |
Kristensen N P. 1984. Studies on the morphology and systematics of primitive Lepidoptera (Insecta)[J]. Steenstrupia, 10: 141-191. |
Mallet J, Singer M C. 1987. Individual selection, kin selection, and the shifting balance in the evolution of warning colours: the evidence from butterflies[J]. Biol J Linn Soc Lond, 32: 337-350. DOI:10.1111/bij.1987.32.issue-4 |
Nardi J, MaGee-Adams S M. 1986. Formation of scale spacing patterns in a moth wing. Ⅰ. Epithelial feet may mediate cell rearrangement[J]. Dev Biol, 116: 278-290. DOI:10.1016/0012-1606(86)90131-4 |
Rydell J, Lancaster C W. 2000. Flight and thermoregulation in moths were shaped by predation from bats[J]. Oikos, 88: 13-18. DOI:10.1034/j.1600-0706.2000.880103.x |
Simonsen T J, Kristensen N P. 2001. Agathiphaga wing vestiture revisited: evidence for complex early evolution of lepidopteran scales (Lepidoptera: Agathiphagidae)[J]. Insect Syst Evol, 32: 169-175. DOI:10.1163/187631201X00128 |
Simonsen T J. 2001. The wing vestiture of the non-ditrysian Lepidoptera (Insecta): Comparative morphology and phylogenetic implications[J]. Acta Zool, 82(4): 275-298. |
SimonsenT J, Kristensen N P. 2003. Scale length/wing length correlation in Lepidoptera (Insecta)[J]. J Nat Hist, 37(6): 673-679. DOI:10.1080/00222930110096735 |
Vukusic P, Sambles J R, Lawrence C R. 1999. Quantified interference and diffraction in single Morpho butterfly scales[J]. Proc R Soc Lond B Biol Sci, 266: 1403-1411. DOI:10.1098/rspb.1999.0794 |
Vukusic P, Sambles J R. 2003. Photonic structures in biology[J]. Nature, 424: 852-855. DOI:10.1038/nature01941 |
Yao Q, Zeng J Y, Zheng Y M, et al. 2007. Characteristics of echolocating bats' auditory stereocilia length, compared with other mammals[J]. Sci China Ser C, 50(4): 492-496. DOI:10.1007/s11427-007-0055-8 |
Zheng X M, Gao X F, Jiang L. 2007. Directional adhesion of superhydrophobic butterfly wings[J]. Soft Matter, 3: 178-182. DOI:10.1039/B612667G |
 2010, Vol. 46
2010, Vol. 46