文章信息
- 胡静静, 沈向, 李雪飞, 赵静, 李欣, 张鲜鲜
- Hu Jingjing, Shen Xiang, Li Xuefei, Zhao Jing, Li Xin, Zhang Xianxian
- 黄连木秋季叶色变化与可溶性糖和矿质元素的关系
- Relationships of Leaf Color Changes and Soluble Sugars and Mineral Elements in Leaves of Pistacia chinensis in Autumn
- 林业科学, 2010, 46(2): 80-86.
- Scientia Silvae Sinicae, 2010, 46(2): 80-86.
-
文章历史
- 收稿日期:2009-02-26
-
作者相关文章
黄连木(Pistacia chinensis),别名药木、药树、楷树、黄连树、药瘤木,属漆树科(Anacardiaceae)黄连木属植物,是我国特有的珍贵乔木风景树种(秦飞等,2007)。黄连木树姿秀丽,春季圆锥状花序颜色亮丽,嫩叶及秋后老叶红艳如霞,种子秋后呈绿、蓝、红等色, 为良好的观叶、观花和观果植物(牛正田,2005)。随着人们对园林绿化要求的提高,在园林绿化树种配置上强调“色、香、味、形”的变化,彩叶植物以其独特、丰富多彩的叶色极大地丰富了城市景观层次(俞禄生等,2003),黄连木还具有芳香气味,有望成为目前园林绿化、美化的新宠。目前,国内学者对彩色植物的研究主要集中在对来自国外引进彩色植物的景观应用、繁育技术、生态适应性及生理生化等方面,对于国内自有的彩色植物研究较少(林敏捷,2007;石进朝等,2007),有关黄连木的研究主要集中在育苗造林技术方面(李朋元等,2007;陈群,2007),关于叶片中化学成分对叶色的影响尚未见报道。
本研究以黄连木实生苗为试材,对其秋季不同叶色树木的叶片进行色素及其可溶性糖和矿质元素测定,并进行相关性分析,明确可溶性糖和各矿质元素含量与色素含量的相关关系,以进一步探索黄连木叶片呈色规律,从而选育出色泽纯正、气味芳香的优良株系,进一步丰富我国原产的观赏树种资源。
1 材料与方法 1.1 试验材料山东农业大学校园内栽植的135株黄连木实生苗,由泰山野生黄连木采种育苗,灌溉条件良好,管理水平一致,树龄16年,2006年于叶片变色时实地观测记录,实生苗由东侧至西依次编号(1号至135号)。本试验选择颜色有代表性的7棵单株为试材。于2007年5, 7, 9, 11月采集鲜样,进行花青苷、可溶性糖及9种矿质元素的测定。2008年在黄连木显色期又进行实地观测记录。
1.2 色素含量的测定选择光照条件一致的树冠外围,于下部,采摘5~6片复叶,设3次重复。花青苷的测定参考仝月澳等(1982)的方法,将叶片取回,洗净,擦干,剪碎后,采用1.5 mol·L-1 HCl:95%乙醇=15:85(v/v)混合液,在黑暗条件下浸提24 h,用岛津UV-2450紫外可见光分光光度计检测535 nm波长的光密度值,参照胡位荣等(2004)的计算方法进行花青苷含量的计算。叶绿素a,b和类胡萝卜素的含量参照Lichtenthaler等(1983)的方法测定,总叶绿素用叶绿素a与b的含量之和表示。
为保证试验的准确性,在相同光源下使用同一相机拍摄。相机机身为Nikon D70s,配置Sigma EX 105mm微距镜头,室内散射光条件下采用中央焦点测光,机顶灯照明,+1.0EV曝光补偿。利用计算机Photoshop CS3软件对黄连木叶片颜色进行测定,选用的彩色图像模式为CMYK模式,CMYK代表印刷上用的4种颜色,C代表青色,M代表洋红色,Y代表黄色,K代表黑色(孙艳华,2008),用C, M, Y, K的百分比值表示叶片的颜色。
1.3 可溶性糖和矿质元素的测定用蒽酮法进行可溶性糖的测定(赵世杰等, 2002)。矿质元素:将叶片用去离子水洗净,擦干,105 ℃杀青15 min,80 ℃烘干至恒重(马建军等,2004),浓H2SO4-H2O2消煮,过滤,用奈氏比色法测定全氮(刘克礼等,2004);用钼锑抗比色法测磷(陈永亮等,2006);HNO3-HClO4硝化,过滤,用SP9-400原子吸收分光光度计测定K, Ca, Mg, Fe, Mn, Cu, Zn等元素,重复3次。
所得数据用DPS3.01, SPSS11.0软件进行方差分析,并将3次重复的平均值进行相关性分析。
2 结果与分析 2.1 黄连木变色期观测黄连木在整个生命活动过程中,随着气候变化的节律,有规律地交替发生着萌芽、开花、展叶、结果、落叶等物候现象。秋季,当日平均气温下降到20℃时,黄连木叶子停止生长,叶片开始变色。当日平均气温下降到15 ℃时, 进入落叶盛期(刘启慎等,1999)。黄连木显色稳定,在不同年份之间变色期有所差异,经过3年实地观测记录,选出了色泽纯正的3个色系。21, 53及89号黄连木叶片的CMYK平均值为C73%, M62%, Y100%, K31%,其中Y值最高,为黄色系;77, 112号其CMYK平均值为C56%, M97%, Y77%, K41%,其中M值最高,为红色系;119, 135号其CMYK平均值为C60%, M82%, Y86%, K43%,M, Y值均较高,为橙色系。
|
|
不同单株的叶片中总叶绿素的含量年动态变化趋势一致(图 1),随着时间的推移,表现为下降—上升—下降的变化过程。与5月相比,7月下降幅度不超过2%,9月回升,达到全年最高值。11月又下降并达到最低值,112号比9月降低了95%,53号降低的最小为57%。11月不同单株叶片中总叶绿素含量不同,53号叶片中的总叶绿素含量最高,77号、112号叶片中的总叶绿素含量最低。

|
图 1 不同单株的叶片中总叶绿素含量的年动态变化 Figure 1 Dynamic change of Chl a+b content in leaves of different trees in a year |
不同单株的叶片中类胡萝卜素含量的年变化动态总趋势(图 2)与总叶绿素相似,但11月红色系黄连木的叶片中类胡萝卜素的含量的平均值最低,黄色系比其高93%,橙色系比其高69%。

|
图 2 不同单株的叶片中类胡萝卜素含量的年动态变化 Figure 2 Dynamic change of carotenoid content in leaves of different trees in a year |
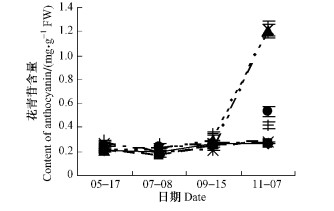
不同单株的叶片中的花青苷含量9月前变化平缓(图 3),7月略有下降,此后渐渐回升,到11月达最大值,根据其年变化动态,测定单株可分成3种类型,平稳型(21, 53, 89号)增加不超过10%,增加型(119和135号)增加100%以下,骤升型(77和112号)增长超过300%。红色系(77, 112号)叶片中花青苷的含量明显高于其他色系的单株,比黄色系高出345.4%,比橙色系高出155.1%。
|
图 3 不同单株的叶片中花青苷含量的年动态变化 Figure 3 Dynamic change of anthocyanin content in leaves of different trees in a year |
不同颜色单株叶片的花青苷和总叶绿素含量在红色系(77和112号)、黄色系(21, 53, 89号)与橙色系(119和135号)之间存在极显著差异(表 2)。黄色系单株的叶片中,花青苷所占的百分数最小,其平均值为0.32%,总叶绿素和类胡萝卜素所占的百分数最大,其平均值分别为0.56%, 0.16%。橙色系单株的叶片中,花青苷所占百分数平均为0.46%。红色系单株的叶片中,花青苷所占的比例最大,其平均值为0.87%,总叶绿素和类胡萝卜素所占的百分数最小,其平均值分别为0.05%, 0.06%。叶片色素含量的变化和比例直接影响黄连木秋色叶的表达。
|
|
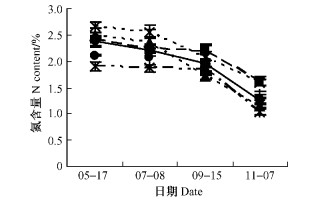
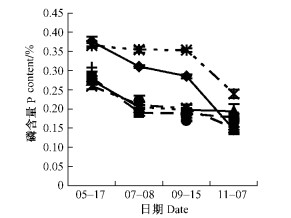
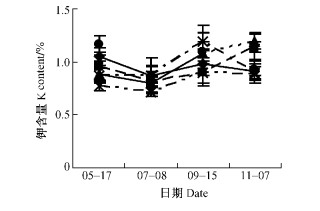
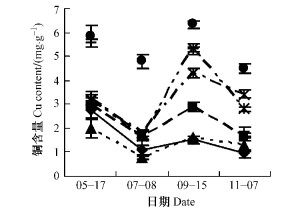
在整个生长季节,黄连木叶片中氮元素含量不断下降,在叶片生长前期处于最高水平达2.5%左右(图 4)。黄连木叶片中磷的含量变化与氮相似,在叶片生长初期处于最高水平,为0.35%左右。7棵单株在整个生长季中,磷的变化趋势可分2种类型,21和112号叶片中磷的含量处于较高水平上下降,其他单株在含量较低水平上逐渐下降(图 5)。与氮、磷含量不同,叶片中钾的含量在年周期内呈波浪状波动。随着果实的生长发育,叶片中钾的含量在7月下降,9月后开始上升,到11月除了53, 77号含量上升外,其余单株的含量都下降(图 6)。黄连木叶片中的钙、镁、锰含量变化相似,在波动中呈上升趋势,在叶片生长初期处于最低水平,平均分别为0.9%, 0.3%, 4 μg·g-1, 到11月达到整个生长季的最高水平,平均分别为1.5%, 0.4%, 20 μg·g-1。叶片中铁、锌的含量在生长初期处于最低水平,平均分别为217.9, 59.9 μg·g-1,随后上升,9月达到最高水平,平均分别为628.3,293.8 μg·g-1。11月又下降。在整个生长期,铜含量波动幅度比较大,119号叶片中铜的含量在整个年周期变化中一直处于最大值(图 7),9月含量最大为6.3 μg·g-1,11月含量最低为4.5 μg·g-1,在同期仍比其他单株叶片中的含量高。
|
图 4 不同单株的叶片中氮的年动态变化 Figure 4 Dynamic change of N content in leaves of different trees in a year |
|
图 5 不同单株的叶片中磷的年动态变化 Figure 5 Dynamic change of P content in leaves of different trees in a year |
|
图 6 不同单株的叶片中钾的年动态变化 Figure 6 Dynamic change of K content in leaves of different trees in a year |
|
图 7 不同单株的叶片中铜的年动态变化 Figure 7 Dynamic change of Cu content in leaves of different trees in a year |
对黄连木7种不同颜色单株叶片中各种化学成分的含量进行方差分析(表 2)。不同色系单株中可溶性糖的含量顺序为红色系、橙色系、黄色系。5种大量元素在53, 89, 135号叶片中的含量顺序为N, Ca, K, Mg, P,在21, 119, 112号叶片中含量的顺序为Ca, N, K, Mg, P;在77号叶片中的含量顺序为Ca, K, N, Mg, P。7棵不同单株的大量元素的含量可分含氮量最大型(53, 89, 135号)和含钙量最大型(21, 119, 112, 77号)。微量元素在77号叶片中的含量顺序为Zn, Fe, Mn, Cu,其他单株叶片中的含量顺序都为Fe, Zn, Mn, Cu。由不同单株叶片中矿质元素的含量顺序看出,在大量元素中氮、钙的含量较高,微量元素中锌、铁的含量较高。
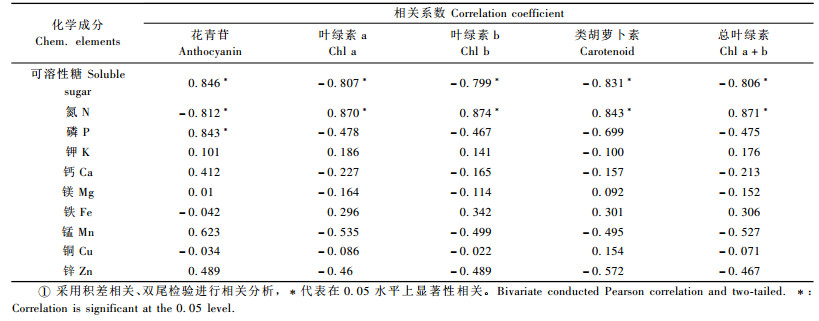
2.6 黄连木叶片中的色素与可溶性糖和矿质元素的相关性分析植物体内的化学成分,对植物色素合成有一定的影响(王庆菊等,2007)。将7棵黄连木叶片中的色素含量与其可溶性糖和9种矿质元素含量进行相关性分析(表 3),与花青苷含量呈正相关且相关系数较大的是可溶性糖、磷、钙、锰、锌,与其呈显著性负相关的是氮;与总叶绿素含量呈正相关的是氮、钾、铁,与其呈负相关的可溶性糖、磷、锰、锌;与类胡萝卜素含量呈正相关的是氮、铁、铜,与其呈负相关的是可溶性糖、磷、锰、锌。可溶性糖、磷与花青苷含量呈显著性正相关,氮与其呈显著性负相关。
|
|
|
|
胡永红等(2004)认为秋色叶的叶色变化主要是由光合产物的变化,引起植物叶片内各种色素的比例发生变化,致使叶片呈现不同色彩。不同叶色的黄连木叶片中的色素含量存在差异,红色系单株叶片中花青苷的含量远高于其他色系的单株,花青苷所占的百分数也最大,远远高于总叶绿素和类胡萝卜素所占的比例。黄色系单株的叶片中,花青苷所占的百分数最小,而总叶绿素和类胡萝卜素所占的百分数最大。橙色系单株的叶片中,花青苷所占的百分数位于两者之间。彩叶植物的叶色表现是遗传因素和外部环境共同作用的结果。Zhang等(2001)认为秋季温度的下降,昼夜温差的增大及日照时间的缩短等不利的环境,反而促进了花色素的合成和积累,所以树木的叶色在秋季变成了红色。高等植物叶片颜色因为3类主要色素含量和分布不同而表现的不同,通过改变植物叶片中各种色素的种类、含量及分布形成了多彩的叶色(姜卫兵等,2005)。叶片色素含量的变化和比例直接影响黄连木叶色的表达。
在花青苷的合成过程中可溶性糖起到信号作用(张学英,2004;Yozo et al., 2004)。Deal(1990)研究认为,夜温高于14 ℃,红叶鸡爪槭(Acer palmatum)的叶色随温度升高转淡,因为,花色苷的合成与碳水化合物的代谢有关,在较高的夜温下,呼吸加强,致使糖分不能积累,花色苷也被消耗,造成叶色褪失。本试验结果也表明:花青苷的含量与可溶性糖呈显著性正相关,此结果与关军峰(2001)在富士苹果果皮中花青苷含量和果肉中可溶性糖含量呈显著性正相关的研究结果一致。
由不同单株叶片中矿质元素的含量顺序看出,在大量元素中钙的含量较高,微量元素中铁的含量较高,可能是花青苷与钙、铁或其他金属离子的络合对颜色起稳定性作用有关(于晓南,2002)。这与前人在核果类果树桃(Amygdalus persica)、毛樱桃(Cerasus tomentosa)(马建军等,2004)等果树上的研究钙、铁的含量分别高于其他常量和微量元素的结果一致,由此可见黄连木可能是喜钙、铁树种。其中,钙与花青苷成正相关,红色系单株叶片中的平均钙含量最高为1.64 μg·g-1,黄色系单株叶片中的钙含量最小为1.44 μg·g-1,橙色系其含量居中为1.46 μg·g-1。铁在橙色系单株叶片中的含量最高平均为505.5 μg·g-1,在红色系单株叶片中的含量最低平均为441.22 μg·g-1。
矿质元素与色素的相关分析表明:对花青苷的含量影响比较大的是氮、磷、钙、锰、锌,其中氮与其呈显著性负相关,磷与其呈显著性正相关。此结果与Steven(2003)对5年生的红枫(Acer rubrum),秋色叶的色泽与夏末时叶片中P的含量有关,减少土壤中P的含量有利于花青苷表达的结果存在差异。Oren等(1997)也指出,适度缺氮、缺磷或者二者同时缺少均可引起花色素苷增加。K与花色苷成正相关,但相关系数不大。于晓南等(2000)研究表明,钾能够促进碳水化合物的合成、积累和运输,增施钾肥有利于花青苷的积累。各种矿质元素与叶绿素、类胡萝卜素含量的相关关系接近,影响最大为N,与两者均呈显著性正相关,这是因为植物叶片中很大一部分N是结合在叶绿素中有关(彭涛等,2006),不同营养元素对植物的色彩影响不同。
陈群. 2007. 黄连木栽培技术[J]. 安徽农学通报, 13(18): 288. DOI:10.3969/j.issn.1007-7731.2007.18.157 |
陈永亮, 周晓燕, 韩士杰. 2006. 不同N素形态对落叶松苗木根/土界面pH值及养分有效性的影响[J]. 林业科学, 42(9): 431-931. |
关军峰. 2001. 果品品质研究[M]. 石家庄: 河北科学技术出版社.
|
何奕昆, 奚惕. 1989. 凤仙花中花色苷累积与苯丙氨酸解氨酶的关系[J]. 植物生理学讯, (2): 35-38. |
胡位荣, 张昭其, 季作梁. 2004. 酸处理对采后荔枝果皮色泽与生理活性的影响[J]. 食品科学, 25(7): 176-180. |
胡永红, 秦俊, 蒋昌华. 2004. 上海地区秋色叶成因的调查与分析[J]. 东北林业大学学报, 32(5): 84-86. |
胡敬志, 田旗, 鲁心安. 2007. 枫香叶片色素含量变化及其与叶色变化的关系[J]. 西北农林科技大学学报:自然科学版, (10): 219-223. |
姜卫兵, 庄猛, 韩浩章, 等. 2005. 彩叶植物呈色机理及光合特性研究进展[J]. 园艺学报, 32(2): 352-358. |
李朋元, 吕进. 2007. 黄连木种子育苗技术[J]. 山东林业科技, (2): 80-82. |
林敏捷. 2007. 彩色植物在园林造景中的应用[J]. 福建热作科技, 32(1): 38-40. |
刘启慎, 谭浩亮, 李建新. 1999. 中国黄连木生长规律的研究[J]. 河南林业科技, 19(2): 3-6. |
刘克礼, 高聚林, 王立刚. 2004. 大豆对氮、磷、钾的平衡吸收动态的研究[J]. 中国油料作物学报, 26(1): 51-54. |
马建军, 张立彬. 2004. 野生欧李生长期矿质营养元素含量的变化[J]. 园艺学报, 31(2): 165-168. |
牛正田, 李涛, 菅根柱, 等. 2005. 黄连木资源概况、栽培技术及综合利用前景[J]. 经济林研究, 23(3): 68-7. |
彭涛, 李鹏民, 贾裕娇, 等. 2006. 介绍两种无损伤测定植物活体叶片色素含量的方法[J]. 植物生理学通讯, 42(1): 83-86. |
秦飞, 郭同斌, 刘忠刚, 等. 2007. 中国黄连木研究综述[J]. 经济林研究, 25(4): 90-96. |
石进朝, 陈兰芬. 2007. 花叶毛白杨组织培养的研究[J]. 西北林学院学报, 22(4): 90-94. |
孙艳华. 2008. 如何通过Photoshop的两类模式控制色形[J]. 印刷质量与标准化, (8): 10-15. |
仝月澳, 周厚基. 1982. 果树营养诊断法[M]. 北京: 农业出版社: 112-115.
|
王庆菊, 胡艳丽, 李晓磊, 等. 2007. 紫叶稠李叶片不同叶序花青苷与化学成分的相关性[J]. 山东农业大学学报:自然科学版, 38(4): 557-560. |
于晓南, 张启翔. 2002. 观赏植物的花色素苷与花色[J]. 林业科学, 38(3): 147-152. DOI:10.11707/j.1001-7488.20020326 |
于晓南, 张启翔. 2000. 彩叶植物多彩形成的研究进展[J]. 园艺学报, 27(增刊): 533-538. |
俞禄生. 2003. 冬季彩色苗木新品种及其在园林中应用[J]. 中国花卉园艺, 4(7): 20-21. |
张学英, 张上隆, 骆军, 等. 2004. 果树花色苷合成研究进展[J]. 果树学报, 21(5): 456-460. |
赵世杰, 史国安, 董新纯. 2002. 植物生理学实验指导[M]. 北京: 中国农业科学技术出版社: 84-99.
|
Deal D L. 1990. Leaf color retention, dark respiration, and growth of red-leafed Japanese maples under high night temperature[J]. J Amer Soc Hort Sci, 115(l): 135-140. |
Lichtenthaler H K, Wellburn A R. 1983. Determinations of total carotenoids and chlorophylls a and b of leaf extracts in different solvents[J]. Biochem Soc T, 11: 591-592. DOI:10.1042/bst0110591 |
Oren-Shamir M, Levi-Nissim A. 1997. Temperature effect on the leaf pig-mentation of Cotinus coggyria'Royal Purple'[J]. Journal Horticulture Science, 72(3): 425-432. DOI:10.1080/14620316.1997.11515530 |
Steven A Messenger, Hruby Bett A. 1990. Response of interveinally chlorotic red maple treated with medicaps or by soil acidification[J]. Environ Hort, 8(1): 5-9. |
Yozo Nagrira, Yoshiro Ozeki. 2004. A system in which anthocyanin synthesis is induced in regererated torenia shoots[J]. J Plant Res, 117: 377-383. DOI:10.1007/s10265-004-0170-6 |
Zhang Z Q, Pang X Q. 2001. Role of ant hocyanin degradation in litchi pericarp browning[J]. Food Chemistry, 75: 217-221. DOI:10.1016/S0308-8146(01)00202-3 |
 2010, Vol. 46
2010, Vol. 46