文章信息
- 宋恩慧, 蔡诚, 魏国, 高慧, 项艳
- Song Enhui, Cai Cheng, Wei Guo, Gao Hui, Xiang Yan
- RNA干涉培育低木质素杨树
- Cultivation of Low Lignin Poplar by RNA Interference
- 林业科学, 2010, 46(2): 39-44.
- Scientia Silvae Sinicae, 2010, 46(2): 39-44.
-
文章历史
- 收稿日期:2008-11-25
-
作者相关文章
杨树(Populus)是世界上分布最广、适应性最强的树种,主要分布在欧洲、亚洲、北美洲的温带、寒带及地中海沿岸国家与中东地区。由于它速生、木材是优良的纸浆原材料而引起广泛关注。木质素是植物体中总量仅次于纤维素的第2大有机物质,占次生物质总量的95%以上,在植物体内具有一定的生理功能(Anterola et al., 2002)。在制浆造纸中,脱出木质素需投入大量化学药品,并产生大量污染环境的废液,且木质素的存在可影响纸浆质量,增加造纸成本,因此采用基因工程技术调控木质素的生物合成,培育低木质素含量的植物新品种,对造纸、纺织和饲草等原料生产来说有重要意义(章霄云等,2006; 梁海泳等,2006; 李金花等,2007)。选择木质素合成的特异途径,即从羟基肉桂基辅酶A酯类到合成木质素单体及其聚合物的过程中涉及的酶作为对象进行遗传操作,可以从根本上降低木质素的含量,从而降低造纸成本以及减少环境污染。肉桂酰辅酶A还原酶(cinnamoyl CoA reductase, CCR)可还原3种羟基肉桂酸的CoA酯,生成相应的肉桂醛,是该酶催化木质素单体生物合成途径的第1个特异步骤,因此对进入木质素合成途径的碳流具有调控作用(Abbott et al., 2002)。目前降低木质素主要采用反义抑制RNA表达,Piquemal等(1998)利用已知的冈尼桉(Eucalyptus gunnii)CCR cDNA序列获得烟草(Nicotiana tabacum)CCR cDNA序列并反义转入烟草中,分析木质素空间分布的结果支持了CCR下调对改善制浆用木材品质的作用。RNAi可以抑制特定基因的表达,有效地使目标基因沉默。研究表明,RNAi广泛存在于从真菌到植物、从无脊椎动物到哺乳动物的各种生物中(Llave et al., 2002; Matzke et al., 2001; Schweizer et al., 2000),利用转基因技术所产生的RNA干涉作用是能稳定遗传的(Chuang et al., 2000),而且转化的RNAi特异性功能DNA片段小,易于获得,有利于研究不同RNAi特异性功能DNA片段干涉效果,其转化后对转化后代农艺性状影响小,遗传稳定性好,正在迅速成为一种基因表达调控的基因工程技术。本文利用优化的农杆菌介导的杨树遗传转化体系(蔡诚等,2008),将肉桂酰辅酶A还原酶RNAi片段表达载体导入南林95杨(Populus × euramericana)中,观察此基因对杨树中木质素合成的影响,旨在探索用这一手段调控植物木质素合成的可行性。
1 材料与方法 1.1 材料南林95杨组培苗,大肠杆菌DH5α、pUCCRNAi载体、pBI121表达载体为安徽农业大学现代生物技术研究室保存,农杆菌LBA4404由安徽农业大学生物质材料与能源实验室惠赠,限制性内切酶及DNA聚合酶、连接酶、Marker λ/HindⅢ、DL2000为TaKaRa公司产品,其他化学试剂均为AR级产品。
1.2 方法 1.2.1 基因组DNA提取及目的片段扩增采集南林95杨新鲜幼嫩叶片提取基因组DNA(汪结明等,2006),根据CCR基因全长基因序列的同源性搜索和比对分析结果设计2对引物,为方便与pUCCRNAi载体连接,在2对引物中分别引入不同的酶切位点,CCR-F: 5′-ACGGGATCCGGTATTG CTATGGAAAGGC-3′(引入BamHⅠ位点); CCR-R: 5′-AAAGTCGACGAGCTCATGGGGTACTCAGGGAAG -3′(引入SalⅠ和SacⅠ位点); CCR-R′: 5′-ACGTCGACTCTAGAATGGGGTACTCAGGGAAG-3′(引入SalⅠ和Xba I位点)。用引物CCR-F, CCR-R及CCR-F, CCR-R′分别对CCR基因进行PCR扩增,扩增条件均为: 94 ℃预变性5 min; 94 ℃ 30 s,63 ℃ 30 s,72 ℃ 30 s,共35个循环; 72 ℃延伸5 min; 4 ℃保温。将PCR产物送上海生工测序并将克隆的基因cDNA序列与GenBank中的序列进行比较。
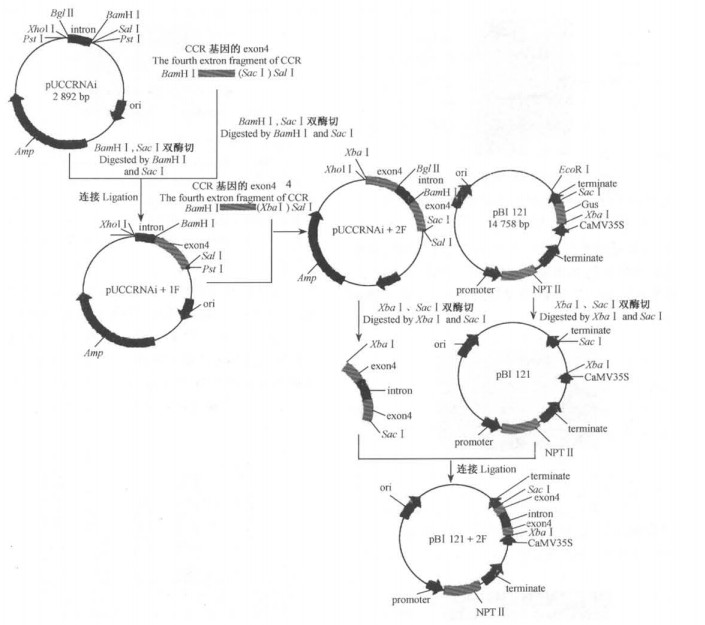
1.2.2 表达载体的构建PCR扩增的CCR基因片段(340 bp)和pUCCRNAi质粒分别用BamHⅠ、SalⅠ酶切、正向连接,得重组质粒pUCCRNAi+1F;重组质粒pUCCRNAi+1F用XhoⅠ,BglⅡ双酶切,PCR扩增片段用BamHⅠ、SalⅠ双酶切,反向连接,构建成含有正反目的片段的pUCCRNAi+2F载体; 用XbaⅠ、SacⅠ双酶切该载体,切出的片段插入到同样酶切的表达载体pBI121中,构建成pBI121+2F表达载体(图 1)。然后用直接导入法将其导入农杆菌LBA4404中。
|
图 1 pBI121+2F载体的构建 Figure 1 Diagram of the construction of pBI121+2F vector F:片段 Fragment. |
叶盘法转化南林95杨,转化体系为外植体预培养7天,在含乙酰丁香酮(Acetosyringone, AS)200 μmol·L-1、OD值为0.6的农杆菌液中侵染20 min,共培养3天,卡那霉素抗性筛选浓度为50 mg·L-1。对转基因植株进行PCR检测,分别对pBI121+2F表达载体中CaMV35S启动子的一段核苷酸、内含子与CCR反向这2个片段进行PCR扩增。检测使用的引物序列分别为: 35S上游引物: 5′-CCACAGATGGT TAGAGAGG -3′; 35S下游引物: 5′-GTCTTGC GAAGGATAGTGG-3′。扩增条件为: 94 ℃预变性5 min; 94 ℃变性30 s、53 ℃退火30 s、72 ℃延伸30 s,共35个循环; 最后72 ℃延伸10 min。内含子+CCR反(I+F)上游引物: 5′-GTACG GACCGTACTACTCT-3′; 内含子+CCR反(I+F)下游引物: 5′-ATGGGGTACTCAGGGAA-3′。扩增条件为: 94 ℃预变性5 min; 94 ℃变性30 s、55 ℃退火30 s、72 ℃延伸30 s,共35个循环; 最后72 ℃延伸10 min。将在PCR检测中显示为阳性的进行Southern杂交检测,Southern杂交检测按Roce公司的DIG杂交试剂盒所示方法进行,杨树总DNA用EcoRⅠ(BamHⅠ)进行酶切,以35S启动子基因片段为模板标记探针,将在检测中均显示为阳性的材料移栽管理。
1.2.4 Klason木质素、综纤维素含量的测定测定Klason木质素及综纤维素含量时,取移栽后生长3个月、生长状态一致的转基因和对照植株。剥去树皮,取茎干,测定Klason木质素与综纤维素含量。每个株系各做1个平行样。Klason木质素的测定按照国家标准GB/T 2677.8-1994,综纤维素的测定按照国家标准GB/T 2677.10-1995进行。
1.2.5 转基因植株纤维长宽比及细胞壁厚度的测定用冰醋酸和30%的双氧水以1:1的比例混合后对同时移栽的转基因植株及对照植株分别进行离析,冲洗干净之后,再用解剖针挑少许置于载玻片上,然后放在100倍的纤维投影仪下测量长度。每一株系测定纤维为200根,精确到0.01 mm。将植株横截面切片在有目镜测微尺的显微镜下测定纤维细胞宽度及双细胞壁厚度,每一株系测定100个。
1.2.6 组织化学染色对转基因植株和对照植株进行Wiesner反应。具体步骤为:将新鲜的木材横截面切片先在2%的间苯三酚溶液中孵育2 min。再用20% HCl封片, 在显微镜下观察、拍照(Coleman et al., 2008)。
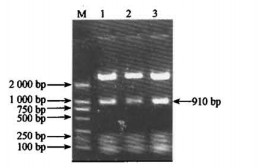
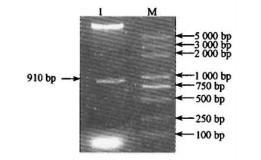
2 结果与分析 2.1 PBI121+2F表达载体的构建把CCR基因扩增出来的正、反向片段分别插入到pUCCRNAi载体,得到pUCCRNAi+2F载体,用XbaⅠ与SacⅠ双酶切,得到910 bp DNA片段,表明干涉片段正反向均已连接到pUCCRNAi载体上(图 2)。将用XbaⅠ与SacⅠ双酶切得到的910 bp DNA片段与同样酶切的PBI121连接,构建成PBI121+2F表达载体,酶切鉴定重组子(图 3),表明构建正确。
|
图 2 载体酶切凝胶电泳 Figure 2 Map of digested vector agarose gel electrophoresis 1, 2, 3: XbaⅠ、SacⅠ双酶切的pUCCRNAi+2F载体pUCCRNAi+2F digested by XbaⅠand SacⅠ; M: DNA marker(DL2000). |
|
图 3 pBI121+2F的酶切验证 Figure 3 Restriction enzyme analysis of pBI121+2F 1.pBI121+2F; M.DNA marker(DL2000 plus). |
用叶盘法对南林95杨进行遗传转化,最后将植株转入到生根培养基,待植株长出健壮的根系后炼苗,3个月后转入大田,共获得抗性植株3株。取转基因植株叶片提取DNA,质粒pBI121+2F为阳性对照,非转化植株为阴性对照,水为空白对照,用设计好的引物进行PCR扩增。从图 4、图 5可以看出,有3株扩增出与阳性对照同样的条带,说明外源基因已经整合到南林95杨中。

|
图 4 转基因植株35S PCR结果 Figure 4 35S segment PCR result of transgenic plants 1-3:转基因植株Transgenic plants; 4:阳性对照Positive plasmid; 5:阴性对照Negative control; 6:空白对照Control; M: DNA marker(EcoRⅠ+HindⅢ). |

|
图 5 转基因植株I+F PCR结果 Figure 5 I+F segment PCR result of transgenic plants 1:空白对照Control; 2:阴性对照Negative control; 3:阳性对照Positive plasmid; 4-6:转基因植株Transgenic plants; M: DNA marker(DL2000). |
将PCR结果显示阳性的转基因植株进行Southern杂交检测,用非转基因植株作为阴性对照,含PBI121+2F的农杆菌LBA4404质粒作为阳性对照,杂交分析结果(图 6)显示,以35S基因片段为探针,转基因植株均出现杂交信号,而未转基因植株未出现杂交信号,此结果表明目的基因已成功地整合到转基因植株基因组中。

|
图 6 转基因植株Southern杂交检测 Figure 6 Southern blotting analysis of transgenic plants 1:阳性对照Positive plasmid; 2,4,6:转基因植株1,2,3被BamHⅠ酶切Transgenic plant 1, 2, 3 digested by BamHⅠ, respectively; 3, 5, 7:转基因植株1, 2, 3被EcoRⅠ酶切Transgenic plant 1, 2, 3 digested by EcoRⅠ, respectively; 8:阴性对照被EcoRⅠ酶切Negative control digested by EcoRⅠ. |
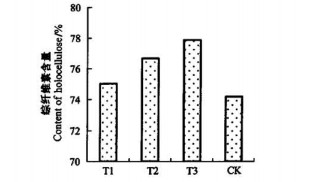
图 7、图 8显示了植株的Klason木质素及综纤维素的平均测定结果:对照植株的Klason木质素含量为20.48%, 转基因株系中木质素含量分别为19.52%,18.13%和17.73%, 平均比对照降低了9.86%;对照植株的综纤维素含量为74.18%,转基因植株中的综纤维素含量分别为75.03%,76.67%和77.89%,平均比对照增加了3.17%。

|
图 7 Klason木质素含量 Figure 7 Contents of Klason lignin T1, T2, T3:转基因植株Transgenic plants; CK:对照植株Control plant. |
|
图 8 综纤维素含量 Figure 8 Contents of holocellulose T1, T2, T3:转基因植株Transgenic plants; CK:对照植株Control plant. |
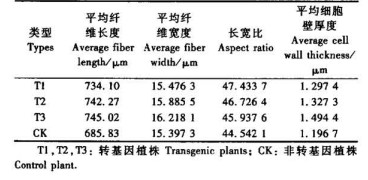
纤维长宽比是影响纸张质量的一个重要的指标,一般认为纤维长宽比越大越有利于造纸,而纤维素含量与细胞壁厚度呈正相关。由表 1可知,转基因植株的纤维长宽比明显高于非转基因植株,这说明转基因植株更适合于造纸,而转基因植株细胞壁的增厚也从侧面反映出纤维素含量的增加。
|
|
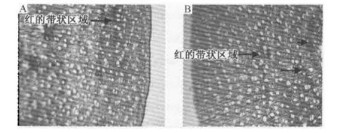
对转基因植株以及对照进行Wiesner染色反应。Wiesner反应主要是对醛类物质特异性染色,反应中染色的深浅一般粗略地反映了木质化部位的木质素总含量(赵华燕等,2002)。对木质素降低幅度大的转基因植株进行组织化学染色,结果(图 9)显示:转基因植株着色区域明显少于非转基因植株,且区域变窄,表明转基因植株的木质素含量低于对照,与Klason木质素测定结果相一致。图 10是转基因植株的生长状态图,表明虽然木质素含量明显降低,但植株生长状态良好。
|
图 9 转基因植株与对照植株的Wiesner反应 Figure 9 Wiesner in trangenic plant and control plant A.转基因植株Transgenic plant; B.对照植株Control plant. |

|
图 10 移栽半年的植株生长状况 Figure 10 The growth of plants transplanted for half a year A.转基因植株Transgenic plant; B.对照植株Control plant. |
杨树是我国主要的纸浆用材树种,利用现代生物技术调节植物木质素的生物合成不仅利于阐明木质素及其他苯丙酸途径衍生物合成的分子机理,而且在优良造纸原料与饲草的生产上具重要应用意义。值得考虑的是,由于木质素重要的生物学功能,降低木质素含量虽利于资源植物的利用,但会给植物自身生长带来不利影响,削弱植物对外界不良环境因素的抵抗,因此木质素在一定范围内的降低须同时兼顾植株的正常生长则更利于造纸工业的需求。本文首次选用肉桂酰辅酶A还原酶CCR基因构建RNAi片段表达载体,将其导入南林95杨,对通过卡那霉素筛选获得的再生植株进行PCR检测及Southern杂交分析证明,CCR基因RNAi片段已整合到南林95杨基因组中,并成功获得了木质素含量明显降低、综纤维素含量增加的转基因植株,且植株生长状态良好,这与之前有关反义抑制CCR基因表达导致植株不能正常生长的报道相矛盾(Piquemal et al., 1998),这可能是由于反义抑制所需目的片段较长,在抑制CCR基因表达的同时也抑制了与CCR基因同源性很高的其他基因所造成的,而在构建RNAi载体的时候,干涉片段只要200~500 bp就足够了,完全可以找出基因的保守的序列作为干涉片段。转基因的目的就是为了获得更适宜造纸的杨树,因此又对其各个造纸指标进行了分析,经过Klason木质素及综纤维素的测定发现其木质素含量明显降低,纤维素含量有一定的提高,这可能是由于木质素含量的降低导致纤维素含量补偿性的增加,进一步证明了CCR基因对木质素合成途径的碳流具有调控作用。纤维长度是评价纤维原料品质的一个重要的指标,它不仅与纸张撕裂度成直线关系,而且长度大有利于提高纸张的抗张强度、耐破度及耐折度。纸张强度实际上是由纤维本身的强度和纤维之间的结合强度决定的。纤维越长,越柔软,纤维就有越多的接触点,交织能力就越强。一般认为纤维宽度对纸张质量无直接影响,但纤维宽度直接影响到纤维的长宽比,纤维长宽比是影响纸张质量的一个重要的指标,一般认为纤维长宽比越大越有利于造纸,而纤维素含量与细胞壁厚度呈正相关,因此又对其纤维长度进行了分析,结果表明转基因杨树的纤维长度以及纤维长宽比均明显大于非转基因植株,表明其更有利于造纸,这就为选育新型的更适于造纸的资源树种开辟了新途径。
蔡诚, 吴大强, 纵方, 等. 2008. 正交设计在杨树最佳遗传转化体系的建立[J]. 核农学报, 22(2): 136-140. |
李金花, 张绮纹, 牛正田, 等. 2007. 木质素生物合成及其基因调控的研究进展[J]. 世界林业研究, 20(1): 29-37. |
梁海泳, 夏秀英, 冯雪松. 2006. UGPase和反义4CL基因对转基因烟草纤维素和木质素合成的调控[J]. 植物生理学通讯, 42(6): 1067-1072. |
汪结明, 项艳, 沈周高, 等. 2006. 杨树基因组DNA提纯方法的优化及其RAPD鉴定[J]. 中国农学通报, 22(5): 59-62. |
章霄云, 郭安平, 贺立卡, 等. 2006. 木质素生物合成及其基因调控的研究进展[J]. 分子植物育种, 4(3): 431-437. |
赵华燕, 魏建华, 张景昱, 等. 2002. 控制COMT与CCoAOMT调控植物木质素的生物合成[J]. 科学通报, 47(8): 604-607. |
Abbott J C, Barakate A, Pincon G, et al. 2002. Simultaneous suppression of multiple genes by single transgenes[J]. Plant Physio1, 128: 844-853. DOI:10.1104/pp.010698 |
Anterola A, Lewis N. 2002. Trends in lignin modification: A comprehensive analysis of the effects of genetic manipulations/mutations on lignification and vascular integrity[J]. Phytoehemistry, 61: 22l-294. |
Chuang Choufen, Meyerowite E M. 2000. Specific and heritable genetic interference by double-stranded RNA in Arobidopsis thaliana[J]. Proc Natl Acad Sci USA, 97: 4985-4990. DOI:10.1073/pnas.060034297 |
Coleman H D, Park J Y, Nair R, et al. 2008. RNAi-mediated suppression of p-coumaroyl-CoA3′-hydroxylase in hybrid poplar impacts lignin deposition and soluble secondary metabolism[J]. PNAS, 105(11): 4501-4506. DOI:10.1073/pnas.0706537105 |
Llave C, Xie Z, Kasschau K D, et al. 2002. Cleavage of Scarecrow-like mRNA targets directed by a class of Arabidopsis mRNA stability in Arabidopsis[J]. Science, 297: 2053-2056. DOI:10.1126/science.1076311 |
Matzke M, Matzke A J, Kooter J M, et al. 2001. RNA-based silencing strategies in plants[J]. Curr Opin Genet Dev, (11): 221-227. |
Piquemal J, Lapierre C, Myton K, et al. 1998. Down-regulation of cinnamoyl-CoA reductase induces significant changes of lignin profiles in transgenic tobacco plants[J]. Plant J, 13: 71-83. |
Schweizer P, Pokorny J, Schulze-Lefert P, et al. 2000. Double-stranded RNA interferes with gene function at the single-cell level in cereals[J]. Plant J, 24(6): 895-903. DOI:10.1046/j.1365-313x.2000.00941.x |
 2010, Vol. 46
2010, Vol. 46