文章信息
- 谢寅峰, 王莹, 张志敏, 方升佐, 王纪
- Xie Yinfeng, Wang Ying, Zhang Zhimin, Fang Shengzuo, Wang Ji
- 青钱柳子叶不定根的发生机制
- Preliminary Studies on Mechanism of Cotyledon Adventitious Root Formation of Cyclocarya paliurus
- 林业科学, 2009, 45(12): 72-76.
- Scientia Silvae Sinicae, 2009, 45(12): 72-76.
-
文章历史
- 收稿日期:2009-01-20
-
作者相关文章
青钱柳(Cyclocarya paliurus)系双子叶植物纲(Dicotyledoneae)胡桃科(Juglandaceae)青钱柳属乔木树种,为我国重点保护的单种属珍稀特有濒危植物之一(郭春兰等,2008),是集药用、材用和观赏等多种价值于一身的珍贵树种(尚旭岚等,2007),具有很高的保护和开发应用价值。但是青钱柳的繁殖困难,主要表现为:1)种子具有深休眠特性,休眠期长达2年,在时间上影响了其繁育进程;2)种子败育很严重,人工育苗出苗率低;3)扦插繁殖难生根,成活率很低(上官新晨等,2006)。这严重影响了青钱柳的开发利用和产业化进程,因此,青钱柳生根及快繁技术的研究对青钱柳资源的开发利用具有重要意义,但青钱柳快繁技术研究难度很大,有关报道甚少,国内外至今尚未建立青钱柳快繁技术体系,其中生根难是其关键技术瓶颈,试管生根研究至今尚未见报道。
由于子叶具有良好的发生不定根潜力和诱导的规律性,加之取材容易,诱导方法简单和重复性好,成为研究难生根木本植物不定根发生较好的模式材料(裴东等,2002)。本试验选用青钱柳子叶为材料,通过外源激素调控,在组织培养条件下进行不定根诱导,并对其生根过程中主要内源激素进行分析,探索内源激素与生根之间的内在联系,初步探讨青钱柳的生根机制,为青钱柳试管苗生根提供理论及技术参考。
1 材料与方法 1.1 供试材料及表面灭菌2006年采自贵州种源的种子,用水筛的方式,取沉淀的饱满种子,进行消毒处理。用70%乙醇将种子浸泡1 min,0.2%HgCl2浸泡20 min,无菌水冲洗5遍,无菌水浸泡过夜,每12 h换一次无菌水;48 h后换上0.1%HgCl2浸泡过夜。接种前,70%乙醇浸泡1 min,0.2%HgCl2浸泡20 min,无菌水冲洗5遍备用(以上操作均是在无菌条件下进行)。
1.2 子叶不定根诱导采用单因素试验设计,对诱导子叶不定根的激素及最适质量浓度进行研究。蒸馏水加琼脂空白培养基作对照,处理为:空白培养基分别添加0.01,0.05,0.25,0.75 mg·L-1 ABA和0.5,2.5,5,10 mg·L-1 IBA。
以上培养基中均添加0.65%的琼脂,pH值调至5.7。每个试管内盛15 mL固体培养基,121 ℃高压灭菌20 min;培养温度25 ℃;光照强度约50 μmol·m-2s-1;光周期:光期14 h,暗期10 h;相对湿度50%~70%。
取上述消毒后洗净的种子在无菌条件下剥取离体胚并切除胚轴,立即置于培养基上,每支试管接种一个完整的子叶,每处理接种60支试管。15天后统计子叶生根率、生根条数、根长和愈伤化程度。
生根率(%)=(产生不定根的子叶/未污染子叶总数)×100%,
平均生根条数为产生不定根的子叶生根数目的平均数。
1.3 内源激素含量测定内源激素提取和测定采用酶联免疫法(吴颂如等,1988)。培养基和培养条件同以上子叶不定根诱导,每处理接种140支试管,重复3次。在接种后的前10天,每2天取样1次,第10~15天时每隔3天取样1次,每次分别取20个外植体。在近胚端的子叶伤口处切取3~5 mm组织,重复3次(裴东等,2003),作为测定内源激素生长素(IAA)、脱落酸(ABA)、赤霉素(GA3)、玉米素核苷酸(ZR)含量的样品。
1.4 数据分析用Excel,STST统计分析软件对数据进行处理,用Duncan氏法进行差异显著性检验,其中百分数经反正弦转换。
2 结果与分析 2.1 不同激素对子叶诱导不定根效果的影响表 1的结果显示,不添加激素的对照培养基和加入0.01~0.5 mg·L-1 ABA的培养基中,子叶不定根诱导率均为0,并随着ABA质量浓度的增加,愈伤化程度逐渐加重。IBA的添加对不定根的发生起到不同程度的诱导作用,在0~1.5 mg·L-1质量浓度范围内,随着质量浓度的增加生根率逐渐增加,当IBA 1.5 mg·L-1时,生根率达到100%。每个外植体发根5~10条,15天后平均生根条数(6.5条)和平均根长(1.5 cm)均为最佳。当IBA质量浓度高于1.5 mg·L-1时,随着质量浓度的增加生根率逐渐降低,而愈伤化程度逐渐加重。因此,低质量浓度IBA有利于诱导生根,而高质量浓度IBA有利于诱导愈伤。
|
|
由于添加1.5 mg·L-1 IBA处理子叶不定根发生率达到100%,而对照无不定根发生,因此对它们内源IAA,ABA,GA,ZR含量的动态变化进行分析比较,以探讨内源激素与子叶不定根发生发育的关系。
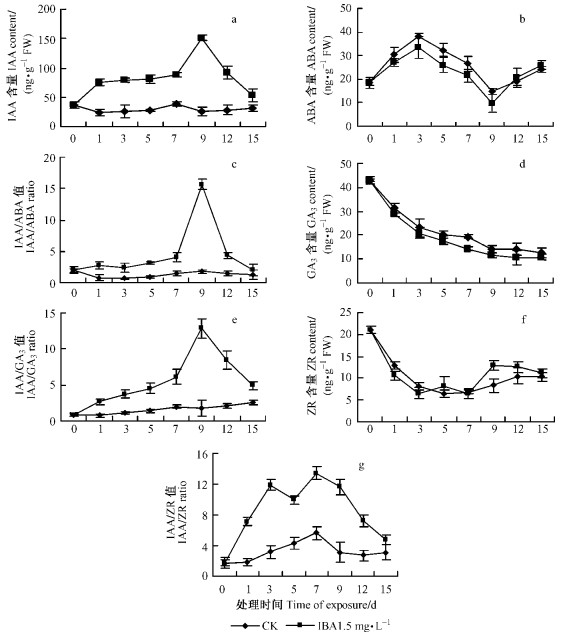
2.2.1 子叶不定根发生及其内源IAA含量变化从图 1a可以看到,加入IBA后,子叶内源IAA含量从36.55 ng·g-1FW增至75.83 ng·g-1FW,增加了1.07倍,而对照内源IAA从36.55 ng·g-1FW降到23.99 ng·g-1FW,下降了34.36%;随后6天内,2种培养基中内源IAA基本无太大变化,直到第9天,加入IBA的培养基中,IAA急剧增至151.15 ng·g-1FW,为初始含量的4.14倍,徒手切片观察显示此时正处于根原基的分化阶段;而未诱导出不定根的空白培养基内源IAA降至25.70 ng·g -1FW,下降了29.69%;随后处于不定根的形成与根的伸长阶段,内源IAA含量逐步降低,直至15天时不定根数量基本稳定;而对照内源IAA含量未表现出明显变化,方差分析显示2处理间内源IAA差异达到极显著水平(F=18.68,F0.01=8.86)。
|
图 1 子叶不定根发生过程中内源激素IAA,ABA,GA3,ZR含量及比值变化 Figure 1 Changes of contents and ratio of endogenous IAA, ABA, GA3, ZR during cotyledon rhizogenesis |
图 1b显示2种处理的内源ABA含量在不定根形成过程中都有一个先上升后下降再上升的过程。并且均在根原基启动时达到了最低值,对照第9天时由起始的18.57 ng·g-1FW降为14.70 ng·g-1FW,IBA处理降为9.67 ng·g-1FW。方差分析显示2处理差异不显著(F=0.47,F0.05=4.6)。在第0~9天内,处理内源ABA含量均低于对照,直到12天后含量开始上升,并且含量超过对照。由此推断,内源ABA对根原基的启动有抑制作用,而外源IBA通过调节内源ABA的相对含量,促进了不定根的形成。
2.2.3 子叶不定根发生及其内源IAA/ABA值变化图 1c显示,对照15天内IAA/ABA值变化较小,第0天时达最大值1.96,第3天达最小值0.67,整个生根过程中内源IAA/ABA值变化不大。而处理IAA/ABA值在0~9天持续增加,直到第9天根原基启动时达到峰值15.63,此后根原基形成与根伸长阶段值逐渐降低至与第0天时基本持平,整个生根诱导与根系伸长阶段,内源IAA/ABA值变化成尖峰型趋势,与对照的变化趋势差别明显。
2.2.4 子叶不定根发生及其内源GA3含量变化图 1d显示出内源赤霉素在不定根诱导过程中基本成下降趋势,对照与处理间差异未达到显著性(F=0.21,F0.05=4.6)。在第0~3天,2处理内源GA3迅速下降,随后的5~15天,内源GA3均缓慢下降,2处理下降趋势一致且差异较小,只是添加外源IBA的GA3含量始终低于对照,据此推断低的GA3水平利于不定根的发生,但内源GA3并不是抑制青钱柳子叶不定根发生的主要因素。
2.2.5 子叶不定根发生及其内源IAA/GA3值变化由图 1e可知,在不定根诱导的前7天,处理IAA/GA3值缓慢上升,到第9天IAA/GA3值明显跃升,达到峰值12.87,增加了14.1倍,随后比值不断下降。而对照整个过程的IAA/GA3值只有不明显的上升趋势,整个过程无峰值出现。无论是IAA/GA3的即时比值还是整体趋势,处理与对照差别明显。与图 1a的趋势基本一致,可以判断主要是IAA的动态变化造成2处理IAA/GA3值之间的差别。
2.2.6 子叶不定根发生及其内源ZR含量变化图 1f显示,在生根诱导的初期,2种处理条件下,内源ZR的含量都有一个急剧下降的过程,其中添加外源IBA的下降趋势更加明显,由20.95 ng·g-1FW降至6.58 ng·g-1FW,之后的4天下降幅度趋于平稳,直到第9天,处理的内源ZR增加至12.98 ng·g-1FW,随后缓慢下降。而对照的变化幅度相对平稳,最低下降到6.52 ng·g-1FW后,又缓慢增长到10.53 ng·g-1FW;2种处理内源ZR的差异未达到显著水平(F=0.07,F0.05=4.6),但在变化趋势上有细微的差异,第9天根原基启动时,处理中内源ZR上升98.5%(对照上升27.3%)。
2.2.7 子叶不定根发生及其内源IAA/ZR值变化从图 1g的曲线变化情况来看,2种处理的内源IAA/ZR值在整个不定根发生过程中表现出先上升再下降的过程,不同的是,对照内源IAA/ZR值成单峰型,峰值出现在第7天,峰值是5.63;处理成双峰型,分别在第3天、第7天达到峰值,分别是11.88,13.43。处理中双峰的出现是由于第5天时,内源ZR有小幅波动。在根原基发生和根的生长过程中,处理内源IAA/ZR值与对照相比,表现出更为明显的下降趋势,直到第15天,降至相近的水平。
3 结论与讨论大量研究表明:在不定根的形成过程中,生长素起着关键作用。外源生长素促进内源IAA积累进而诱导生根,已在多种植物生根研究上获得支持。本研究表明:添加不同质量浓度IBA对青钱柳子叶不定根发生均有一定程度的促进作用,最佳处理质量浓度为1.5 mg·L-1,生根率可达到100%,内源激素分析表明外源IBA显著提高了青钱柳子叶组织内源IAA的水平进而诱导和促进发生不定根,这与前人(Heloir et al., 1996;Gatineau et al., 1997)对核桃(Juglans regia)嫩茎生根的研究结果一致,即外源IBA促进内源IAA积累进而诱导生根。结合青钱柳子叶在对照培养基和添加外源IBA培养基中的IAA动态变化规律和生根结果,可以初步推断在培养或诱导初期,组织内源IAA水平的提高在启动根原基分化中发挥重要作用,不定根的发育与根的伸长只需要相对较低的内源IAA水平。
夏小华(1994)的研究显示,内源GA3含量过高是导致青钱柳插条生根困难的原因之一,而添加外源ABA将有利于抑制过高的内源GA3,可能对生根有促进作用,陆玲等(1992)对黄瓜(Cucumis sativus)子叶不定根的诱导试验也表明外源ABA通过对子叶内源GA3的拮抗,促进了生根。基于上述原因,本文设计了外源ABA对青钱柳子叶不定根的调节作用,但结果并未得到预期的效果,可能与不同材料本身的遗传生理特性差异有关。此外,从子叶不定根诱导中内源ABA的变化趋势也可以看出,不定根启动时,需要较低的内源ABA含量,外源IBA降低了内源ABA而有利于生根。因此,外源ABA的加入,不仅对生根无益,可能还起抑制作用。关于ABA与生根的关系有不同的研究结果,刘桂丰等(2001)发现落叶松(Larix gmelinii)扦插生根的主要抑制物质是内源ABA,而对于需要ABA作为生根促进因子的植物,陆玲等(1992)认为ABA能促进根原基形成,不一定是ABA的直接效应,很可能是通过对赤霉素或细胞分裂素的拮抗而起作用,外源ABA的添加可能确实拮抗了青钱柳子叶内源GA3,并且较低的内源GA3含量可能也有利于不定根的发生(生根诱导过程中GA3呈下降趋势),但从生根(IBA处理)与未生根(对照)的GA3变化的比较可以发现,两者之间并无显著差异,说明GA3可能不是子叶不定根发生中的主要影响因素,由于诱导青钱柳子叶不定根发生过程中内源IAA起主导作用,外源ABA不能提高内源IAA,因此即使拮抗了内源GA3,对子叶不定根发生也无有效促进作用,有关机制尚需进一步研究。
不同内源激素对不定根诱导的作用不一,特别是内源激素之间的平衡(比值)对生根的影响更大(师晨娟等,2006)。外源激素的作用是通过改变各种内源激素的含量变化而达到一个动态平衡来间接诱导不定根的发生和分化(汪天等,2000)。本试验结果也表明,除了IAA对照与处理之间表现出显著差异,其他3种激素(特别是GA3和ABA)两者间差异并不明显。而IAA/ABA,IAA/GA,IAA/ZR值对照与处理之间均有明显差异,根原基的启动与IAA的含量及IAA/ABA,IAA/GA,IAA/ZR值成正相关。ABA与IAA基本呈现出此消彼长的趋势,即根原基启动时,ABA降到最低,IAA含量达到最高;不定根形成与伸长过程中,则出现相反的结果,与詹亚光(2001)、张晓平等(2004)的研究结果基本符合。IAA/ABA值更好的反映出不定根的发生能力,即IAA与ABA的相对含量比单个内源激素的绝对含量对生根的影响更大(张梅春等,2007)。IAA/ABA值较大时,有利于不定根原基的启动,反之则抑制根原基的启动,促进不定根的形成与根的伸长,该结果与郭素娟等(2004)、凌宏勤(2001)、郑均宝(1991)等人提出的IAA/ABA值调控不定根的发生的结论也是一致的。IAA/GA3和IAA/ZR值也比单一GA3和ZR更能反映青钱柳子叶不定根发生过程中内源激素的变化规律。
总之,各内源激素的绝对含量和相对比值与不定根的诱导和发生均有一定关系,青钱柳子叶不定根发生过程中IAA起了关键性的作用,而IAA/ABA,IAA/GA和IAA/ZR值的变化能较好地反映生根启动过程中内源激素间平衡的需求,较高的IAA/ABA,IAA/GA3值有利于不定根的启动和发生,GA3可能不是影响不定根发生的关键因素。青钱柳属于难生根树种,本文以青钱柳子叶为材料主要对不定根的诱导及其生根机制进行了初步探讨,本研究结果为青钱柳组培快繁及生根研究提供参考。
郭春兰, 上官新晨, 蒋艳, 等. 2008. 不同理化因子对青钱柳愈伤组织生长和黄酮类化合物合成的影响[J]. 安徽农业大学学报, 35(3): 430-435. |
郭素娟, 凌宏勤, 李凤兰. 2004. 白皮松插穗生根的生理生化基础研究[J]. 北京林业大学学报, 26(2): 43-48. DOI:10.3321/j.issn:1000-1522.2004.02.009 |
凌宏勤. 2001. 白皮松扦插繁殖技术及生理学和解剖学研究. 北京林业大学硕士学位论文, 45-48. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y403959
|
刘桂丰, 杨传平, 曲冠止, 等. 2001. 落叶松杂种插穗生根过程中4种内源激素的动态变化[J]. 东北林业大学学报, 29(6): 8-18. |
陆玲, 周燮. 1992. ABA与GA3对黄瓜离体子叶和石刁柏茎生根的影响[J]. 植物生理学报, 18(2): 173-178. DOI:10.3321/j.issn:1671-3877.1992.02.008 |
裴东, 袁丽钗, 谷瑞升, 等. 2003. 核桃子叶不定根发生调控的研究[J]. 林业科学, 39(6): 33-40. DOI:10.3321/j.issn:1001-7488.2003.06.006 |
裴东, 袁丽钗, 奚声珂, 等. 2002. 核桃品种试管嫩茎生根的研究[J]. 林业科学, 38(3): 32-38. |
上官新晨, 郭春兰, 蒋艳, 等. 2006. 培养基和植物激素对青钱柳茎段和叶片愈伤组织诱导的研究[J]. 江西农业大学学报, 28(5): 678-682. DOI:10.3969/j.issn.1000-2286.2006.05.009 |
尚旭岚, 徐锡增, 方升佐. 2007. 青钱柳离体胚的培养及快速繁殖[J]. 南京林业大学学报:自然科学版, 31(1): 101-104. |
师晨娟, 刘勇, 王春城, 等. 2006. 青海云杉扦插的年龄效应及其生根机理研究[J]. 西北农林科技大学学报:自然科学版, 34(12): 101-104. |
汪天, 许成林, 何云核. 2000. 黄刺玫插穗生根能力及其机理的探讨[J]. 安徽农业大学学报, 27(3): 221-224. DOI:10.3969/j.issn.1672-352X.2000.03.004 |
吴颂如, 陈婉芬, 周燮. 1988. 酶联免疫法(ELISA)测定内源植物激素[J]. 植物生理学通讯, 25(5): 53-57. |
夏小华. 1994. 神茶原料青钱柳扦插繁殖试验初报[J]. 蚕桑茶叶通讯, (2): 12-14. |
詹亚光, 杨传平, 金贞福, 等. 2001. 白桦扦插生根的内源激素和营养物质[J]. 东北林业大学学报, 29(4): 1-4. DOI:10.3969/j.issn.1000-5382.2001.04.001 |
张梅春, 敖曼, 孙万吉, 等. 2007. 紫杉扦插插穗生根机理的研究[J]. 辽宁林业科技, 33(2): 33-35. DOI:10.3969/j.issn.1001-1714.2007.02.011 |
张晓平, 方炎明, 黄绍辉. 2004. 杂种鹅掌楸扦插生根过程中内源激素的变化[J]. 南京林业大学学报:自然科学版, 28(3): 79-82. |
郑均宝. 1991. 几种木本植物插穗生根与内源IAA, ABA的关系[J]. 植物生理学报, 17(3): 313-316. DOI:10.3321/j.issn:1671-3877.1991.03.005 |
Gatineau F, Fouche J G, Kevers C. 1997. Quantitative variations of indolyl compounds including IAA, IAA-aspartate and serotonin in walnut microcuttings during root induction[J]. Biol Plant, 39: 131-137. DOI:10.1023/A:1000377511120 |
Heloir M C, Kevers C, Hausman J F, et al. 1996. Changes in the concentrations of auxins and polyamines during rooting of in-vitro-progagated walnut shoots[J]. Tree Physiology, 16(5): 515-519. DOI:10.1093/treephys/16.5.515 |
 2009, Vol. 45
2009, Vol. 45

