文章信息
- 何永涛, 石培礼, 徐玲玲.
- He Yongtao, Shi Peili, Xu Lingling
- 拉萨-林芝植被样带不同群落类型的细根生物量
- Biomass of Fine Root in Different Community Type on the Tibetan Vegetation Transect
- 林业科学, 2009, 45(10): 148-151.
- Scientia Silvae Sinicae, 2009, 45(10): 148-151.
-
文章历史
- 收稿日期:2008-04-18
-
作者相关文章
2. 国家气象中心生态与农业气象室 北京 100081
2. National Meteorological Center of China Meteorological Administration Beijing 100081
细根通常是指植被地下根系中直径小于2 mm的根,其生产和周转直接影响着整个生态系统的碳平衡和养分循环。在森林生态系统中约3%~84%(大部分为10%~60%)的净初级生产力被用于细根的生产(张小全等,2001);而细根的周转则是森林土壤C累积的最大输入量,如果忽略细根的生产、死亡和分解,土壤有机物质和养分元素的周转将被低估20%~80%(Vogt et al., 1986;1996)。然而,由于地下根系分布不均匀,而且被土壤覆盖,这就增加了对根系研究的难度,在以往的植被生态学研究中根系往往都成了人们回避的问题(黄建辉等,1999)。但是随着全球气候变化的日益突出,生态系统碳平衡成了目前生态学研究中的热点问题,而细根在其中的作用也成了人们关注的焦点(Nadelhoffer et al., 1992;Rasse et al., 2001;Matamala et al., 2003;Majdi et al., 2005;杨丽韫等,2007)。
青藏高原被称为“世界第三极”,沿海拔梯度依次分布着不同的群落类型,从高海拔地区的高寒荒漠草甸一直到亚热带常绿阔叶林都有分布。长期以来,由于受交通条件和自然环境的限制,该地区的自然植被尚未受到人类活动过多的干扰,加之该地区又处于全球变化的敏感地区,这就为我们提供了难得的研究场所。关于青藏高原地区植被生物量的研究也已经有了初步的结果(罗天祥等,1998;1999;2002;Luo et al., 2002),但对森林中细根生物量的研究尚未见报道。因此本研究选择拉萨-林芝植被样带上几类典型的森林群落作为研究对象,通过土钻法对其细根生物量进行初步研究,探讨细根沿海拔梯度在不同林地中的分布格局,为估计青藏高原地区植被在全球碳循环中的作用提供基础数据。
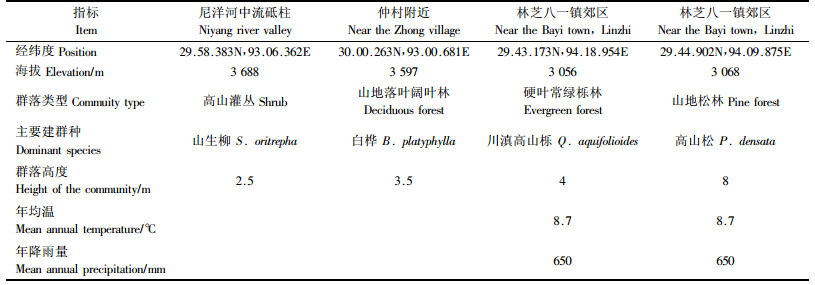
1 研究地区概况拉萨-林芝植被样带最高处为海拔5 025 m的米拉山口,最低处为海拔3 000 m的林芝八一镇,该样带上沿海拔梯度依次分布有高寒草甸、高山灌丛、山地落叶阔叶林、温性硬叶常绿栎林和山地松林等不同群落类型的植被。沿海拔梯度依次选择了其中林地的典型代表类型共计4个,分别是山生柳(Salix oritrepha)灌丛、白桦(Betula platyphylla)林、高山松(Pinus densata)林、川滇高山栎(Quercus aquifolioides)林,取样地点和具体林地概况如表 1所示。
|
|
采用土钻(内径3.5 cm)取样法。取样时间为2003年8月,此时为青藏高原植被生长的盛季。具体取样方法为:在每块林地按照平均木的标准分别选取优势树种,即在山生柳灌丛内选取山生柳,白桦林内选取白桦,高山松林内选取高山松,川滇高山栎林内选取川滇高山栎,以各树种各选取7~10株,各样地的具体取样概况见表 2。在每株平均木树冠边缘与其树干基部连线的1/2处,分4个方向打取4个土钻。每个土钻按10 cm进行分层取样,取至50 cm;将每株平均木的4个土钻样品分别按照同一土层进行混合。
|
|
取回的细根样品放入冰箱内保存。对每一个细根样品先浸泡1天后,用筛孔为0.2 mm的筛子反复淘洗。洗净土壤后放入蒸发皿中,用镊子将细根(直径≤2 mm)从杂质中分离,去除草本植物的根系,同时依据根系的颜色、外形、弹性等特征,结合漂浮法对根系进行死活的区分。
细根区分后,装入纸袋并标记,在60 ℃的恒温下烘干至恒质量,然后用精度为0.000 1的分析天平称质量,按以下公式计算细根生物量:
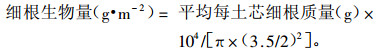
|
统计出每一样品的细根生物量,再将每株树木4个取样点的数值平均作为每株树木不同深度的活根和死根生物量;然后按照每个样地取样的树木株数,分别计算出每一样地活根和死根生物量的平均值和标准差。
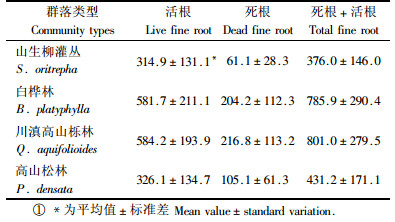
3 结果 3.1 不同群落的细根生物量结果表明,在调查的4类林地中,细根生物量最高的是2类矮林,即川滇高山栎林和白桦林地,细根生物量达到了近800 g·m-2;其次是高山松疏林,细根的生物量为(431.2±171.1) g·m-2;山生柳灌丛的细根生物量则相对较小,为(376.0±146.0)g·m-2(表 3)。
|
|
从活细根的生物量来看,仍以白桦林和川滇高山栎林的活细根生物量为多,分别达到了(581.7±211.1) g·m-2和(584.2±193.9)g·m-2,而山生柳灌丛和高山松林二者的活细根生物量则非常接近,分别为(314.9±131.1)g·m-2和(326.1±134.7)g·m-2。死细根生物量的分布则表现出了与细根现存总量相同的趋势,即2类矮林最高,其次是高山松疏林,山生柳灌丛则最低。
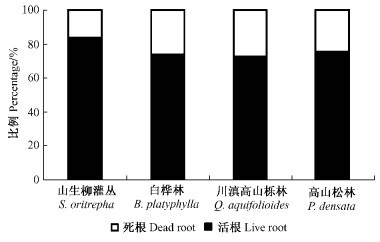
以死根和活根在细根中所占的比例统计,则活根在现在细根生物量中都占据了绝对的优势,均超过了70%,其中比例最高的是山生柳灌丛,83.8%。其他3类林地活根所占的比例则都相差不大,均在75%左右(图 1)。
|
图 1 不同林地死细根与活细根的比例 Figure 1 Ratio of live fine root and dead fine root |
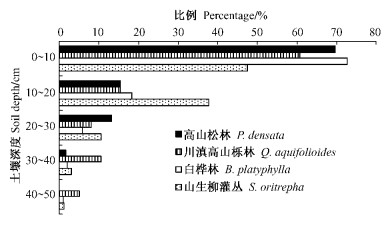
细根在不同林地土壤中的垂直分布总体表现为,细根生物量集中分布在土壤的表层,尤其是0~10 cm以内,且随着土层的加深而逐渐减少。0~10 cm的土层内集中了各林地中的的大部分细根,其中除山生柳灌丛较少外,为47.4%,其他3类林则都超过了总量的60%,其中白桦林为72.7%,高山松林为69.6%,川滇高山栎林为60.6%。而若以0~20 cm土层内的细根生物量来看,则集中了其细根生物总量的3/4(图 2)。
|
图 2 不同林地细根生物量的垂直分布 Figure 2 Vertical distribution of fine root in different soil layers |
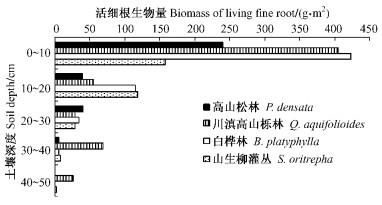
活细根在各林地中的垂直分布也表现出了相似的趋势,即大部分根系都分布在土壤的最上一层,即0~10 cm。其中在山生柳灌丛和白桦林10~20 cm的土壤中,仍然存在着密度较高的活细根,分别达到了118.3 g·m-2和115.4 g·m-2。随着土层的加深,活细根的密度则迅速降低,当土壤深度达到30 cm以下,除川滇高山栎林外,其他3类林地土壤中的活细根密度已经都低于10 g·m-2。其中高山松林土层较为浅薄,其40~50 cm土层内已没有细根的存在。而川滇高山栎林的活细根则在30~40 cm时又出现了一个丰富层,活细根生物量达到了69.0 g·m-2,甚至高于10~20 cm的土层,其在40~50 cm时的活细根密度仍然达到了26.1 g·m-2(图 3),这可能与该区域土层深厚有关。
|
图 3 不同土层活细根的垂直分布 Figure 3 Vertical distribution of live fine root in different soil layers |
与活细根生物量的垂直分布格局相类似,死细根在各林地中的分布也表现为集中分布在上层,随着土层的深入而迅速减少,但各类林地又有各自的特点。山生柳灌丛死细根的密度高峰并不是出现在土壤的最上层,而是出现在10~20 cm的土壤中;白桦林的死细根则集中出现在0~10 cm的土层中,占所有死亡细根的72.3%;而川滇高山栎林的死细根则表现为随着土层的加深而逐渐减少的趋势。高山松林的死细根主要出现在0~30 cm的土层中,在30 cm以下的土层中存在的死细根量极少,30~40 cm土层中的细根为仅为1.1 g·m-2,而40 cm以下的土层中则没有细根的存在(图 4)。

|
图 4 不同土层死细根的垂直分布 Figure 4 Vertical distribution of dead fine root in different soil layers |
由于生长环境的差异往往会导致植物产生不同的生存对策,从而也会影响到森林生态系统中对能量和物质的分配,而细根控制着森林生态系统主要的营养物质吸收和周转,因此其生物量大小可反映出生态系统在不同环境条件下的生长适应对策。在本研究中,按群落外貌可将这4类林地分为3类,即灌丛(山生柳灌丛)、矮林(白桦林和川滇高山栎林)以及疏林(高山松林)。而其细根的生物量分布也呈现出不同的特征,其中2类矮林较为接近,其细根生物量分别为(785.9±290.4) g·m-2和(801.0±279.5)g·m-2,而灌丛和高山松疏林则较为接近。这说明在相似的生长条件下,不同的植被群落有不同的生活对策,不同森林生态系统将光合作用产生的能量分配给不同的组成部分,从而导致了细根生物量的差异,而这种差异又产生了不同的植被生活型;不同生长条件下具有相似生活型的植被则具有类似的生长适应对策。这提示我们在以后的研究中应进一步分析细根生长与其具体环境之间的关系,以探讨细根在与环境之间相互作用的机制和意义。
黄建辉, 韩兴国, 陈灵芝. 1999. 森林生态系统根系生物量研究进展[J]. 生态学报, 19(3): 270-277. DOI:10.3321/j.issn:1001-9332.1999.03.004 |
罗天祥, 李文华, 冷允法, 等. 1998. 青藏高原自然植被总生物量的估算与净初级生产量的潜在分布[J]. 地理研究, 17(4): 337-344. DOI:10.3321/j.issn:1000-0585.1998.04.001 |
罗天祥, 李文华, 罗辑, 等. 1999. 青藏高原主要植被类型生物生产量的比较研究[J]. 生态学报, 19(6): 823-831. DOI:10.3321/j.issn:1000-0933.1999.06.010 |
罗天祥, 石培礼, 罗辑, 等. 2002. 青藏高原植被样带地上部分生物量的分布格局[J]. 植物生态学报, 26(6): 668-676. DOI:10.3321/j.issn:1005-264X.2002.06.006 |
杨丽韫, 罗天祥, 吴松涛. 2007. 长白山原始阔叶红松(Pinus koraiensis)林及其次生林细根生物量与垂直分布特征[J]. 生态学报, 27(9): 3609-3617. DOI:10.3321/j.issn:1000-0933.2007.09.008 |
张小全, 吴可红. 2001. 森林细根生产和周转研究[J]. 林业科学, 37(3): 126-138. DOI:10.3321/j.issn:1001-7488.2001.03.021 |
Luo T X, Li W H, Zhu H Z. 2002. Estimated biomass and productivity of natural vegetation on the Tibetan Plateau[J]. Ecological Applications, 12(4): 980-997. DOI:10.1890/1051-0761(2002)012[0980:EBAPON]2.0.CO;2 |
Matamala R, Gonzalez-Meler M A, Jastrow J D, et al. 2003. Impacts of fine root turnover on forest NPP and soil C sequestration potential[J]. Science, 302: 1385-1387. DOI:10.1126/science.1089543 |
Majdi H, Pregitzer K, Moren A S, et al. 2005. Measuring fine root turnover in forest ecosystems[J]. Plant and Soil, 276: 1-8. DOI:10.1007/s11104-005-3104-8 |
Nadelhoffer K J, Raich J W. 1992. Fine root production estimates and belowground carbon allocation in forestry ecosystems[J]. Ecology, 73: 1139-1147. DOI:10.2307/1940664 |
Rasse D P, Longdoz B, Ceulemans R. 2001. TRAP: a modeling approach to below-ground carbon allocation in temperate forests[J]. Plant and Soil, 229: 281-293. DOI:10.1023/A:1004832119820 |
Vogt K A, Crier C C, Vogt D J. 1986. Production, turnover, and nutrient dynamics of above-and belowground detritus of world forests[J]. Advance Ecology Research, 15: 303-377. DOI:10.1016/S0065-2504(08)60122-1 |
Vogt K A, Vogt D J, Palmioto P A. 1996. Review of root dynamics in forest ecosystems grouped by climate, climatic forest type and species[J]. Plant and Soil, 187: 159-219. |
 2009, Vol. 45
2009, Vol. 45