文章信息
- 李玉灵, 王玉魁, 王俊刚, 三木直子, 坂本圭児, 吉川賢.
- Li Yuling, Wang Yukui, Wang Jungang, Miki Naoko, Sakamoto Keiji, Yosikawa Ken
- 水分胁迫条件下臭柏匍匐茎的蒸腾和吸水特性
- Transpiration and Water Uptake of Sabina vulgaris Stolon under Water Stress
- 林业科学, 2009, 45(9): 48-52.
- Scientia Silvae Sinicae, 2009, 45(9): 48-52.
-
文章历史
- 收稿日期:2008-09-24
-
作者相关文章
2. 国家林业局泡桐研究开发中心 郑州 450003;
3. 日本冈山大学大学院环境学研究科 冈山 7008530;
4. 北京林业大学水土保持学院 北京 100083
2. Paulownia Research & Development Center of the State Forestry Administration Zhengzhou 450003;
3. Grad Sch Env Sci, Okayama Univ Okayama Japan 7008530;
4. College of Soil and Water Conservation, Beijing Forestry University Beijing 100083
毛乌素沙地位于我国鄂尔多斯高原中部,20世纪60年代以来由于过牧和过垦,导致大片土地的荒漠化。为改善和防止荒漠化的继续扩展,人们不断地实施植物固沙,并取得了一些效果,但水分是该地区植被恢复与重建的最大限制因子,盲目的人为绿化活动会加剧土壤干旱。所以,利用低耗水乡土树种,恢复原有植被是人们所期待的(吉川賢,1995)。
臭柏(Sabina vulgaris)是毛乌素沙地唯一天然匍匐针叶灌木,从土壤水分条件较好的丘间低地到土壤较为干旱的固定沙地均有连片分布,具有很高的防风固沙价值和药用价值,是毛乌素沙地等半干旱地区的优良造林树种(Kang et al., 2003;吉川賢等,2004),引起国内外学者的关注,并就其生理生态学特性进行诸多研究(王林和等,1998;吉川賢,1998;温国胜等,2002;张国盛等,2004;2005),但有关臭柏群落拓展机制的研究尚未见报道。
臭柏在幼树阶段是直立生长的,当枝高达到30~40 cm时,转为匍匐生长,形成匍匐茎,匍匐茎触地生长,经沙埋后匍匐茎上的不定根原基发育能生出大量的不定根(王林和等,2002),此时匍匐茎和其地上枝条、地下不定根构成了一个潜在的克隆分株。伴随克隆分株不断扩展、伸长,匍匐茎上小枝也不断生长壮大,一定时间后触地并产生不定根,成为下一级克隆分株匍匐茎。这样周而复始,匍匐茎纵横交错,不断向外延伸,最后地上、地下逐渐趋于郁闭形成单一的臭柏纯林。匍匐茎的形成和不定根的出现是臭柏进入成年阶段的主要形态标志。在臭柏群落的发展过程中携有不定根的匍匐茎在不同土壤条件下的克隆生长和拓展起了决定性的作用,可以认为匍匐茎对于异质土壤生境有其特殊的适应策略。特别是匍匐茎主根区和不定根区处于异质土壤水分生境时,不定根可能缓解匍匐茎整体的干旱胁迫,匍匐茎上不同部位小枝或许有不同耐旱策略。本研究以成木阶段臭柏匍匐茎上小枝的蒸腾、吸水为主要研究内容,通过有无不定根匍匐茎及其匍匐茎不同部位小枝的水分生理特性的比较,研究臭柏匍匐茎对干旱胁迫的适应性,进而阐述臭柏群落在拓展过程中对干旱环境的适应策略,为半干旱地区植被恢复与重建中植物种的选择提供参考依据。
1 材料与方法 1.1 试验材料供试材料是1995年从内蒙古林学院带往日本冈山大学苗圃培育的扦插苗,生根扦插苗于1996年12月11日移植于石砾土栽培装置中,该装置1 h自动灌水1次,循环利用(图 1)。移植后为保证苗木成活,首先只用Hogland培养液水培。

|
图 1 石砾土栽培装置 Figure 1 Water cultivation system |
水分胁迫处理开始于1997年6月12日,水分胁迫区共12株在培养液中加入PEG(polyethylene glycol,分子质量6 000),用来调节溶液渗透势。共2个对照区15株只供给培养液,溶液渗透势近似为0.0 MPa(pF2.3);水分胁迫区每升培养液中加入50 g PEG,溶液渗透势为-0.1 MPa (pF3.0)。毛乌素沙地固定沙丘天然分布臭柏群落的土壤pF值为2.8~3.8(增田拓郎等,1998),丘间低地pF值为2.3左右(温国胜等,2000),因此水分胁迫区和对照区的水分条件基本反映了臭柏天然分布的固定沙丘和丘间低地的土壤水分条件。为减少由于蒸发和植物营养的吸收所引起的培养液浓度及养分构成变化的影响,每6周换1次培养液。
1.2.2 人工培养不定根试验为模拟毛乌素沙地匍匐茎生长特性,在2002年4月进行不定根培养试验。将上述对照区和水分胁迫区臭柏匍匐茎的中间部位埋于充填沙土的长方形花盆中(23 cm×54 cm×23 cm),使不定根强制发生。用于培养不定根的土壤始终保持湿润条件,也就是主根区土壤水分条件有对照和水分胁迫2个处理区各6株,而不定根所处土壤水分条件始终是湿润条件。
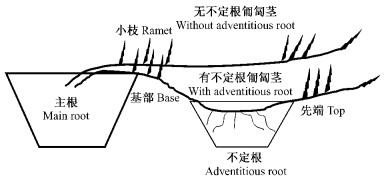
1.2.3 测定项目和方法不定根发生后,于2004年8月5日、8月29日、9月18日,在不定根两侧的匍匐茎先端和基部选择长势良好的小枝各3个,用便携式光合测定系统(Li-6400,Li-Cor Inc.)测定其当年叶的蒸腾速率和气孔导度的日变化(图 2)。从日变化数据计算日最大气孔导度、日最大蒸腾速率和日蒸腾量。同时,用压力室植物水势仪(modle 600,PMS Instrument Co.)测定正午和黎明前叶水势。以上测定结束后,在2004年9月下旬用pV技术(丸山温等,1983)测定叶片质壁分离时的水势(ψwtlp)和充分吸水时的渗透势(ψssat)以及细胞体积弹性率(ε)。各项指标的计算公式如下:
|
图 2 测定枝 Figure 2 Measurement branchs |
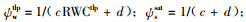
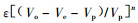
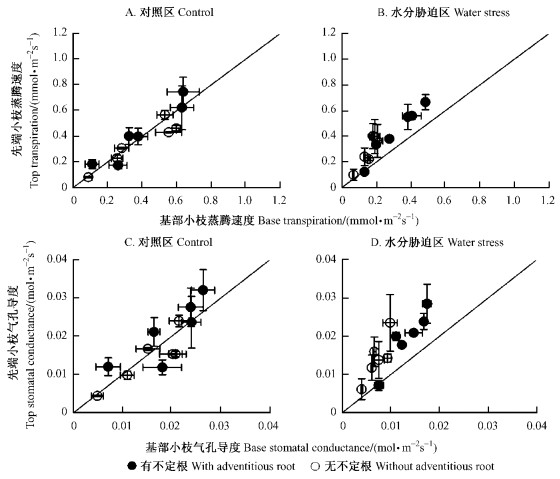
为了比较匍匐茎不同部位蒸腾速率和气孔导度的变化,以匍匐茎基部小枝数据为横坐标,匍匐茎先端数据为纵坐标做成图 3,图中直线斜率为1。在对照区,无论有无不定根,蒸腾速率、气孔导度均位于斜线两侧,说明部位间差异很小;在水分胁迫区,无论有无不定根,各点位于斜线上方,先端小枝均显示出较高的值,说明先端小枝蒸腾速率、气孔导度均大于基部小枝。图 4表示匍匐茎不同部位正午和黎明前水势。在对照区,有不定根和无不定根匍匐茎的正午和黎明前水势在部位间均未见差异;但是在水分胁迫区,正午水势在部位间出现显著差异,先端小枝水势明显下降。
|
图 3 蒸腾速率(A,B)和气孔导度(C,D)在匍匐茎不同部位间的关系 Figure 3 Relationships between tip and base of stolon in transpiration rate (A, B) and stomatal conductance (C, D) |

|
图 4 各处理区匍匐茎部位间黎明前水势(A,B)和正午水势(C,D)的比较 Figure 4 Comparisons of leaf water potential at predawn (A, B) and at midday (C, D) between top and base of stolon on each treatment 不同字母表示差异显著, 纵轴表示标准误差 Different letters indicate significant differences(t-test, P<0.05)。 |
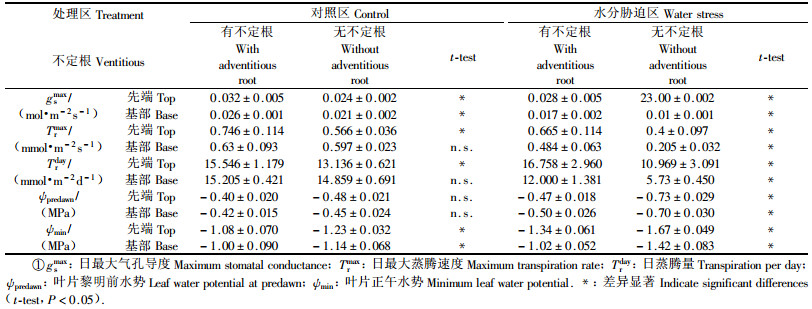
如表 1所示,在水分胁迫区,不论是先端还是基部,有不定根匍匐茎的各项指标都显著高于无不定根匍匐茎,说明无不定根匍匐茎受到水分胁迫后先端和基部蒸腾活性均受到抑制。在对照区,与无不定根匍匐茎先端小枝相比,有不定根匍匐茎的先端小枝显示较高的蒸腾活性,黎明前的水势以及基部的日最大蒸腾速率、日蒸腾量无论有无不定根,均未出现显著性差异(P < 0.05)。可见,由于不定根的存在,改变了蒸腾对匍匐茎内水势的影响,其影响程度在水分胁迫条件下更为显著。
|
|
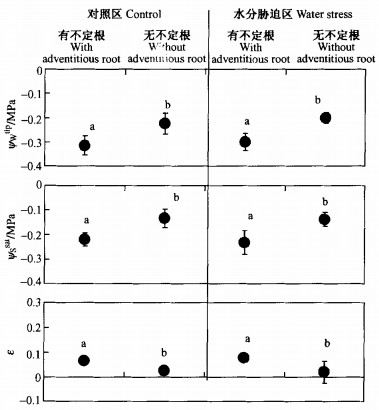
统计检验P-V曲线各参数在匍匐茎部位间无显著差异,如图 5所示,取各部位的平均值,求出匍匐茎质壁分离时的水势(ψwtlp)和充分吸水时的渗透势(ψssat)以及细胞体积弹性率(ε),进行比较。
|
图 5 水分特性参数 Figure 5 Leaf water relation parameters |
无论是对照区还是水分胁迫区,有不定根匍匐茎的ψwtlp和ψssat都显著的低于无不定根匍匐茎,而ε值显著高于无不定根匍匐茎。由此可见:无论有无水分胁迫,有不定根的匍匐茎都能降低渗透势,进行渗透调节。而且,失水时,坚硬的细胞壁使膨压迅速下降,保证气孔尽快关闭;而无不定根匍匐茎ψwtlp和ψssat都比有不定根匍匐茎高,吸水能力降低。而柔软的细胞壁缓和了因水分损失而导致的膨压改变,从而保证细胞的生理活性。
3 结论与讨论 3.1 匍匐茎不同部位小枝蒸腾和吸水的差异基部小枝受到水分胁迫后减少蒸腾(图 3),从而避免正午水势的降低(图 4),而先端小枝为保证旺盛的气体交换,积极蒸腾,维持较高的蒸腾活力,使正午水势有明显下降趋势,但黎明前水势和基部一样能够得到恢复。这一特性对臭柏的旺盛生长,在干旱条件下灌丛的扩大显然是有利的(Miki et al., 2003);另一方面,在对照区,不论有无不定根,这种部位间的差异很小。也就是说,当土壤水分条件良好时,基部的小枝能够和先端的小枝一样,保持较高的气孔导度,维持旺盛的气体交换。因此,无论不定根是否存在,水分胁迫会改变匍匐茎不同部位的蒸腾失水和吸水特性,或者说,臭柏匍匐茎根据土壤水分条件的不同,调节不同部位的失水和吸水量,以适应不同的土壤水分条件。
3.2 不定根的作用在水分胁迫条件下,无不定根匍匐茎的气孔导度、蒸腾速率的日最大值以及日蒸腾量都较低,出现关闭气孔抑制蒸腾的倾向。虽然蒸腾被强烈抑制,但是正午水势还是下降明显,黎明前水势不能像有不定根匍匐茎那样恢复到较高的值(表 1)。相反,有不定根匍匐茎即使在水分胁迫条件下,白天能够维持旺盛的蒸腾,夜间充分吸水,使黎明前水势恢复到较高状态。植物体黎明前水势是反映植物与土壤水分平衡的指标(Sellin,1999)。无不定根匍匐茎对于白天蒸腾损失的水分,在夜间未能得到充分补充。由此可见,不定根对匍匐茎夜间吸水有很大作用。图 5所示的ψwtlp,ψssat值,无论有无不定根,均未看到处理区间的差异,臭柏不会因为水分胁迫而启动渗透调节机制。但是,由于不定根的存在,会降低质壁分离时的水势和充分吸水时的渗透势,进行渗透调节,从而提高吸水力。而且有不定根的匍匐茎,无论是否受到水分胁迫,其细胞体积弹性率都较大(图 5),细胞壁坚硬,稍有水分损失叶片膨压就会急速下降。在干旱条件下膨压的下降对气孔的关闭有较大影响(Miki et al., 2003)。叶细胞膨压的降低导致气孔保卫细胞膨压的降低,从而引起气孔关闭(Pierce et al.,1980)。所以,有不定根匍匐茎可能具备这样的细胞功能,在水分胁迫条件下,通过降低膨压,使保卫细胞失水,气孔迅速关闭。而且,有不定根匍匐茎不仅能够抑制失水,在白天还具有维持较高水势,保持蒸腾活性的能力(表 1)。由此推测:有不定根匍匐茎不但具有回避失水的叶细胞构造,而且由于不定根的存在,迅速补充失水,维持较高的蒸腾活性,从而保持旺盛的蒸腾活力和气体交换。
在干旱条件下,臭柏幼树为了保持较高的吸水力,降低了T/R比(李玉霊等,2003)。根据本研究的结果,成木阶段的臭柏是通过匍匐茎部位间的调整和不定根的发育提高吸水能力,这些特性使得臭柏群落在干旱沙丘上的生长、扩展成为可能。特别是不定根的作用,对臭柏的克隆拓展有其特殊意义。关于不定根的克隆整合机制及其对匍匐茎克隆生长的贡献意义尚需进一步探讨。
李玉霊, 林万里子, 坂本圭児, 等. 2003. 水ストレスが臭柏(Sabina vulgaris Ant.)とカイヅカイブキ(Juniperus chinensis var. kaizuka Hort.)の地基部の発葉に与える影嚮[J]. 日本緑化工学会議, 29(1): 107-112. |
丸山温, 森川靖. 1983. 桿の水分特性の测定—P-V曲线法—[J]. 日本林学会議, 65(1): 23-28. |
王林和, 董智, 张国盛, 等. 1998. 毛乌素沙地臭柏新梢生长规律的研究[J]. 内蒙古林学院学报, 20(3): 15-21. |
王林和, 张国盛, 刘美珍, 等. 2002. 毛乌素沙地臭柏不定根发生特性的研究[J]. 林业科学, 38(5): 156-159. DOI:10.3321/j.issn:1001-7488.2002.05.026 |
温国胜, 図子美和子, 坂本圭児, 等. 2000. 慢性的な水ストレス下での臭柏の生育經過[J]. 日本緑化工学会議, 25(3): 242-248. |
温国胜, 王林和, 吉川贤. 2002. 中国半干旱地に生育する臭柏の生理的特性と生态的特性[J]. 日本绿化工学会志, 27(3): 526-532. |
吉川賢. 1995. 地球の砂漠化を防止する[J]. 森林科学, 14: 2-7. |
吉川賢. 1998. 砂漠化防止への挑戰[M]. 东京: 中央公論社, 69-76.
|
吉川賢, 山中典和, 大手信人. 2004. 乾燥地の自然と緑化-砂漠化地域の生態系修復に向けて-[M]. 东京: 共立出版社, 12-19.
|
张国盛, 刘海东, 李玉灵, 等. 2004.切断匍匐茎对臭柏叶绿素荧光特性的影响. 40(3): 60-65. http://www.linyekexue.net/CN/abstract/abstract5870.shtml
|
张国盛, 刘海东, 李玉灵, 等. 2005. 毛乌素沙地臭柏匍匐茎蒸腾速率和水势的日变化[J]. 干旱区资源与环境, 19(6): 173-180. DOI:10.3969/j.issn.1003-7578.2005.06.035 |
增田拓郎, 小林葉明, 森本幸裕, 等. 1998. 中国毛鳥素沙地にける土壤水分条件と園柳の根系分布について[J]. 造图雑志, 51: 126-131. |
Kang M Y, Dong S, Huang X, et al. 2003. Ecological regionalization of suitable trees, shrubs and herbages for vegetation restoration in the farming-pastoral zone of northern China[J]. Acta Botanica Sinica, 45(10): 1157-1165. |
Miki N, Otsuki K, Sakamoto K, et al. 2003. Leaf water relations in Pinus densiflora Sieb. et Zucc. on different soil moisture conditions[J]. J For Res, 8: 153-161. DOI:10.1007/s10310-002-0021-z |
Pierce M, Raschke K. 1980. Correlation between loss of turgor and accumulation of abscisic acid in detached leaves[J]. Planta, 148: 174-182. DOI:10.1007/BF00386419 |
Sellin A. 1999. Dose pre-dawn water potential reflect conditions of equilibrium in plant and soil water status[J]. Acta Oecol, 20(1): 51-59. DOI:10.1016/S1146-609X(99)80015-0 |
 2009, Vol. 45
2009, Vol. 45