文章信息
- 万雪琴, 张帆, 夏新莉, 尹伟伦.
- Wan Xueqin, Zhang Fan, Xia Xinli, Yin Weilun
- 镉胁迫对杨树矿质营养吸收和分配的影响
- Effects of Cadmium Stress on Absorption and Distribution of Mineral Nutrients in Poplar Plants
- 林业科学, 2009, 45(7): 45-51.
- Scientia Silvae Sinicae, 2009, 45(7): 45-51.
-
文章历史
- 收稿日期:2008-01-05
-
作者相关文章
2. 北京林业大学生物科学与技术学院 北京 100083
2. College of Biological Science and Biotechnology, Beijing Forestry University Beijing 100083
由于“三废”排放和污水灌溉等原因,镉已成为土壤和水体的主要污染物之一,并对自然生态系统和人类健康构成严重威胁.对植物而言,镉没有任何功能,当叶片组织的镉含量达到3~10 mg·kg-1时,就会导致生物产量的显著下降(Bahlsberg-Pahlson, 1989).当前,有关镉与植物相互作用关系的研究已经很多,但植物对镉的解毒和中毒机制依然不清,一些矛盾和异常现象尚无法解释(万雪琴等,2008; Baryla et al., 2001; Haag-Kerwer et al., 1999).在矿质营养方面,镉胁迫显著影响植物对养分的吸收、转运、分配和代谢,但由于研究所用的材料、镉源、处理方式、浓度和时间多不相同,所得结果也不尽相同,甚至有相互矛盾之处.这使得镉对植物矿质营养的作用规律依然很不清楚.杨树(Populus)是世界上分布最广、栽培最多的树种,具有重要的生态和经济价值.虽然杨树对镉的富集系数较低(Robinson et al., 2000),但不同无性系间存在显著差异(Laureysens et al., 2004; Godbold et al., 1991),加上其突出的速生丰产性能可以将土壤重金属污染治理与城乡绿化、防护林和短周期工业人工林生产有机结合,发挥很好的生态、经济和社会效益,因此在欧美国家被广泛应用于污染土壤的植物修复(Robinson et al., 2000;Laureysens, 2004).本研究就镉胁迫对杨树矿质营养吸收和分配的影响进行研究,有助于揭示植物对镉的解毒和中毒机制,指导杨树在土壤重金属污染治理中的应用.
1 材料与方法试验材为欧美杂交杨无性系XMH-4(Populus deltoides × P.nigra)、MH-8(P.trichocarpa × P.deltoides)和XMH-10(P.deltoides× P.nigra).2004年4月以插条形式将上述材料从美国引进到中国,在北京等地的引种试验中,上述材料均表现出良好的适应性、速生性和抗病性.2006年用这3个无性系的插条进行水培,容器为长100 cm、宽50 cm和高25 cm的塑料盆,盆内盛60 L培养液,用一泡沫浮于培养液面作为插条的固定支持物,每盆每无性系扦插10株,随机排列,共4盆;扦插后先用自来水培养20天,生根后用Hoagland全营养液培养,其中3盆加入Cd(NO3)2进行处理,处理浓度分别为2.810,5.620和11.24 mg·L-1,对应的Cd浓度分别为25,50和100 μm,另外1盆设为对照,不添加Cd(NO3)2.
处理5个月后,分无性系取处理和对照植株的成熟叶、衰老叶、茎干及根系,用以分析Cd,K,Ca,Na,Mg,Fe,Mn,Zn,Cu,Mo,P和B的含量.叶片和根系样品取样后用双蒸水冲洗,茎干样品剥皮后用美工刀削成细屑,所有样品在80℃烘干后用研钵研成粉末.元素分析采用HNO3-H2SO4-HCLO4消解,电感耦合等离子体发射光谱仪(ICP-OES, OPTIMA 2000A,U.S.A.)测定(吴建之等, 1999).差异显著性分析和相关性分析由SPSS(11.0)相应模块完成.
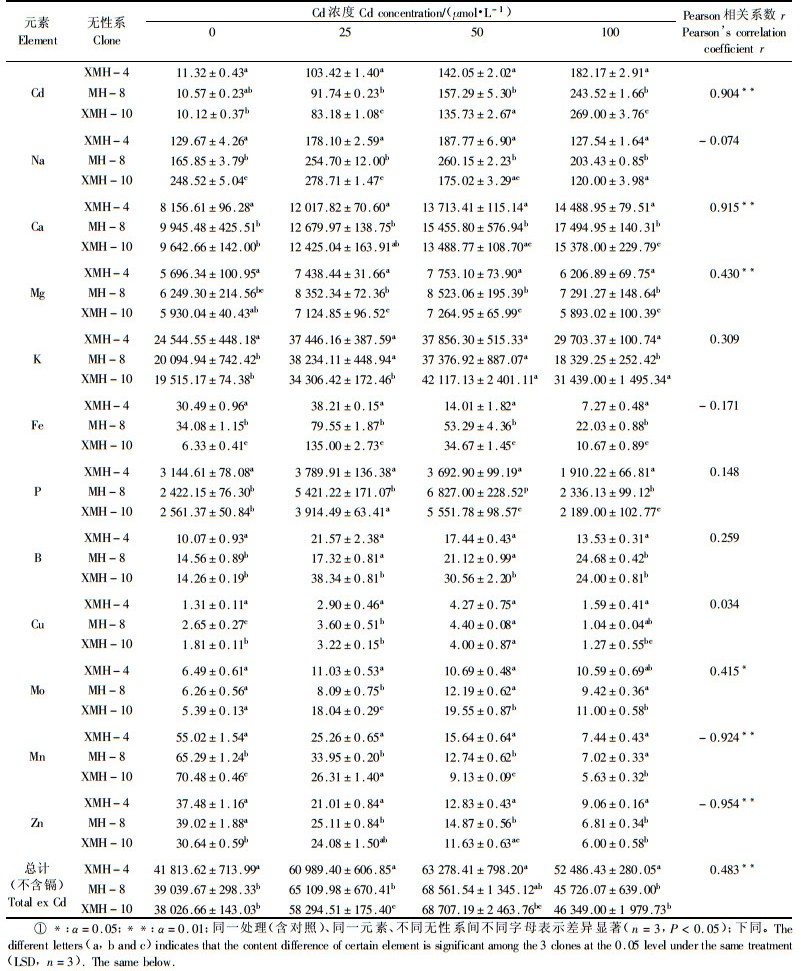
2 结果与分析 2.1 镉胁迫对成熟叶矿质营养的影响随着培养液Cd浓度的升高,功能叶中的镉含量呈线性增加,其他矿质元素含量的变化有3种类型:1) Ca含量与Cd浓度呈明显正相关;2)Mn和Zn含量与Cd浓度呈显著负相关;3) Na,Mg,K,Fe,P,B,Cu和Mo含量在25和50 μmol·L-1Cd处理下显著高于对照,而在100 μmol·L-1处理下又明显下降(表 1).除Cd外的11种元素的总含量也表现为在25和50 μmol·L-1 Cd处理下显著高于对照,而在100 μmol·L-1处理时又明显降低,但其总离子含量仍高于对照.因此,较低浓度的镉处理可增加大多数元素在成熟叶片中的含量,而较高浓度的镉处理则会降低矿质养分在叶片中的含量.在镉胁迫导致成熟叶出现明显黄化症状时,Mg,Fe,Cu,Ca和K的含量都高于对照植株,因此镉胁迫下的黄化不是由于亏缺这些元素造成的.
|
|
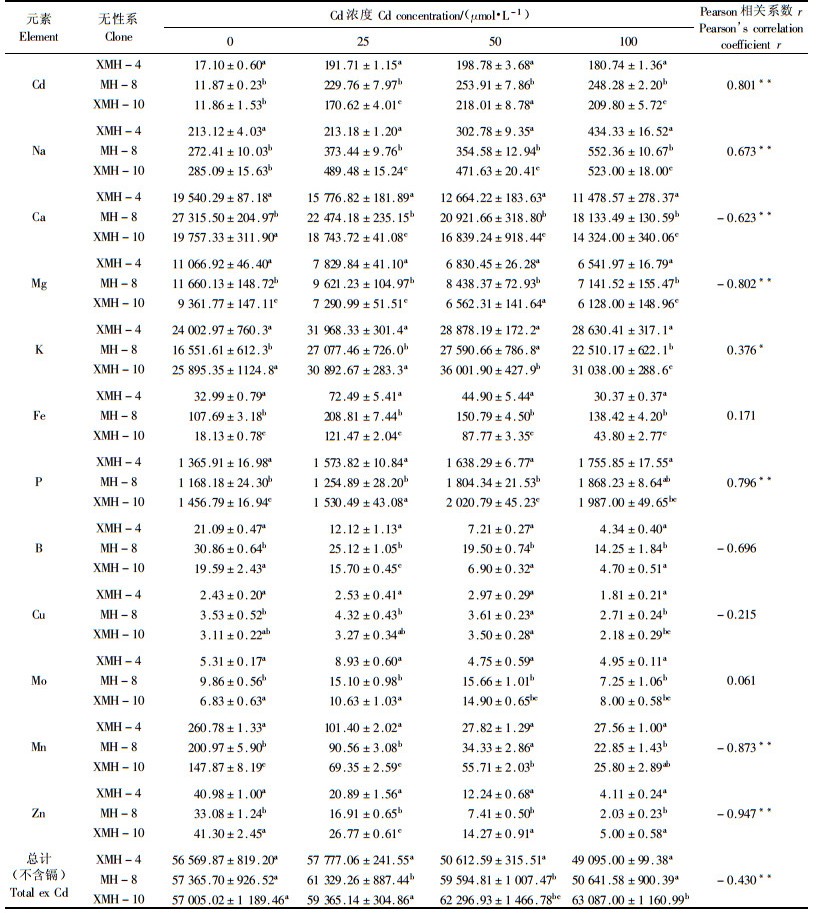
衰老叶中Cd含量在25 μmol·L-1处理下就达到很高水平,50和100 μmol·L-1镉处理下Cd含量更高(表 2).这说明在低浓度Cd处理下,衰老叶对Cd的富集作用明显高于功能叶.这可能是植株的一种脱毒机制,即将Cd转移和限制在新陈代谢和生理功能弱的衰老叶片,以尽可能减少Cd对功能叶片的伤害.其他矿质元素在衰老叶中的含量也表现为3种类型:1) Na,P与Cd处理浓度极显著正相关;2) Ca,Mg,B,Mn和Zn与Cd处理浓度显著负相关;3) K,Fe,Cu和Mo在25和50 μmol·L-1处理下含量增加,而在100 μmol·L-1处理下又显著降低.11种元素总量(不含镉)在25和50 μmol·L-1镉处理下增加,在100 μmol·L-1镉处理下有所降低(表 2).
|
|
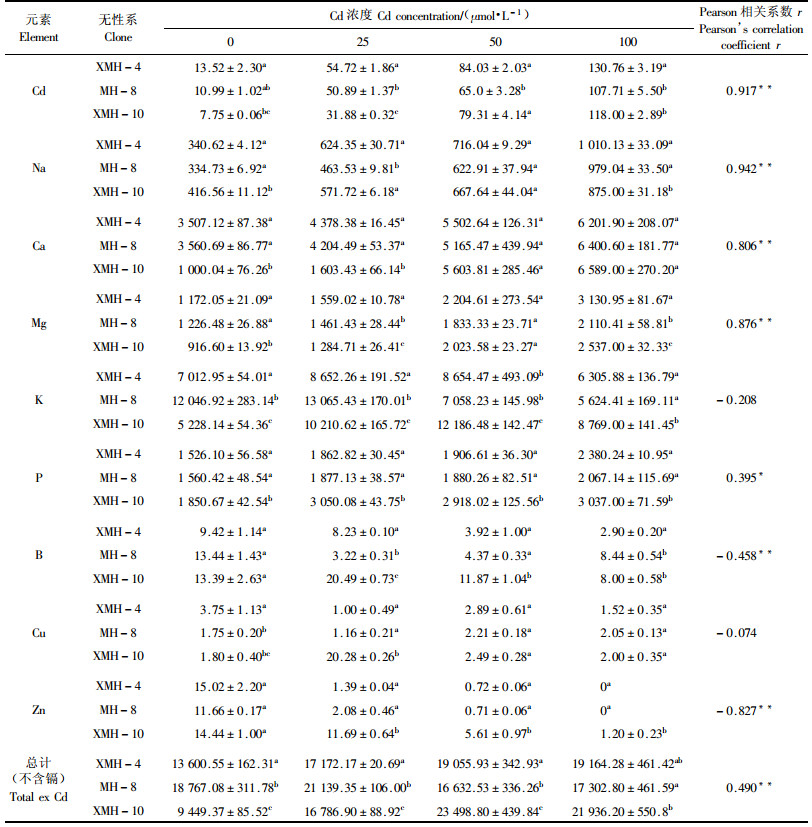
各元素在茎干木质部的含量明显低于叶和根,一些微量元素如Fe,Mn和Mo浓度过低,测试误差较大,故此处不对其进行分析.木质部的Cd含量随着处理浓度的增加而显著升高,其他矿质元素的变化情况大致是:Na,Ca,Mg和P 4种元素含量与Cd处理浓度呈显著正相关;Zn和B的含量随Cd浓度升高而呈线性下降,K表现为在25 μmol·L-1镉处理下升高,而在50和100 μmol·L-1镉处理下又降低;Cu在3个无性系间变化较大,规律不明显.木质部中的总矿质营养含量在XMH-4和XMH-10上表现为随镉处理浓度增加而升高,而MH-8在50和100 μmol·L-1镉处理下略有下降(表 3).
|
|
根系是植株中富集Cd最多的器官,其含量远远超过功能叶、衰老叶和茎干木质部.根系是Cd进入植株体内的最初器官,根系对Cd有显著的截留作用,将绝大部分的Cd束缚在根里,只有约10%的镉被转运到地上部分器官.在25 μmol·L-1处理下,根系对Cd的富集系数高达1001,远超过功能叶的33,衰老叶的70和木质部的20.Cd对根系中矿质营养的影响表现为:K随Cd浓度升高而增加(r=0.826, P<0.01);Fe,Zn,Cu和Mo在25和50 μmol·L-1镉处理下高于对照,而在100 μmol·L-1镉处理下有所下降;Ca,Mg,P,Mn,Na和B 6种元素含量与Cd浓度显著负相关.根系的总矿质养分含量明显下降,这主要是由大量元素Ca和P含量显著下降引起的(表 4).
|
|
表 1~4列出了在不同浓度镉处理下,同一元素在不同器官中的含量变化情况.在25和50 μmol·L-1处理下,杨树根、茎和叶的K,Fe,Cu和Mo含量均提高,说明该浓度的镉处理增加了这4种元素的吸收量;对Zn而言,其在根系中的含量明显增加,但在地上部分的含量则显著减少,说明镉阻止了Zn从根部运输到地上部分;Mn在3种浓度下各个器官的含量均显著降低,说明Cd处理显著降低杨树对Mn的吸收量;Ca在3个浓度下,Mg在25和50 μmol·L-1浓度下在成熟叶和木质部含量上升,在老叶和根的含量下降,这说明在3个浓度镉处理下导致的失绿症不是由于缺Ca引起的,在25和50 μmol·L-1浓度下的失绿症也不是由于缺Mg引起的;P和Na在地上部分含量显著增加,在根系的含量明显减少,说明Cd处理能增加P和Na向地上部的分配;在25和50 μmol·L-1处理下,功能叶和茎木质部的总元素(镉元素除外)含量显著升高,衰老叶基本不变,根系则显著降低,这说明这2个浓度的镉处理促进了植物对矿质养分的吸收和向地上转运的比例;在100 μmol·L-1镉处理下,杨树对多数元素的吸收量显著降低.
2.6 镉胁迫下不同无性系矿质元素含量的差异从表 1~4可以看出,相同浓度镉处理下,成熟叶、衰老叶和茎木质部中的镉含量在3个无性系间存在广泛的显著差异(P<0.05),在根系中只有50 μmol·L-1镉处理下XMH-10才与其他2个无性系有显著差异.这说明不同无性系对镉的吸收和富集能力存在明显差异,因此,筛选对镉具有较高富集效应和抗性的杨树无性系用于土壤和水体镉污染的植物修复是可行的.在对照和不同浓度的镉处理下,相同器官中同一元素的含量在不同无性系间存在着广泛差异(P<0.05),如25μmol·L-1镉处理下成熟叶片中的Cd,Na,Mg和Fe(表 1),衰老叶片中的Na,Ca,Mg,Mn,Zn和Fe(表 2),茎木质部的Na,K,B和Zn(表 3),根系中的Na,K,B和Zn(表 4).
3 结论与讨论植物根系对镉有显著的截留作用,起到解毒害的作用,这已为众多的研究所证实(Benavides et al., 2005; Polle et al., 2004; Hart et al., 1998).本研究结果也表明杨树根系吸收并截留了绝大多数的镉离子.根系对镉的截留主要是依靠细胞中的谷胱甘肽和一些含硫化合物与镉离子形成稳定的螯合物而实现的(Polle et al., 2004; Benavides et al., 2005; 张军等, 2006).本研究发现衰老叶的镉含量显著高于成熟叶片,这可以有效降低镉在新陈代谢旺盛的成熟叶中的含量,并且可以通过叶片凋落的形式排出植株体外,从而减轻对植株的毒害.因此,衰老叶对镉的富集效应可能是植物对镉胁迫的另外一种适应机制.
本研究结果表明,低浓度镉处理会增加植物对多数矿质元素(Na,K,Mg,Fe,P,Zn,B,Cu和Mo)的吸收,而高浓度的镉处理则会减少植物对矿质营养的吸收.这与一些研究结果(徐勤松等, 2004; 袁祖丽等, 2005)一致.因此,镉对植物矿质营养的影响具有明显的剂量效应,即组织中矿质元素的含量与培养介质中的镉浓度呈抛物线关系,每种元素都存在一个镉临界阈值,不同元素的阈值可能差异较大,而同一元素在不同植物中的阈值可能不同.本研究中,Mn在各器官中的含量与镉浓度呈极显著负相关,而K在各组织中的含量与镉浓度呈极显著正相关.这与其他一些研究(程旺大等,2005;Ghnaya et al., 2005)的结果相反,其可能原因是试验材料和镉浓度的差异,即本试验中Mn对镉的临界阈值低于25 μmol·L-1,而K对镉的临界阈值高于100μmol·L-1.
镉能与Ca,Cu和Fe等二价阳离子发生置换反应,从而增加游离金属离子的浓度,对组织造成氧化伤害(Polle et al., 2004;Benavides et al., 2005).由于单纯的置换只会改变元素存在的状态,并不会增加元素含量,因此25和50 μmol·L-1镉处理所导致多数元素含量的增加必有其他原因.徐勤松等(2004)认为镉处理下Fe含量的提高是由于Cd与EDTA络合的稳定性高于Fe与EDTA络合的稳定性,从而使培养液中的Fe2+更易于被吸收所致,但这不能解释无EDTA情况矿质元素含量增加的现象.在镉胁迫下,以下因素不利于植物对矿质元素的吸收和运输:1)镉对矿质离子的竞争抑制;2)镉抑制蒸腾作用,使矿质元素运输速率降低;3)镉抑制参与矿质元素运输的相关蛋白及酶的活性;4)镉抑制光合和呼吸作用,使主动运输所需的能量降低;5)镉导致膜脂过氧化和蛋白质羰基化,增加细胞膜透性.在较低浓度(25和50μmol·L-1)镉处理下,镉导致的细胞膜透性的增加有利于元素经被动运输进入共质体;另外,镉造成的生物量降低对元素起到一定的“浓缩”作用,从而使多数矿质元素在植株中的含量提高.在100μmol·L-1的高浓度镉处理下,上述第1)~4)项对元素主动吸收的抑制作用增大,同时过高的Cd浓度通过破坏细胞膜上的离子通道和离子载体使元素的被动吸收速率降低,从而出现高浓度镉处理导致植物对矿质元素的吸收显著降低的现象.
程旺大, 姚海根, 张国平, 等. 2005. 镉胁迫对水稻生长和营养代谢的影响. 中国农业科学, 38(3): 528-537. DOI:10.3321/j.issn:0578-1752.2005.03.016 |
万雪琴, 张帆, 夏新莉, 等. 2008. 镉处理对杨树光合作用及叶绿素荧光参数的影响. 林业科学, 44(6): 73-78. DOI:10.3321/j.issn:1001-7488.2008.06.013 |
吴建之, 葛滢. 1999. 植物标样多元素测定的五种前处理方法比较. 光谱学与光谱分析, 19(3): 369-372. DOI:10.3321/j.issn:1000-0593.1999.03.032 |
徐勤松, 施国新, 周耀明, 等. 2004. 镉在黑藻叶细胞的亚显微定位分布及毒害效应分析. 实验生物学报, 37(6): 461-468. DOI:10.3321/j.issn:1673-520X.2004.06.006 |
袁祖丽, 马新明, 韩锦峰, 等. 2005. 镉胁迫对烟草营养器官发育及矿物质元素的影响. 河南科学, 23(5): 679-682. DOI:10.3969/j.issn.1004-3918.2005.05.017 |
张军, 束文圣. 2006. 植物对重金属镉的耐受机制. 植物生理与分子生物学学报, 32(1): 1-8. |
Bahlsberg-Pahlson A-M. 1989. Toxicity of heavy metals (Zn, Cu, Cd, Pb) to vascular plants. Water, Air and Soil Pollution, 47: 287-319. DOI:10.1007/BF00279329 |
Baryla A, Carrier P, Franck F, et al. 2001. Leaf chlorosis in oil seed rape plant (Brassica napus) grown on cadmium-polluted soil: caused and consequences for photosynthesis and growth. Planta, 212(5/6): 696-709. |
Benavides M, Gallego S, Tomaro M. 2005. Cadmium toxicity in plants. Brazilian Journal of Plant Physiology, 17(1): 21-34. DOI:10.1590/S1677-04202005000100003 |
Ghnaya T, Nouairi I, Slama I, et al. 2005. Cadmium effects on growth and mineral nutrition of two halophytes: Sesuvium portulacastrum and Mesembryanthemum crystallinum. Journal of Plant Physiology, 162(10): 1133-1140. DOI:10.1016/j.jplph.2004.11.011 |
Godbold D L, Litzinger M, Griese C. 1991. Cadmium toxicity in clones of Populus tremula. Water, Air and Soil Pollution, 57-58(1): 209-215. DOI:10.1007/BF00282884 |
Haag-Kerwer A, Schafer H J, Heiss S, et al. 1999. Cadmium exposure in Brassica juncea causes a decline in transpiration rate and leaf expansion without effect on photosynthesis. Journal of Experimental Botany, 50(341): 1827-1835. |
Hart J J, Welch R M, Norvell W A, et al. 1998. Characterization of cadmium binding, uptake, and translocation in intact seedlings of bread and durum wheat cultivars. Plant Physiology, 116(4): 1413-1420. DOI:10.1104/pp.116.4.1413 |
Laureysens I, Blust R, De Temmerman L, et al. 2004. Clonal variation in heavy accumulation and biomass production in a poplar coppice culture: Ⅰ. Seasonal variation in leaf, wood and bark concentrations. Environmental Pollution, 131(3): 485-494. DOI:10.1016/j.envpol.2004.02.009 |
Polle A, Schützendübel A. 2004. Heavy metal signaling in plants: linking cellular and organismic responses//Hirt A, Shinozaki K. Plant responses to abiotic stress. Berlin: Springer-Verlag, 187-216.
|
Robinson B H, Mills T M, Petit D, et al. 2000. Natural and induced cadmium-accumulation in poplar and willow: implication for phytoremdiation. Plant and Soil, 227(301): 306. |
 2009, Vol. 45
2009, Vol. 45