文章信息
- 王秋玉, 张金然, 杨传平.
- Wang Qiuyu, Zhang Jinran, Yang Chuanping.
- 白桦种群间木材纤维性状的表型变异与分子标记的遗传多态性
- Phenotypic Variation in Wood Fiber Properties And Genetic Diversity in Molecular Marker among the Populations of Betula platyphylla
- 林业科学, 2007, 43(11): 37-42.
- Scientia Silvae Sinicae, 2007, 43(11): 37-42.
-
文章历史
- 收稿日期:2006-12-22
-
作者相关文章
2. 呼和浩特职业学院 呼和浩特 010051
2. Huhhot Vocational Institute Huhhot 010051
白桦(Betula platyphylla)属于桦木科(Betulaceae)桦木属(Betula),是一种分布较广的落叶阔叶树种,在我国东北、华北、西北等地区的木材生产中占有重要位置。同时因其生长快、成熟早,纹理细致,颜色洁白,表面光滑度高,木质素含量低,纤维性状优良等特点,已被公认为优良的造纸原材料。在国家“八·五"计划中,白桦被列为国家林业科技攻关的树种,在良种生产等方面作了大量工作,但在白桦木材品质和纤维材选育方面的系统研究还较少,郭明辉等(1999;2000)对不同种源白桦木材密度和生长轮宽度径向变异模式进行了研究;还利用新开发的木材解剖构造计算机视觉系统测试了白桦木材解剖构造的变化特点,揭示白桦木材解剖特征的径向变异规律,探讨不同海拔高度的白桦木材解剖特征,为白桦林的定向培育和木材加工利用提供理论指导。赵西平等(2005)对白桦小径木锯材干燥质量的影响因素进行了研究,结果表明小径木材质较差,心边材的纤维长度差异较大,且比成熟材小得多。因此,如何利用传统的林木育种手段结合现代分子生物学技术培育出纤维性状优良、生长快的白桦纤维材优良新品种是急待解决的问题。
本研究以我国东北地区5个白桦天然种群为研究材料,采用宏观与微观研究相结合的方法,对来自不同种群的木材纤维形态性状的表型变异进行测定的同时,采用RAPD和ISSR分子标记技术检测其DNA水平上的遗传多态性,为今后合理保存和有效利用白桦天然种质资源提供理论依据。
1 材料与方法 1.1 试验材料试验材料来自辽宁新宾林业局、吉林汪清林业局、黑龙江尚志地区帽儿山实验林场、小兴安岭的金山屯林业局和大兴安岭的塔河林业局5个地区的白桦天然林,各天然种群的地理气候因子见表 1。每个地点随机采集20个样本,共100个样本。每个样本包括白桦叶片及相应木芯(用孔径0.5 cm的生长锥在胸高处与树干垂直钻取木芯)。
|
|
由于白桦各种群树龄不同(表 1),而白桦在15年以后进入成熟期,因此,为了分析的可靠性,选取各种群18~31年的木材样品进行木材纤维性状测定。采用硝酸离析法离析出木材纤维,每株随机取30根完整的纤维,在XSTkZ型投影显微镜下测定纤维长、宽,并计算出长宽比。运用SPSS软件对测得数据进行分析。
1.2.2 基因组DNA的提取与检测采用改良的CTAB法(Doyle et al., 1990)提取白桦叶片基因组DNA,-20 ℃保存备用。利用美国Perkin Elmer公司生产的UV/VIS Spectrometer Lambda Bio10测定所得DNA的含量和纯度。同时,利用琼脂糖凝胶电泳检测提取DNA的完整性。
以提取的基因组DNA为模板,根据Williams 等(1990)给出的框架,在保持基本成分不变的基础上,逐一对其进行RAPD和ISSR反应成分调整,得到优化的反应体系和扩增程序。ISSR扩增体系:在20 μL反应体系中,含1×PCR Buffer,2.0 mmol·L-1MgCl2,160 μmol·L-1dNTP,0.4 μmol·L-1引物,1 UTaq DNA聚合酶,40 ng模板DN A。扩增程序:94 ℃预变性5 min, 94 ℃变性30 s, 55 ℃退火45 s,72 ℃延伸90 s,35个循环,最后72 ℃延伸10 min。RAPD扩增体系:反应总体积20 μL,含1×PCR buffer,2.0 mmol·L-1MgCl2,1 60 μmo·L-1 dNTP,0.5 μmol·L-1引物,1 U TaqDNA聚合酶,30 ng模板。RAPD扩增程序:94 ℃预变性5 min, 94 ℃变性1 min, 37 ℃退火1 min,72 ℃延伸2 min,40个循环,最后72 ℃延伸10 min。
1.2.3 数据处理与统计分析扩增产物用1.5%的琼脂糖凝胶(含0.5 μ L·mL-1 EB)电泳检测。利用UVP凝胶成像系统GDS7600(Gel Documentation Syste ms)Labworks对电泳胶照相。由软件分析得到各条谱带的分子量大小,根据所得谱带的引物及分子量大小得到相应标记位点。电泳图谱中的每一条谱带均代表了引物与模板DNA互补结合的一对位点,经过统计分析,最后人工将所得到的RAPD和ISSR位点形成0/1矩阵(有带记为1,无带记为0)。RAPD和ISSR标记为显性标记,对于异交植物而言,它不能区分纯合和杂合基因型从而无法直接估计种群内基因频率,这是显性标记的一个缺陷(Khasa et al., 1996)。本研究将每个RAPD和ISSR扩增条带看作具有2个等位基因(1和0)的复等位基因位点。另外,本研究材料是从5个白桦天然成熟林中分别随机抽取20个样本组成的随机样本群体,样本群体处于随机交配状态,可以假设群体内基因频率处于Hardy-Weinberg平衡,通过隐性基因型的频率(q2), 利用p2+2pq+q2=1(p为显性基因频率,q为隐性基因频率)计算各基因的频率用于下一步统计(钱韦等, 2001)。采用该方法可以提供所需的遗传参数,一般来说,往往低估种群内遗传变异水平,但用于种群遗传多样性检测还是可行的。
利用POPGEN32软件计算观测等位基因数(na)、有效等位基因数(ne)、Shan non信息指数(I*)等能够反映白桦种群遗传多样性水平的遗传参数;应用MEGA软件构建各种群间遗传关系聚类图;运用ARLEQUIN2.000软件中的AMOVA程序分析种群的遗传分化程度;运用SPSS软件中的Bivariate程序,将得到的全部多态性位点分别与纤维长、宽和纤维长宽比进行相关分析。
2 结果与分析 2.1 白桦种群间木材纤维形态性状的变异对5个白桦种群内20个单株木材纤维形态性状进行测定,结果表明帽儿山种群的木材纤维长而细,长宽比较大,变异较小;塔河种群木材纤维细而长短居中,但纤维长和宽度在个体间变异较大;新宾和汪清种群纤维短而粗。但5个种群的纤维长度均符合纤维材标准(表 2)。
|
|
方差分析表明,白桦木材纤维长在种群间差异不显著,而纤维宽和长宽比在5个种群间差异显著(F纤维宽=3.157*, F长宽比=2.646*),说明各种群所处地区的地理气候条件对白桦的木材纤维长度生长无明显影响,但对木材的纤维宽度影响较大,从而也影响纤维长宽比的值。
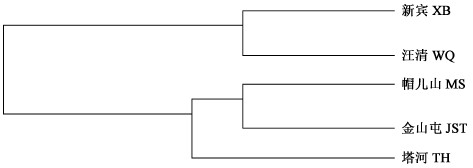
根据每个种群的纤维长和宽2个性状的平均值,利用SPSS软件中欧氏距离平方法对其进行聚类分析(图 1)。5个种群划分为2个表征群,即新宾与汪清种群聚为一类,帽儿山、金山屯和塔河种群聚为一类。
|
图 1 种群间纤维形态特征的聚类分析 Fig. 1 Cluster analysis of the fiber properties in the populations |
对来自文献检索的40个ISSR引物和60个RAPD引物进行筛选(Robert et al., 2003; Cheng et al., 2004),共筛选出重复性好、特异性高的ISSR和RAPD引物各11个。
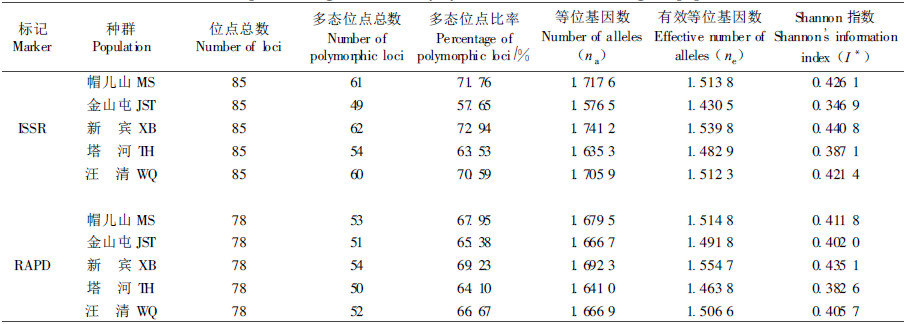
2.2.1 种群的遗传多样性对5个白桦种群的100个个体进行ISSR-PCR检测,11个引物共检测到85个位点,其中多态位点68个,总多态位点比率为80%。5个种群的多态位点百分率介于57.5%~72.94%,说明各种群内的遗传多态性水平较高,种群间的多态性差异不大。其中新宾的最高,金山屯的最低(表 3)。按所检测的多态位点的丰富程度,5个种群的顺序为:新宾>帽儿山>汪清>塔河>金山屯。此外,白桦各种群间等位基因数、有效等位基因数和Shannon指数(I*)由大到小排列顺序与多态位点比率基本相同,均为新宾、帽儿山、汪清、塔河或金山屯。通过以上分析表明白桦种群的遗传多样性水平较高。来自较低纬度的新宾和帽儿山种群的遗传多样性更高些,而处于大小兴安岭的塔河和金山屯种群的遗传多样性较低。
|
|
RAPD-PCR检测结果表明11个引物共检测出78个位点,多态位点有72个,总多态位点比率为9 2.31%,5个种群的多态位点百分率变化在64.10%~67.95%之间(表 3),多态性位点比率最高为新宾种群,最低的是塔河种群,而其他各项基因多样性指标在种群间的变化与ISSR- PCR检测结果基本一致,由大到小排序均为:新宾、帽儿山、汪清、金山屯、塔河。
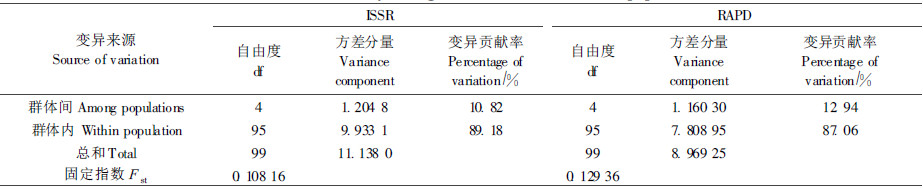
2.2.2 白桦种群间的遗传分化AMOVA分析表明白桦种群内方差分量贡献率占89.18%和87.06%,而群体间方差分量的贡献率仅占10.82%和12.94%,说明白桦的遗传变异主要存在于种群内(表 4)。这一结果与多态位点百分率分析结果相符。
|
|
根据Nei(1978)的方法计算白桦种群间的遗传一致度(I)和遗传距离(D)(表 5)。ISSR-PCR检测结果为群体的遗传一致度在0.898 6~0.962 7之间,平均值为0.922 9,表明白桦种群间的遗传相似程度较高,但也存在一定的差异。新宾与汪清和帽儿山种群遗传距离最近,分别为0.038 0和0.0 42 3,与塔河和金山屯相距最远,分别为0.063 1和0.107 0。在5个种群中,新宾与汪清和帽儿山种群首先聚在一起,最后是塔河和金山屯(图 2a)。从地理距离看,新宾和汪清与帽儿山种群相距较近,而与塔河和金山屯种群相距较远, 由此可见, 种群间遗传相似程度除受其种群遗传结构制约外, 也是各种群长期适应所在地的气候土壤等环境条件的结果。
|
|
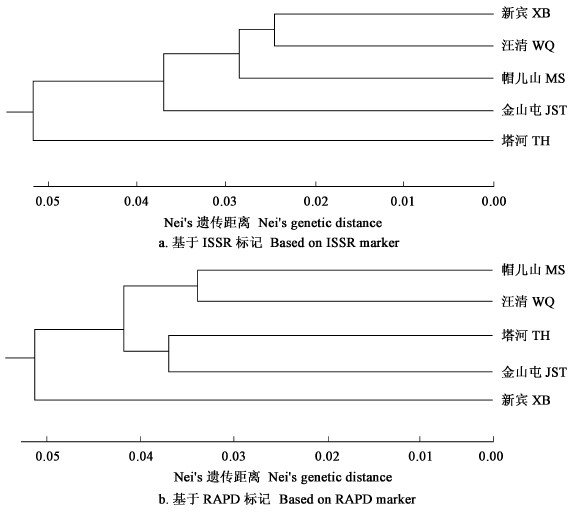
|
图 2 基于RAPD和ISSR标记的种群间遗传距离聚类图 Fig. 2 Cluster dendrogram based on genetic distance among populations by RAPD and ISSR markers |
RAPD-PCR检测结果表明,白桦种群间遗传距离在0.067 6~0.156 8之间,平均值为0.08 9 8。汪清和帽儿山遗传距离较近(0.067 6),遗传相似系数较高;塔河和金山屯遗传距离较近(0.073 8)。这些种群在地理距离上也相距较近,因此,帽儿山和汪清种群聚为一类,塔河和金山屯种群聚为一类;与ISSR标记分析结果很相似,但也有不同,位于长白山系的汪清和帽儿山种群地理距离最近,首先聚为一类,而位于大小兴安岭的塔河和金山屯种群的距离也相对较近,因此聚在一起,辽宁新宾种群相对独立(图 2b),这可能与它所处的地理位置有关。这一结果也表明白桦种群间遗传相似程度具有一定的生态适应性。
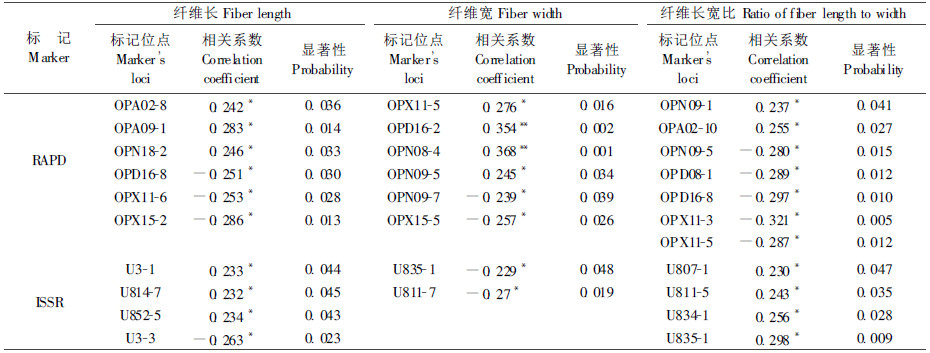
2.3 白桦木材纤维性状与RAPD以及ISSR标记的相关性应用SPSS软件,将具有多态性的68个ISSR标记位点和72个RAPD标记位点与白桦的纤维长、宽和长宽比分别进行相关分析,获得了与各纤维性状显著相关的标记位点(表 6)。结果表明,与纤维长相关的标记位点共有10个,相关系数均达到显著水平,其中有6个标记位点为正相关,4个为负相关。正相关系数为0.232~0.283,负相关系数在-0.263~-0.251之间。与纤维宽相关的标记位点有8个,4个标记位点为正相关,4个为负相关,其中OPD16-2、OPN08-4与纤维宽呈极显著正相关,其余均为显著相关。ISSR的2个标记位点均与纤维宽呈负相关。与纤维长宽比相关的标记位点有11个,6个标记位点为正相关,5个为负相关,均达到显著水平,正相关系数为0.230~0.298,负相关系数为-0.280~-0.321。
|
|
纤维形态特征直接决定着木材的物理力学性质,影响着木材的加工利用。尤其在制浆造纸方面,关系着制浆造纸的质量。纤维长度与纤维长宽比是衡量纸浆材性能好坏的重要参数(Panshin et al., 1980)。一般认为,纤维越长,纸张的强度越高。木材纤维长度小于1.0 mm、长宽比值小于50的纤维不适合造纸(Taylor, 1968),在本研究中5个种群的纤维长度均值都大于1.0 mm,纤维长宽比都大于50,因此都适用于纸浆材。而且,5个种群的纤维长度没有明显差异,但纤维宽度差异显著,进而导致木材纤维长宽比差异显著。其中帽儿山、塔河和金山屯的纤维长宽比较大,新宾和汪清纤维长宽比较低。也就是说来自较高纬度的3个种群纤维形态更好一些,而来自较低纬度的种群木材纤维较差,其中,帽儿山种群最好,汪清种群最差。
利用ISSR和RAPD 2种标记研究5个白桦种群的遗传多样性,2种标记所得的研究结果基本一致,即白桦天然种群具有很高的遗传多样性。相比之下,处于较低纬度的新宾和帽儿山种群遗传多样性更高些,而处于大小兴安岭的金山屯和塔河种群的遗传多样性较低。不论是纤维形态性状还是DNA分子标记检测,帽儿山种群均具有较高的遗传多样性,这与东北地区白桦种源遗传多样性的研究结果基本一致(姜静等, 2001)。采用2种标记方法进行的种群间聚类具有较高的一致性,即地理距离相近的种群首先聚在一起, 这一结果与基于木材纤维性状的表型聚类基本一致,辽宁的新宾和吉林的汪清种群一般聚在一起,而黑龙江北部的金山屯和塔河种群聚在一起,黑龙江南部的帽儿山种群有时与前者先聚,有时与后者先聚。总之,2种标记的聚类都表明种群间遗传距离和实际地理距离具有一定的相关性。
2种标记的AMOVA分析表明:白桦种群的遗传变异主要来自于群体内部(ISSR标记为89.18%,RAPD标记为87.06%),群体间遗传变异较小。一般认为,群体遗传分化指数在0~0.05之间,群体遗传分化较弱;0.05~0.15之间,群体遗传分化中等;0.15~0.25之间,群体遗传分化较大;当遗传分化指数大于0.25时,表示分化极大(刘萍等, 2004)。本研究使用的固定指数(Fst)是反映群体间基因频率差异的指标, 可表示群体间特定位点的遗传分化, 固定指数越大, 表示该位点在群体间分化越大, 固定指数为0, 表示群体间该位点不发生分化。在ISSR标记检测中白桦种群间Fst=0.108 17,RAPD标记检测中Fst =0.129 36,都表明白桦群体间的遗传分化处于中等水平。姜静等(2001)采用RAPD技术对东北地区白桦种源遗传变异的研究也表明了遗传变异主要分布在种源内部的个体之间,与本文的研究结果基本一致。
木材纤维形态性状是复杂的数量性状,它是由个体基因型与外界生态环境相互作用的结果。对优良的纤维形态性状基于表型选择一直没有取得突破性的进展。分子标记技术的出现,为人们从分子水平上选育优良纤维性状的工业用材提供了技术支持。但目前利用分子标记对表型性状的辅助选择均基于高密度遗传图谱的构建和基因定位,还没有更直接、快速和有效的方法将表型性状和分子标记联系起来。在本研究中,通过对种群间木材纤维性状与分子标记的相关分析,得到了一些相关信息,但这些标记位点是否与决定白桦木材纤维性状的基因有直接联系,以及能否将这些位点用于未来的白桦遗传图谱的完善和数量性状的基因定位还有待于进一步研究。
郭明辉, 鲁英, 王万进, 等. 1999. 不同种源白桦木材密度和生长轮宽度径向变异模式. 东北林业大学学报, 27(4): 29-32. DOI:10.3969/j.issn.1000-5382.1999.04.007 |
郭明辉, 潘月洁, 陈广胜. 2000. 不同海拔高度白桦木材解剖特征径向变异. 东北林业大学学报, 28(4): 25-29. DOI:10.3969/j.issn.1000-5382.2000.04.007 |
姜静, 杨传平. 2001. 用RAPD技术对东北地区白桦种源遗传变异的分析. 东北林业大学学报, 29(2): 30-34. DOI:10.3969/j.issn.1000-5382.2001.02.008 |
刘萍, 孟宪红, 孔杰, 等. 2004. 中国对虾微卫星DNA多态性分析. 自然科学进展, 14(3): 333-338. DOI:10.3321/j.issn:1002-008X.2004.03.015 |
钱韦, 葛颂. 2001. 居群遗传结构研究中显性标记数据分析方法初探. 遗传学报, 28(3): 244-255. |
赵西平, 郭明辉, 朱熙岭. 2005. 小径木白桦锯材干燥质量的影响因素分析. 北京林业大学学报, 27(增刊): 47-50. |
Wu Chengjun, Cheng Zaiquan, Huang Xingqi, et al. 2004. Genetic diversity among and within populations of Oryza granulata from Yunnan of China revealed by RAPD and ISSR markers: implications for conservation of the endangered species. Plant Science, 167(1): 35-42. DOI:10.1016/j.plantsci.2004.02.022 |
Doyle J J, Doyle J L. 1990. Isolation of plant DNA from fresh tissue. Focus, 12(1): 13-15. |
Khasa P D, Dancik B P. 1996. Rapid identification of white-Engelmann species by RAPD markers. Theor Appl Genet, 92: 46-52. DOI:10.1007/BF00222950 |
Nei M. 1978. Estimation of average heterozygosity and genetic distance from a small number of individuals. Genetics, 89: 583-590. |
Panshin A J, Zeeuw C. 1980. Text book of wood technology. New Youk: Mc Graw-Hill Book Company: 83-90. |
Robert P A, Andrea E S, Naresh Pandey R. 2003. The concordance of terpenoid, ISSR and RAPD markers, and ITS sequence data sets among genotypes: an example from Juniperus. Biochemical Systematics and Ecology, 31(4): 375-387. DOI:10.1016/S0305-1978(02)00157-6 |
Taylor F W. 1968. Variation in size and proportion of wood elements in yellow poplar. Wood Sci Techn, 2: 153-165. |
Williams J G K, Kubelik A R, Livak K J, et al. 1990. DNA polymorphisms amplified by arbitrary primers are useful as genetic markers. Nucleic Acids Res, 18: 6531-6535. DOI:10.1093/nar/18.22.6531 |
 2007, Vol. 43
2007, Vol. 43