文章信息
- 金群英, 林二培, 彭华正, 桑庆亮, 华锡奇.
- Jin Qunying, Lin Erpei, Peng Huazheng, Sang Qingliang, Hua Xiqi.
- 早竹TB1同源基因的克隆和表达分析
- Cloning and Expression Analyzing of TB1 Homologous Gene in Phyllostachys violascens
- 林业科学, 2007, 43(8): 41-47.
- Scientia Silvae Sinicae, 2007, 43(8): 41-47.
-
文章历史
- 收稿日期:2006-07-26
-
作者相关文章
2. 浙江大学生命科学学院 植物生理生化国家重点实验室 杭州 310058
2. State Key Laboratory of Plant Physiology and Biochemistry College of Life Sciences, Zhejiang University Hangzhou 310058
竹子是禾本科(Poaceae)植物中最大的一族,全世界竹种总计1 200种以上(方伟, 1995)。竹子与水稻(Oryza sativa)、小麦(Triticum aestivum)等其他禾本科植物有着显著的不同,如快速生长能力、较高的木质化程度、开花规律的独特性等,并且常常形成大面积竹林,成为森林资源的重要组成部分。竹子地下茎(竹鞭)的生长和繁殖规律是竹子最重要的特色之一,按照地下茎的分枝类型,竹子基本上可分为3种,即散生竹(单轴型地下茎)、丛生竹(合轴型地下茎)和混生竹(兼有单轴和合轴型)(耿伯介等,1996;Li et al., 2006)。竹鞭上的侧芽在不同的发育阶段和环境中,可长成新鞭,也可以发育成竹笋。竹笋的快速生长能力使竹子成为世界上长得最快的植物。因此,竹笋发育过程的机制研究是竹子生长发育研究的热点。
现有的研究大多从解剖和生理的角度来探讨竹笋发育过程的有关问题,如张卓文等(1996)研究了早竹在不同发育阶段的解剖学特点,根据笋形成过程中外部形态和内部结构变化,将其划分为休眠期、萌动期、发育前期、发育中期、发育后期及出笋期。胡超宗等(1996)检测了雷竹鞭侧芽在分化过程中的激素变化,发现GA3、ZT和IAA的浓度在分化前明显增加。丁兴萃(1997)研究了毛竹(Phyllostachys edulis)笋体发育过程中不同部位IAA、GA3和ABA的活性及含量变化,发现在笋体生长初期IAA和GA3的浓度极高。更精确的酶联免疫检测表明,较高的生长素和细胞分裂素浓度与雷竹笋芽分化有关,而较高的生长素浓度也与竹笋的进一步快速生长状态相一致(黄坚钦等,2002)。上述研究虽然揭示了竹笋生长过程的一些特点,但是存在一些问题值得进一步探讨,例如生长素对植物的形态发育调节非常重要,生长素功能的发挥不仅与植物局部生长素浓度有关,还与植物生长激素受体的敏感性、其他激素信号途径和发育相关基因的表达有关(Woodward et al., 2005)。因此,现有的仅从营养激素水平进行的研究有相当大的局限性,有必要在此基础上开展竹笋发育基因调控机制的研究。另外,由于竹笋并非均匀整体,检测各种调控信号的空间分布是非常重要的,而现有一些取样和检测方法,即便是单个笋的取样,也容易把个体内部的内源激素差异相抵消,难以合理地解释竹笋的发育过程,甚至容易得出错误的结论。
竹笋的形成和生长发育过程涉及侧枝形态发生,探讨侧枝发育有关基因在竹笋发育过程中的作用,对于阐明竹笋发育基因调控机制有重要意义。现已发现参与侧枝发生的基因有的主要参与侧芽分生组织启动,也有的调控侧芽的长出(Ward et al., 2004)。玉米(Zea mays)Teosinte branched1(TB1)基因通常被认为是影响侧芽的长出,对于玉米的侧枝形成有重要的调控作用(Doebley et al., 1997)。目前,该同源基因的研究主要集中在水稻和高粱(Sorghum bicolor)等禾本科植物中(Takeda et al., 2003; Kebrom et al., 2006)。最近,对拟南芥(Arabidopsis thaliana) TCP基因家族序列和功能的深入研究发现,BRC1有可能是TB1基因在双子叶植物中的同源基因(Aguilar-Martinez et al., 2007)。竹子是颇具特色的禾本科植物,其侧枝发生过程较为复杂,特别是竹笋的形成和生长过程更是十分独特,而目前尚无竹子TB1同源基因的研究报导。
早竹(Phyllostachys violascens)是一个研究竹笋发育分子机制的重要模型。一方面,早竹出笋早,出笋量大,是优良的笋用竹种;另一方面,有关早竹出笋的生理生化机制已经有较多的研究基础(胡超宗等,1996;黄坚钦等,2002;何奇江等, 2005)。因此,本文从早竹中克隆了TB1的相似基因,通过序列进化分析,以及RT-PCR和原位杂交等检测,推测PpTB1很可能与禾本科其他植物TB1同源基因的作用相似。另外,TB1同源基因也可能在竹子分类和进化分析上有重要价值。
1 试验材料与方法 1.1 材料早竹(Phyllostachys violascens)、菲白竹(Pleioblastus fortunei)和乌脚绿竹(Bambusa odashimae)样品均取自浙江省林业科学研究院竹类植物园。
1.2 核酸提取DNA提取样品来自嫩叶,采用CTAB法。RNA提取样品来自竹笋,采用TRIZOL (BBI)提取(方法参照说明书),提取产物经电泳和吸光度检测完整性和纯度,用于RT-PCR分析的RNA样品A260/280 >2.0。
1.3 组织切片和原位杂交分析切取竹笋顶端0.5 cm左右,4%多聚甲醛磷酸缓冲液(pH 7.0)4 ℃固定过夜,酒精梯度脱水,二甲苯脱色,石蜡包埋,旋转切片机(Leica RM2135)切片10 μm,镜检挑选完整切片,按简化的原位杂交方法操作(Braissant et al., 1998)。构建核酸探针的模板为包含PpTB1编码区(CDS)的pBluescript质粒,反义和正义RNA探针分别由T3和T7 RNA聚合酶转录线性化后的质粒得到。另外挑选的一部分切片用于埃希氏苏木精染色,常规组织切片分析。
1.4 基因克隆和序列分析基因克隆采用BD SMARTTM RACE cDNA Amplification Kit (Clontech)试剂盒的3′RA CE方法,上游基因特异性引物为tb1f1: 5′GGAGTCCCATCAGTAAAGC3′。PCR扩增的片段经T-easy (promega)克隆,挑选3个克隆进行ABI377测序。从竹子基因组中克隆TB1同源基因片段,采用引物为tb1f1和tb1r1: 5′CGCATCCGG TTCTTCTCCTTGGT3′,扩增程序为:94 ℃ 4 min; 94 ℃ 30 s, 58 ℃ 60 s, 72 ℃ 1 min(30循环); 72 ℃ 5 min。序列比对采用Vector NTI suite9.0的组件AlignX完成(gap opening penalty 4, gap extension penalty 0.2 and PAM protein weight matrix)。分子进化树由MEGA3.1的邻接法(Neighbor-Joining)构建,1000次重复置信度分析。
1.5 RT-PCR检测利用BD SMARTTM RACE cDNA Amplification Kit (Clontech)进行逆转录,检测引物为tb1f2: 5′- AGGACGGCTCCAGCAGCCTCT-3′, tb1r2: 5′-GTGCGGGA GTAGTTCTAATACCGT-3′。对照PpACT1的扩增引物为act-f1: 5′-TTCATTG GTATGGAAGCTGCTG-3′和act-r1: 5′-GTAGCTTACATGGCAA GGACTTG-3′。所有PCR产物经测序确认。
2 结果与分析 2.1 PpTB1是TB1同源基因根据水稻和玉米的TB1同源基因的保守性,在5′UTR(Untranslated Region)区设计特异性引物,利用3′RACE从早竹笋芽的cDNA样品中克隆到一个1 296 bp基因片段。该序列包含1个编码349个氨基酸的阅读框,在氨基酸水平上与玉米TB1相似性达64.7%,定名为PpTB1。经BLAST搜索,发现PpTB1与来自Danthoniopsis dinteri的TB1同源基因(DdTB1)一致性最高。推定氨基酸序列的比对表明(图 1),PpTB1和DdTB1的一致性达71.7%,和玉米为64.7%,和水稻则只有62.6%。PpTB1含有保守的SP区、TCP区和R区,属于TCP基因家族的一个成员(图 1)。利用PpTB1基因两端的特异性引物,进一步从早竹基因组上克隆到该基因,证实该基因同已知的TB1同源基因一样没有内含子。上述基因序列组成和结构的相似性说明PpTB1很可能是TB1的同源基因。

|
图 1 TB1同源基因推定氨基酸序列比对 Fig. 1 Alignment of the putative amino acid sequence of TB1 homologous genes PpTB1、OsTB1、ZmTB1和DdT B1分别为早竹、水稻、玉米和Danthoniopsis dinteri TB1同源基因的推定氨基酸序列。黑底白字表示氨基酸相同,黑底灰字表示保守,灰底白字表示相似氨基酸,虚线表示空缺。保守区如图标识所示,分为SP区、TCP区和R区。已报导的DdTB1基因的编码区尚不完整,因此只能比较部分推定氨基酸序列。 Sequence alignment of the deduced amino acids of Phyllostachys violascens PpTB1(DQ842222), Oryza sativa OsTB1 (AY286002), Zea mays ZmTB1 (TB1, U94494) and Danthoniopsis dinteri DdTB1(AF322134) was conducted with AlignX. Regions of identity (white letter with black background), conservation (gray letter with black background), similarity (white letter with gray background) and gap (dashed) are indicated. The SP, TCP and R domain are predicted according to the characteristics of ZmTB1.Only partial putative amino acids sequence is considered for DdTB1 since its coding sequence is uncompleted. |
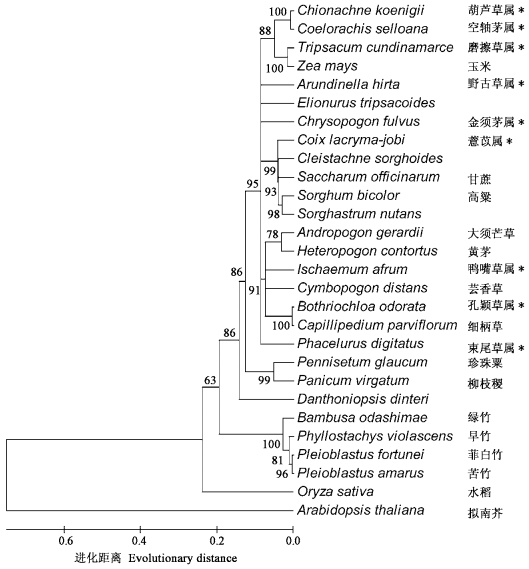
为进一步分析竹子TB1相似基因与已知TB1同源基因的相互关系,根据PpTB1序列特点,从乌脚绿竹、菲白竹和苦竹(Pleioblastus amarus)的基因组中克隆到TB1相似基因片段747 bp,分别命名为DeTB1、PfTB1和PaTB1。DNA序列比对表明,PpTB1与DeTB1、PfTB1和PaTB1的一致性分别为97.1%、9 8.4%和99.2%(图 2)。在此基础上,利用MEGA3.1进行了TB1同源物蛋白分子进化的重构,计算机模拟分析表明该进化树总体上具有较高的置信度(图 3)。从图中可以发现,拟南芥推定的TB1同源物BRAC1与其他禾本科TB1同源物的遗传距离较远,水稻TB1同源物较早从禾本科植物中分离出来,而竹子TB1同源物的分歧时间则介于水稻和现有其他TB1同源物之间。由于进化分析是证明同源基因的最有力证据(Theissen, 2005), 因此,上述结果进一步表明PpTB1、DeTB1、PfTB1和PaTB1是TB1同源基因。另外,该拓扑结构暗示,在竹亚科内部,混生竹种(菲白竹和苦竹)与散生竹种(早竹)的分歧时间较近,与丛生竹种(乌脚绿竹)的分歧时间较远,这一结论与现有的关于丛生竹较为原始的竹种系统分类观点一致。

|
图 2 4个竹子TB1基因相似序列比对 Fig. 2 Alignment of the four bamboo TB1-like sequences PpTB1、PaTB1、PfTB1和DeTB1分别表示早竹、苦竹、菲白竹和乌脚绿竹TB1同源基因部分序列。点号表示相同序列,不同的碱基用字母标出。 Sequence alignment of the partial gene sequences of Phyllostachys violascens PpTB1, Pleioblastus amarus PaTB1 (DQ910764), Pleioblastus fortunei PfTB1(DQ842225) and Bambusa odashimae DeTB1 (DQ842224) was conducted with AlignX. Regions of identity (dot) and difference (corresponding base) are indicated. |
|
图 3 部分TB1同源物的分子进化树分析 Fig. 3 The phylogeny reconstruction of the putative TB1-like homologs 该进化树主要根据SP区、TCP区、R区的氨基酸序列构建,采用邻接法,1 000次重复置信度分析。图中以物种名称指代同源基因,中文名空白处或星号标注表示其中文种名不清,进化树分支上的数字表示置信度百分数,标尺表示采用邻接法计算的进化距离。乌脚绿竹、早竹、菲白竹和苦竹为本文所克隆TB1相似基因,其余物种序列参考文献(Lukens et al., 2001)。 The phylogeny was reconstructed using SP, TCP and R domain by Neighbor-Joining method with Dayhoff Matrix Model and 1 000 bootstrap replicates, where number beside nodes stands for bootstrap value and the below scale stands for evolutionary distance. The homologous genes are indicated by species names, where Phyllostachys violascens, Pleioblastus amarus, Pleioblastus fortunei and Bambusa odashimae represent the genes cloned in this paper and the others come from reference (Lukens et al., 2001). |
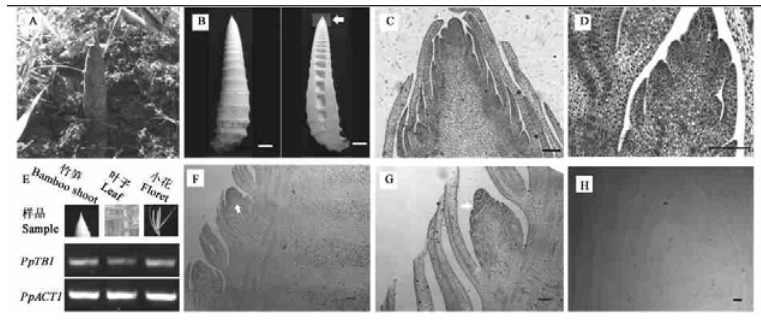
通过RT-PCR分析和原位杂交分析,可以进一步揭示PpTB1基因的表达特点,这对于揭示PpTB1基因在竹笋中的功能有重要意义。竹子不同器官RT-PCR分析表明,PpTB1不仅在笋中表达,在叶片和花器官中也有表达(图 4E)。显微切片显示,竹笋在一个非常小的空间中包含了许多复杂的分枝结构(图 4A, B, C, D)。原位杂交分析表明,PpTB1在侧芽的顶端有较强的表达,而在笋体的其他部位信号较弱(图 4F, G, H)。由此推测,PpTB1基因与竹子的侧芽发育有关。上述基因表达分析,特别是竹笋的原位杂交分析揭示,虽然PpTB1基因在竹子的各组织器官中均有表达,但是在组织器官内部的表达分布显然是不均匀的。由此,也进一步说明,在竹笋发育过程中,检测各种调控信号的空间分布是非常重要的,可以避免混合取样导致内部差异的抵消,有利于真正阐明各种调控信号的调控规律。
|
图 4 PpTB1的基因表达分析 Fig. 4 The gene expression analysis of Phyllostachys violascens PpTB1 A.竹笋; B.左半边为剥去笋壳后竹笋整体,右半边为内部切面,标尺为2 cm;C.竹笋顶部切片,位置如图B中箭头所示;D.笋中侧芽的局部放大;E.PpTB1基因在不同组织样品中的RT-PCR分析,PpACT1为ACTIN对照;F, G. PpTB1基因在竹笋中表达的原位杂交分析,主要表达位置如箭头所示;H.原位杂交正义探针的对照。C, D, F, G, H的标尺均为100 μm。 A. Bamboo shoot; B. The whole bamboo shoot without shell (left) and the longitudinal section (right), bar=2 cm; C. The microsection of apical part of bamboo shoot; D. The microsection of lateral bud of bamboo shoot; E. The RT-PCR analysis of PpTB1 expression among different tissues and organs with PpACT1 as a positive control; F, G. The in situ hybridization of PpTB1 expression in bamboo shoot which is mainly indicated by arrows; H. The negative control of PpTB1 in situ hybridization with sense probe. In C, D, F, G, H: bar = 100 μm. |
TB1基因属于高等植物所特有的TCP基因家族。根据基因序列的结构特征,TCP基因除了以玉米的TB1基因为代表,还包括金鱼草的CYC基因以及水稻的PCF1和PCF2基因(Cubas et al., 1999)。TCP基因编码的产物均有一个结构相似的TCP保守区,该保守区包含不典型的螺旋-环-螺旋结构(bHLH),可能与DNA的结合以及蛋白质的相互作用有关。另外,TB1同源物在上述保守区下游还有一个保守的R结构域(R-domain),可能形成一个亲水性α螺旋。目前已有研究的TCP基因均与分生组织发育有关,如CYC控制花分生组织的生长,TB1影响腋芽分生组织的生长,而PCF1和PCF2则是调控分生组织细胞分裂的有关基因。由此,可以推测TCP基因编码产物的上述结构特点与植物分生组织调控紧密相关。
虽然在墨西哥类蜀黍(Zea mays ssp. pamiglumis)进化为玉米的过程当中,TB1基因发挥了实质性的作用(Doebley et al., 1995; 1997),但是分子进化的分析表明,这一进化过程并没有对TB1的编码区形成正向选择,而是与启动子的序列进化有关系(Wang et al., 1999),即关于玉米分枝形态的进化选择主要影响了TB1基因的表达。因此,TB1编码区的中性进化方式使得它适合作为玉米及其近缘种的系统进化分子标记(Lukens et al., 2001)。有趣的是,水稻TB1同源基因不仅在编码序列上与玉米TB1基因非常相似,它们在基因组上的与其他基因的位置关系也是对应的,即存在所谓的局部共线性(Takeda et al., 2003)。近年来,竹子分子水平上的研究表明,竹子的基因组复杂度与水稻相似,特别是丛生竹,其基因组大小相当于多倍体的水稻(Gielis et al., 1997)。樊龙江等(2006)利用8个全长mRNA基因序列比较了麻竹(Dendrocalamus latiflorus)、绿竹和毛竹等竹类植物与水稻、玉米、大麦和小麦等禾本科作物之间的差异,发现竹类植物与水稻有着更相似的基因序列特征(GC含量分布和密码子使用频率)。由此,可以推测竹子TB1同源基因很可能与玉米TB1同源基因有着相似的序列进化特征。
竹子的分类问题是竹子研究中的一个突出问题,这是由于竹类植物开花周期长,多数竹子较少开花,偶有开花的也多不育,而花和果实等生殖器官却是竹亚科分属及属以上分类等级的主要依据(耿伯介,1982)。因此,在生殖性状不明的情况下,竹子分类常以营养性状为主,但营养体的特性容易受该竹种所处生长环境的影响,从而导致错误鉴定。随着竹子分子生物学研究的开展,分子进化方法与经典分类学研究方法的结合,有助于解决一些竹子分类的争论(李淑娴等,2002)。而利用同源基因的进化关系来推断各属的分类进化关系是其中一个较为有效的途径,但是由于对竹子遗传学背景研究较少,选择合适的同源基因较为困难。对于TB1同源基因,虽然其在竹子中是否存在自然选择尚有待克隆更多的基因序列进行分析和比较,但是本文通过不同竹种TB1同源基因的克隆和初步的序列分析(图 2),揭示TB1基因有可能作为竹子分类进化的分子标记。
3.2 TB1基因的表达和功能玉米tb1突变体的基因功能研究表明,TB1基因抑制玉米侧芽的长出(Doebley et al., 1997)。突变体表型分析和原位杂交分析显示,TB1基因在叶腋分生组织和穗原基的雄蕊部分表达,抑制侧芽的生长和雄花序的产生,促进顶端优势和雌花序的形成,由此表明,TB1基因的功能与其基因表达特点是紧密相关的(Hubbard et al., 2002)。水稻OsTB1的转基因研究表明,OsTB1的过量表达能抑制水稻侧芽的生长,但不影响侧芽的形成,利用GUS报告基因检测发现OsTB1在水稻整个侧芽、茎顶分生组织基部、木髓部维管组织和叶片结合处等部位表达(Takeda et al., 2003)。高粱(Sorghum bicolor)SbTB1基因也具有上述类似的表达规律和功能,进一步的研究还表明该基因受光敏色素B调节(Kebrom et al., 2006)。早竹PpTB1基因的原位杂交分析表明,PpTB1也集中在竹笋的侧芽、茎顶分生组织基部等处表达,由此可以推测PpTB1也可能与竹子侧芽的长出有关。在竹子的发育过程中,不仅是竹笋的形成和生长过程,还有新竹鞭的形成都涉及不同位置侧芽的长出,因此,进一步探索该基因的功能对于理解竹笋发育规律和竹子生长规律有着重要的价值,对于将来进一步利用基因工程技术开展竹笋丰产调控也有着重要意义。
另外值得一提的是,最近拟南芥上也开展了TB1相似基因的功能研究,这一研究结果暗示TB1同源基因在双子叶植物之中也是存在的(Aguilar-Martinez et al., 2007)。因此,借助于模式植物拟南芥初步验证竹子TB1基因的功能是下一步值得探索的重要思路。
丁兴萃. 1997. 毛竹笋体生长发育过程中内源激素的动态分析. 竹子研究汇刊, 16(2): 53-62. |
樊龙江, 郭兴益, 马乃训. 2006. 竹类植物与水稻等其它禾本科作物的系统进化关系及基因序列组成的比较. 林业科学研究, 19(2): 165-169. DOI:10.3321/j.issn:1001-1498.2006.02.007 |
方伟. 1995. 竹子分类学. 北京: 中国林业出版社.
|
耿伯介. 1982. 世界竹亚科各属的考订. 竹子研究汇刊, 1(1): 1-19. |
耿伯介, 王正平, 叶光汉, 等. 1996. 中国植物志:第九卷第一分册. 北京: 科学出版社.
|
何奇江, 汪奎宏, 华锡奇, 等. 2005. 雷竹开花期内源激素、氨基酸和营养成分含量变化. 林业科学, 41(2): 169-173. |
胡超宗, 金爱武, 张卓文. 1996. 竹鞭侧芽分化过程中内源激素的变化. 浙江林学院学报, 13(1): 1-4. |
黄坚钦, 刘力, 章滨森, 等. 2002. 雷竹地下鞭侧芽内源激素的动态变化研究. 林业科学, 38(3): 38-41. DOI:10.3321/j.issn:1001-7488.2002.03.007 |
李淑娴, 尹佟明, 邹惠渝, 等. 2002. 用水稻微卫星引物进行竹子分子系统学研究初探. 林业科学, 38(3): 42-48. DOI:10.3321/j.issn:1001-7488.2002.03.008 |
张卓文, 胡超宗, 金爱武. 1996. 雷竹鞭侧芽发育为笋的形态结构观察. 竹子研究汇刊, 15(2): 60-66. |
Aguilar-Martinez J A, Poza-Carrion C, Cubas P. 2007. Arabidopsis BRANCHED1 acts as an integrator of branching signals within axillary buds. Plant Cell, 19(2): 458-472. DOI:10.1105/tpc.106.048934 |
Braissant O, Wahli W. 1998. A simplified in situ hybridization protocol using non-radioactively labeled probes to detect abundant and rare mRNAs on tissue sections. Biochemica, 1: 10-16. |
Cubas P, Lauter N, Doebley J, et al. 1999. The TCP domain: a motif found in proteins regulating plant growth and development. Plant J, 18(2): 215-222. |
Doebley J, Stec A, Gustus C. 1995. Teosinte branched1 and the origin of maize: evidence for epistasis and the evolution of dominance. Genetics, 141: 333-346. |
Doebley J, Stec A, Hubbard L. 1997. The evolution of apical dominance in maize. Nature, 386: 385-388. DOI:10.1038/386385a0 |
Gielis J, Valente P, Bridts C, et al. 1997.Estimation of DNA content of bamboos using flow cytometry and confocal laser scanning microscopy//Chapman G. The Bamboos. Academic Press, London, 215-223
|
Hubbard L, McSteen P, Doebley J, et al. 2002. Expression patterns and mutant phenotype of teosinte branched1 correlate with growth suppression in maize and Teosinte. Genetics, 162: 1927-1935. |
Kebrom T H, Burson B L, Finlayson S A. 2006. Phytochrome B represses Teosinte Branched1 expression and induces sorghum axillary bud outgrowth in response to light signals. Plant Physiology, 140: 1109-1117. DOI:10.1104/pp.105.074856 |
Li Dezhu, Wang Zhengping, Zhu Zhengde, et al. 2006.The flora of China: Vol.22. Beijing: Science Press; St. Louis: Missouri Botanical Garden Press, 7-8
|
Lukens L, Doebley J. 2001. Molecular evolution of the teosinte branched gene among maize and related grasses. Mol Biol Evol, 18(4): 627-638. DOI:10.1093/oxfordjournals.molbev.a003843 |
Takeda T, Suwa Y, Suzuki M, et al. 2003. The OsTB1 gene negatively regulates lateral branching in rice. Plant J, 33: 513-520. DOI:10.1046/j.1365-313X.2003.01648.x |
Theissen G. 2005. Birth, life and death of developmental control genes: new challenges for the homology concept. Theory in Biosciences, 124: 199-212. DOI:10.1007/BF02814484 |
Wang R L, Stec A, Hey J, et al. 1999. The limits of selection during maize domestication. Nature, 398(6724): 236-239. |
Ward S P, Leyser O. 2004. Shoot branching. Current Opinion in Plant Biology, 7: 73-78. DOI:10.1016/j.pbi.2003.10.002 |
Woodward A, Bartel B. 2005. Auxin: regulation, action, and interaction. Annals of Botany, 95: 707-735. DOI:10.1093/aob/mci083 |
 2007, Vol. 43
2007, Vol. 43

