文章信息
- 郭同斌, 嵇保中, 诸葛强, 黄敏仁.
- Guo Tongbin, Ji Baozhong, Zhuge Qiang, Huang Minren.
- 转基因杨树对杨小舟蛾幼虫解毒酶活性的影响
- Effect of Transgenic Poplars on the Activities of Detoxification Enzymes in Micromelalopha troglodyta Larvae
- 林业科学, 2007, 43(5): 59-63.
- Scientia Silvae Sinicae, 2007, 43(5): 59-63.
-
文章历史
- 收稿日期:2005-08-19
-
作者相关文章
2. 南京林业大学森林资源与环境学院 南京 210037
2. College of Forest Resources and Environment, Nanjing Forestry University Nanjing 210037
昆虫解毒酶是一类异质酶系,能够代谢大量的内源或外源底物,这些解毒酶系主要包括酯酶(esterase)、羧酸酯酶(carboxylesterase, CarE),多功能氧化酶(mix-function oxidase, MFO)和谷胱甘肽S-转移酶(glutathione s-transferase, GST)等(丁双阳等,2001a)。对杀虫剂解毒代谢能力的增强是害虫产生抗药性的重要机理之一。在许多情况下,抗药性的产生是由于昆虫对杀虫剂的代谢能力提高,代谢杀虫剂的解毒酶可使有毒的外来化合物氧化、还原或水解,增加其产物的水溶性,从而使它们更容易从昆虫体内排出(翟启慧,1995;Mohan et al., 2003)。上述酶类除作用于化学药剂,其活性变化也可受植物中广泛存在的次生代谢物质的影响。Ortego等(1998)和Mukanganyama等(2003)研究证实玉米抗虫次生物质DIMBOA能够抑制禾谷缢管蚜(Rhopalosiphum padi)和西非蛀茎夜蛾(Sesamia nonagrioides)的中肠酯酶活力,用含DIMBOA不同添加浓度(0.5~4 mmol·L-1)的人工饲料饲喂禾谷缢管蚜,结果酯酶活性的抑制率达50%~75%。转基因杨树所表达的杀虫蛋白作为一种外源毒素,与杀虫剂和植物次生代谢物质一样,也能引起昆虫体内解毒酶活性变化,从而影响转基因植物的杀虫效果、使用寿命以及害虫的抗性发展等。丁双阳等(2001a;2001b)测定了转Bt和转CpTI基因杨树对美国白蛾(Hyphantria cunea)幼虫中肠解毒酶和乙酰胆碱酯酶活力的影响,认为转基因杨树对幼虫中肠酯酶、羧酸酯酶和多功能氧化酶等解毒酶活性的抑制可能是其毒杀害虫的作用机制之一。郭同斌等(2004)研究证实转Bt基因杨树(NL80106)对杨小舟蛾(Micromelalopha troglodyta)具有显著的杀虫活性,但转基因植物对杨小舟蛾体内解毒酶的影响还未见报道。为探明转基因杨树对杨小舟蛾的杀虫机理,本文以转Bt单基因和转Bt+CpTI双价基因杨树(NL80106)大田移植植株为材料,系统测定了杨小舟蛾幼虫取食转基因杨树叶片后,其中肠和血淋巴酯酶、羧酸酯酶的活性变化,研究了转基因杨树对害虫生理生化的影响,为其在防治中的应用及其抗性治理提供依据。
1 材料与方法 1.1 供试杨树品种及虫源转Bt单基因和转Bt+CpTI双价基因杨树无性系FB56、D18及未转化的对照(CK)杨树NL80106均由南京林业大学林木遗传和基因工程实验室提供,并于2002年春季定植于徐州市林业站苗圃,定植密度3万株·hm-2。2004年3月底前从林间采集杨小舟蛾越冬蛹,经室内饲养得到的幼虫用对照杨树叶片饲喂至3龄作为试验虫源。
1.2 转基因杨树饲喂处理取个体大小一致、刚蜕皮的3龄幼虫,饥饿2 h后分别用FB56、D18的大田移植植株顶部第3、4片展开叶进行室内群体饲养(郭同斌等,2004),饲喂至4、12、24、36和48 h后解剖并截取中肠,或提取血淋巴。对照用未转化杨树NL80106的叶片饲养至相应时间处理。
1.3 中肠酶源制备每个转基因杨树饲喂的每个时间处理计10头幼虫,5次重复共50头作为提取中肠的虫源。将10头幼虫置于预冷的蜡盘中截取中肠,后于-20 ℃冰箱中冰冻贮存。测定前取出稍融后,置于预冷的玻璃匀浆器中,加入4.0 mL 0.02 mol·L-1磷酸盐缓冲液(pH 7.0,含1%的聚乙烯吡咯烷酮)在冰浴中匀浆,匀浆液用GL-160G-Ⅱ型高速冷冻离心机(上海安亭仪器厂)0 ℃,10000r·min-1离心20min,取上清液作为酶源。
1.4 血淋巴酶源制备每个转基因杨树饲喂的每个时间处理计10头幼虫,3次重复共30头作为提取血淋巴的虫源。在冰盘上用眼科剪小心剪破供试昆虫的腹足,用微量毛细吸管从每头幼虫体内准确吸取5 μL,10头幼虫共50μL血淋巴,置于盛有2mL 0.02mol·L-1磷酸盐缓冲液(含少量苯基硫脲,防止血液氧化)的塑料离心管中,混匀后用GL-160G-Ⅱ型高速冷冻离心机0 ℃,10000r·min-1离心20min,取上清液作为酶源。
1.5 酯酶和羧酸酯酶的活力测定酯酶的活力测定参照Han等(1998)、陈松等(2002)和李飞等(2003)的方法(测定羧酸酯酶时,反应缓冲液中含3×10-5 mol·L-1毒扁豆碱)。酶反应体系为:于酶标板加样孔中依次加入150μL固牢兰RR盐和α-醋酸萘酯混合液,50μL 0.02mo l·L-1,pH 7.0的磷酸盐缓冲液,最后加入25μL酶液,迅速置于BIO-RAD Model 550型酶标仪(Microplate Read er)中检测,25 ℃,450nm,每隔25s读取光密度值1次,共记录20个值。每个中肠酶和血淋巴酶液标本重复测定3次。固牢兰RR盐和α-醋酸萘酯的配制浓度分别为1.5和3.0mmol·L-1,反应浓度分别为1和2mmol·L-1。
对上述相同饲喂时间测定的酶活力指标,采用SAS统计软件多重比较重复t检验法,测验不同转基因杨树叶片处理的平均酶活力与对照叶片处理的平均酶活力的差异显著性(高惠璇等,1995)。
1.6 酶源蛋白质含量测定采用考马斯亮蓝G-250染色法(王淳本,2003)测定各处理的酶源蛋白质含量。
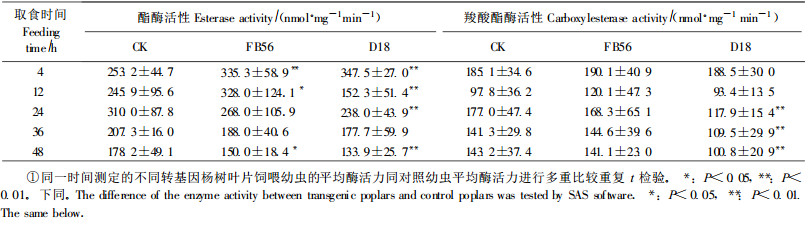
2 结果与分析 2.1 转基因杨树对中肠酯酶和羧酸酯酶活性的影响用FB56、D18和CK杨树叶片饲喂杨小舟蛾幼虫不同时间后测定其中肠酯酶和羧酸酯酶活性,结果见表 1。
|
|
杨小舟蛾幼虫取食CK杨树叶片4~12 h,中肠酯酶活性变化较为平缓,12 h后活性上升,24 h后下降。而取食转Bt单基因杨树叶片4~12 h,中肠酯酶活性变化平缓,12~48 h持续下降。取食转Bt+CpTI双价基因杨树4 h后,中肠酯酶的活性下降,12 h后开始回升,但24~48 h又持续下降。同取食CK杨树的幼虫中肠酯酶活性相比,取食转Bt单基因杨树4、12 h,中肠酯酶的活性显著高于CK,其中取食4 h与CK有极显著差异(P<0.01),12 h与CK有显著差异(P<0.05),表明害虫取食转Bt单基因杨树的初期,中肠酯酶活性较高,但取食24 h后活力开始受到抑制,取食24、36、48 h时,中肠酯酶平均活力分别较对照下降了13.5%、9.3%、15.8%;其中24、36 h抑制不明显,与CK的差异不显著;而48 h则与CK有显著差异(P<0.05),表明活性受到显著抑制。杨小舟蛾幼虫取食转双价基因杨树4 h的中肠酯酶活性极显著高于CK(P<0.01),但取食12 h后活性开始受到强烈抑制,取食12、24、48 h的活力与CK均存在极显著差异(P<0.01),分别比对照下降了38.1%、23.2%、24. 9%;取食12 h后达到活性抑制高峰(表 1)。因此,用上述2种转基因杨树饲喂杨小舟蛾幼虫,虽中肠酯酶活力在饲喂初期均高于对照,但随后即受到转基因杨树所表达的杀虫蛋白的抑制,表明害虫取食转基因杨树后,中肠酯酶活力先升高,然后在一定时间内受到抑制。进入抑制高峰的时间以转双价基因杨树为早(饲喂12 h);转双价基因杨树对中肠酯酶活力的抑制作用大于转Bt单基因杨树。
2.1.2 对中肠羧酸酯酶活性的影响用转Bt单基因杨树饲喂4~12 h,杨小舟蛾幼虫中肠羧酯酶活性高于对照,但差异不显著;24 h后中肠羧酯酶活性与CK均无显著差异。因此,害虫取食转Bt单基因杨树后,其中肠羧酸酯酶的活性没有受到显著抑制,表明转Bt单基因杨树对杨小舟蛾幼虫中肠羧酸酯酶的抑制能力不强。用转双价基因杨树饲喂4~12 h,其中肠羧酸酯酶活性与CK几乎无差异,但饲喂12 h后活性开始受到抑制,24 h达到抑制高峰。用转双价基因杨树饲喂24、36、48 h,幼虫中肠羧酸酯酶平均活性与对照均有极显著差异(P<0.01),分别比对照下降了33.4%、22.5%、29.6%(表 1)。因此,杨小舟蛾取食转双价基因杨树12 h后,其中肠羧酸酯酶的活力受到了显著抑制,转双价基因杨树对幼虫中肠羧酸酯酶的抑制作用显著大于转Bt单基因杨树。
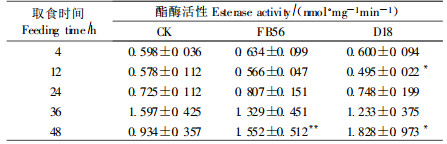
2.2 转基因杨树对血淋巴酯酶活性的影响用FB56、D18和CK杨树叶片饲喂杨小舟蛾幼虫不同时间后测定其血淋巴酯酶活性,结果见表 2。
|
|
用转Bt单基因杨树叶片饲喂4~36 h后,杨小舟蛾幼虫血淋巴酯酶活性持续上升,与用CK杨树饲喂的血淋巴酯酶活性无显著差异,表明前36 h内转基因杨树对血淋巴酯酶无抑制作用。饲喂36~48 h,对照血淋巴酯酶活性开始下降,而用转Bt单基因杨树叶片饲喂幼虫的血淋巴活性显著上升,48 h时两者有极显著差异(P<0.01),表明转Bt单基因杨树对杨小舟蛾幼虫血淋巴酯酶活性无抑制作用。用转双价基因杨树叶片饲喂的杨小舟蛾幼虫血淋巴酯酶活性变化,与转Bt单基因杨树的情况类似,转基因杨树和对照杨树饲养的幼虫血淋巴酯酶活性变化都表现为前36 h活力持续上升,36~48 h前者仍持续上升,而后者下降。用转双价基因杨树处理12、36 h,幼虫血淋巴酯酶平均活性较对照分别下降了14.4%、21.9%,其中12 h与对照有显著差异(P<0.05);但36~48 h时的活力不仅未受抑制,反而上升,与对照有显著差异(P<0.05,表 2)。因此,取食转双价基因杨树叶片的幼虫血淋巴酯酶活性在饲养初期受到抑制,但后期活性上升,未受到显著影响。
3 结论与讨论酯酶和羧酸酯酶是昆虫体内重要的解毒酶系,对分解外源有毒物质、维持正常生理代谢起着重要作用。张少燕等(2004)用含不同浓度Bt毒蛋白的人工饲料饲喂棉铃虫(Helicoverpa armigera),随着Bt毒蛋白浓度的升高,幼虫体内羧酸酯酶活力呈升高趋势。丁双阳等(2001a)研究证实转Bt基因杨树对美国白蛾幼虫中肠酯酶和羧酸酯酶有明显抑制作用,饲喂时间越长,活力下降越多,饲喂48 h后活性分别比对照降低了73.58%和56.55%。美国白蛾幼虫取食转CpTI基因毛白杨叶片后,中肠酯酶和羧酸酯酶的活力也受到明显抑制,饲喂48 h后分别比对照降低76.42%和73.91%(丁双阳等,2001b)。
本研究表明:杨小舟蛾幼虫取食2种转基因杨树叶片后,其中肠酯酶活力在饲喂初期均显著高于对照,表明害虫在取食转基因杨树的初期,Bt、CpTI等杀虫蛋白会引起中肠酯酶活力上升,以适应外界有毒物质的影响,这与张少燕等(2004)的报道一致。但取食一定时间后中肠酯酶和羧酸酯酶的活力受到了明显抑制,抑制的时间和强度取决于所饲喂的转基因杨树品种:取食转Bt单基因杨树的幼虫中肠酯酶活力在饲喂24 h开始受到抑制,48 h受到显著抑制;而转双价基因杨树在饲喂12 h受到极显著抑制。转Bt单基因杨树对杨小舟蛾幼虫中肠羧酸酯酶的抑制能力不强,但转双价基因杨树具有较强的抑制作用,饲喂24、36、48 h的中肠羧酸酯酶活力与对照存在极显著差异。转基因杨树通过抑制杨小舟蛾幼虫中肠酯酶和羧酸酯酶这2种重要的解毒酶活性而干扰昆虫正常的生理代谢,这可能是转基因抗虫杨树毒杀害虫的作用机制之一。转基因杨树(NL80106)对杨小舟蛾幼虫中肠2种解毒酶的抑制作用不如丁双阳等(2001a;2001b)报道的显著,其原因可能与转基因杨树杀虫蛋白表达量的高低及试虫本身的生理生化特性有关。此外,转双价基因杨树对2种解毒酶的抑制作用大于转Bt单基因杨树,这与作者对2种转基因杨树杀虫活性的生测结果是一致的(郭同斌等,2004)。
钟国华等(2001)用从杜鹃中分离的四环二萜类抗虫物质(闹羊花素Ⅲ)处理菜粉蝶(Pieris rapae)幼虫,中肠和血淋巴酯酶活性受到显著抑制。沙槎云等(1992)用Bt的2个菌株感染4龄末和5龄初粘虫(Mythimna separata)幼虫,4龄末幼虫血淋巴酯酶带与对照有差异,而5龄初幼虫的酯酶带与对照无明显变化。本研究表明:转Bt单基因和转双价基因杨树对杨小舟蛾幼虫中肠酯酯活力具有显著抑制作用,但对血淋巴酯酶的活性均没有显著影响。其原因可能与转基因杨树所表达的Bt、CpTI蛋白的杀虫机理有关。昆虫中肠为多种病原微生物、农药和各种毒素的作用靶标(王晓容,2000),Bt杀虫晶体蛋白的主要作用靶标为昆虫中肠,CpTI等丝氨酸蛋白抑制剂主要抑制中肠道内消化蛋白酶的活性(Knowels,1994;王琛柱等,1997)。Bt毒素或CpTI被害虫摄入后直接作用于幼虫中肠,因而它们对中肠解毒酶系活性的影响可能会大于对血淋巴解毒酶活性的影响。此外,乙酰胆碱酯酶(acetylcholinesterase, AChE)通常被认为是杀虫剂作用的靶标,丁双阳等(2001a;2001b)研究发现转Bt基因杨树对美国白蛾幼虫中肠乙酰胆碱酯酶活性无明显影响,转CpTI基因杨树对乙酰胆碱酯酶表现为全程受到抑制。本研究未能测出中肠乙酰胆碱酯酶的活力,但在整条虫体或头部中均检测到乙酰胆碱酯酶的活力,说明杨小舟蛾幼虫中肠乙酰胆碱酯酶分布极少,测定幼虫取食转基因植物后对该酶的影响意义不大。
陈松, 杨亦桦, 吴益东. 2002. 不同种群棉铃虫三龄幼虫酯酶活性频率分布与抗药性的关系. 昆虫学报, 45(6): 733-738. DOI:10.3321/j.issn:0454-6296.2002.06.006 |
丁双阳, 李怀业, 李学锋, 等. 2001a. 转Bt基因杨树对美国白蛾幼虫中肠解毒酶及乙酰胆碱酯酶的影响. 东北林业大学学报, 29(3): 28-30. |
丁双阳, 李怀业, 李学锋, 等. 2001b. 转CpTI基因杨树对美国白蛾幼虫中肠解毒酶及乙酰胆碱酯酶的影响. 东北林业大学学报, 29(5): 100-102. |
高惠璇, 李东风, 耿直, 等. 1995. SAS系统与基础统计分析. 北京: 北京大学出版社, 117-138.
|
郭同斌, 嵇保中, 诸葛强, 等. 2004. 转Bt基因杨树(NL-80106)对杨小舟蛾抗虫性研究. 南京林业大学学报:自然科学版, 28(6): 5-9. |
李飞, 韩召军, 唐波. 2003. 抗性品系棉蚜乙酰胆碱酯酶和羧酸酯酶的变异. 昆虫学报, 46(5): 578-583. DOI:10.3321/j.issn:0454-6296.2003.05.007 |
沙槎云, 谢强江. 1992. 感染苏云金杆菌后粘虫血淋巴中血细胞数量、蛋白质和酯酶的变化. 昆虫知识, 29(4): 215-217. |
王淳本. 2003. 蛋白质的定量测定//王淳本. 实用生物化学与分子生物学实验技术. 武汉: 湖北科学技术出版社, 202-204
|
王琛柱, 钦俊德. 1997. 植物蛋白酶抑制素抗虫作用的研究进展. 昆虫学报, 40(2): 212-218. DOI:10.3321/j.issn:0454-6296.1997.02.020 |
王晓容. 2000. 昆虫中肠生理与病理研究进展. 仲恺农业技术学院学报, 13(1): 58-68. |
钟国华, 胡美英, 林进添, 等. 2001. 闹羊花素-Ⅲ对菜粉蝶幼虫血淋巴和中肠酯酶的影响. 华中农业大学学报, 20(1): 15-19. DOI:10.3321/j.issn:1000-2421.2001.01.004 |
翟启慧. 1995. 昆虫分子生物学的一些进展:杀虫剂抗性的分子基础. 昆虫学报, 38(4): 493-501. DOI:10.3321/j.issn:0454-6296.1995.04.014 |
张少燕, 李典谟, 谢宝瑜. 2004. Bt毒蛋白对棉铃虫的生长发育和相关酶活性的影响. 昆虫知识, 41(6): 536-540. DOI:10.3969/j.issn.0452-8255.2004.06.008 |
Han Z, Moores G D, Denholm I, et al. 1998. Association between biochemical markers and insecticide resistance in the cotton aphid, Aphis gossypii Glover. Pesticide Biochemistry and Physiology, 62: 164-171. DOI:10.1006/pest.1998.2373 |
Knowles B H. 1994. Mechanism of action of Bacillus thuringiensis insecticidal δ-endotoxins. Advances in Insect Physiology, 24: 275-308. DOI:10.1016/S0065-2806(08)60085-5 |
Mohan M, Gujar GT. 2003. Local variation in susceptibility of the diamondback moth, Plutella xylostella (Linnaeus) to insecticides and role of detoxification enzymes. Crop Protection, 22: 495-504. DOI:10.1016/S0261-2194(02)00201-6 |
Mukanganyama S, Figueroa C C, Hasler JA, et al. 2003. Effects of DIMBOA on detoxification enzymes of the aphid Rhopalosiphum padi (Homoptera: aphididae). J Insect Physiol, 49(3): 223-229. DOI:10.1016/S0022-1910(02)00269-X |
Ortego F, Ruiz M, Castanera P. 1998. Effect of DIMBOA on growth and digestive physiology of Sesamia nonagrioides (Lepidoptera: Noctuidae) larvae. J Insect Physiol, 44(2): 95-101. DOI:10.1016/S0022-1910(97)00103-0 |
 2007, Vol. 43
2007, Vol. 43