文章信息
- 李春秀, 齐力旺, 史胜青, 汪阳东, 王建华, 张守攻.
- Li Chunxiu, Qi Liwang, Shi Shengqing, Wang Yangdong, Wang Jianhua, Zhang Shougong.
- 毛白杨纤维素合酶基因(PtoCesA1)的克隆及其在烟草中的遗传转化
- Isolation and Transformation in Nicotiana tabacum of a Cellulose Synthase Gene (PtoCesA1) from Populus tomentosa
- 林业科学, 2007, 43(3): 39-45.
- Scientia Silvae Sinicae, 2007, 43(3): 39-45.
-
文章历史
- 收稿日期:2005-12-09
-
作者相关文章
纤维素的基本单位是吡喃式D-葡萄糖,以β-1, 4-糖苷键相连,其葡萄糖残基约为2 000~2 500个。植物中的纤维素主要是以小微纤丝的形式存在,一般微纤丝是由36根β-1, 4 -葡糖苷链结晶而成,它是植物细胞里的主要成分。自然界每年有1 800亿t的纤维素生成,是地球上最丰富的生物大分子和重要的可再生资源(Delmer, 1999)。随着社会的快速发展,人类对植物纤维的需求激增,而过度利用自然界的植物纤维资源将对人类生存造成极大的破坏。植物纤维素生物合成机制的研究对材质改良、木材定向培育以及农业、造纸等化工业都十分重要,因此通过了解植物纤维素的生物合成机制,进而改善植物纤维的品质与产量就显得十分必要。相关研究已持续了30多年,但进展非常缓慢。1996年在棉花(Gossypium hirsutum)中克隆了第1个植物纤维素合酶基因,随后在拟南芥(Arabidopsis thaliana)全基因组测序后,发现了10个纤维素合酶基因(Li et al., 1993; Pear et al., 1996)。林木中克隆的第1个纤维素合酶基因是美国密西根大学从欧洲颤杨(Populus tremuloides)中得到的PtrCesA1基因,它是一个在木质部特异表达的纤维素合酶基因,共有2 973 bp,与次生壁的形成有关,在次生壁形成的时期,该纤维素合酶基因的表达丰度最高,该基因表达还受外来物理拉力信号的调控(Wu et al., 2000)。随后美国密西根大学先后报道了欧洲颤杨的PtrCesA2,PtrCesA3,PtrCesA4,PtrCesA5,PtrCesA6,PtrCesA7共6个基因(Samuga et al., 2002; Kalluri et al., 2003; 2004), 通过对以上基因的表达时期和部位的分析,发现PtrCesA1,PtrCesA2,PtrCesA3 的表达时期与表达部位很相似,因此推测这3个基因可能是在同一个纤维素合酶复合体中,共同完成杨树的次生壁的合成(Samuga et al., 2004);而PtrCesA4,PtrCesA5,PtrCesA7的表达时期和部位相似,推测它们可能与初生壁的形成相关(Kalluri et al., 2004); PtrCesA6与茎的伸长生长有关,在杨树枝条的快速生长期表达丰度高(Liang et al., 2004)。除了欧洲颤杨,在杂交杨(Populus tremula×P. tremuloides)中也克隆了纤维素合酶基因,同时还报道了几个类纤维素合酶基因(cls)参与纤维素的生物合成(Soraya et al., 2004)。虽然已克隆部分杨树纤维素合酶基因,目前还没有杨树纤维素合酶基因的转基因功能的研究报道。
毛白杨(Populus tomentosa)是我国特有的优质乡土树种,在杨属树种中,毛白杨以其速生丰产、纤维长度较长,成为最适的纸浆用材林树种之一。因此本研究选用毛白杨为材料来研究其纤维素合酶基因,克隆了PtrCesA1的同源基因毛白杨纤维素合酶基因PtoCesA1,构建了全长正义植物表达载体,进行了烟草(Nicotiana tabacum)的遗传转化,分析了转基因烟草的表型特征,为鉴定该基因的功能提供了试验证据。
1 材料与方法 1.1 材料植物材料为3年生毛白杨;植物表达载体pBI121(中国林业科学研究院分子生物学重点实验室提供);pGEM-T载体(Promega);RNase A (Takara);蛋白酶(华绿渊生物试剂公司);Taq DNA聚合酶(Promega);IPTG、X-gal、氨苄青霉素、卡那霉素和羧苄青霉素(Sigma);cDNA合成试剂盒(Clontech);Triziol RNA提取试剂盒(Invitrigion)。
1.2 方法 1.2.1 RNA纯化取毛白杨2年生枝条的皮下形成层及次生木质部组织(Hu et al., 1998),迅速放入液氮中研磨成粉末状,并立即放入Triziol RNA提取液中,按照Invitrigion公司Triziol试剂盒的操作方案纯化RNA。
1.2.2 cDNA的合成及克隆cDNA用Smart cDNA Library Construction Kit (Clontech)合成。设计引物PA1FF:5′-GTCGACCCACGCGTCCGTCTTGAAAGAATA-3′;PA 1 FR:5′-CCCCAAAATACTGGGAGAGACTTATTGGAG-3′,以毛白杨CDNA为模板进行PCR反应,条件为:94 ℃预变性5 min;94 ℃ 30 s与68 ℃ 3 min为1个循环,共35个循环;72 ℃延伸7 min。回收PCR产物,取5 μL回收的DNA片段连接到T-载体上,转化大肠杆菌(Escherichia coli) DH 5α菌株,蓝白斑筛选,质粒提取,酶切鉴定片段大小后进行测序鉴定。
1.2.3 植物表达载体的构建cDNA的PCR扩增,PCR产物的回收、连接、酶切,感受态细胞制备,质粒DNA的提取、连接、转化,以及琼脂糖凝胶电泳分析均按萨母布鲁克等(2001)的方法进行, 构建的正义植物表达载体命名为pBIPA1。
1.2.4 农杆菌转化按照萨母布鲁克等(2001)的方法制备农杆菌(Agrobacterium)GV3101感受态,采用热激法将质粒pBIPA1和pBI121转化到农杆菌GV3101,热激温度为42 ℃,时间为90 s。
1.2.5 根癌农杆菌介导的遗传转化和转基因植株再生接种转化农杆菌阳性单克隆在含卡那霉素50 mg·L-1的LB培养基中振荡培养过夜,取5 mL菌液加入50 mL含卡那霉素50 mg·L-1的LB培养基中,200 r·min-1振荡培养至OD600为0.5左右备用。用解剖刀将鲜嫩的烟草组培苗叶划成条状,放入备好的菌液中5 min,取出沥干后,共培养3 d,再转入含有卡那霉素和氨苄青霉素的选择培养基中分化再生抗性植株。
1.2.6 转化植株PCR和Southern鉴定用CTAB法提取转化烟草植株的基因组DNA。PCR鉴定采用25 μL体系。具体条件为94 ℃预变性5 min;94 ℃ 1 min和68 ℃ 1 min 30 s为一个循环,共35个循环;72 ℃延伸7 min。转化烟草的PCR分子检测采用插入基因片段和载体上的nptⅡ基因序列PCR联合检测。设计引物CC1F:5′-TGGTCTAGAGTGGCT TACTTCTGTCATATG-3′;CC1R:5′-CTCGGATCCAGGATGCACATTGCCTCTCGA-3′和引物nptⅡ F:5′-AACAAGATGGATTGCACGCAGGTTCTCCGG-3′;nptⅡR:5′-GAACT CGTCAAGAAGGCGATA GAAGGCGAT-3′,同时检测插入基因片段和表达载体的nptⅡ基因片段。
Southern杂交按照DIG High Prime DNA Labeling and Detection Starter Kit Ⅰ试剂操作指南进行, 转基因烟草基因组DNA用内切酶FoxⅠ消化。探针设计选取nptⅡ基因中约350 bp的DNA片段为杂交探针。
1.2.7 转基因烟草的表型测定测定转基因阳性烟草的株高、节间距、基径、叶片的长度和宽度;测定次生木质部厚度、胞壁厚度。
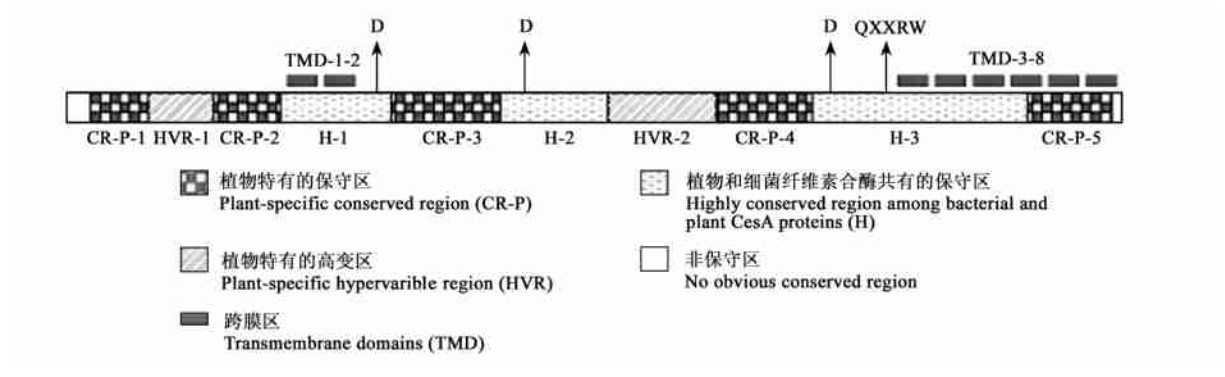
2 结果与分析 2.1 基因克隆以毛白杨cDNA为模板,克隆了基因PtoCesA1, 其基因序列为3 215 bp, 与欧洲颤杨的PtrCesA1的同源性为97%(Joshi,2003)。该基因具有开放的阅读框,编码区在52~2 988碱基之间,为2 937 bp, 编码979个氨基酸。将其与典型的植物纤维素合酶基因(Richmond et al., 2000;Richmond,2000)进行比较,结构特点如图 1:具有纤维素合酶共有的D,D,DQXXRW保守区,5个植物纤维素合酶所特有的保守区CR-P,2个植物纤维素合酶基因所特有的高变区,8个跨膜区,因此确认3 215 bp的DNA片段为毛白杨的一个全长纤维素合酶基因,命名为PtoCesA1基因(GenBank注册号DQ004570)。
|
图 1 PtoCesA1纤维素合酶的结构 Fig. 1 Structure of PtoCesA1 cellulose synthase |
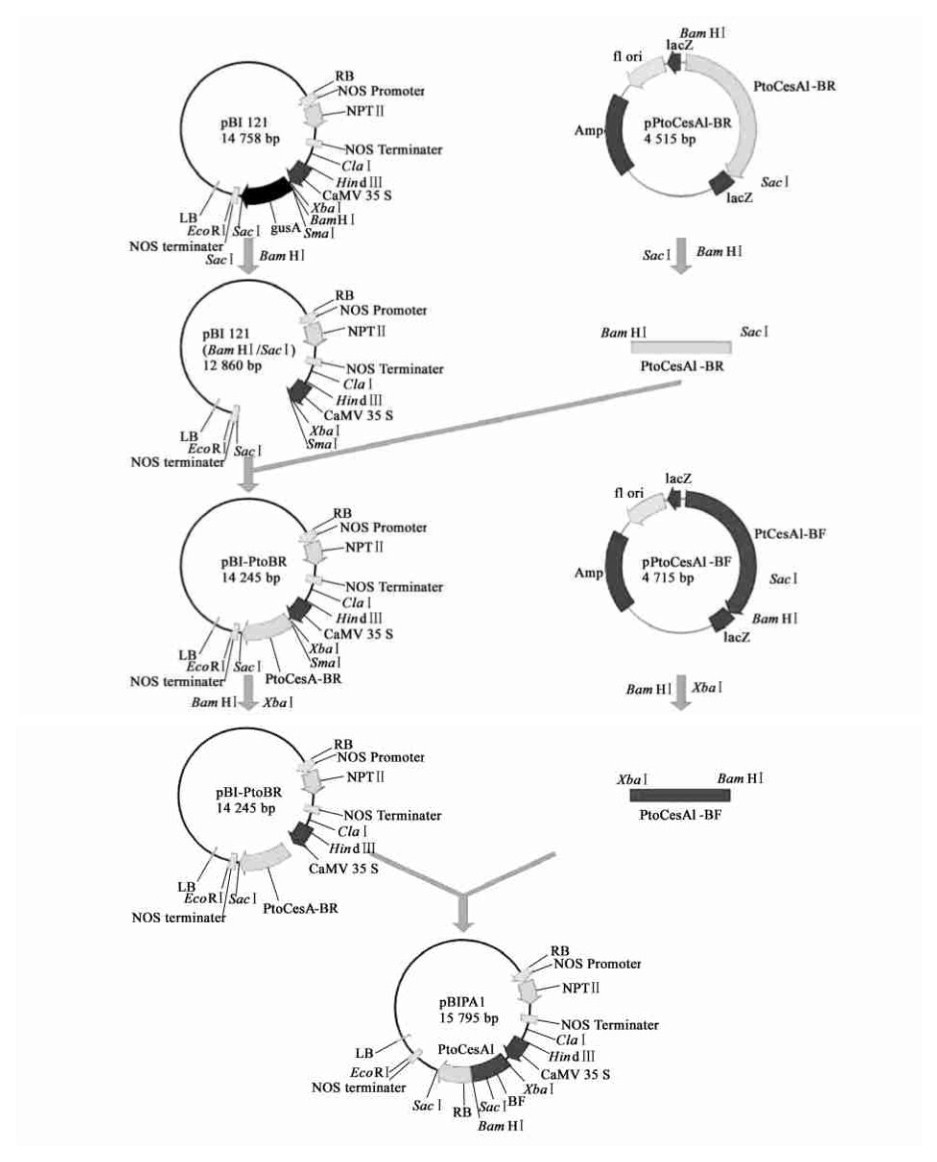
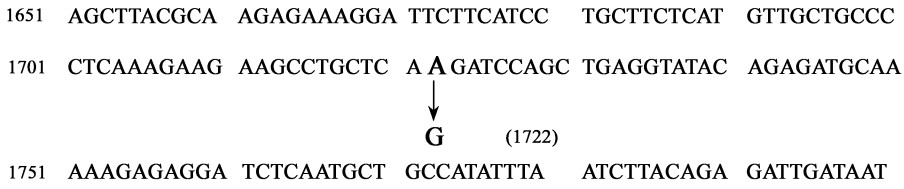
采取了如下策略将全长基因两步克隆到植物表达载体pBI121中(图 2)。从编码区的第1个碱基开始计数,从1 772至1 728的碱基序列与BamHⅠ的碱基序列只相差一个碱基,即1 722位的碱基A,它在编码氨基酸的密码子中正好为第3个碱基,根据氨基酸密码子的规律,密码子第3个碱基的变化不会影响它所编码的氨基酸(图 3),因此通过设计引物:pa1bamhr 5′-gct gga tcc tga gca ggc ttc ttc ttt gag-3′和pa1bamhf 5′-tca gga tcc agc tga ggtplant-specific conserved region ata cag aga tgc-3′将1 722位的碱基A变为碱基G(下划线的G),引入了酶切位点BamHⅠ。以引入的BamHⅠ酶切位点为分界点将全长基因分为PtoCesA1-BR和PtoCesA1-BF两段。其中PtoCesA1-BF带有SacⅠ酶切位点。先利用SacⅠ和BamHⅠ 2个酶切位点将不带SacⅠ酶切位点PtoCesA1-BR连入植物表达载体pBI121中,然后利用BamHⅠ和XbaⅠ酶切位点将PtoCesA1-BF连入pBI121-BR载体上,构建好的表达载体命名为pBIPA1。总体的构建策略见图 2。
|
图 2 PtoCesA1基因植物表达载体的构建 Fig. 2 Construction of plant expression vector of PtoCesA1 |
|
图 3 同义突变引入BamHⅠ在PtoCesA1中的位置 Fig. 3 Introduction BamHⅠ site in PtoCesA1 by synonymous mutation |
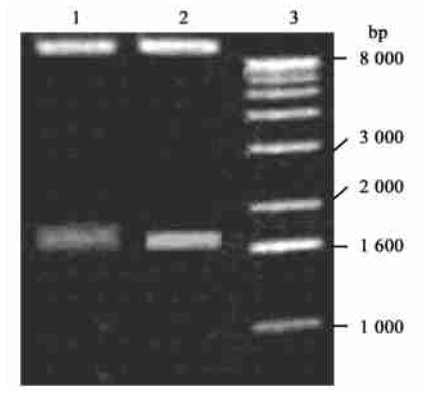
根据表达载体pBIPA1酶切位点的分析,该载体经SacⅠ单酶切后与用XbaⅠ和BamHⅠ双酶切后,应出现2条带谱,一条带谱超过8.0 kb,一条为1.7 kb左右。pBIPA1表达载体质粒DNA酶切电泳后出现如下电泳谱(图 4),符合预期结果。用PtoCesA1基因的两端引物进行PCR检测扩增出预期目的大小的片段(图 5)。证明全长基因PtoCesA1基因已构建到植物表达载体pBIPA1中。
|
图 4 植物表达载体pBIPA1的酶切电泳图 Fig. 4 Identification of pBIPA1 by digestion 1: SacⅠ酶切产物Digestion by SacⅠ; 2: XbaⅠ和BamHⅠ双酶切产物Digestion by XbaⅠ and BamHⅠ; 3:分子量标记Molecular weight marker. |
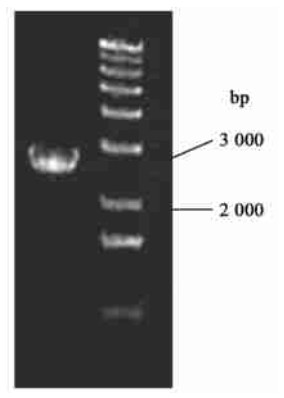
|
图 5 植物表达载体pBIPA1的PCR鉴定 Fig. 5 PCR identification of PtoCesA1 from pBIPA1 |
转基因烟草的PtoCesA1基因片段检测和nptⅡ序列检测都为阳性,PCR检测的电泳图见图 6。
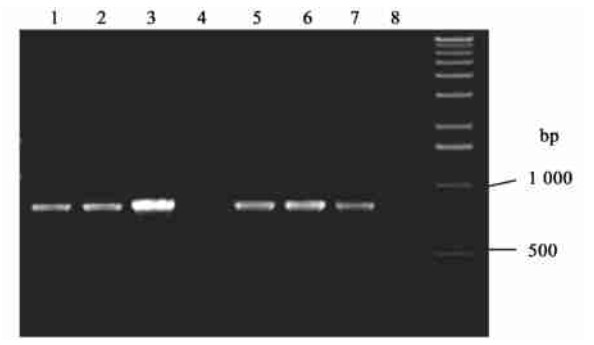
|
图 6 pBIPA1表达载体转基因烟草的nptⅡ和PtoCesA1基因片段联合PCR联合检测 Fig. 6 Co-detection of nptⅡ gene and PtoCesA1 fragment of transgenic tobacco with pBIPA1 1-3:扩增的PtoCesA1基因片段PtoCesA1 fragment of transgenic tobacco; 4,8:阴性对照Non-transformed tobacco sample as negative control; 5-7:扩增的nptⅡ基因片段nptⅡ fragment of transgenic tobacco. |
为了进一步证明目的基因片段已整合到转基因植株的基因组中,提取PCR检测为阳性的植株的基因组DNA进行Southern杂交检验(图 7)。以未转化的烟草基因组DNA为阴性对照。试验结果表明:转化PtoCesA1基因的烟草基因组DNA酶切的片段能够与nptⅡ基因片段标记的探针结合;而对照烟草的基因组DNA酶切的片段不能与nptⅡ基因片段标记的探针结合,说明外源基因已经整合到烟草的基因组中。
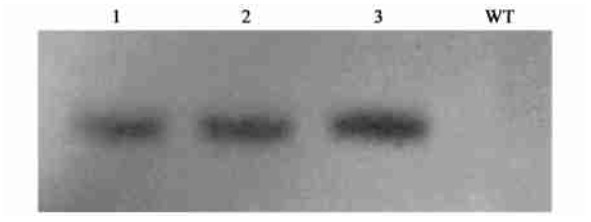
|
图 7 PtoCesA1转基因烟草的Southern杂交结果 Fig. 7 Southern detection of transgenic tobacco with PtoCesA1 1-3:转基因烟草植株Transgenic tobacco with PtoCesA1;WT:野生型烟草(阴性对照) Wild type tobacco (negative control).转基因烟草基因组DNA用内切酶FoxⅠ消化DNA of transgenic tobacco digested by FoxⅠ. |
转基因烟草表现为植株生长受到抑制,植株高度低于对照植株,基径和叶片均小于对照植株。转基因植株的基部木质部厚度也比对照植株和野生型植株小,纤维细胞壁厚度也有所减小(图 8,表 1)。而空载体pBI121的转基因烟草与野生型烟草的表型差异不显著。

|
图 8 PtoCesA1转基因烟草的表型 Fig. 8 Morphologic features of transgenic tobaccos with PtoCesA1 1,2:转基因植株 Transformed plant with PtoCesA1;ck: pBI121空载体对照植株 pBI121 control plant. |
|
|
植物纤维素合酶基因的研究近年来获得了可喜的进展,在40多个不同植物中,已有164 000多个与纤维素合酶基因相关的序列报道,序列比较分析表明,不同物种之间的同源纤维素合酶基因的同源性远高于同一物种中不同纤维素合酶基因之间的同源性(Saxena et al., 2005)。拟南芥纤维素合酶基因突变体的发现为纤维素合酶基因精细功能的研究提供了可能,在拟南芥已获得纤维素合酶基因的突变体5个,相应的纤维素合酶基因功能得到了初步鉴定(周晓馥等,2002)。但林木作为多年生植物,其纤维素合酶基因的功能研究非常困难。在欧洲颤杨中先后报道了PtrCesA1,PtrCesA2, PtrCesA3, PtrCesA4, PtrCesA5, PtrCesA6共6个基因(Reiter,2002; Satoshi et al., 2002; Zhong et al., 2003),但由于纤维素合酶基因较长,全长转基因功能鉴定相对困难,至今都还没有转基因的功能研究报道,各基因的确切功能及各基因的相互作用模式都还不清楚。在烟草和拟南芥中开展的纤维素合酶基因转基因功能的研究,都是从反义敲除的途径来研究的,均没有纤维素合酶基因正义全长转基因的研究报道。Burton等(2000)利用病毒诱导植物纤维素合酶基因沉默的方法来研究CesA基因的功能,将与CesA基因相关的3个特异cDNA片段分别插入马铃薯(Solanum tuberosum)X病毒载体中,接种到烟草上进行基因功能分析。结果感染的植株表现出节间缩短、小叶和侏儒症状,叶表面由于缺少纤维素而表现为细胞膨胀,叶片的多聚糖含量降低了25%。CesA基因的转录水平降低,表明cDNA片段沉默了一个或多个纤维素合酶基因的表达。
本研究从中国的乡土树种毛白杨中克隆得到了欧洲颤杨PtrCesA1基因的同源基因PtoCesA1,构建了全长的正义植物表达载体,获得了烟草转基因植株。阳性转基因植株的表型与已报道的烟草纤维素合酶基因反义转基因植株表型有相似之处,都表现为植株的生长受到抑制,即解剖和显微构造上出现木质部的厚度和纤维细胞壁厚度有所下降,形态特征表现为植株的株高降低,叶片变小。这些研究结果说明,本研究克隆的毛白杨的纤维素合酶基因直接参与植物纤维素的生物合成。但是,为什么正义植物表达载体在烟草中的表达会抑制植株的生长?现有的研究结果表明,单个纤维素合酶是组装在纤维素复合体中参与纤维素的生物合成。也就是说,复合体中某一个纤维素合酶的过量表达不会影响纤维素合酶复合体的数量,不会促进纤维素的合成(Doblin et al., 2002)。本研究的结果显示,PtoCesA1基因的过量表达不但没有促进植株的生长,反而抑制了植株的生长。试验结果和预期结果的差异,可以用转基因研究中常见的转录后基因沉默现象(PTGS)得到合理的解释,即正义转基因植株由于转录后基因的沉默,表现出反义抑制的表型。Napoli等(1990)最早发现了这一现象,他们利用查尔酮合酶基因CHS转化紫花矮牵牛(Petunia hybrida),预期使花色加深,结果却得到许多浅色和杂色花,因此发现了基因沉默。Jorgensen(1990)则将这一现象称为共抑制现象(co-suppression)。随后Guo等(1995)在线虫的par-1基因研究中,向线虫注射反义RNA,期望造成par-1基因失活,却发现注射正义R NA的对照也出现par-1基因关闭现象。Fire等(1998)明确了造成这种现象的原因是双链RNA的作用,在动物中被称之为RNA干扰(RNA interference)。在植物研究中,这种由双链RNA诱导的抑制基因表达的现象,一般被称为转录后基因沉默(PTGS)(Baulcombe, 2000)。可见pBIPA1在烟草中的表达可能在烟草体内转录形成了双链RNA(dsRNA),诱导抑制了PtoCesA1在烟草中的内源同源基因的表达,影响了烟草纤维素的生物合成,从而抑制了转基因烟草的生长。另一方面,还可以从纤维素生物合成的机制角度分析其原因,可能PtoCesA1在转基因植株中的过量表达,使纤维素合酶复合体中某一个亚基的相似亚基过量表达,打破了纤维素合酶复合体组装的外部环境,进而影响了复合体的组装,从而影响了纤维素的生物合成(Robyn, 2001)。下一步将利用本研究获得的全长正义表达载体的转基因植株作为材料,研究其外源基因在植株内表达情况和作用机制,为研究纤维素合酶作用机制提供更好的理论依据。
周晓馥, 王景余, 王兴智. 2002. 植物纤维素合成酶基因的研究进展. 遗传, 24(3): 376-378. DOI:10.3321/j.issn:0253-9772.2002.03.039 |
萨母布鲁克J, 拉塞尔D W. 2001. 分子克隆实验指南. 3版. 黄培堂等, 译. 北京: 科学出版社, 2-137
|
Baulcombe D A. 2000. Silence that speaks volumes. Nature, 404: 804-808. DOI:10.1038/35009245 |
Burton R A, Gibeaut D M, Bacic A, et al. 2000. Virus-induced silencing of a plant cellulose synthase gene. Plant Cell, 12(5): 691-706. DOI:10.1105/tpc.12.5.691 |
Delmer D P. 1999. Cellulose biosynthesis: exciting times for a difficult field of study. Annu Rev Plant Physiol Plant Mol Biol, 50: 245-276. DOI:10.1146/annurev.arplant.50.1.245 |
Doblin M S, Kurek L, Jacob-wilk D, et al. 2002. Cellulose biosynthesis in plants: from genes to rosettes. Plant Cell Physiol, 43: 1407-1420. DOI:10.1093/pcp/pcf164 |
Fire A, Xu S Q, Montgonery M K, et al. 1998. Potent and a specific genetic interference by double 2 stranded RNA in Caenorhabditis elegans. Nature, 391: 806-811. DOI:10.1038/35888 |
Guo S, Kemphues K J. 1995. par-1, a gene required for establishing polarity in C. elegans embryos, encodes a putative Ser/Thr kinase that is asymmetrically distributed. Cell, 81(4): 611-620. DOI:10.1016/0092-8674(95)90082-9 |
Hu W J, Kawaoka A, Tsai C J, et al. 1998. Compartmentalized expression of two structurally and functionally distinct 4-coumarate: CoA ligase genes in aspen (Populus tremuloides). Proc Natl Acad Scu USA, 95(9): 5407-5412. DOI:10.1073/pnas.95.9.5407 |
Jorgensen R. 1990. Altered genes expression in plants due to trans interactions between homologous genes. Trends Biotechnol, 8(12): 340-344. |
Joshi C P. 2003. Xylem specific and tension stress responsive expression of cellulose synthase genes from aspen trees. Appl Bioche Biotechnol, 105-108: 17-25. |
Kalluri U C, Joshi C P. 2003. Isolation and characterization of a new, full-length cellulose synthase cDNA, PtrCesA5 from developing xylem of aspen trees. J Exp Bot, 54(390): 2187-2188. DOI:10.1093/jxb/erg232 |
Kalluri U C, Joshi C P. 2004. Differential expression patterns of two cellulose synthase genes are associated with primary and secondary cell wall development in aspen trees. Planta, 220(1): 47-55. DOI:10.1007/s00425-004-1329-z |
Li L, Brown R M Jr. 1993. [beta]-glucan synthesis in the cotton fiber Ⅱ: Regulation and kinetic properties of [beta]-glucan synthases. Plant Physiol, 101(4): 1143-1148. DOI:10.1104/pp.101.4.1143 |
Liang X, Joshi C P. 2004. Molecular cloning of ten distinct hypervariable regions from the cellulose synthase gene superfamily in aspen trees. Tree Physiol, 24(5): 543-550. DOI:10.1093/treephys/24.5.543 |
Napoli C, Lemieux C, Jorgensen R. 1990. Introduction of chimeric chalcne synthase gene into Petunia result in reversible cosuppression of homologous gene in trans. Plant Cell, 2(4): 279-289. DOI:10.2307/3869076 |
Pear J, Kawagoe Y, Schrechengost W. 1996. Higher plants contain homologs of the bacterial CelA genes encoding the catalytic subunit of the cellulose synthase. Proc Natl Acad Sci USA, 93: 12637-12642. DOI:10.1073/pnas.93.22.12637 |
Reiter W D. 2002. Biosynthesis and properties of the plant cell wall. Curr Opin in Plant Biol, 5: 536-542. DOI:10.1016/S1369-5266(02)00306-0 |
Richmond T A, Somerville C R. 2000. The cellulose synthase superfamily. Plant Physiol, 124: 495-498. DOI:10.1104/pp.124.2.495 |
Richmond T. 2000. Higher plant cellulose synthases. Genome Biol, 1(4): 3001-3006. |
Robyn M. 2001. Cellulose: How many cellulose synthases to make a plant?. Current Biology, 11: 213-216. DOI:10.1016/S0960-9822(01)00068-9 |
Samuga A, Joshi C P. 2004. Cloning and characterization of cellulose synthase-like gene, PtrCSLD2 from developing xylem of aspen trees. Physiol Plant, 120(4): 631-641. DOI:10.1111/j.0031-9317.2004.0271.x |
Samuga A, Joshi C P. 2002. A new cellulose synthase gene(PtrCesA2) from aspen xylem is orthologous to Arabidopsis AtCesA7(irx3)gene associated with secondary cell wall synthesis. Gene, 296(1/2): 37-44. |
Satoshi K, Tetsuo K. 2002. Recent progress in cellulose biosynthesis. J Plant Res, 115: 297-302. DOI:10.1007/s10265-002-0037-7 |
Saxena I M, Brown R M. 2005. Cellulose biosynthesis: current views and evolving concepts. Ann Bot, 96(1): 9-21. DOI:10.1093/aob/mci155 |
Soraya D, Henrik A, Peter N, et al. 2004. Identification and expression analysis of genes encoding putative cellulose synthases (CesA) in the hybrid aspen, Populus tremula (L.) × P. tremuloides (Michx.). Cellulose, 11(3/4): 301-312. DOI:10.1023/B:CELL.0000046408.84510.06 |
Wu L, Joshi C P, Chiang V L. 2000. A xylem-specific cellulose synthase gene from aspen(Populus tremuloides) is responsive to mechanical stress. Plant J, 22(6): 495-502. DOI:10.1046/j.1365-313x.2000.00758.x |
Zhong R, Morrison W H, Freshour G D, et al. 2003. Expression of a mutant form of cellulose synthase AtCesA7 causes dominant negative effect on cellulose biosynthesis. Plant Physiol, 132(2): 786-795. DOI:10.1104/pp.102.019331 |
 2007, Vol. 43
2007, Vol. 43


