文章信息
- 陈辉, 李宗波, 唐明.
- Chen Hui, Li Zongbo, Tang Ming.
- 华山松大小蠹成虫触角感受器的扫描电镜观察
- Scanning Electron Microscope Observation on Antenna of Dendroctonus armandi (Coleoptera :Scolytidae)
- 林业科学, 2006, 42(11): 156-158.
- Scientia Silvae Sinicae, 2006, 42(11): 156-158.
-
文章历史
- 收稿日期:2005-08-12
-
作者相关文章
小蠹虫在入侵、定居和繁殖的整个生命过程中, 无论是种内与种间的信息通讯与配偶的寻找, 还是在寄主树木组织内的取食和繁殖数量的调节, 均依赖于广泛分布于小蠹虫触角上的各种感受器(尤其是化学感受器)来接受或感受寄主树木次生代谢物质的引诱和对异性的准确定位(Byers, 1995; 陈辉, 2003)。Thomas等(1991)研究表明:寄主树皮含有引诱小蠹虫取食的化学刺激物, 轻微损伤或风折等造成的寄主损伤有利于引诱小蠹虫的入侵危害。Hynum等(1990)认为山松大小蠹(Dendroctonus penderosa)入侵数量取决于寄主树木树皮萜烯和β -水芹烯的浓度。Silverstein(1970), Kinzer等(1969)指出西松大小蠹(D.brevicomis)雌成虫产生的性外激素(+)-exo -brevicomin、(-)-frontalin与寄主分泌的月桂烯具有协同作用, 能引诱西松大小蠹在寄主树木上的集中危害。Whitehend(1981)、Hallberg(1982)、毋亚梅等(2000)、王玉刚等(2003)分别利用扫描电镜对山松大小蠹、云杉八齿小蠹(Ips typographus)、松纵坑切梢小蠹(Tomicus piniperda)、红脂大小蠹(D.valens)触角感受器进行了观察, 表明触角上分布着大量的化学感受器, 在寄主选择和食物鉴别上具有重要的作用。触角是昆虫最主要的感受器官, 研究触角感受器的形态、结构和分布是探索昆虫嗅觉行为和识别机制的前提。华山松大小蠹(D.armandi)是华山松(Pinus armandi)的初期性蛀干害虫, 主要危害健康华山松, 导致健康华山松树势迅速衰弱诱发大量次期性小蠹虫的集中危害, 从而成为秦岭巴山林区健康华山松的毁灭性先锋害虫和华山松小蠹生态系统的先驱。同时, 华山松大小蠹的持续发生也成为秦岭巴山林区森林生态系统保护的最大障碍之一(陈辉, 1999)。本研究旨在通过对华山松大小蠹雌雄成虫触角形态特征、感受器类型、分布特点、感受器数量的研究, 为揭示华山松大小蠹与寄主植物挥发性物质之间的关系, 以及华山松大小蠹对健康华山松的选择机制奠定基础。
1 材料与方法 1.1 材料来源华山松大小蠹成虫采集于西北农林科技大学火地塘教学实验林场。在火地塘各林分内选择被华山松大小蠹入侵危害的寄主华山松, 在被害树木地径至树高3 m以下剥去华山松韧皮部, 在韧皮部和木质部间采集华山松大小蠹成虫, 装入冰壶带回。
1.2 采样地概况火地塘林场位于陕西秦岭南坡安康地区宁陕县境内, 33°25′—33°29′N, 108°25′—108°30′ E, 海拔1 500 ~ 2 450 m, 属山地温带气候, 主要成林树种包括华山松、油松(P.tabulaeformis)、落叶松(Larix gmelinii)、锐齿栎(Quercus aliena var.acuteserrata)、红桦(Betula albo-sinensis)和糙皮桦(B.utilis)。
1.3 研究方法取华山松大小蠹雌、雄成虫各12头, 用2.5 %戊二醛固定24 h, 0.1 mol·L-1磷酸缓冲液洗涤30 min, 1 %四氧化锇固定2 h, 30 %、50 %、70 %、80 %、90 %和无水乙醇进行逐级脱水, 乙酸异戊酯处理10 min, 临界点干燥, 真空喷金(铂金)2 ~ 3 h。将经上述处理过的华山松大小蠹置于JSM -840扫描电镜下(加速电压20 kV), 观察触角形态特征、感受器类型及分布特点。
触角感受器的类型主要依据Schneider(1964)的方法和特征进行归类, 触角感受器百分率=(某种感受器的数量/感受器总数量)×100 %, 感受器数量特征采用SEM Image进行统计。
2 结果与分析 2.1 触角形态特征华山松大小蠹雌雄成虫在触角颜色、形状、大小及感受器类型、分布特点、着生规律均无明显差异(图版Ⅰ-1)。华山松大小蠹成虫触角呈膝状, 分为柄节(scape)、鞭节(funicle)和锤头部(club)3部分(殷惠芬等, 1984)。柄节1节, 粗长, 棒锤状, 长156 μm, 最宽处50 μm, 最窄处21 μm, 与头部接触处有一凹陷(图版Ⅰ-2);鞭节6节, 第1节呈念珠状, 长47 μm, 第2、3、4、5、6节呈套筒状, 长度分别为26、12、12、10和57 μm, 从第2节开始逐渐变粗(图版Ⅰ-1)。锤头部拟4节, 长273 μm, 纵截面形似梯形, 下底263 μm, 上底68 μm, 有3条带组成, 带与带之间互相平行(图版Ⅰ-3、4)。华山松大小蠹成虫触角柄节、鞭节和锤头部分布着不同类型的感受器, 且柄节和鞭节表面具明显的瓦棱状花纹(图版Ⅰ-5、6)。柄节感受器数量最少, 仅占总感受器的2.3 %, 且长短粗细变异较大; 鞭节感受器数量较少, 占总感受器的7.4 %, 但在第2鞭节上没有任何感受器(图版Ⅰ-7);锤头部感受器数量最多, 占总感受器的90.3 %(图版Ⅰ-1、4)。
|
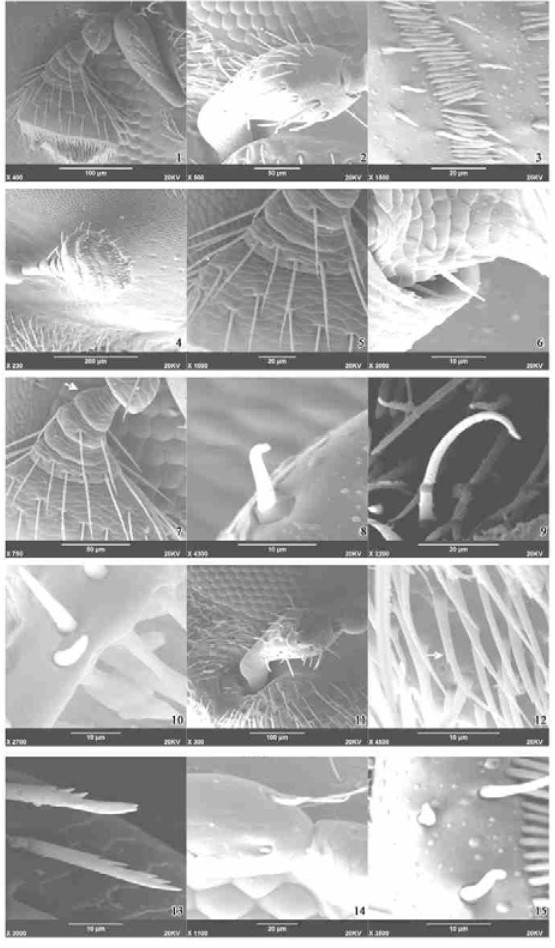
图版Ⅰ Plate Ⅰ 1.触角整体及各节形状特征;2.触角与头部连接处凹陷;3.锤头部排列分布的毛型感受器;4.锤头部及 3条平行条带;5.鞭节锯齿 型感受器及瓦棱状花纹;6.柄节与鞭节连接处的刺型感受器及瓦棱状花纹;7.第 2 鞭节;8.毛型感受器(短);9.毛型感受器(长); 10.栓锥型感受器;11.柄节锯齿型感受器;12.锤头部的锯齿型感受器;13.锯齿感受器锯齿形状;14.柄节末端的芽型感受器;15. 锤头部芽型感受器。 1.Whole antenna and their features of every segments;2.Sunken area between head and antenna ;3.Lined sensilla trichodea in the club;4.Three parallel strips of antenna in the club;5.Sawtooth-shaped sensilla in funicle and their pattern;6.Sensilla chaeticum between scape and funicle ;7.The second funicle ;8.Sensilla trichodea (short);9.Sensilla trichodea (long);10.Sensilla styloconica ;11.Sawtooth-shaped sensilla in the scape ; 12.Sawtooth-shaped sensilla in the club;13.Sawtooth shape ;14.Bud-shaped sensilla in the terminal scape;15.Bud-shaped sensilla in the club. |
华山松大小蠹成虫触角感受器有毛型感受器、栓锥型感受器、锯齿型感受器、刺型感受器和芽型感受器5种类型。
1) 毛型感受器(sensilla trichodea)数量最多, 直立或弯曲, 表面光滑(图版Ⅰ-8、9);长度7 ~ 41 μm, 多数在10 μm左右, 以带状或随机分布于锤头部和带与带之间, 并在锤头部1、2、3节排成3条平行的带(图版Ⅰ-3, 4)。
2) 栓锥型感受器(sensilla styloconica)直立, 形似锥子(图版Ⅰ-10), 长度10 ~ 50 μm, 多数在15 μm左右, 是锤头部最长的感受器, 散生在锤头部半球形的突起上, 数量仅次于毛型感受器, 多数与毛型感受器混生。
3) 锯齿型感受器(zigzag sensilla)直立, 形似锯齿(图版Ⅰ-5), 数量少于毛型和栓锥型感受器, 长度22 ~ 70 μm, 多数在30 μm左右, 分布于柄节和鞭节, 偶见于锤头部(图版Ⅰ-5、11、12)。每个感受器具有8 ~ 15不等的锯齿, 与主轴呈30°夹角, 一直延伸到顶端(图版Ⅱ-13)。
4) 刺型感受器(sensilla chaeticum)直立, 形似竹签, 长度11 μm左右, 分布于柄节和鞭节连接处的凹陷中, 散生, 数量较少(图版Ⅰ-6)。
5) 芽型感受器(bud-shaped sensilla)短小, 形似禾谷种子刚发出来的芽, 长度1 ~ 3 μm; 分布于柄节背面末端、鞭节和柄节的连接处或触角锤头部(图版Ⅱ-14、15), 数量极少。
2.3 感受器的特点与分布规律华山松大小蠹成虫触角柄节、鞭节和锤头部感受器的类型和分布具有明显的差异, 从柄节到锤头部, 感受器的数量逐渐增多, 类型也相应增加。柄节、鞭节和锤头部感受器分别占总感受器的2.3 %, 7.3 %, 90.4 %。此外, 各种感受器在触角上的分布明显不同, 锯齿型感受器和刺型感受器仅分布于柄节、鞭节和锤头状的基节上, 偶尔在锤头部的顶端分布; 芽型感受器分布于柄节, 极少数分布在锤头部毛型感受器带之间; 毛型感受器和栓锥型感受器仅分布于锤头部, 并在锤头部排成3条带(图版Ⅰ-4), 带与带之间分布着毛型和栓锥型感受器。
3 讨论华山松大小蠹成虫触角感受器种类和形态与松纵坑切梢小蠹(毋亚梅等, 2000)、红脂大小蠹(王玉刚等, 2003)具有一定的相似性, 而与鳞翅目(王桂荣等, 2002)、膜翅目(马瑞燕等, 2000)和其它鞘翅目昆虫(Elspeth et al., 1999)有很大的差别。同时, 昆虫触角感受器存在属的相似性和种间的差异性, 华山松大小蠹、松纵坑切梢小蠹、红脂大小蠹成虫触角上分布着毛型感受器、锯齿型感受器、芽型感受器、刺型感受器4种类型的感受器, 其中华山松大小蠹毛型感受器与松纵坑切梢小蠹、红脂大小蠹相似, 在锤头部排列成3条带, 但锯齿形感受器、刺型感受器、芽型感受器与松纵坑切梢小蠹和红脂大小蠹在触角各节的分布明显不同; 栓锥型感受器广泛地分布于华山松大小蠹和松纵坑切梢小蠹锤头部, 而红脂大小蠹触角上没有栓锥型感受器的分布。小蠹虫触角感受器的类型和分布规律与寄主树木挥发性物质的识别和反应密切相关, 具有相同感受器类型和分布规律的小蠹虫可能意味着具有相似的寄主感受行为和选择行为。华山松大小蠹集中分布于秦岭巴山林区, 主要危害30年以上健康华山松, 偶尔入侵危害油松, 而红脂大小蠹传入我国后在山西、陕西等省发生, 主要危害树势衰弱的油松, 这种寄主树木选择的差异性和华山松大小蠹与红脂大小蠹的近缘性, 是华山松大小蠹与红脂大小蠹成虫触角感受器类型和分布差异的主要原因。
陈辉. 2003. 化学信息素对小蠹虫的入侵危害的调控. 林业科学, 39(6): 154-158. DOI:10.3321/j.issn:1001-7488.2003.06.026 |
陈辉, 袁锋. 1999. 秦岭华山松小蠹生态位研究. 林业科学, 35(4): 40-44. DOI:10.3321/j.issn:1001-7488.1999.04.007 |
马瑞燕, 杜家纬. 2000. 昆虫的触角感受器. 昆虫知识, 37(3): 179-183. DOI:10.3969/j.issn.0452-8255.2000.03.020 |
王玉刚, 张真, 王鸿斌, 等. 2003. 红脂大小蠹成虫触角扫描电镜的观察. 林业科学研究, 16(6): 726-730. DOI:10.3321/j.issn:1001-1498.2003.06.012 |
王桂荣, 郭予元, 吴孔明. 2002. 棉铃虫触角感受器的超微结构观察. 中国农业科学, 35(12): 1479-1482. DOI:10.3321/j.issn:0578-1752.2002.12.008 |
毋亚梅, 周楠, 张立新, 等. 2000. 松纵坑切梢小蠹成虫触角的扫描电镜观察. 西南林学院学报, 20(1): 40-47. |
殷惠芬, 黄复生, 李兆麟, 等. 1984. 中国经济昆虫志:第29册. 北京: 科学出版社.
|
Byers J A.1995.Host tree chemistry affecting colonization in bark beetles//Card R T, Bell W J.Chemical Ecology of Insects.Academic Press, New York, 154-213
|
Elspeth B, Roberto R. 1999. Functional anatomy of sensory structures on the antennae of Psylliodes chrysocephala L.(Coleoptera :Chrysomelidae). International Journal of Insect Morphology and Embryology, 28: 291-300. DOI:10.1016/S0020-7322(99)00032-X |
Hallberg E. 1982. Sensory organs in Ips typographus (Insecta :Coleoptera)fine structure of the sensilla of the maxillary and labial palps. Acta Zool, 63: 191-198. DOI:10.1111/j.1463-6395.1982.tb00778.x |
Hynum B G, Berryman A A. 1990. Dendroctonus ponderosae (Coleoptera:Scolytidae)preaggregation landing and gallery initiation on lodgepole pine. Can Entomol, 112: 185-191. |
Kinzer D N, Fentiman A F, Page T L. 1969. Bark beetle attractants:identification, synthesis, and bioassay of a compound isolated from Dendroctonus. Naturwissenschafen, 221: 477-478. |
Schneider D. 1964. Insect antennae. Annu Rev Entomol, 9: 103-122. DOI:10.1146/annurev.en.09.010164.000535 |
Silverstein R M.1970.Methodology for isolation and identification of insect pheromones examples from Coleoptera//Wood D L, Silverstein R W, Nakajima M.Control of Insect Behavior by Nature Product.Academic Press, New York, 285-299
|
Thomas H A, Richmond J A, Bradley E L.1991.Bioassy of pine bark extracts as bitting stimulants for the southern pine beetle.USDA Forest Serv Res, Note SE -302
|
Whitehend A T. 1981. Ultrastructure of sensilla of the female mountain pine beetle Dendroctonus ponderosae (Coleoptera :Scolytidae). Journal of Insect Morphol & Embryol, 16: 484-492. |
 2006, Vol. 42
2006, Vol. 42

