文章信息
- 王鸿斌, 王玉刚, 张真, 金幼菊, 周淑芷.
- Wang Hongbin, Wang Yugang, Zhang Zhen, Jin Youju, Zhou Suzhi.
- 油松挥发性物质分析及红脂大小蠹的触角电位反应
- The Volatile Components of the Chinese Pine and the EAG Responses of the Dendroctonus valens (Coleoptera:Scolytidae)
- 林业科学, 2006, 42(5): 84-88.
- Scientia Silvae Sinicae, 2006, 42(5): 84-88.
-
文章历史
- 收稿日期:2004-05-19
-
作者相关文章
2. 北京林业大学生物中心 北京 100083;
3. 中国农业大学IPMIST实验室 北京 100094
2. College of Biology Science and Technology, BFU Beijing 100083;
3. IPMIST Lab., CAU Beijing 100094
松树是我国重要的森林资源之一,主要有马尾松(Pinus massoniana)、油松(P. tabulaeformis)、云南松(P. yunnanensis)和红松(P. koraiensis)等,总面积约为4 000万hm2。长期以来,随着人工林面积不断的增加,森林生态环境的不断恶化以及气候的反常,致使松树资源受到各种虫害的严重威胁。红脂大小蠹(red turpentine beetle),又名强大小蠹(Dendroctonus valens)(殷惠芬,2000)属于鞘翅目(Coleoptera)小蠹科(Scolytidae)大小蠹属(Dendroctonus),在我国为一新记录的传入种。它是该属害虫中体形最大的一种,主要危害以松树为主的针叶树干基和根部。在其原产地——美国、墨西哥、加拿大是一个广泛分布,但危害较小的森林害虫(Bright et al., 1976; Furniss et al., 1997; Cibrian et al., 1995)。自1998年在我国山西发现红脂大小蠹危害健康油松以来,其危害程度日趋严重,现已扩展到河南、河北和陕西,给我国林业造成了严重损失。它可导致几年生至几十年生的树木在较短的时间内死亡,且扩散蔓延迅速。据统计,1999年底,该虫在河北、河南、山西3省发生面积52.6万hm2,其中严重危害13万hm2,个别地区油松死亡率高达30%,已导致600多万株的松树枯死(李计顺等,2001);2000年仅在山西省,危害面积已达16.29万hm2,成灾面积9.11万hm2,已有342.4万株成材油松受害枯死。虫害发生区涉及山西省境内的晋城市、长治市、太原市、阳泉市、临汾地区、晋中地区、吕梁地区、忻州地区等8个地市和省直中条山、太岳山、吕梁山、关帝山、黑茶山等5个森林经营局以及天龙山、乌金山等国家、省级自然保护区、森林公园。严重受害林地的有虫株率达80%,松树死亡率达30%以上。红脂大小蠹危害的严重程度不亚于国家级森林植物检疫对象美国白蛾(Hyphantria cunea)和松材线虫(Bursaphelenchus xylophilus)病,已成为我国林业生产重要的森林害虫之一1)。
1) 吴坚,杨忠歧,宋玉双,等. 2000.赴美红脂大小蠹防治考察报告.中国林业科学研究院森林生态环境与保护研究所
研究表明:树体挥发性物质的组分可以提供给小蠹虫有关树是否易于攻击的信息(Erbilgin et al., 2000)。寄主树的挥发性物质是对红脂大小蠹起到干扰选择与聚集的主要化学物质(Vite et al., 1962)。雌雄红脂大小蠹被受伤树和病树分泌的树脂所吸引(Borden et al., 1985),并经常攻击那些已经被其他小蠹虫攻击过的树干的基部(Hobson et al., 1993)。松树体内单萜类物质的浓度在干旱、根部真菌的感染、落叶的影响下发生改变(Klepzig et al., 1995)。蠹虫的侵入也会引起寄主树单萜类物质的浓度及其释放速率的改变。
因此,了解红脂大小蠹在我国的主要寄主油松的挥发物自然状况及蠹害侵入的反应,是更好地利用其特性进行信息素监测控制的前提和基础。为了对该种害虫的信息素及其在寄主选择和为害机制中的作用进行研究,王鸿斌等(2005)明确了油松挥发物质的基本成分有25种,本文重点分析了红脂大小蠹成虫羽化高峰期油松主要成分萜烯类及红脂大小蠹对其的触角电位反应,结果报道如下。
1 材料和方法 1.1 油松挥发性物质的分析 1.1.1 样品的采集于2002年5月在山西省沁源县赤石桥乡榆坪口东坡的山上使用了循环采气的方式进行了样品的原始状态下的活体采集。试验采用北京市劳动保护科学研究所,北京市新华劳动科贸有限公司生产的QC-1大气采集仪。吸附剂采用从迪马公司购进的Tenax-GR。采集了包括未受害树的树干及松针、已受害的油松的树干及松针的挥发性物质,每种5个重复。将树干用宽50 cm的聚乙烯薄膜包裹,用封口机将其密封,两端垫上脱脂棉,用铁丝扎紧,使树干内部成为一个密闭的环境。将大气采集仪两端的管子插入到聚乙烯薄膜的内部。先将包裹处的空气用大气采集仪排空,补充入经过滤的空气后,再加上吸附管进行样品的采集。采集松针挥发性物质时,选择枝干,用聚乙烯薄膜套袋从顶端套入50 cm,密封套袋口,插入采集管进行采集。样品的采集时间为0.5 h,气体流速为0.5 L·min-1。被采集油松树干的直径在22~25 cm之间。每个吸附管内装入经活化处理后100 mg的Tenax-GR。
1.1.2 样品的分析在北京林业大学生物中心,通过热脱附-低温-捕集装置与气相色谱质谱联用,对样品进行分析。气相色谱-质谱联用中气相色谱为CE INSTRUMENT公司的TRACETM 2000,质谱为FINNIGAN公司的VOYAGER MASS。热脱附仪采用CHROMPACK公司的CP-4010TTI/TCT。TCT操作条件为:载气压力20 kPa,进样口温度250 ℃,冷阱温度-120 ℃,热脱附温度250 ℃(10 min),进样时冷阱温度260 ℃(1 min);GC分析条件为:色谱柱CP-Sil8 Low Bleed/MS(60 m×0.25 mm×0.25 μm),分流方式1:6.75,载气压力:20 kPa,初始温度40 ℃(保持3 min);以6 ℃·min-1程序升温至250 ℃(保持3 min);MS工作条件为:EI源,电子能量70 eV,质量范围29~350 u,扫描速度0.4 s·scan-1,GC/MS接口温度250 ℃,离子源温度200 ℃,灯丝电流150 μA。
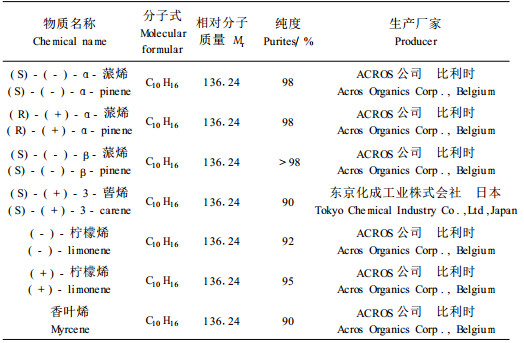
1.2 红脂大小蠹对油松挥发性物质触角电位的反应红脂大小蠹采自山西省沁源县赤石桥乡庄儿上村。采回后6.5 ℃下保存待用。试验所用触角电位仪为荷兰SYNTECH公司生产的IDAC-232。刺激控制装置为CS-05,EAG探针的内部放大系数为10×,刺激持续1 s,脉冲气体流速为600 mL·min-1,持续的空气流速为2 000 mL·min-1。试验用表 1所示物质原液20 μL,以空白刺激作为对照。同一个样品用于对所有不同虫子进行刺激,同一个虫子要接受每一个样品的刺激。样品的刺激顺序由计算机生成的随机数确定。分雌雄各重复5次。
|
|
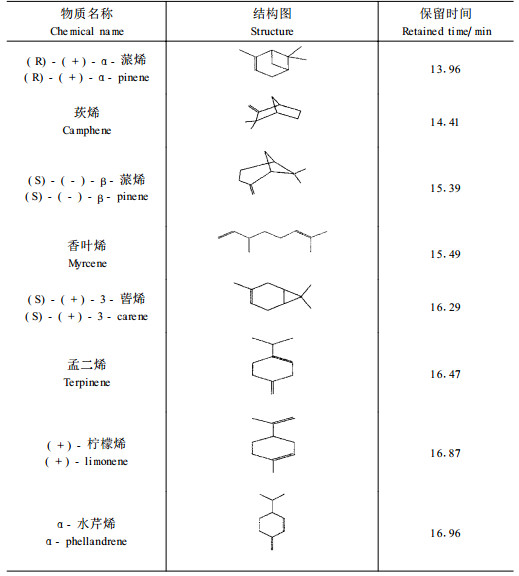
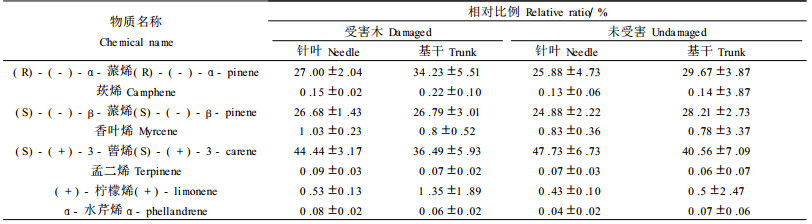
经过气相色谱和质谱的分析,用标准样品内标分析比较,发现5月采集的所有样品中萜烯类含量最多,主要为(S)-(+)-3-蒈烯,(R)-(+)-α-蒎烯和(S)-(-)-β-蒎烯, 占萜烯总量的97%以上。另外还含有少量的(+)柠檬烯、(S)-(-)-α-蒎烯、香叶烯、莰烯、孟二烯和水芹烯等成份,以及微量的芳香族和烷烃类化合物。油松主要萜烯类挥发性组分和测试结果如表 2。已受红脂大小蠹危害和未受害油松的主要挥发性萜烯组分平均相对含量见表 3。
|
|
|
|
表 3表明:未受害油松和受害油松中(S)-(+)-3-蒈烯相对含量针叶比树干高,(R)-(+)-α-蒎烯相对含量针叶比树干低,但差异不显著,受害油松针叶和树干(S)-(-)-β-蒎烯基本相似,而未受害油松针叶比树干(S)-(-)-β-蒎烯少。无论对于针叶还是树干,受害木中(S)-(+)-3-蒈烯比例显著低,而(+)-柠檬烯、(R)-(+)-α-蒎烯则相对偏高,其他成分比例则相对变化不大(P=0.05)。
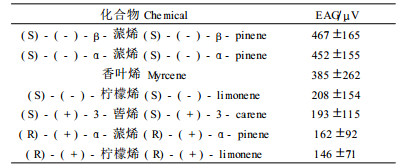
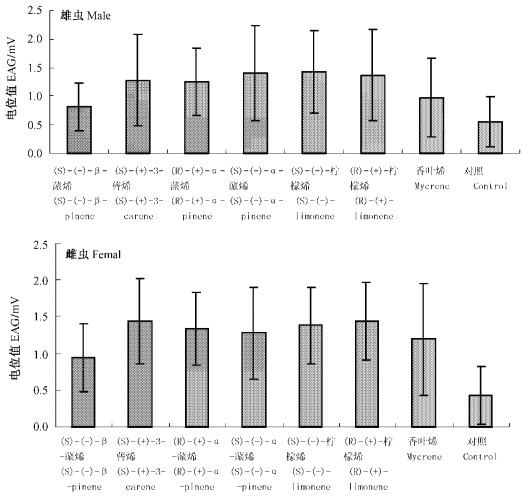
2.2 红脂大小蠹对油松挥发性物质触角电位的反应红脂大小蠹对油松挥发性物质触角电位的反应见图 1,雄性红脂大小蠹对各种物质的反应中只有(-)-柠檬烯的触角电位反应值与对照之间的差异达到了显著性的水平。(S)-(-)-α-蒎烯、(+)-柠檬烯和(S)-(+)-3-蒈烯与对照达到了90%的显著性差异。各种刺激化合物引起的触角电位的反应之间没有显著性的差异。雌性红脂大小蠹(图 2)对(S)-(+)-3-蒈烯、(+)-柠檬烯、(-)-柠檬烯、(R)-(+)-α-蒎烯、(S)-(-)-α-蒎烯和香叶烯的反应与对照之间达到了显著性的差异。各种刺激化合物引起的触角电位反应之间没有显著性的差异。雌虫对树体挥发性物质的反应较雄虫强烈。
|
图 1 各种化合物的触角反应值 Fig. 1 EAG Response of D. valens to host monoterpenes |
野外诱捕的结果显示:(S)-(+)-3-蒈烯的吸引作用最强,增加柠檬烯能显著降低诱芯的引诱作用(Sun et al., 2004)。在油松挥发性萜烯类中也是(S)-(+)-3-蒈烯所占的比例也最多,山西未受害油松中比例显著高于受害油松,说明油松受害后树体对其的引诱作用降低,而(+)-柠檬烯、(R)-(+)-α-蒎烯则相对较低,(S)-(+)-3-蒈烯的含量较少,被危害油松树干中成份与此相反。触角电位的研究结果是柠檬烯和(S)-(+)-3-蒈烯的作用最强,结合野外引诱结果说明:前者是抑制作用,后者是引诱作用。雌性红脂大小蠹对树体挥发性物质的触角电位的反应较雄性强烈,尤其对(S)-(+)-3-蒈烯的作用最强,这与雌虫先侵入树体,而后再诱引雄虫入侵的现象恰好吻合。Rudinsky等(1976)在研究黄杉大小蠹(Dendroctonus pseudotsugae)时,提出声音信号和化学信号一起在小蠹虫与寄主之间起着共同作用,化学信息的刺激能激发雌雄虫发出的摩擦声音的频率和强度,而又能诱发雌雄虫产生不同的信息素,产生聚集和趋避作用。而红脂大小蠹雌雄存在明显不同的声音信号,因此,笔者推测:在红脂大小蠹寻找寄主树的过程中,雌虫在树体利他激素的作用下先行到达寄主树,雄虫在雌虫分泌的信息素和树体分泌的利他激素共同作用下,入侵寄主树,实现侵入过程,而后雄性红脂大小蠹发出尖锐的声音和趋避信息,驱避其他雄性红脂大小蠹的入侵,实现1:1的配对,这方面的研究尚无相关研究。对性信息素及雄虫发出的声音的作用还需要进一步试验研究证实。
国内红脂大小蠹触角电位的反应与国外的结果有显著的不同。White等(1993)研究认为,雌性和雄性红脂大小蠹对树体挥发性物质的反应没有什么不同。另外他们测定的红脂大小蠹对各种挥发性物质的反应值的大小顺序也与实验结果有差异。最为明显的差异为对(S)-(-)-β-蒎烯的反应(表 4和表 5),在Hobson的试验过程中红脂大小蠹对(S)-(-)-β-蒎烯的反应最为强烈,对(R)-(+)-柠檬烯的反应最弱,但是在作者的试验中对(S)-(-)-β-蒎烯最弱,对(+)-柠檬烯的反应却高居第2位。对其他各种物质反应也都不同。引起这种差异的原因可能有几个方面,一是寄主不一样,在美国主要危害黄松(P. pondersae),糖松(P.lambertiana),而在中国主要危害油松,也危害华山松(P. armandi)、白皮松(P. bungeana)等,不同松树种类的挥发物成分是不一样的,Hobson等(1993)的研究主要是针对美国黄松和糖松。从美国两种松树的挥发物含量(表 6),中可以看出,(S)-(-)-β-蒎烯和(S)-(-)-α-蒎烯的含量较大,触角电位的反应也较强,而油松中(S)-(+)-3-蒈烯含量最大,而相应的触角电位反应和野外引诱作用也较强,但柠檬烯含量很少,触角电位反应也很大,红脂大小蠹对寄主挥发物的反应的产生机制还有待于进一步研究,但可以肯定寄主挥发物成分的不同,会影响小蠹虫的反应;另外环境条件的改变,也可能对此产生影响。所有这些问题都有待于深入研究。
|
|
|
|
李计顺, 常国彬, 宋玉双, 等. 2001. 实施工程治理控制红脂大小蠹虫灾——对红脂大小蠹暴发成因及治理对策的探讨. 中国森林病虫, 4: 141-144. |
殷惠芬. 2000. 强大小蠹的简要的形态学特征和生物学特征. 动物分类学报, 25(1): 43, 120. |
王鸿斌, 张真, 孔祥波, 等. 2005. 油松萜烯类挥发物释放规律与红脂大小蠹危害关系研究. 北京林业大学学报, 27(2): 75-80. DOI:10.3321/j.issn:1000-1522.2005.02.015 |
Borden J H. 1985. Aggregation pheromones//Gilbert L I eds. Comprehensive Insect Physiology Biochemistry and Pharmacology. Oxford: Pergamon Press, 257-285
|
Bright D E. 1976. Insects and Arachnids of Canada. Part2. The bark beetles of Canada and Akaska. Coleoptera: Scolytidae. Can Dep Agric Publ, #1576
|
Cibrian T D, Montiel J T, Bolanos R C, et al. 1995. Forest insects of Mexico. Universidad Autónoma Chapingo
|
Erbilgin N, Raffa K E. 2000. Opposing effects of host monoterpenes on responses by two sympatric species of bark beetles to their aggregation pheromones. Journal of Chemical Ecology, 26(11): 2527-2548. DOI:10.1023/A:1005532612117 |
Furniss R L, Carolin V M. 1997. Western forest insects. USDA For Ser Misc Publ, #1339
|
Hobson K R, Wood D L, Cool L G, et al. 1993. Chiral specificity in responses by the bark beetle Dendroctonus valens to host kairomones. Journal of Chemical Ecology, 19(9): 1837-1846. DOI:10.1007/BF00983790 |
Klepzig K D, Smalley E B, Raffa K F. 1995. Dendroctonus valens and Hylastes porculus. (Coleoptera:Scolytidae):vectors of pathogenic fungi (Ophiostomatales) associated with red pine decline disease. Great-Lakes-Entomologist, 28(1): 81-87. |
Rudinsky J A, Ryker L C, Michael R R, et al. 1976. Sound production in Scolytidae: Female sonic stimulus of male pheromone release in two Dendroctonus beetles. J Insect Physiol, 22: 1675-1681. DOI:10.1016/0022-1910(76)90061-5 |
Sun Jianghua, Miao Zhengwan, Zhang Zhen, et al. 2004. Red Turpentine Beetle, Dendroctonus valens LeConte (Coleoptera: Scolytidae), response to host semiochemicals in China. Environmental Entomology, 33(2): 206-212. DOI:10.1603/0046-225X-33.2.206 |
Vite J P, Gara R I. 1962. Volatile attractants from ponderosa pine attacked by bark beetles(Coleoptera:Scolytidae). Contrib Boyce Thompson Inst, 21: 251-274. |
White P R, Kenneth R, Hobson K R. 1993. Stereospecific antennal response by red turpentine beetle, Dendroctonus valens to chiral monoterpenes from ponderosa pine resin. Journal of Chemical Ecology, 19(10): 2193-2202. DOI:10.1007/BF00979657 |
 2006, Vol. 42
2006, Vol. 42