文章信息
- 任琴, 金幼菊, 胡永建, 陈华君, 李镇宇.
- Ren Qin, Jin Youju, Hu Yongjian, Chen Huajun, Li Zhenyu.
- 马尾松诱导挥发性有机化合物的快速变化
- Rapid Changes of Induced Volatile Organic Compounds in Pinus massoniana
- 林业科学, 2006, 42(4): 65-70.
- Scientia Silvae Sinicae, 2006, 42(4): 65-70.
-
文章历史
- 收稿日期:2005-01-12
-
作者相关文章
当植物受到虫害后,最直接的防御是释放挥发性有机化合物(Farmer, 2001)。棉花(Gossypium hirsutum)被鳞翅目幼虫咬食后,(E, E)-α-法尼烯、(E)-β-法尼烯、(E)-β-罗勒烯、里哪醇等释放量增加(Paul et al,1997),油松(Pinus t abulaeformis)受害后针叶中精油萜烯含量中α-胡椒烯的增加最为明显(李镇宇等,1998)。天牛取食复叶槭(Acer negundo)后研究其时间动态变化规律,发现取食后9 h多数挥发物的释放率达到第1个峰值,在经过短时间下降后又逐渐上升,48 h达到最大值(李继泉等,2002);当复叶槭受到干旱胁迫时,9种化合物释放量升高(包括:丁醇、戊醇、反-2-己烯-1-醛、顺-3-己烯-1-醇、戊醛、戊酸、己醛、己酸、苯乙酮),其中丁醇、戊醇和顺-3-己烯-1-醇能引起光肩星天牛的触角电位反应(Jin et al., 2004)。马尾松(Pinus massonina)是我国南方主要林木及采脂树种,但常遭受马尾松毛虫(Dendrolimus punctatus)的危害,周期性暴发成灾。本试验通过未受害、虫害、人工剪叶3种处理,研究马尾松挥发物释放时间的动态变化,以探索挥发物的性质及作用机理,提出新的害虫防治策略。
1 材料与方法 1.1 材料选用江西农业大学水库后山马尾松天然林作为试验树种,由江西农业大学提供马尾松毛虫3龄幼虫。
1.2 植物挥发物的采集2004年6月在马尾松林中选择树龄相同、长势一致的6株做标记。其中2株分别接入一定量的马尾松毛虫3龄幼虫,在3 d内分别造成轻度受害(针叶损失量达25%~40%)和重度受害(针叶损失量达60%~75%)。另取2株树样根据接虫松树受害程度进行人工剪叶,模拟2种不同受害程度。轻度受害在处理后的第1、2、4、8、24、48、72、96 h分别从上述松树取样;重度受害后取样至72 h。其他2株松树作为健康对照。取样方法为动态顶空收集法。
1.3 植物挥发物的测定取样后用采用TCT-GC-MS进行测定。具体方法参见文献(李继泉等,2002),并加以修改。
采用Xcalibur 1.2版本软件,NIST 98谱图库兼顾色谱保留时间进行马尾松挥发物成分的鉴定。通过面积归一化法以各类挥发物的相对含量定量。
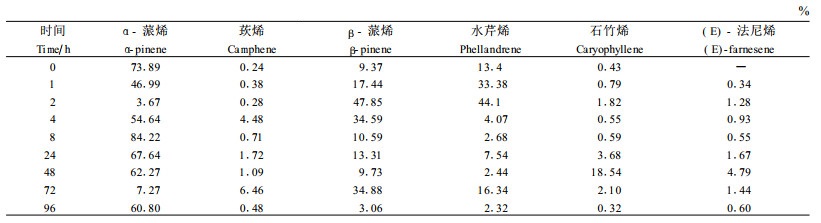
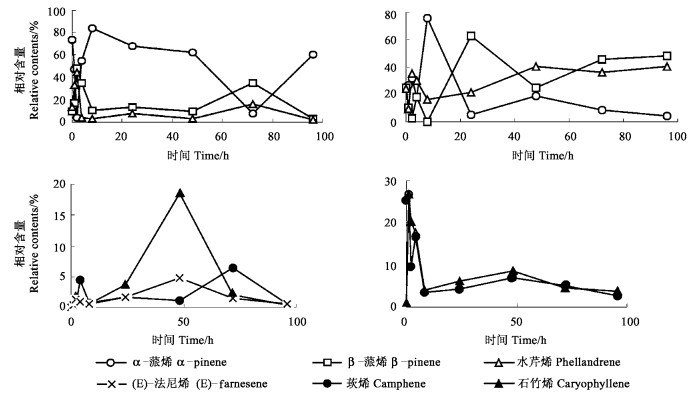
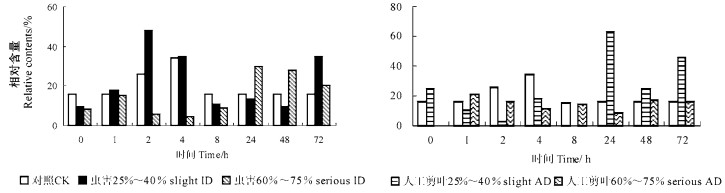
2 结果与分析 2.1 不同受害方式诱导马尾松挥发性物质的快速变化对接虫和人工剪叶处理的马尾松针叶内挥发性化学物质的测定结果表明(图 1、2):与对照相比,轻度虫害后α-蒎烯在8 h升至最高,莰烯、β-蒎烯、水芹烯、石竹烯、法尼烯均在1 h升高,但莰烯72 h达到高峰,β-蒎烯、水芹烯2 h达到最高,石竹烯、法尼烯48 h达到高峰;轻度机械损伤后,α-蒎烯8 h升至最高,莰烯、石竹烯1 h达到高峰;β-蒎烯、水芹烯24 h后才会达到高峰。尽管受害方式不同,但α-蒎烯相对含量出现高峰的时间相同,其他萜烯的相对含量出现高峰的时间没有明显的规律性。重度虫害后检测到的挥发物除水芹烯、石竹烯外,其余均在1 h升高,α-蒎烯4 h达到高峰,三环萜、β-蒎烯、莰烯、月桂烯、水芹烯、石竹烯均在24 h达到高峰,法尼烯72 h含量最高;重度机械损伤后,α-蒎烯在整个取样时序内的相对含量均低于对照,没有出现变化,其余各类挥发物出现释放高峰的时间多在1 h或2 h,可以看出机械损伤检测到的挥发物种类略少于虫害,释放高峰早于虫害;α-蒎烯在不同受害方式中释放高峰出现的时间相同,没有显著的规律性。笔者认为,α-蒎烯可能只是针叶树树脂中的主要组成成分,但在抗虫中的作用未见报道。另外,2 h采样的测定结果多数挥发物相对含量较低,其原因可能是与1 h采样点相距较近,植物没有完全恢复正常生长。
|
图 1 马尾松轻度虫害(左)与轻度人工剪叶(右)后挥发物的变化 Fig. 1 Changes of volatile of P. massoniana after slight ID (left) and AD (right) |
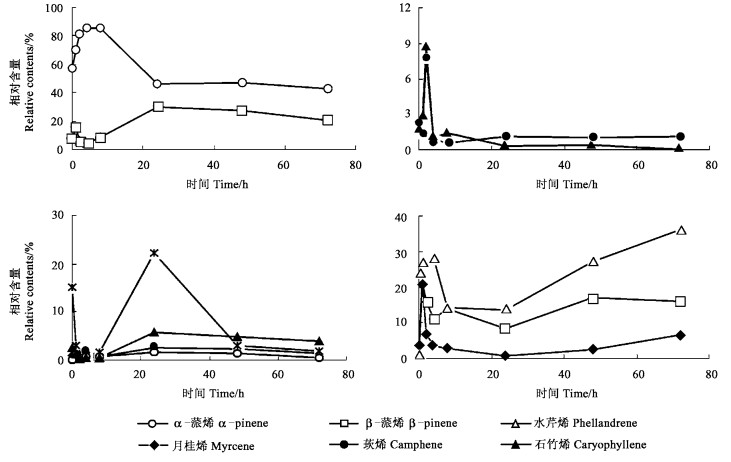
|
图 2 马尾松重度虫害(左)与重度人工剪叶(右)后挥发物的变化 Fig. 2 Changes of volatile of P. massoniana after serious ID (left) and AD (right) |
植物本身处于一种基础代谢与次生代谢的交替开放变化过程中,未受害的马尾松挥发物始终维持着代谢的最低水平,它们的变化遵循着昼夜节律变化规律,即夜间挥发物释放少而最大光合期间释放量大(Diane et al, 2003)。植物受害后,其抗性功能也处于这种动态的变化过程中,能在相对较短的时间释放出大量的挥发性化学物质(Paul et al, 1999),这种应激反应是一种时态的变化,因而在时间上产生了植物的快速诱导抗性(刘兴平等,2003)。
虫害后植物释放的挥发物来自受害处,这与未损伤或机械损伤的植株挥发物的释放有明显的区别。棉花叶上的腺体损伤引起了贮藏部位的萜烯大量释放(Loughrin et al., 1994)。因此,虫害和机械损伤检测到的挥发物释放高峰和相对含量都有差别。
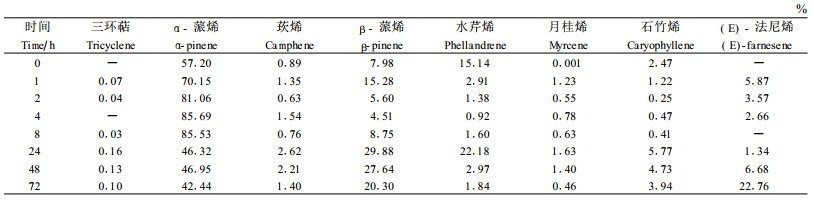
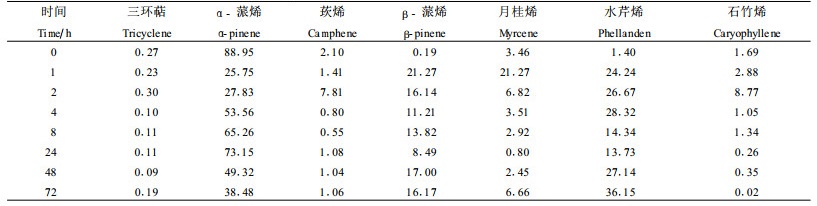
2.2 不同受害程度诱导马尾松挥发性化学物质的快速变化 2.2.1 轻度与重度虫害对马尾松挥发物的诱导变化测定结果表明:重度受害诱导的挥发物种类多于轻度受害,除轻度虫害后能够检测到的挥发物之外,三环烯、月桂烯等轻度受害中未检测到的挥发物在重度受害中均出现而且变化明显;重度虫害挥发物释放高峰的时间有一定的规律性,除α-蒎烯、(E)-法尼烯外,其余变化明显的挥发性化学物质均在受害后24 h达到高峰,而且重度虫害后挥发物相对含量的高峰值低于轻度虫害(表 1~3)。
|
|
|
|
|
|
在针叶树的防御反应中,萜烯类物质是重要的抗虫物质,分泌含有高浓度的单萜类树脂是针叶树抗虫的主要手段,这一点已在试验中得到证实。但萜烯等物质受诱导产生的浓度与为害程度及时间有很大关系。受害程度的强弱对马尾松诱导挥发性化学物质的变化有一定的影响。当马尾松针叶损失量达到25%~40%时,马尾松所释放的挥发性化学物质含量显著增加,引发松树产生诱导化学防御的能力最强;当马尾松针叶损失量达到60%~75%时,挥发性化学物质释放量虽然比健康对照植株高,但多数释放量低于轻度虫害。笔者认为这是因为马尾松受到重度虫害后,由于失叶过多,导致水分代谢和光合作用受阻,影响了马尾松的初生代谢,进而使次生代谢减弱甚至停止。可以看出马尾松的诱导抗虫性并非表现为线性关系,而是与受害程度呈“开-关”(on-off)式效应(娄永根等,1997)。此外,植物用于防御的能量和物质是有限的,马尾松受害后不可能长期产生高浓度的萜烯化合物来抵抗马尾松毛虫的连续侵害(李镇宇等,1998),而是快速、间断和被调节的,从而避免消耗太多的资源,这样利于马尾松的生长发育。
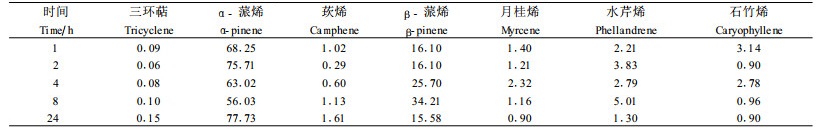
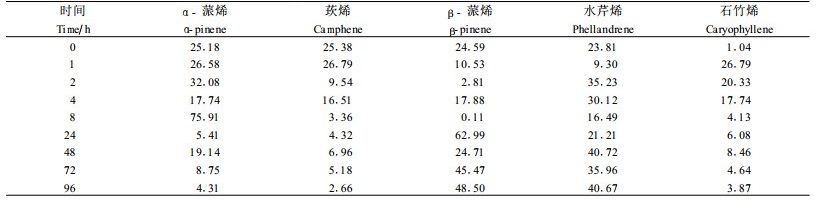
2.2.2 轻度与重度人工剪叶对马尾松挥发物的诱导变化不同程度的人工剪叶使马尾松挥发性化学物质的释放量增加,多数挥发性化学物质在1 h或2 h升高,但轻度受害后挥发物相对含量出现高峰的时间没有规律性变化;重度人工剪叶检测到的挥发物种类多于轻度人工剪叶;α-蒎烯在重度人工剪叶取样时序内的相对含量低于对照,其余各类挥发物除水芹烯外相对含量出现高峰的时间均在1 h或2 h(表 3~5)。
|
|
|
|
人工剪叶模拟虫害的目的是为了比较2种受害方式对植物挥发性化学物质的变化是否有一致性,是否可用人工剪叶代替虫害。试验结果表明,马尾松虫害与人工剪叶后都能使挥发物的相对含量提高,挥发物种类基本一致,只是释放高峰出现时间及释放量均有一定的差别。戈峰等(1997)发现人工剪叶模拟为害与害虫危害类似,同样对松毛虫具有调控作用。因此,以人工剪叶模拟虫害,能够达到调控马尾松毛虫种群的目的,减轻松毛虫危害,延缓其暴发周期。
2.3 马尾松挥发性化学物质β-蒎烯的诱导变化在所检测到的植物挥发性化学物质中,β-蒎烯备受关注。试验中用不同方式及不同程度处理马尾松后,β-蒎烯有明显的变化(图 5、6),轻度虫害处理后β-蒎烯的相对含量在2 h时比对照增加46.29%,72 h增加53.84%;重度虫害后24 h β-蒎烯的相对含量比对照增加46.12%, 72 h增加20.7%。轻度人工剪叶后24 h β-蒎烯的相对含量比对照增加74.44%,72 h增加64.6%;重度人工剪叶后1 h β-蒎烯相对含量比对照增加24.33%,72 h增加0.46%。但在2 h、8 h采样点上,β-蒎烯含量降低,可能是由于受害后针叶量减少而使挥发物释放量减少所致。本试验中β-蒎烯对马尾松毛虫的作用还需要通过生测试验来加以研究。如欧洲赤松(P. sylvestris)的β-蒎烯对纵坑切梢小蠹(Tomicus piniperda)的忌避作用。曹骥(1984)的研究结果证明,β-蒎烯具有抗虫性质,取食高β-蒎烯含量的松针对马尾松种群的增长有不利影响。马尾松毛虫抗性研究组(1990)测定表明抗11植株中β-蒎烯的含量比对照增加168.1%。经试验抗11对松毛虫具有拒产卵性和拒食性,这与β-蒎烯含量有关。李镇宇等(1997)比较了樟子松( P. sylvestris var. mongolica)和油松对赤松毛虫(D. spectabilis)的抗性,发现油松针叶中β-蒎烯含量最高达16.9%,而樟子松为8. 7%,相差近1倍,这是赤松毛虫成虫趋向油松针叶上产卵,但幼虫取食油松后死亡率高于樟子松的主要原因。赵成华等(1995)发现β-蒎烯对马尾松毛虫雌性触角电生理(EAG)反应,证实β-蒎烯对松毛虫具有引诱作用。因此,深入研究β-蒎烯的合成及释放机理,对植物的抗虫研究有重要意义。
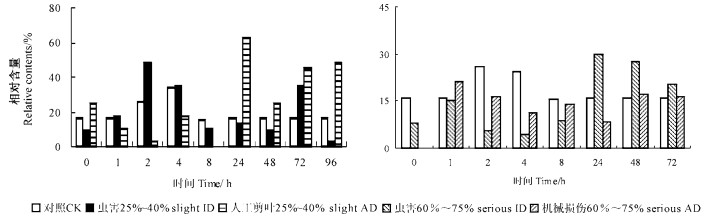
|
图 3 不同受害方式对β-蒎烯含量的影响 Fig. 3 Effect on contents of β-pinene at different treatments |
植物叶片通常释放出少量的挥发性化学物质,但是当植物受到植食性昆虫为害后,会释放大量的挥发物以应激。植物受害后的应激反应是一种时态变化(王燕等,2001)。对马尾松进行接虫咬食为害、剪叶受害、未受害3种处理后,其针叶内挥发性化学物质的相对含量随取样时间而变化。不同受害方式对马尾松挥发物的释放有不同影响:人工剪叶检测出的挥发物种类少于虫害,释放高峰早于虫害。同一受害方式的不同受害程度对挥发物的快速诱导变化不同:与对照相比,轻度虫害后莰烯、β-蒎烯、水芹烯、石竹烯、(E)-法尼烯在1 h升高,但挥发物相对含量出现高峰的时间没有明显的规律性,而重度虫害后三环萜、月桂烯、莰烯、β-蒎烯、水芹烯、石竹烯24 h达到高峰;人工剪叶使马尾松轻度受害后,有些挥发物1 h达到高峰,有些24 h后才升至最高,相对含量出现高峰的时间没有明显的规律性;而人工剪叶重度损伤后,挥发物出现释放高峰的时间多在1 h或2 h。在整个快速诱导过程中,挥发物β-蒎烯的相对含量明显升高,72 h仍高于对照,说明该化合物在马尾松的诱导抗性中具有重要作用。
|
图 4 不同受害程度对β-蒎烯含量的影响 Fig. 4 Effect on content of β-pinene at different degrees |
植物的应激功能是建立在植物本身的自主调控、动态变化代谢的过程上。当植物受到胁迫时,植物将根据胁迫的大小而作出相应的应激反应(王海波,1993)。萜烯类化学物质的大量释放是针叶树最重要的防御措施之一,直接影响着植食性昆虫行为,有助于天敌和寄生蜂区分植物是否被侵害,利于寄主定位或捕食。这些植物受害后的信号导致了植物-植食性昆虫-天敌3营养层的相互作用(Paul et al., 1999);也是植物诱导化学防御的主要形式之一,这一研究不仅能在理论上加深对3营养层关系的认识,而且在实践上从一个侧面补充和完善害虫综合治理理论(娄永根等,1997)。另外,对害虫生物防治的研究也有重要意义。
植物释放挥发性化学物质的量和组成通常受到植物自身昼夜节律、环境因素的影响(Andre et al., 2001)。挥发性化学物质的分子机理方面已取得了一定的进展,其代谢途径及其调控机理的还需深入研究,以此探明植物的抗虫化学机制。
被诱导出的挥发物与马尾松毛虫行为之间的相互关系有待于进一步的生测试验来明确。
曹骥. 1984. 作物抗虫原理及应用. 北京: 科学出版社.
|
戈峰, 李典谟, 邱业先. 1997. 松树受害后一些化学物质含量的变化及其对马尾松毛虫种群参数的影响. 昆虫学报, 40(4): 337-342. DOI:10.3321/j.issn:0454-6296.1997.04.001 |
李继泉, 樊慧, 金幼菊, 等. 2002. 光肩星天牛取食后复叶槭挥发物的释放机制. 北京林业大学学报, 24(5/6): 170-174. |
李镇宇, 陈华盛, 袁小环, 等. 1998. 油松对赤松毛虫的诱导化学防御. 林业科学, 34(2): 43-49. DOI:10.3321/j.issn:1001-7488.1998.02.007 |
李镇宇, 李凯, 周青, 等. 1997. 秦皇岛地区樟子松引种及其对赤松毛虫抗性分析. 北京林业大学学报, 19(4): 39-44. DOI:10.3321/j.issn:1000-1522.1997.04.007 |
刘兴平, 戈峰, 陈春平. 2003. 我国松树诱导抗虫性研究进展. 林业科学, 39(5): 119-128. DOI:10.3321/j.issn:1001-7488.2003.05.018 |
娄永根, 程家安. 1997. 植物的诱导抗虫性. 昆虫学报, 40(3): 321-327. |
马尾松毛虫抗性研究组. 1990. 抗性植株的抗性机制研究. 林业科学, 26(2): 133-140. |
王燕, 戈峰, 李镇宇. 2001. 马尾松诱导化学物质的时空动态. 生态学报, 21(8): 1256-1261. DOI:10.3321/j.issn:1000-0933.2001.08.007 |
王海波. 1993. 昆虫胁迫下的植物应激反应模式. 生态学杂志, 12(6): 46-48. DOI:10.3321/j.issn:1000-4890.1993.06.012 |
赵成华, 伍德明, 阎云花. 1995. 马尾松针叶中挥发性成分的鉴定及其对马尾松毛虫的触角电位反应. 林业科学, 31(2): 125-131. |
Andre K, Baldwin I E. 2001. Defensive function of herbivore-induced plant volatile emissions in nature. Science, 291(16): 2141-2144. |
Diane M. M, Gershenzon J, Bohlmann J. 2003. Induction of volatile terpene biosynthesis and diurnal emission by methyl jasmonate in foliage of norway spruce. Plant Physiology, 132(3): 1586-1598. |
Farmer E E. 2001. Surface-to-air signals. Nature, 149(6): 854-856. |
Jin Youju, Li Jiquan, Li Jianguan, et al. 2004. Olfactory response of Anoplophora glabripennis to volatile compounds from ash-leaf maple. Scientia Silvae Sinicae, 40(1): 99-105. |
Loughrin J H, Heath R R, Turlings T C, et al. 1994. Diurnal cycle of emission of induced volatile terpenoids by herbivore-injured cotton plants. Proc Natl Acad Sci USA, 91: 11836-11840. DOI:10.1073/pnas.91.25.11836 |
Paul W P, James H T. 1999. Plant volatiles as a defense against insect herbivores. Plant Physiology, 121(2): 325-331. |
 2006, Vol. 42
2006, Vol. 42