文章信息
- 王冬梅, 张志毅, 安新民, 李善文, 何承忠.
- Wang Dongmei, Zhang Zhiyi, An Xinmin, Li Shanwen, He Chengzhong.
- 毛白杨AP3同源基因(PtAP3)的克隆及其在烟草中的正反义转化初报
- Cloning of an APETALA3 Homologous Gene (PtAP3)from Populus tomentosa andPreliminary Study on Its Sense and Anti-Sense Transformation in Tobacco
- 林业科学, 2005, 41(6): 35-42.
- Scientia Silvae Sinicae, 2005, 41(6): 35-42.
-
文章历史
- 收稿日期:2004-01-12
-
作者相关文章
高等植物的开花发育一直是研究的热点, 近年来, 有关花分生组织特征基因和花器官特征基因在拟南芥(Arabidopsis)、金鱼草(Antirrhinum)等植物中相继得到分离。这些基因的发现, 使得人们对植物的成花和花器官的发生与发育机制的认识进入到分子水平。目前已在拟南芥和金鱼草中建立了“ABC”模型(Coen et al., 1991; Chasan, 1991), 该模型认为, 控制拟南芥花器官特征的基因可分为A、B、C3类: A类基因包括APETALA1(AP1)和APETALA2(AP2); B类基因包括APETALA3(AP3)和PISTILLA(PI); C类基因有AGAMOUS(AG)。每类基因均在相邻2轮花器官中起作用, 这些基因单独或相互作用决定花器官的特征, 其中AP2单独决定萼片的形成, AP3或PI与AP2共同作用决定花瓣的形成, 而AP3或PI与AG的作用决定雄蕊的特征, AG的单独作用决定心皮的特征。此外A类基因与C类基因之间存在拮抗作用。这些基因编码的蛋白为转录因子, 其中大多数含有非常保守的MADS-box, 称为MADS-box基因(Yanofsky et al., 1990)。另外2个MADS-box基因系:D类基因参与了胚珠特征的决定(Angenent et al., 1995; Colombo et al., 1995), E类基因在MADS-box蛋白复合物的形成中起着关键的作用(Pelaz et al., 2000; Honma et al., 2000)。
毛白杨(Populus tomentosa)是我国特有的白杨派树种, 雌雄异株, 但偶见雌雄同株现象, 雌株较少(张志毅等, 1992)。杨树的花不同于拟南芥等模式植物的4轮花器官结构, 仅由苞片和雄蕊/雌蕊2轮结构组成(Sheppard et al., 2000)。这种结构差异的分子机制尚不清楚。早在20世纪80年代, 董源(1982;1984)就进行了毛白杨的胚胎学观察研究, 之后朱大保(1990)对毛白杨的有性生殖能力进行了研究, 张志毅等(1992;2000)先后对毛白杨开花结实特性和三倍体毛白杨的有性生殖能力进行了研究。近年来, 国外对杨树开花及花器官发育的分子生物学的研究进展很快。Sheppard等(2000)分离了毛果杨(Populus trichocarpa)APETALA3同源基因(PTD), 并对其时空表达进行了研究。与毛果杨开花及花器官发育相关的拟南芥LFY、AG、APETALA1同源基因PTLF、PTAG、PTAP1相继得到分离(Rottmann et al., 2000; Meilan et al., 2001)。毛白杨在我国分布广、面积大, 在生态防护林和工业用材林建设中发挥着重要的作用, 但长期以来存在育种周期较长和开花污染严重的环境问题。然而迄今为止, 在国内关于毛白杨开花发育相关基因的研究还未见报道。为此开展了毛白杨AP3同源基因的分离等相关研究工作, 这对揭示毛白杨开花的分子机理具有重要的理论意义, 并为通过基因工程手段缩短育种年限和抑制开花污染的研究奠定基础。
1 材料与方法 1.1 材料毛白杨试材取自北京林业大学苗圃, 在春季分别取毛白杨的雌性无性系(5082)和雄性无性系(L50)的幼叶用于提取基因组DNA, 进行PCR和Southern杂交分析。
1.2 方法 1.2.1 植物基因组DNA的制备按照王关林等(2002)所述方法提取。
1.2.2 PCR反应根据毛果杨AP3同源基因(PTD)的核酸序列, 设计合成了5'端引物(5'-TTGGATCC ATGGGTCGTGGAAAGA-3')和3'端引物(5'-AAGAGCTCTCAAGGAAGGCGAAGTT-3')。以毛白杨雄株基因组DNA为模板, 用上述引物进行PCR扩增。50μL PCR反应体系包括1×PCR buffer(Tris 10 mmol·L-1, pH8.3, KCl 50 mmol·L-1, MgCl2 2.5 mmol·L -1)中, 含毛白杨雄株基因组DNA 50 ng, 各1μL 10 pmol· μL-1的5'端引物和3'端引物, 2.5单位的Taq DNA聚合酶。反应先在94 ℃预变性5 min, 然后在94 ℃变性40 s、60 ℃复性40 s、72 ℃延伸2 min条件下进行30轮循环, 最后在72 ℃延伸10 min, 4 ℃保存。
1.2.3 PCR产物重组入pGEMⓇ-T easy载体回收凝胶中的PCR产物, 采用QIAquickⓇ Gel Extraction Kit (QIAGEN)纯化, 然后与pGEMⓇ-T easy载体(Promega)连接。连接产物转化大肠杆菌TG1菌株感受态细胞, 在LB/Amp/IPTG/X-gal平板上筛选重组质粒。重组质粒进行PCR、质粒长度和限制性内切酶酶切鉴定。
1.2.4 DNA序列测定及分析采用双脱氧终止法, PE公司377型自动测序仪测定重组质粒DNA序列。所得序列采用GenBank上的Blast进行同源性检索, 并运用Seqaid Ⅱ、Clutalx、Bioedit和DNAMAN等软件进行翻译、比较和作图分析。
1.2.5 探针制备与Southern杂交分析将上述PCR产物进行纯化, 在37 ℃下用DIG-11-dUTP标记20 h, 制备成杂交探针。分别以毛白杨雌、雄植株的幼叶为材料, 按照王关林等(2002)所述方法分别提取基因组DNA。取10μg雌雄株基因组DNA, 分别用Bam HⅠ、EcoRⅠ、hindⅢ酶切, 然后在0.8%琼脂糖凝胶电泳分离, 通过20×SSC转移到带正电荷的尼龙膜上。在42 ℃预杂交30 min, 然后加入探针在55 ℃杂交14~16 h。在20~25 ℃下用2×SSC/0.1% SDS(w/v)洗膜(2×5 min), 然后在65 ℃下用0.5×SSC/0.1% SDS(w/v)洗膜(2×15 min)。最后按照DIG DNA Labeling and Detection Kit (Roche)说明书进行免疫检测。
1.2.6 正反义植物表达载体的构建分别用BamHⅠ/SacⅠ和BamHⅠ/XbaⅠ对上述阳性重组质粒DNA和pBI121质粒DNA双酶切, 分别回收释放出的目的基因及基因片段和pBI121, 在T4-DNA连接酶作用下分别进行连接, 连接产物分别转化大肠杆菌TG1感受态细胞, 在含Kan的LB平板上筛选重组质粒, 并进行PCR(正义载体引物和反应条件同上述PCR。反义载体引物为:5'端引物5'-GGATTGATGTGATATCTCCACTG-3'和3'端引物5'-CCACAGTTTTCGCGATCCAGACT-3', 反应条件同上述PCR)、酶切和测序鉴定, 获得毛白杨PtAP3的正反义表达载体。
1.2.7 烟草的转化及转基因烟草的PCR检测挑取含有目标载体的农杆菌GV3101单菌斑于含有链霉素和卡那霉素的LB中, 在28 ℃下培养24 h。将无菌普通烟草(Nicotiana tabacum)叶片切成1~2 cm2小块, 预培养2 d后, 在上述菌液的10倍稀释液中浸泡5 min, 转入含羧苄青霉素(Cb, 500 mg·L-1)和卡那霉素(Kan, 100 mg·L-1)的MS培养基上进行筛选。待转化的烟草叶盘出现抗性芽后, 将抗性芽切下并置于生根培养基MSr(Cb, 250 mg·L-1; Kan, 100 mg·L-1)中生根, 使其长成完整植株。提取转基因烟草植株和对照植株的基因组DNA作为PCR反应的模板, PCR引物和反应条件同上述表达载体构建时相同。
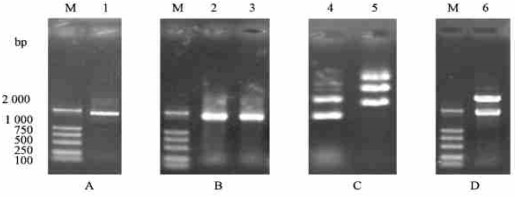
2 结果与分析 2.1 毛白杨AP3同源基因的分离克隆为了从毛白杨中分离AP3同源基因, 首先根据毛果杨AP3同源基因(PTD)设计合成了一对PCR引物, 利用PCR技术从毛白杨雄性植株基因组DNA中分离AP3同源基因(PtAP3)。PCR结果如图 1A所示, 扩增出一条长度大约为1.8 kb的DNA条带。将该条带回收纯化, 并与pGEMⓇ-T easy载体连接, 转化大肠杆菌TG1感受态细胞, 通过Amp和蓝白斑筛选, 获得重组质粒PTAP3XA-1和PTAP3XA-2。进一步进行PCR检测表明, 以重组质粒DNA为模板, 可扩增出与毛白杨雄株基因组DNA的PCR产物大小完全一致的DNA条带(图 1B)。质粒长度检测表明, 重组质粒比pBS的长度明显变长(图 1C), 用BamHⅠ和SacⅠ双酶切后释放出一条与PCR产物长度一致的DNA片段(图 1D)。说明PCR产物已经克隆入pGEMⓇ-T easy载体中。
|
图 1 毛白杨雄株AP3同源基因的克隆 Fig. 1 Cloning of AP3 homologous gene from male clone of P. tomentosa M. DL-2000 marker; 1. PCR产物PCR product of genomic DNA; 2, 3.PtAP3XA-1和PtAP3XA-2的PCR产物PCR products of PtAP3XA-1 and PtAP3XA-2;4.质粒pBSThe plasmid pBS; 5.重组质粒The recombinant plasmid; 6.重组质粒用BamHⅠ和Sac Ⅰ双酶切The recombinant plasmid digested with BamHⅠ and SacⅠ; A. PCR扩增产物PCR product of genomic DNA; B.重组质粒的PCR检测PCR tests of the recombinant plasmid; C.重组质粒长度检测Test of length of the recombinant plasmid; D.重组质粒的双酶切鉴定The recombinant plasmid digested with restriction endonucleases. |
测定重组质粒的DNA序列, 表明克隆的PCR产物长1 813 bp(包括引入的5’和3’端的酶切位点)。结合真核生物基因组DNA内含子的一般剪切规律, 并运用BCM Gene Finder主页(http://dot.imgen.bcm.tmc.edu:933I/gene-finder/gf.html)上的SPL (search for poten tial splice sites)程序对该序列进行拼接分析, 结果表明该基因序列包括7个外显子和6个内含子(1st exon 9……196; 1stintron 197……331; 2nd exon 332 ……398; 2nd intron 399……491; 3rd exon 492……553; 3rd intron 554……664; 4th exon 665……764; 4th intron 765……1323; 5thexon 1324……1365; 5th intron 1366…… 1446; 6th exon 1447…… 1491; 6th intron 1492…… 1592; 7th exon 1593…… 1805), 编码238个氨基酸(采用Seqaid Ⅱ推导)(图 2)。在第1个外显子中包括有MADS-box基因所特有的非常保守的序列(图 2划线部分), 推测该基因为MADS-box基因家族的一个成员, 其编码的蛋白可能具有转录因子的功能。

|
图 2 毛白杨雄株AP3同源基因(PtAP3)全长序列和推导的氨基酸序列 Fig. 2 The full nueclotide and deduced amino acid sequence of putative AP3 homologous gene(PtAP3) from male clone of P. tomentosa 小写字母为非编码序列, 大写字母为编码序列。 The small letters belong to non-coding sequence, and the capital letter belong to coding sequence. |
采用DNAMAN软件绘制了毛白杨AP3同源基因的结构和酶切图谱(图 3), 其中第1、2、3、4个外显子分布于该基因序列中的前1/2段, 而第5、6、7个外显子则分布于该基因序列的后1/3段, 第4个内含子是该序列中最大的内含子(559 bp)。除在PCR扩增时5'和3'端引入的BamHⅠ和SacⅠ位点外, 在516 bp、719 bp和862 bp处分别存在有EcoRⅤ、NdeⅠ和XbaⅠ酶切位点, 这为进一步进行Southern和Northern杂交分析制备探针、基因组DNA酶消化和功能研究提供了重要的信息。

|
图 3 毛白杨雄株AP3同源基因(PtAP3)结构和酶切图谱 Fig. 3 Structural and restriction map of AP3 homologous gene from male clone of P. tomentosa (PtAP3) |
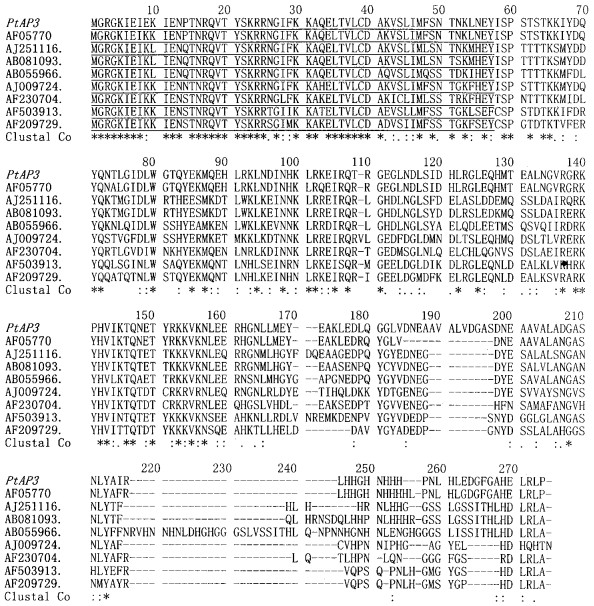
在GenBank进行Blast检索, 结果表明毛白杨与毛果杨(Populus trichocarp., AF057708)AP3同源基因编码的氨基酸序列具有82%同源性, 而与苹果(Malus domestic., AJ251116, AB081093)、玫瑰(Rosa rugos., AB055966)、百合(Lilium regale, AF503913, AB071378)、矮牵牛(Petunia hybrida, AF230704)和大丁草(Gerbera hybrid., AJ009724)的同源性则分别为60%、60%、55%、52%和52%。采用Bioedit和Clustalx软件对分别来自毛白杨、毛果杨、苹果、玫瑰、大丁草、矮牵牛、百合和萱草(Hemerocallis hybrid cultivar, AF209729)的AP3同源基因的氨基酸序列进行比较分析, 发现来自不同植物的AP3同源基因其编码的氨基酸序列在近5'端有较高的同源性(图 4), 而该区域属于高等植物非常保守的MADS-box基序(motif), 是转录因子的一个重要特征。因此, 推测本研究获得的毛白杨AP3同源基因可能具有转录因子的功能。
|
图 4 几种植物AP3同源基因编码的氨基酸同源性比较 Fig. 4 Similarity of amino acid sequences coded by AP3 homologous gene of several plants 采用Clustalx软件引入(--)以达到最大的同源性; 保守的MADS-box序列用下划线表示, 完全保守和适当替代的氨基酸分别用“*”、“:”和“.”表示。The amino acid sequences have been aligned by introducing gaps (--) to maximize homology (Clustal W software). Conserved MADS-box motif are underlined, and totally conserved and conservatively replaced amino acids are indicated by asterisks and dots, respectively. AF057708:毛果杨Populus trichocarpa; AJ251116 and AB081093:苹果Malus domestica; AB055966:玫瑰Rosa rugosa; AJ009724:大丁草Gerbera hybrida; AF230704:矮牵牛Petunia hybrida; AF503913:百合Lilium regale; AF209729:萱草Hemerocallis hybrid cultivar. |
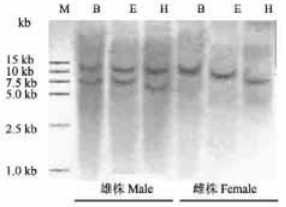
为证实获得的毛白杨雄性植株AP3同源基因的真实性, 用DIG标记的PtAP3制作探针, 杂交转有经BamHⅠ、EcoRⅠ和hindⅢ酶切过的雄、雌株基因组DNA的尼龙膜, 结果表明:在较高严谨度的洗膜条件下, 获得了理想的杂交信号, 说明PtAP3的确来自毛白杨基因组; 毛白杨雄、雌性植株基因组DNA杂交印迹显著不同, 其中在雄株基因组DNA中存在双拷贝AP3同源基因或者说存在同源性极高的2个成员, 而在雌株基因组DNA中则只有单拷贝的AP3同源基因(图 5)。
|
图 5 毛白杨雄雌株基因组DNA的Southern印迹分析 Fig. 5 Southern blot analysis of DNA from male andfemale clones of P. tomentosa using probe of PtAP3 M: DL15 000 marker; B: BamHⅠ; E: EcoRⅠ; H: hindⅢ. |
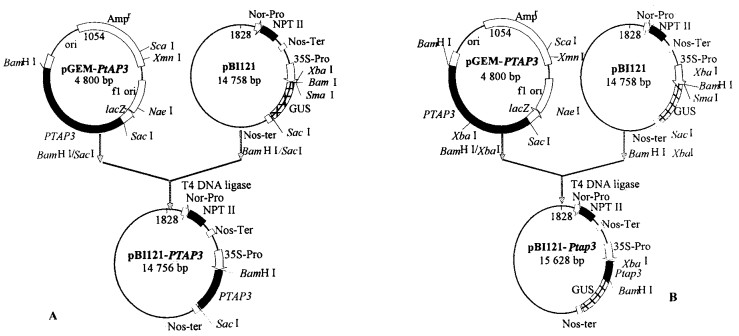
为了进一步研究毛白杨AP3同源基因PtAP3在雄蕊发育中的功能, 将重组质粒pGEM-PtAP3 与pBI121分别用BamHⅠ/SacⅠ和BamHⅠ/XbaⅠ进行消化, 然后回收相应条带, 在T4-DNA连接酶作用下进行连接, 构建成正反义植物表达载体(图 6)。经抗Kan筛选获得重组质粒pBI121-PtAP3和pBI121-Ptap3。PCR检测表明, 分别以pBI121-PtAP3和pBI121-Ptap3为模板, 能够扩增出1.8 kb和约1.1 kb(包括870 bp的目的序列及大约230 bp的35S启动子和GUS基因序列)的条带, 与插入片段的长度一致(图 7A, B)。进一步的酶切试验表明, 分别用BamHⅠ/SacⅠ和BamHⅠ/XbaⅠ对pBI121-PtAP3与pBI121-Ptap3进行消化, 可释放出1.8 kb和870 bp的条带(图 7C, D)。以上试验证明已经成功构建了毛白杨PtAP3的正反义表达载体。
|
图 6 毛白杨PtAP3正反义表达载体的构建 Fig. 6 Construction of sense and anti-sense expression vectors of PtAP3 A.毛白杨PtAP3正义表达载体构建Construction of sense expression vector of PtAP3; B.毛白杨PtAP3反义表达载体构建Construction of anti-sense expression vector of PtAP3. |
|
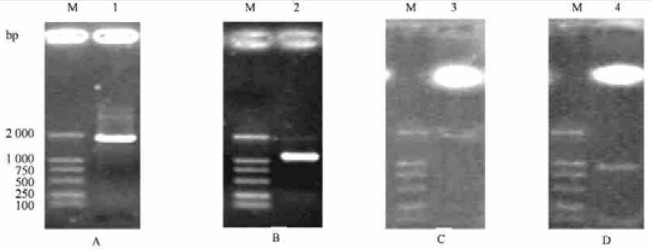
图 7 毛白杨PtAP3正反义表达载体的PCR和酶切鉴定 Fig. 7 The tests of PCR and digestion of both sense and anti-sense expression vectors of PtAP3 A.正义表达载体pBI121-PtAP3的PCR检测The test of PCR of pBI121-PtAP3; B.反义表达载体pBI121-Ptap3的PCR检测The test of PCR of pBI121-Ptap3; C. pBI121-PtAP3的酶切鉴定The test of digestion of pBI121-PtAP3; D. pBI121-Ptap3的酶切鉴定The test of digestion of pBI121-Ptap3.M. DL-2000 Marker; 1. pBI121-PtAP3的PCR产物PCR product of pBI121-PtAP3; 2. pBI121-Ptap3的PCR产物PCR product of pBI121-Ptap3; 3. pBI121-PtAP3的酶切产物pBI121-PtAP3 digested with BamHⅠ and SacⅠ; 4. pBI121-Ptap3的酶切产物pBI121-Ptap3 digested with BamHⅠ and XbaⅠ. |
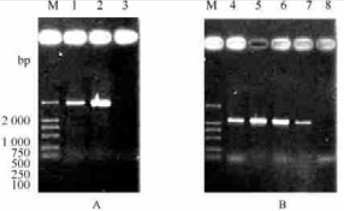
用含有正反义植物表达载体的农杆菌GV3101与烟草叶片共培养(图 8A, L:正义, R:反义), 待分化出抗性芽后, 将抗性芽切下在含羧苄青霉素(Cb, 500 mg·L-1)和卡那霉素(Kan, 100 mg·L-1)的MS培养基上进行培养(图 8B, L:正义, R:反义), 长到适当时机转入生根培养基MSr(Cb, 250 mg·L-1; Kan, 100 mg·L-1)中生根, 使其长成完整植株(图 8C正义, D反义)。然后提取这些抗性苗和对照植株的基因组DNA进行PCR检测, 结果如图 9所示, 表明获得了1个正义转化的烟草植株(图 9A)和3个反义转化的烟草植株(图 9B)。

|
图 8 烟草叶盘转化及抗卡那植株的获得 Fig. 8 Generation of Kan-resistant plantlets from tobacco leaf disks A.叶片与农杆菌共培养The tobacco leaf disks infected by Agrobacterium; B.抗性芽培养Kan-resistant shoots from tobacco leaf disks; C.抗性植株生根(正义转化) Culture of regenerated shoots(sense transformation) on generation medium; D.抗性植株生根(反义转化) Culture of regenerated shoots(anti-sense transformation) on generation medium. |
|
图 9 转基因烟草植株的PCR检测 Fig. 9 Transgenic tobacco plantlets verified by PCR A.正义转化植株的PCR检测The sense transgenic plant verified by PCR; B.反义转化植株的PCR检测The antisense transgenic plants verified by PCR. M. DL-2000 Marker; 1.正义转化植株The sense transgenic palnt; 2.阳性对照(pBI121-PtAP3) The positive control (pBI121-PtAP3); 3.非转化植株The non-transgenic plant; 4~6.反义转化植株The antisense transgenic plants; 7.阳性对照(pBI121-Ptap3) The positive control (pBI121-Ptap3); 8.非转化植株The non-transgenic plant. |
迄今为止已从多种草本植物中分离克隆了AP3同源基因, 如拟南芥、金鱼草、矮牵牛、马铃薯(Solanum tuberosum)等。对于木本植物而言, 则仅从苹果、美洲黑杨等分离到AP3同源基因。本研究通过PCR技术首次从毛白杨雄株分离克隆了AP3的同源基因PtAP3, 表明AP3同源基因广泛存在于高等植物中。
AP3同源基因的突出特点是含有非常保守的MADS-box, 一般认为该区域的功能是与DNA的结合有关。因MADS-box具有与DNA结合和形成二聚体的功能而参与转录调控, 故这些基因编码的蛋白属于转录因子。在许多植物中存在保守的MIKC结构(Alvarez-Buylla et al., 2000).在MADS-box的下游, 还含有较为保守的氨基酸序列K-box, MADS-box和K-box间的I区以及C末端区域。进一步的研究表明, MADS-box和I区域是与DNA结合所必须, I和K区有助于这些蛋白形成二聚体且影响二聚体的特异性(Riechmann et al., 1996a; 1996b), 而且AP3蛋白也是以二聚体的形式结合到DNA上。芯片杂交结果表明受AP3和PI调节的相关基因数量较小, 暗示许多在花瓣和雄蕊发育中作用的基因并不具有组织特异性, 而可能在其他的发育过程中也发挥作用(Moriyah et al., 2003)。PtAP3与其他几种植物的AP3同源基因具有较高的同源性, 尤其是在MADS-box区域同源性极高, 因此, PtAP3蛋白也应属转录因子。在拟南芥中AP3是一个花器官特征基因, 属于“ABC”模型的B类基因, AP3或PI与AG的作用决定雄蕊的特征(Honma et al., 2000; Pelaz et al., 2001)。最新的研究结果表明, AP3和PI直接调节参与响应花瓣和雄蕊形态发生基本细胞过程所必需的基因(Moriyah et al., 2003; Kramer et al., 2003)。本研究从毛白杨雄性植株分离克隆了PtAP3基因, 该基因可能在毛白杨花器官雄蕊的发育中具有重要的功能。进一步的Southern杂交分析显示, PtAP3基因在毛白杨雄雌株基因组DNA中同时存在, 但有明显差异, 在雄株中存在双拷贝PtAP3或可能存在另一同源性极高的同源基因, 而在雌株中为单拷贝PtAP3。Meilan等(2001)的研究证实了毛果杨AP3同源基因(PTD)除在雄花花原基中强烈表达外, 在雌花花原基中也有强烈的表达。
有关研究表明, 毛白杨雄株虽多, 但花粉败育现象严重(张志毅等, 1992)。而且毛白杨具有5~10年的童期, 育种周期较长。以上这些特性给毛白杨杂交育种工作带来许多困难。为了克服毛白杨花粉败育、花量少等育种中的困难, 同时也为了进一步研究毛白杨AP3同源基因的功能, 本研究构建了PtAP3的正反义表达载体, 通过农杆菌介导转化烟草并获得了一些正反义的转基因烟草植株, 进一步的分子检测和形态学观测正在进行。同时, 正在开展毛白杨的遗传转化工作, 未来获得的转化植株将可能减轻花粉的败育而提高其生活力, 这将为毛白杨杂交育种探索一条新的途径。
另外, 毛白杨作为我国北方城市重要的绿化树种, 在绿化、美化城市环境的同时, 由于雄株散粉和雌株飞絮又给城市环境造成一定的“污染”。尤其是育性好的杨树雄性植株飞散花粉, 使周围环境中可吸入颗粒物的密度增加, 是较为严重的过敏源之一; 在北方城市中每年春暖花开时节, 雌性杨树飞絮已成为影响环境质量的重要因子, 受到社会的广泛关注。为此本研究设计了PtAP3基因的部分反义序列(包括内含子), 连接于质粒pBI121的35S启动子之后, 构建成毛白杨AP3同源基因的反义表达载体, 用于转化毛白杨以抑制该基因的表达。由于在反义序列中引入内含子, 可对PtAP3基因的表达起到超抑制的效果。希望实现干扰毛白杨等杨柳科树种的开花及花器官发育, 达到改善环境质量的目的。
本研究分离克隆了毛白杨AP3同源基因PtAP3., 同时构建了其正反义表达载体, 用于毛白杨和烟草等的遗传转化研究。目前, 本实验室正在分离毛白杨LEAFY和AGAMOUS等与开花发育相关的基因, 进而研究分析这些基因在开花发育过程的时空表达规律, 将有助于从分子水平上理解毛白杨开花及花器官发育的机理, 为通过基因工程手段解决毛白杨育种存在的育种周期长、开花造成的环境“污染”、转基因受体的安全性问题等奠定了基础, 同时也为杨柳科其他树种的相关遗传改良提供借鉴。
董源. 1982. 毛白杨胚胎学观察. 北京林学院学报, (4): 80-92. |
董源. 1984. 毛白杨胚胎学观察. 北京林学院学报, (1): 83-94. |
王关林, 方宏筠. 2002. 植物基因工程. 第二版.北京: 科学出版社.
|
张志毅, 黄智慧, 张东芳, 等. 1992. 毛白杨标本园无性系开花结实的研究. 北京林业大学学报, 14(增3): 43-51. |
张志毅, 于雪松, 朱之悌. 2000. 三倍体毛白杨有性生殖能力的研究. 北京林业大学学报, 22(6): 1-4. DOI:10.3321/j.issn:1000-1522.2000.06.001 |
朱大保. 1990. 毛白杨有性生殖能力的研究. 北京林业大学学报, 12(1): 1-9. |
Alvarez-Buylla E R, Pelaz S, Liljegren S J, et al. 2000. An ancestral MADS-box gene duplication occurred before the divergence of plants and animals. Proc Natl Acad Sci USA, 97: 5328-5333. DOI:10.1073/pnas.97.10.5328 |
Angenent G C, Franken J, Busscher M, et al. 1995. A novel class of MADS box genes is involved in ovule development in Petunia. Plant Cell, 7: 1569-1582. |
Chasan R. 1991. Modeling flowers. Plant Cell, 2: 845-847. |
Coen E S, Meyerowitz E M. 1991. The war of the whorls: genetic interactions controlling flower development. Nature, 353: 31-37. DOI:10.1038/353031a0 |
Colombo L, Franken J, Koetje E, et al. 1995. The petunia MADS box gene FBP11 determines ovule identity. Plant Cell, 7: 1859-1868. |
Honma T, Goto K. 2000. The Arabidopsis floral homeotic gene PISTILLATA is regulated by discrete cis-elements responsive to induction and maitenance signals. Development, 127: 2021-2030. |
Kramer E M, Di Stilio V S, Schlüter P M. 2003. Complex patterns of gene duplication in the APETALA3 and PISTILLATA lineages of the ranunculaceae. Int J Plant Sci, 164(1): 1-11. DOI:10.1086/344694 |
Meilan R, Brunner A M, Skinner J S. 2001.Modification of flowering in transgenic trees. In: Morohoshi N, Komamine A(Eds). Molecular Breeding of Woody Plants. Elsevier Science BV, 247-256
|
Moriyah Z, Irish V F. 2003. Global identification of target genes regulated by APETALA3 and PISTILLATA floral homeotic gene action. The Plant Cell, 15: 207-222. DOI:10.1105/tpc.006353 |
Pelaz S, Ditta G S, Wisman E, et al. 2000. B and C floral organ identity functions require SEPALLATA MADS-box genes. Nature, 405: 200-203. DOI:10.1038/35012103 |
Pelaz S, Gustafson-Brown C, Kohalmi S E, et al. 2001. APETALA1 and SEPALLATA3 interact to promote flower development. Plant J, 26: 385-394. |
Riechmann J L, Krizek B A, Meyerowitz E M. 1996a. Dimerization specificity of Arabidopsis MADS domain homeotic proteins APETALA1, APETALA3, PISTILLATA, and AGAMOUS. Proc Natl Acad Sci USA, 93: 4793-4798. DOI:10.1073/pnas.93.10.4793 |
Riechmann J L, Krizek B A, Meyerowitz E M. 1996b. DNA-binding properties of Arabidopsis MADS domain homeotic proteins APETALA1, APETALA3, PISTILLATA, and AGAMOUS. Nucleic Acids Res, 24: 3134-3141. DOI:10.1093/nar/24.16.3134 |
Rottmann W H, Meilan R, Sheppard L A, et al. 2000. Diverse effects of overexpression of LEAFY and PTLY, a poplar (Populus) homolog of LEAFY/FLORICAUL., in transgenic poplar and Arabidopsis. The Plant Journal, 2213: 235-245. |
Sheppard L A, Brunner A M, Krutovskii K V, et al. 2000. DEFICIENS homolog from the dioecious tree black cottonwood is expressed in female and male floral meristems of the two-whorled, unisexual flowers. Plant Physiol, 124(2): 627-640. DOI:10.1104/pp.124.2.627 |
Yanofsky M F, Ma H, Bowman J L, et al. 1990. The protein encoded by the Arabidopsis homeotic gene agamous resembles transcription factors. Nature, 346: 35-39. DOI:10.1038/346035a0 |
 2005, Vol. 41
2005, Vol. 41

