文章信息
- 谈建康, 孔繁翔.
- Tan Jiankang, Kong Fanxiang.
- 酸沉降和铝对马尾松菌根共生体碳代谢影响
- Effects of Acid Precipitation and Al on Carbon Metabolism in Mycorrhizal Symbionts of Pinus massoniana
- 林业科学, 2005, 41(6): 23-27.
- Scientia Silvae Sinicae, 2005, 41(6): 23-27.
-
文章历史
- 收稿日期:2003-09-27
-
作者相关文章
2. 中国科学院南京地理与湖泊研究所 南京 210008
2. Nanjing Institute of Geography and Limnology, Chinese Academy of Sciences Nanjing 210008
在酸沉降环境中铝毒是植物受到的最主要毒害之一。铝在土壤中能以单核铝(Al3+)、聚合铝(Al13)、络合物(Al-F、Al-SO4)或螯合物等多种形态存在, 并对生态系统产生复杂伤害(Parker et al., 1992; 周国逸等, 1995; 孔繁翔等, 2000), 影响植物碳水化合物的合成和供应, 导致某些消耗能量的抗胁迫生理活动受阻(Brown et al., 1985; 孔繁翔等, 1997; 2002)。而植物在环境胁迫下能通过积累碳水化合物以提高细胞质水势、消耗碳水化合物提供能量, 以及形成菌根共生体, 将葡萄糖和果糖合成海藻糖、甘露醇等机制来增强植物对酸沉降的耐受能力(Thompsonm et al., 1984; Willenborg et al., 1990; Christian et al., 1991; 周崇莲等, 1993)。研究证明海藻糖的存在与菌根植物的强抗逆性有着密切的关系。Christian等(1991)发现在发育良好的菌根中, 海藻糖的合成率明显高于遭受损伤的植物根系, 植物活力明显增强。但是目前我国在酸沉降条件下植物菌根共生体内糖的代谢和转运方面的研究仍然有限。本文以马尾松(Pinus massoniana)菌根共生体内葡萄糖和海藻糖以及葡萄糖-6-磷酸脱氢酶(G6PDHase)和海藻糖酶(THase)作为分子生态毒理学指标, 从物质转运和能量转化的角度来探讨酸沉降对菌根植物的胁迫机理和菌根植物提高抗性能力的生理生化基础。
1 材料与方法 1.1 马尾松培养与菌根的形成将人工基质[活性炭:珍珠岩为1:1, 加入改良的Melin-Norkran液体培养基(Guttenberger et al., 1992)]加至2块玻板(15 cm×13 cm)之间, 厚度为1~1.5 cm。接种彩色豆马勃(Pisolithus tinctorius), 28 ℃培养2周后, 植入马尾松幼苗, 以未接种真菌的培养基为对照, 26 ℃光照(光暗比为12 h:12 h)培养4周, 用不同pH值(6.0、4.0、3.0、2.0)的铝溶液处理(铝理论浓度为75、150 μmol·L-1), 每天滴加5 mL, 连续处理4周。取样镜检确认菌根共生体的形成, 用蒸馏水清洗样品。
1.2 马尾松干质量和叶绿素测定取新鲜样品8株称质量并用ADVANTAGE(美国)冷冻干燥机冷冻干燥4 d, 再称质量并计算干质量。叶绿素测定采用丙酮比色法(张志良, 1993)。
1.3 碳水化合物测定可溶性糖含量用蒽酮法测定。海藻糖和葡萄糖测定:分别取根、茎、叶干样品在液氮中研磨, 加提取液(体积分数:乙醇:氯仿:水=12:5:3)抽提, 5 000×g离心20 min, 取上清液, 提取3次, 合并提取液, 转入分液漏斗, 加水分层, 取上层水离心去氯仿, 用0.1 mol·L-1 NaOH调pH值至7.0, 在45 ℃减压浓缩。高效液相色谱(WATERS 600)测定海藻糖、葡萄糖含量。色谱条件:流动相为高纯水, 流速0.6 mL·min-1, 156示差检测器, HP色谱数据处理系统。
1.4 根系碳水化合物代谢酶活性测定称取一定量根系干样品, 加入1 mL Tris-H3BO3缓冲液(0.01 mol·L-1 Tris, 0.05 mol·L-1 H3BO4, 0.05 mol·L-1 EDTA), 冰浴中抽提10 min, 4 ℃离心(10 000×g)10 min, -28 ℃保存上清液。G6PDHase活性按Kong(1995)的方法, THase活性测定采用Araujo等(1989)的方法。
1.5 数据分析用SPSS软件包进行数理统计分析。
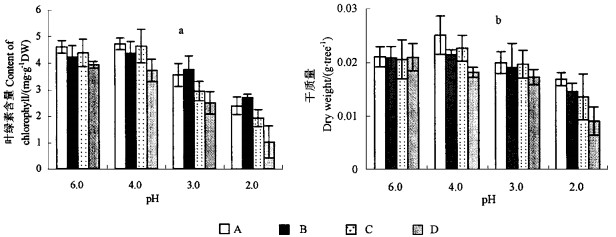
2 结果和分析 2.1 酸沉降和铝胁迫对马尾松叶绿素和干质量的影响叶绿素含量变化如图 1a。当pH值低于4.0时, 在菌根植株中叶绿素含量随着pH值降低而减少, 在pH 2.0时分别降低为pH 6.0时对照的51.9%、64.1%;未形成菌根植株内叶绿素含量明显低于菌根植株对照(P<0.01), 在pH 2.0时分别降低为pH 6.0时对照的44.2%、26.1%。同时, 在pH值为3.0和2.0时酸沉降和铝胁迫的增强明显减少马尾松干质量(图 1b), 未形成菌根植株干质量低于菌根植株对照。叶绿体是植物体内比较敏感的细胞器, 在逆境中由于膜脂过氧化造成叶绿体严重损伤而叶绿素减少, 进一步影响了植物有机物质的合成(孔繁翔等, 1997; Araujo et al., 1989)。在酸沉降和铝胁迫下, 马尾松体内叶绿素含量急剧减少, 直接导致植物光合作用减弱, 减少了植物体内有机物合成, 明显抑制了马尾松干质量积累, 并且叶绿素和干质量呈较好的正相关性(r= 0.949)。
|
图 1 酸沉降和铝对马尾松叶绿素含量和干质量的影响 Fig. 1 Effects of acid precipitation and Al on contents of chlorophyll and dry weight of P. massoniana A.接种P. tinctorius与75 μmol·L-1铝处理组Inoculated with P. tinctorius and treated with 75 μmol·L-1 Al; B.接种P. tinctorius与150 μmol·L-1铝处理组Inoculated with P. tinctorius and treated with 150 μmol·L-1 Al; C.未接种P. tinctorius与75 μmol·L-1铝处理组No inoculated with P. tinctorius and treated with 75 μmol·L-1 Al; D.未接种P. tinctorius与150 μmol·L-1铝处理组No inoculated with P. tinctorius and treated with 150 μmol·L-1 Al.下同。The same below. |
酸沉降和铝胁迫对可溶性糖在马尾松不同器官内积累影响不一(图 2)。叶片中可溶性糖随着酸沉降增强和铝浓度增加而显著降低; 菌根植株内可溶性糖含量明显高于未形成菌根植株对照, 并与叶绿素含量呈较好的正相关(r= 0.897)。植物通过光合作用合成糖并积累在植物体内, 由此推断酸和铝胁迫下叶绿素的减少直接导致了糖合成减少。茎内可溶性糖在pH 4.0时增加15%~30%, 当pH值小于4.0时可溶性糖含量减少, 但减少幅度小于叶片内糖含量变化(pH 2.0时可溶性糖含量为最高值的73.5%)。根系可溶性糖在pH值大于3.0时明显增加, 但pH值小于3.0时可溶性糖含量降低, 且明显低于茎内糖含量。

|
图 2 酸沉降和铝胁迫对马尾松根、茎、叶内可溶性糖含量的影响 Fig. 2 Effects of acid precipitation and Al on soluble sugars in roots, stems and leaves of P. massoniana |
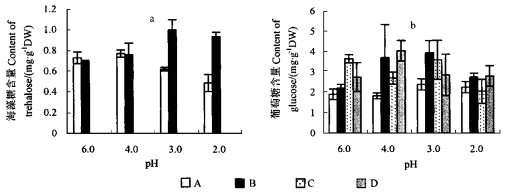
低铝(75 μmol·L-1)胁迫下, 马尾松菌根内海藻糖含量随pH降低而减少(图 3a), 而高铝(150 μmol·L-1)胁迫下, 海藻糖含量增加并明显高于低铝对照, 在pH值为3.0和2.0时分别为低铝对照的146%和193%;未形成菌根植株根系无海藻糖。在低铝胁迫下, 菌根根系内葡萄糖含量随着pH值降低而增加(图 3b), 未形成菌根根系内葡萄糖含量明显高于菌根对照; 在高铝胁迫下, 菌根内葡萄糖含量高于低铝胁迫对照, 并随着pH值降低呈先升后降的趋势, 未形成菌根根系内葡萄糖含量亦呈先升后降的趋势。由此可以认为酸沉降和铝胁迫能诱导菌根体内葡萄糖积累, 但强酸(pH 2.0)胁迫抑制葡萄糖的积累, 菌根的形成能减少其他糖类向葡萄糖的转化。
|
图 3 酸沉降和铝胁迫对马尾松根海藻糖和葡萄糖含量的影响 Fig. 3 Effects of acid precipitation and Al on trehalose and glucose in P. massoniana roots |
在低铝胁迫下, 菌根植株茎内葡萄糖含量无明显变化(图 4a), 未形成菌根植株茎内含量明显高于菌根植株对照; 高铝胁迫下菌根植株和未形成菌根植株茎内葡萄糖含量高于低铝胁迫对照, 并随着pH值的降低呈先升后降的趋势。叶片内葡萄糖含量如图 4b。在低铝胁迫下, 形成菌根的植株叶片内葡萄糖含量随着pH值的降低而增加, 而高铝胁迫下菌根植株叶内葡萄糖含量呈先升后降的趋势。未形成菌根的植株叶片内葡萄糖含量变化明显高于形成菌根植株对照, 但在pH 2.0时葡萄糖含量显著减少并低于菌根植株对照, 证实酸雨和铝胁迫的增强能诱导马尾松叶片内其他形式如蔗糖和淀粉等向葡萄糖形式的转化, 但在强酸(pH 2.0)胁迫下葡萄糖积累反而受抑制。

|
图 4 酸沉降和铝胁迫对马尾松茎、叶葡萄糖含量的影响 Fig. 4 Effects of acid precipitation and Al on glucose in stems and leaves of P. massoniana |
在低铝胁迫下马尾松菌根内G6PDHase的活性在不同程度酸沉降下均保持较低水平(图 5a), 而未形成菌根根系G6PDHase明显升高, 但在pH 2.0的处理下酶活性急剧下降, 可能在强酸胁迫下酶的活性受到抑制。高铝胁迫下菌根内G6PDHase活性显著高于低铝胁迫, 且随着pH值的降低呈上升趋势; 未形成菌根根系G6PDHase随着pH值下降而明显降低。THase活性如图 5b, 随着pH值降低, 低铝胁迫下菌根根系内THase活性明显升高, 但高铝胁迫下pH小于4.0时, 酶活性逐渐降低; 未形成菌根根系内THase活性在低铝和高铝胁迫下均保持在较低的水平。

|
图 5 酸沉降和铝胁迫对马尾松根系G6PDHase和THase活性的影响 Fig. 5 Effects of acid precipitation and Al on the activities of G6PDHase and THase in roots of P. massoniana |
在植物体内, 糖是光合作用所产生的能量储存形式, 也是植物生理活动所需能量的直接提供者(Christian et al., 1991; Dighton et al., 1991; 孔繁翔等, 1997)。植物体内可溶性糖含量的增加, 能够提高细胞内水势, 为酶反应提供足够的自由水环境, 对细胞起着保护作用(Christian et al., 1991)。本试验中低强度的酸沉降和铝胁迫诱导了可溶性糖在马尾松茎和根系内大量积累, 不仅为植物根系抗胁迫提供大量能量来源, 也直接提高了植物抗胁迫能力; 但在胁迫强度过高时可溶性糖含量明显减少。由此推断, 马尾松通过光合作用合成糖, 并通过茎运输到根系供给其必要的物质和能量。在外界胁迫下, 植物通过茎向下运输大量糖以满足根系耐受胁迫所需的碳水化合物和能量, 茎内可溶性糖含量随之增加, 但随着叶片光合能力减弱和糖合成减少, 向下运输的糖也随之减少。同时在强酸沉降下, 植株茎内的可溶性糖明显积累并高于根部糖含量, 可能由于糖向下传运机制受到抑制, 导致糖在茎内大量积累而根系糖供应不足。
在外界胁迫下, 植物也能分解体内淀粉和蔗糖成大量葡萄糖, 以提高植物抗胁能力(Christian et al., 1991; 孔繁翔等, 2002), 但强胁迫下该机制受到抑制, 导致葡萄糖含量随着pH值降低呈先升后降的趋势。菌根真菌能利用地上部分转运来的葡萄糖合成海藻糖, 成为真菌中特有的碳水化合物储存形式(孔繁翔等, 1997; 2000)。周崇莲等(1993)研究认为, 菌根真菌内的碳源主要由植物提供, 菌根内可溶性糖的增加有利于菌根的形成和海藻糖的合成, 从而提高植物的抗胁迫能力。虽然该结论有很大的争议, 但本试验海藻糖结果支持这一观点, 在低强度胁迫下菌根根系可溶性糖及葡萄糖含量增加, 海藻糖含量同时明显增加。而在高铝胁迫下, 葡萄糖积累明显受到酸沉降抑制, 但海藻糖含量仍然明显增加, 这与Kong(1995)的结果一致, 菌根根系在外界强酸沉降胁迫下海藻糖含量增加而葡萄糖含量减少, 进一步证实了酸沉降影响菌根根系不同形态糖互相转化的观点。
G6PDHase催化葡萄糖-6-磷酸进入戊糖磷酸途径, 而葡萄糖-6-磷酸主要来源于葡萄糖(孔繁翔等, 1997; Christian et al., 1991), 因此, G6PDHase活性的升高将导致葡萄糖大量分解。低强度Al胁迫诱导了G6PDHase活性以消耗更多的葡萄糖产生能量以抵抗外界胁迫, 但随着胁迫强度增强, G6PDHase酶活性受到抑制, 葡萄糖消耗产能减少, 但葡萄糖含量并没有相应地因分解减少而增加, 可能在酸沉降下各种酶活性相应受到抑制, 导致其他形式的碳水化合物分解成葡萄糖的绝对量减少。研究认为, 低强度的铝和酸沉降诱导了G6PDHase活性的增强, 但酸沉降诱导了葡萄糖含量的增加, 提高了细胞的抗胁能力(Christian et al., 1991), 也为G6PDHase分解糖产能提供了大量底物。而在高强度胁迫下G6PDHase酶受到抑制, 但强胁迫同时导致葡萄糖的积累和转运机制失衡, 因此强酸和Al胁迫下G6PDHase酶活性和葡萄糖含量无明显的相关性。THase活性的升高促进了海藻糖转化为葡萄糖, 海藻糖含量降低(Araujo et al., 1989; 孔繁翔等, 1997); Kong(1995)研究证明在强酸雨和铝的共同作用下, 菌根真菌中THase活性下降, 可以减缓海藻糖的分解, 保持菌根较高的抗性。本试验中高铝胁迫抑制了THase的活性, 海藻糖含量明显增加, 两者趋势呈较好的一致性(r=-0.857)。在未形成菌根根系中THase活性保持在较低水平。
孔繁翔, 胡伟, 桑伟莲, 等. 2002. 二氧化硫对地衣中共生藻菌营养关系影响研究. 应用生态学报, 13(2): 151-155. DOI:10.3321/j.issn:1001-9332.2002.02.006 |
孔繁翔, 刘营, 章敏. 1997. 菌根及酸沉降对菌根影响的研究进展. 环境科学研究, 10(6): 15-19. DOI:10.3321/j.issn:1001-6929.1997.06.006 |
孔繁翔, 桑伟莲, 蒋新, 等. 2000. 铝对植物毒害及植物抗铝作用机理. 生态学报, 20(5): 855-862. DOI:10.3321/j.issn:1000-0933.2000.05.023 |
张志良. 1993. 植物生理学实验指导. 北京: 高等教育出版社, 18-91.
|
周崇莲, 郭良栋. 1993.酸雨对马尾松和杉木菌根发育和酶活性的影响.见: 冯宗炜.酸雨对生态系统的影响——西南地区酸雨研究.北京: 中国科学技术出版社, 118-132
|
周国逸, 小仓纪雄. 1995. 模拟酸雨的土壤淋洗液对马尾松华山松幼苗生长的影响. 应用与环境生物学报, 1(2): 138-144. DOI:10.3321/j.issn:1006-687X.1995.02.006 |
Araujo P S, Panek A C. 1989. Determination of trehalose in biological samples by a simple and stable trehalase preparation. Anal Biochem, 176(2): 432-436. |
Brown M T, Wilkins D A. 1985. Zinc tolerance of mycorrhizal betula. New Phytol, 99(1): 101-106. DOI:10.1111/j.1469-8137.1985.tb03640.x |
Christian P A, Paul T R. 1991. Stress interactions and mycorrhizal plant response: understanding carbon allocation priorities. Eviron Pollut, 73: 217-244. DOI:10.1016/0269-7491(91)90051-W |
Dighton J, Jansen A E. 1991. Atmospheric pollutants and ectomycorrhizae: more questions than answers?. Environ Pollut, 73: 179-204. DOI:10.1016/0269-7491(91)90049-3 |
Guttenberger M, Hampp R. 1992. Ectomycorrhizins-symbiosis-specific or artifactual polypeptides from ectomycorrhizas?. Planta, 18: 129-136. |
Kong F X. 1995. Influence of copper, manganese and pH on the growth and several enzyme activities in mycorrhizal fungus Amanita muscaria. Chemosphere, 30(1): 199-207. DOI:10.1016/0045-6535(94)00393-9 |
Parker D R, Bertsch P M. 1992. Formation of the Al3+ tridecameic polycation under diverse synthesis conditions. Envion Sci Technol, 26: 914-921. DOI:10.1021/es00029a007 |
Thompsonm G W, Medve R J. 1984. Effects of aluminum and manganese on the growth of ectomycorrhizal fungi. Appl Environ Micro, 48: 556-564. |
Willenborg A, Schmitz D, Lelley J. 1990. Effect of environmental stress factors on ectomycorrhizal fungi in vitro. Can J Bot, 68: 1741-1752. DOI:10.1139/b90-224 |
 2005, Vol. 41
2005, Vol. 41

