文章信息
- 王明旭, 朱水芳, 罗宽, 周李华, 赵文军.
- Wang Mingxu, Zhu Shuifang, Luo Kuan, Zhou Lihua, Zhao Wenjun.
- 松材线虫rDNA-ITS2的TaqMan探针实时荧光PCR检测
- Studies on Real-Time Fluorescent PCR With TaqMan Probe for rDNA-ITS2 of Pine Wood Nematode(Bursaphelenchus xylophilus)
- 林业科学, 2005, 41(2): 82-85.
- Scientia Silvae Sinicae, 2005, 41(2): 82-85.
-
文章历史
- 收稿日期:2004-10-18
-
作者相关文章
2. 湖南省森林病虫害防治检疫总站 长沙 410007;
3. 中国检验检疫科学研究院动植物检疫研究所 北京 100029
2. General Station of Forest Pest Management and Quarantine, Hunan Province Changsha 410007;
3. Institute of Animal and Plant Quarantine, CAIQ Beijing 100029
松材线虫病(Bursaphelenchus xylophilus)是当前严重危害和威胁我国松林安全的最主要入侵有害生物(祝列克,2002),世界四大林木病害之一(全国森林病虫兽害防除协会,2002),也是世界重要检疫性有害生物;检疫要求与措施的实施严重影响国际贸易,对经济社会影响很大。松材线虫rDNA由保守的18S、5.8S和28S基因编码区以及非编码的间隔区ITS组成,ITS高度变异,所以作为松材线虫和拟松材线虫(B. mucronatus)分子鉴定的理想区域。近几年来,以rDNA为基础的PCR-RFLP和PCR-SSCP技术(张立海等,2002;Wahori et al., 1998)检测松材线虫的方法提高了检测的准确性,但这些方法过程繁杂,操作步骤多,同时需要PCR后处理,不仅需要的仪器多,时间长,而且电泳时使用的溴化乙锭对人体有害,实验过程容易受到污染和出现假阳性结果。在rDNA中,松材线虫和拟松材线虫的ITS2种间差异最大(17.5%~19.2%)1)。因此,笔者以rDNA-ITS2为靶区设计了TaqMan探针,对松材线虫大量DNA和单条松材线虫进行实时荧光PCR检测技术研究,以期获得一种检测松材线虫的快速、简单、准确、灵敏的新方法。
1) 张立海. 2000.松材线虫rDNA的PCR鉴定.广州:华南农业大学,硕士论文
1 材料与方法 1.1 材料本试验所用的松材线虫株系采自我国松材线虫病发生区,其中0703、0704、0801、0802、0806、CZBx、GDBx采自广东,AnfBx、MABx采自安徽,NJ05、CqBx采自江苏,ZjFy采自浙江,USABx为我国出入境检疫检验机关截获;拟松材线虫株系XBm、X140采自湖南省张家界。
本试验用Faststart TaqDNA聚合酶、dATP、dTTP、dCTP、dGTP、PCR缓冲液、MgCl2购自Roche公司。
1.2 方法 1.2.1 线虫培养将兰变菌(Ceratocystis sp.)移到PDA培养基上,培养4~5 d当菌丝即将长满时接入分离好的线虫,在25 ℃条件下培养1周左右,用漏斗法分离,离心后收集线虫悬浮液贮存于4 ℃冰箱中备用。
1.2.2 大量DNA提取参考Wahori等(1995)的方法。将200 μL线虫悬浮液与200 μL抽提缓冲液(200 mmol·L-1 NaCl, 200 mmol·L-1 Tris-HCl, 100 mmol·L-1 EDTA, 2%SDS, 200 μg·mL-1 Pork, pH 8.0)混合,用磨口研棒研磨,65 ℃孵育1~2 h;加入苯酚:氯仿:异戊醇(25:24:1),混匀,4 ℃,13 000 r·min-1离心10 min, 回收上相,如此重复3次,加入2倍体积的无水乙醇(-20 ℃预冷);-20 ℃放置20 min后,13 000 r·min-1离心10 min; 用70%乙醇(-20 ℃预冷)沉淀,室温下晾干;加入20~50 μL TE (10 mmol·L-1 Tris-HCl, 1mmol·L-1 EDTA,pH 8.0)溶解DNA,置于-20 ℃冰箱保存待用。
1.2.3 单条线虫DNA提取单条线虫DNA采取超低温极速冷冻法,此方法是在贺水山(2002)方法基础上的改进,即在解剖镜下,用移液枪吸取3 μL含单条线虫的悬浮液至PCR反应管中,然后加入TE(10 mmol Tris-HCl, 1 mmol EDTA, pH8.0)缓冲液至总体积14.8 μL。把PCR反应管放置于-70 ℃冰箱中冷冻10 min, 取出后在悬浮液融化前用移液枪头轻轻掏碎,作为PCR反应的DNA模板。
1.2.4 TaqMan探针与引物的设计与合成从Genbank中调出松材线虫和拟松材线虫的rDNA序列,用Omiga软件找出ITS2区域,按照TaqMan探针设计原理,用primer express软件在种间差异大的区域设计松材线虫引物BXF:5′-GGCGAGAGGGCTTCG-3′,BXR:5′-CGCCGTTGAAACAACATCAC-3′和探针BXP:5′-ATTGTCGTGCGCGGCTAAACCGT-3′。引物和探针由上海博亚生物技术公司合成,探针5′端标记报告荧光染料6-Carboxyfluorescein(FAM),3′端标记淬灭荧光染料Tetramethycarbo xyrhodamine(TAMRA)。
1.2.5 实时荧光PCR反应体系大量DNA反应体系:10×PCR反应缓冲液2.5 μL,MgCl2 (25 mmol·L-1)2 μL,dNTP (2.5 mmol·L-1)2 μL,BXF引物(10 μmol·L-1) 2 μL,BXR引物(10 μmol·L-1) 2 μL,BXP探针(10 μmol·L-1) 1 μL,TaqMan聚合酶(5 U·mL-1) 0.2 μL,模板DNA4.0 μL,加灭菌ddH2O至25 μL。单条线虫的反应体系:10×PCR反应缓冲液2.5 μL,MgCl2 (25 mmol·L-1)2 μL,dNTP (2.5 mmol·L-1)0.5 μL,BXF引物(10 μmol·L-1) 2 μL,BXR引物(10 μmol·L-1) 2 μL,BXP探针(10 μmol·L-1) 1 μL,TaqMan聚合酶(5 U·ml-1) 0.2 μL,单条线虫TE悬浮液14.8 μL。
1.2.6 样品检测将样品放入ABIPRISM7700 96孔反应板上,打开计算机。点击SDS1.91软件,设置反应条件,第一个循环为95 ℃ 10 min;后40个循环为95 ℃ 15 s,60 ℃ 1 min。点击运行,进行PCR反应,1 h 54 min反应结束,保存文件,打开软件,分析ΔRn值(第n循环时的荧光信号增加值)与循环数。
1.2.7 松材线虫rDNA基因序列测定以松材线虫rDNA为模板,用引物5′-ACCTTCGGCTGGATCATTAC-3′和5′-TTCAACCAATTCCGACAACA-3′进行PCR反应,取40 μL PCR产物交上海博亚生物技术公司纯化后,根据四色荧光末端终止法原理,用ABI 3730测序仪测定核苷酸序列。
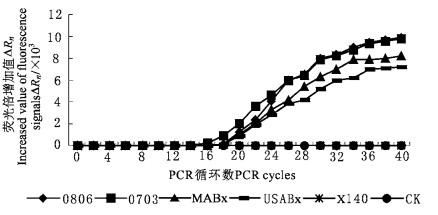
2 结果与分析 2.1 ITS2 TaqMan探针检测松材线虫大量DNA用BXP探针检测4种松材线虫株系和1种拟松材线虫株系,4种松材线虫株系表现为阳性扩增,Ct值为15.5~17.5,检测到荧光信号ΔRn为7 000~9500。而拟松材线虫和水对照未有荧光信号,表现为阴性(图 1)。说明BXP探针对松材线虫的特异性,可明显地区分松材线虫和拟松材线虫,对快速诊断松材线虫具有实用价值。
|
图 1 BXP探针实时荧光PCR结果图 Fig. 1 Results of RTF PCR generated by BXP probe |
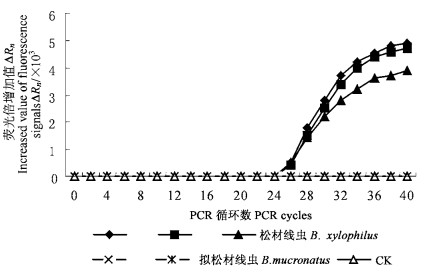
用BXP探针检测单条松材线虫和拟松材线虫,3条松材线虫表现明显的阳性特征,40个PCR循环时的荧光信号增加值最低达3 800,最高达4 900。而拟松材线虫和对照没有荧光信号,表现为明显的阳性(图 2)。可见,检测单条松材线虫时,虽然样品中特异性模板DNA含量很低,且有蛋白质和其他DNA存在的情况下,BXP探针仍然表现高度的特异性。
|
图 2 BXP探针检测单条线虫实时荧光PCR结果 Fig. 2 Results of single nematode RTF PCR generated by BXP probe |
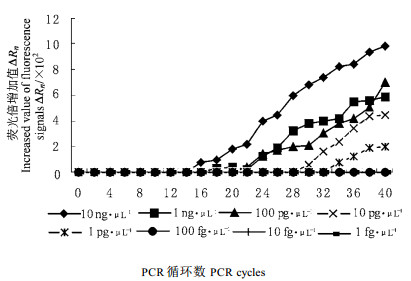
将松材线虫的DNA稀释为10、1 ng·μL-1,100、10、1 pg·μL-1,100、10、1 fg·μL-1作为模板加入到引物BXF/BXR,BXP探针的反应体系中,其检测到的稀释最低浓度为1 pg·μL-1(图 3)。
|
图 3 BXP探针检测的灵敏度 Fig. 3 Sensitivity of RTF PCR generated by BXP probe |
以0703株系为代表的测序结果显示,所克隆的rDNA序列长为766 bp(图 4), 与GenBank中gi33943122、gi33943123、gi4249371、gi3661141和gi37665561等松材线虫株系的同源性100%,表明BXP TaqMan探针检测到的松材线虫株系的正确性。

|
图 4 松材线虫0703株系rDNA序列 Fig. 4 The rDNA sequence of 0703 strain of B. xylophilus |
用BXP探针检测13个松材线虫株系、1个拟松材线虫株系和1个空白对照,40个循环结束时,13个松材线虫株系产生强烈的荧光信号,最低ΔRn值为3 800,最高达到10 000,而拟松材线虫和对照则无荧光信号,进一步证实了BXP可以作为特异性探针用于松材线虫的实时荧光PCR检测。
3 结论与讨论本试验利用松材线虫和拟松材线虫的rDNA-ITS2种间差异显著特性,设计TaqMan探针,用实时荧光PCR的检测方法能准确地区别2种线虫,并结合简单、快速处理单条线虫的方法,无需进行DNA的提取,提高了检测的速度,整个过程不到3 h,适用于松材线虫的快速检测。
松材线虫是一种重要的国内外检疫性有害生物,对松科植物的致病性强,与其相似的拟松材线虫的致病性弱,在实际检测工作中容易对二者产生混淆。而对松材线虫的检测正确与否是决定采取检疫监管措施的重要依据,因此建立快速、简单、准确、灵敏的检测是及时发现、封锁和扑灭疫情的关键,具有重要的实践意义。目前,松材线虫的检测方法有流胶检测法、形态学检测法、化学检测法和分子生物学检测法。流胶检测法主要根据松材线虫危害后松树树脂分泌停止而进行检测,由于影响松树流胶的因素很多,该方法对于非疫情发生区的早期诊断有局限性。从形态学上正确地鉴定松材线虫对一些非专业从事植物线虫的人员来说有一定的困难。pH值检测法(王玉嬿等,2001)、纤维素酶扩散检测法(蒋丽雅等,1995)和显色法(王明旭等,2004)等化学检测方法虽然检测的时间短,但不稳定,需要进一步完善。PCR-RAPD(汪来发等,1999;Irdani et al., 1995)、PCR-RFLP和PCR-SSCP等基于常规PCR的分子生物学检测技术有助于提高检测的准确性,但这些方法均需PCR后处理,检测的时间需要一天甚至几天才能完成,而且在后处理过程中常因出现污染而影响检测结果的准确性和可靠性。实时PCR技术在同一密闭试管中,实现PCR扩增与靶核苷酸探针杂交同时进行,与传统的PCR相比,其污染可能是最低的,检测需要的时间更短,灵敏度高(朱水芳,2003)。用实时荧光PCR方法检测松材线虫,符合有害生物检疫检验工作中所要求的简单、快速、准确、灵敏的标准,在实践中具有重要的推广应用价值。
贺水山, 闻伟刚, 杨兰英, 等. 2002. 松材线虫PCR快速检测方法研究. 植物检疫, 16(6): 321-324. DOI:10.3969/j.issn.1005-2755.2002.06.001 |
蒋丽雅, 王晓芸. 1995.松材线虫虫体提取液和分泌液中纤维素酶的定性检测.见: 杨宝君.中国松材线虫病的流行与治理.北京: 中国林业出版社, 60-61
|
王明旭, 张志飞, 罗宽, 等. 2004. 松材线虫快速检测技术方法比较研究. 湖南农业大学学报, 30(3): 239-242. |
王玉嬿, 李海燕. 2001. 几种松树松材线虫病木和健康木pH值差异的研究. 植物病理学报, 31(4): 342-348. DOI:10.3321/j.issn:0412-0914.2001.04.011 |
汪来发, 王杨, 杨宝君. 1999. 运用RAPD研究松材线虫与拟松材线虫的亲缘关系. 云南农业大学学报, 14(增刊): 119. |
张立海, 廖金铃, 冯志新. 2001. 松材线虫rDNA的测序和PCR-SSCP分析. 植物病理学报, 32(1): 84-89. DOI:10.3321/j.issn:0412-0914.2001.01.013 |
朱水芳. 2003. 实时荧光聚合酶链反应(PCR)检测技术. 北京: 中国计量出版社.
|
祝列克. 2002. 要重视和防范外来有害生物的入侵危害. 中国森林病虫, 21(6): 36-39. DOI:10.3969/j.issn.1671-0886.2002.06.012 |
全国森林病虫兽害防除协会. 2002.  .东京: 松尾印刷株式会社, 243 .东京: 松尾印刷株式会社, 243
|
Braasch H, Burger M W, Pastrik K H. 1995. Differentiation of three Bursaphelenchus species by means of PAPD-PCR. Nachrichtenblatt des Deutschen Pflanzenschutzdienstes, 47(12): 310-314. |
Irdani T, Caroppo S, Ambrogioni L. 1995. Molecular identification of pine wood Bursaphelenchus species. Nematologia Mediterranea, 23(Suppl.): 99-106. |
Wahori H, Tsuda K, Kanzaki N, et al. 1998. PCR-RFLP and sequencing analysis of ribosomal DNA of Bursaphelenchus nematodes related to pine wilt disease. Fundam Appl Nematol, 21(6): 655-666. |
 2005, Vol. 41
2005, Vol. 41
