文章信息
- 曾杰, 郑海水, 甘四明, 白嘉雨.
- Zeng Jie, Zheng Haishui, Gan Siming, Bai Jiayu.
- 广西西南桦天然居群的表型变异
- Phenotypic Variation in Natural Populations of Betula alnoides in Guangxi, China
- 林业科学, 2005, 41(2): 59-65.
- Scientia Silvae Sinicae, 2005, 41(2): 59-65.
-
文章历史
- 收稿日期:2002-11-04
-
作者相关文章
自从19世纪达尔文等人发现物种的变异以来,到20世纪60年代等位酶分析技术的出现,表型性状一直是研究物种变异和进化的主要标记。天然居群的表型变异研究能够使我们初步了解类群遗传变异的大小,是人工驯化和遗传育种研究的基础,也是揭示类群适应性的有效途径之一。因此,尽管天然居群表型性状的变异研究因条件难以控制以进行严密的试验设计(葛颂等,1994),因而不能区分环境效应和遗传效应对表型变异的贡献(Olfelt et al., 2001),但利用表型性状揭示天然居群遗传变异及其格局的方法目前仍然为许多学者所应用(Xie et al., 1995;Volis et al., 1998;Daehler et al., 1999;Jonas et al., 1999;Jenczewski et al., 1999;陈益泰等,1999;向志强等,1999;周福军等,2001)。
西南桦(Betula alnoides)是北半球桦木科桦木属分布最南的暖热类群,天然分布于印度半岛北部、缅甸以及印支半岛各国,我国云南省、广西壮族自治区和海南省亦有其天然分布(Zeng et al., 1999)。西南桦树干通直圆满,其木材具密度适中、纹理优美、不翘不裂、易于加工等优良特性,广泛应用于高级建筑装饰和高档家具制作,具有很高的经济价值。而且,西南桦是我国云南、广西等西部省(区)水源涵养林区(天然次生林)的主要树种之一,具有重要的生态价值。目前西南桦已在华南和西南地区诸省(区)大面积推广,已成为我国热带、南亚热带地区的主要造林树种之一。以往的研究主要集中在西南桦的驯化栽培技术,“九五”期间完成了其分布区调查(曾杰等,1999),而西南桦的遗传变异尚缺乏研究。
广西壮族自治区的西南桦主要分布于其西部和西北部。境内由于喀斯特地貌的广泛分布,使西南桦的天然分布区与不适宜西南桦生长的石质山地形成斑块镶嵌。近十多年来的过度采伐更加重了西南桦天然生境的破碎化。研究这种状况下西南桦天然居群的表型变异及其地理变异格局,具有理论价值和实践意义。因此本文选择了广西壮族自治区西南桦天然分布区开展表型变异研究,为西南桦的遗传改良研究奠定基础,为制定西南桦育种策略和天然林持续利用对策提供科学依据。
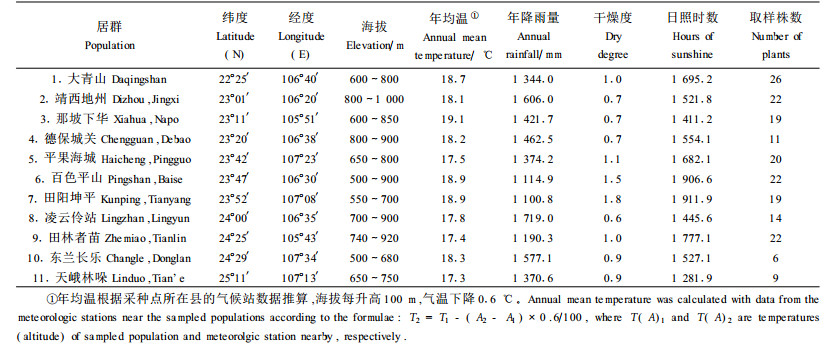
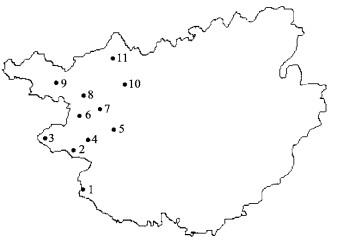
1 材料与方法 1.1 取样依据西南桦在广西壮族自治区的分布范围,大致均匀地选取15个县(市)进行调查。由于近十几年来西南桦天然林砍伐甚剧,部分县市已无较集中分布的西南桦采种母树,仅于11个县(市)调查到西南桦天然林(图 1)。各调查地点西南桦天然林的基本情况见表 1。
|
图 1 11个西南桦取样居群在广西的位置 Fig. 1 The geographical distribution of B.alnoides and the location of 11 sampled populations in Guangxi, China |
对于每个调查林分,原则上选取不少于20株的结实母树,样株之间相距50 m以上。由于取样居群偏小或调查困难,4个居群的取样母树数与20株相距甚远。采集果穗的同时,选取标准枝制作标本,带回室内调查叶片特征。种子经自然干燥后保存于冰箱冷藏室(4 ℃左右)待用。
|
|
从每株采种母树的标本上随机选取6~10片发育完满的完整叶片调查侧脉数、叶长、叶宽、叶基至最宽处距离(简称基宽距,下同)、叶柄长、叶基角,应用直尺、量角器等常规测量工具量测。每个家系随机选取4份100粒种子,用1/10 000天平称量后计算千粒重;随机选取30粒完整的种子,测量种子长、种子宽和种翅宽。具体方法是,运用倒置显微镜将种子放大后将图像输送至电脑,用直尺在电脑屏幕上直接量测,或用Photoshop软件量测,放大倍数为66.7。
1.3 数据处理与分析在所测定表型性状指标的基础上,计算叶片和种子的长宽比,分别作为叶片和种子的形状指数。应用变异系数以及巢式方差分析等方法分析各表型性状在居群内和居群间的变异情况,居群内和居群间方差分量的计算参照李斌等(2002)的方法;利用相关分析对表型性状间及其与地理、气候变量间进行相关分析,探讨西南桦表型变异的地理格局;应用各表型性状求算居群间Mahalanobis距离,将它与对应的地理距离进行相关分析,并运用UPGMA在NTSYS软件上作居群关系树状图。所有统计分析运用SPSS8.0和SAS软件进行。
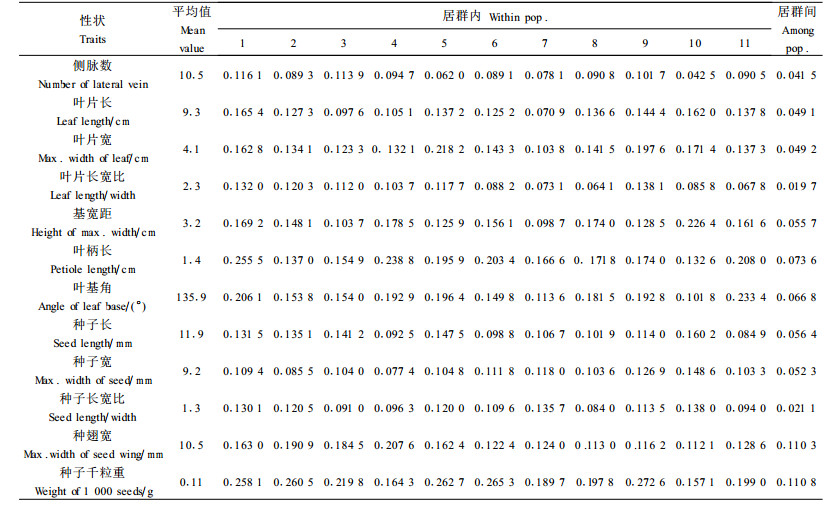
2 结果与分析 2.1 居群内和居群间的表型变异变异系数可以反映表型性状在居群内和居群间的变异,从而揭示其变异格局。从表 2可以看出,居群内各表型性状的变异大小因性状而异。在所调查的表型性状中,以侧脉数、叶柄长的变异最小,平均变异系数小于0.1;种子千粒重的变异最大,平均变异系数大于0.2。形状指数的变异小于大小性状的变异。综合分析各种性状可以看出,居群1的变异最丰富,其次是居群9和5,居群7的变异最小。
居群间各表型性状的变异系数是在居群平均值的基础上求得的。比较居群间各表型性状的变异系数,以叶片长宽比和种子长宽比为最小,以种子千粒重和种翅宽为最大。以变异系数作为指标,比较居群内和居群间的变异发现,各表型性状在居群内的变异均大于居群间的变异。而且各表型性状在居群间的变异系数一般小于居群内变异系数的最低值,仅叶柄长例外(表 2)。在12个表型性状中,叶片长宽比、种子长宽比在居群内和居群间的变异系数相差最为悬殊,而叶柄长、种翅宽在居群内和居群间的变异系数相差最小。
|
|
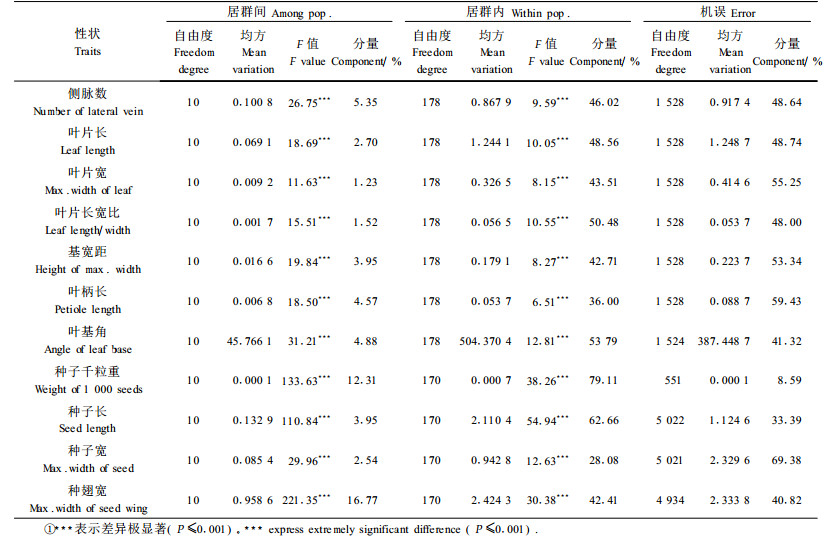
巢式方差分析亦可以揭示居群内和居群间的变异,而且可以划分居群内和居群间变异组分。由于种子长宽比不存在居群分化,因此仅对其余11个性状的巢式方差分析结果进行分析(表 3)。结果表明,各性状指标在居群内以及居群间均存在极显著的差异,而且各性状在居群内的变异分量远大于居群间,其比值为2.5~35.5。其中种翅宽的比值最小,叶宽以及叶长宽比的比值最大。巢式方差分析的结果与变异系数的结果基本一致。
|
|
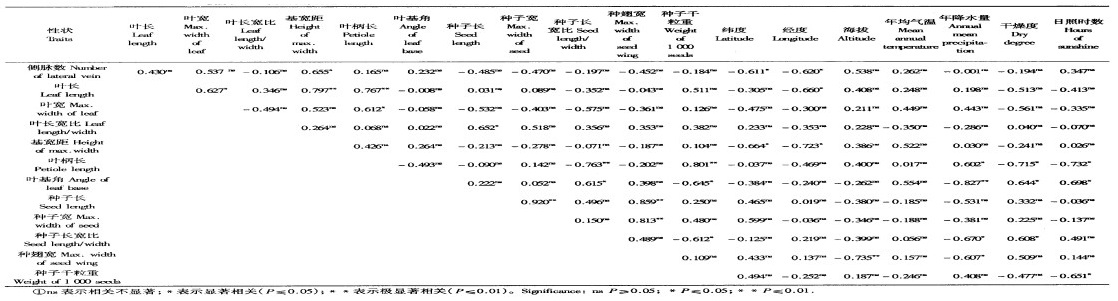
表 4中显示了各表型性状间及其与地理、气候因子间的相关性。生殖性状与营养性状间存在显著相关,如种子长宽比、种子千粒重与叶柄长相关极显著,与叶基角显著相关;种子长与叶片长宽比显著相关。营养性状的地理变异趋势较明显,其中侧脉数、基宽距都与经度、纬度呈现显著的负相关,即越往东北方向,侧脉数和基宽距越小;叶片长与经度亦呈现显著的负相关。而在生殖性状中,仅种翅宽与海拔显著负相关。
|
|
表型性状与气候因子的相关分析表明,在营养性状方面,叶柄长与年降水量呈现显著相关,与干燥度、日照时数呈显著负相关;而叶基角则相反,与年降水量呈现极显著的负相关,而与干燥度、日照时数显著相关。在生殖性状中,种子长宽比、种翅宽与年降水量显著负相关,种子千粒重与日照时数亦显著负相关,种子长宽比与干燥度相关显著。各表型性状与年均气温相关不显著,可能与采种点间温度变化幅度小有关(表 1)。
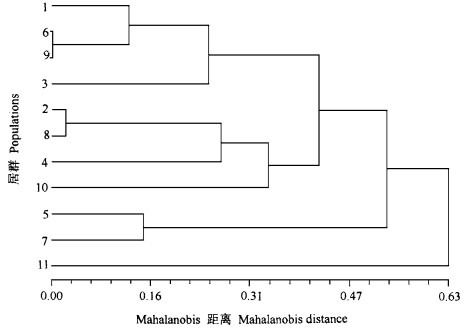
2.3 居群分类从居群关系树状图(图 2)可以看出,11个居群大体上可以分为4类,其中居群1、3、6和9归为一类,居群2、4、8、10归为一类,居群5和7归为一类,居群11单独为一类。地理上相邻的居群并没有聚在一起。本文将居群间的Mahalanobis距离与地理距离进行相关分析,发现两者之间相关不显著(R=0.200 3,P=0.143)。这可能与不适宜西南桦生长的石质岩溶地区的阻隔有关。居群6和9位于土山,尽管相距较远,但是从目前尚存的小苗、幼树分析,以前西南桦在此区域是连续分布的,所以两者间的Mahalanobis距离几乎为0。居群5和7亦是如此。居群6与8虽然在地理上相距较近,但是分属于不同的流域。居群2、4、8、10有一个共同点,都位于土山(丘)与石山(丘)接邻地区,即2种土地类型的生态交错带。居群11单独归为一类,可能与其位于西南桦分布区的北缘有关。
|
图 2 11个西南桦居群的关系树状图 Fig. 2 Dendrograms of 11 populations using UPGMA clustering method for Mahalanobis distances derived from phenotypic traits in B.alnoides |
表型性状变异往往具有适应和进化上的意义,如叶柄长度不仅影响树汁的传导,而且影响叶片的空间分布,从而对光的截留具有重要作用(Bacilieri et al., 1995),种子大小的变异与诸如种子萌发等各种适应性状有关,对幼苗性状产生重要作用,从而影响一个物种对某个生境的入侵和存活(Susko et al., 2000)。无论在西南桦居群内还是居群间,叶片与种子大小性状的变异系数比相应的形状指数大,反映了其叶片和种子形状的稳定性。其种子千粒重在所有性状中变异最大,与其对环境影响反应最敏感有关,因为林木结实特征受环境条件影响大。而种子千粒重与地理变量间相关并不显著,说明可能还有其他局域环境条件如小气候、土壤特征等对种子千粒重影响更大,有待从小尺度上开展研究。通过居群分类发现,位于土山(丘)和石山(丘)生态交错带的2、4、8、10四个居群归为一类,似乎有针对土壤类型的自然选择因素存在。种子千粒重、种翅宽与种子散布的距离有关,种翅与海拔呈现极显著负相关,可能与不同海拔的风速差异有关。因为低海拔地区风速小,而种翅大有助于增加种子散布范围进而有利于维持物种生存,所以种翅与海拔的这种关系可能是西南桦对环境的一种适应性表现。在所调查的12个表型性状中,侧脉数、叶片长、基宽距和种翅宽与地理变量显著相关,反映了较明显的地理变异趋势。
西南桦的表型性状在居群内和居群间均存在丰富的变异,居群内的变异远远大于居群间的变异,即居群分化较小。究其原因,可以从几个方面加以解释:1)根据葛锦芳(1985)的推测,广西壮族自治区的西南桦是从云南沿着南盘江扩散而来,居群分化的历史较短,所以居群间的分化较小;2)西南桦的大规模采伐始于20世纪80年代,由于时间较短,所导致的生境破碎化对西南桦天然居群的表型变异尚无显著影响;3)本研究的调查范围仅限于广西壮族自治区,而且西南桦只在其西南部、西部和西北部有分布,其经度、纬度和海拔跨度较小,分别为1°51′、2°46′和500 m。陈益泰等(1999)对四川省桤木(Alnus cremastogyne)居群的研究也得出了相似的结果。而向志强等(1999)研究海南岛的海南粗榧(Cephalotaxus mannii)居群的表型变异发现,同一性状在居群间和居群内的变异基本接近。2类树种在居群表型变异格局上的差异是由其树种特性以及进化历史等所决定的。
西南桦表型变异研究对开展良种选育、种质资源保存以及天然林保护和经营具有十分重要的意义。由于西南桦居群分化较小,在进行西南桦良种选育时,可以适当减少抽样居群数,增加居群内的家系数。由于良种选育工作刚刚起步,各地生产部门可以就近进行单株选优,采集优树上的种子发展西南桦人工林。在种质资源迁地或就地保存时,可以选择变异较为丰富的居群,如1、9和5三个居群;考虑到西南桦居群对不同立地的潜在适应性差异,也必需选择适生于土石山(丘)生态交错带的居群,如2、4、8和10居群;居群11比较独特,而且是北缘居群,亦必需加以考虑。原则上,由于西南桦天然林资源破坏十分严重,应尽可能多地保护和经营现存的资源,对上述居群必需加以重点保护。
陈益泰, 李桂英, 王惠雄. 1999. 桤木自然分布区内表型变异的研究. 林业科学研究, 12(4): 379-385. DOI:10.3321/j.issn:1001-1498.1999.04.009 |
葛锦芳. 1985. 云南桦木科植物的分类与地理分布. 西南林学院学报, (1): 1-8. |
葛颂, 洪德元. 1994.遗传多样性及其检测方法.见: 钱迎倩, 马克平主编.生物多样性研究的理论与方法.北京: 中国科学技术出版社, 123-140
|
李斌, 顾万春, 卢宝铭. 2002. 白皮松天然群体种实性状表型多样性研究. 生物多样性, 2: 181-188. DOI:10.3321/j.issn:1005-0094.2002.02.008 |
向志强, 付永川, 刘玉成, 等. 1999. 不同种群中海南粗榧(Cephalotaxus mannii)形态变异研究. 广西植物, 19(2): 131-135. DOI:10.3969/j.issn.1000-3142.1999.02.006 |
曾杰, 郑海水, 翁启杰. 1999. 我国西南桦的地理分布与适生条件. 林业科学研究, 12(5): 479-484. DOI:10.3321/j.issn:1001-1498.1999.05.006 |
周福军, 颜庭芬, 阎秀峰, 等. 2001. 高山红景天形态分化与生存环境关系的研究. 植物研究, 21(1): 90-96. DOI:10.3969/j.issn.1673-5102.2001.01.024 |
Bacilieri R, Ducousso A, Kremer A. 1995. Genetic, morphological, ecological and phenological differentiation between Quercus petraea(Matt.) Liebl. and Quercus robur L. in a mixed stand of northwest of France. Silvae Genetica, 44(1): 1-10. |
Casas A, Caballero J, Valiente-Banuet A, et al. 1999. Morphological variation and process of domestication of Stenocereus stellatus(Cactaceae) in central Mexico. American Journal of Botany, 86: 522-533. DOI:10.2307/2656813 |
Daehler C C, Yorkston M, Sun W, et al. 1999. Genetic variation in morphology and growth characters of Acacia koa in the Hawaiian Islands. International Journal of Plant Science, 160(4): 767-773. DOI:10.1086/314163 |
Irwin R E. 2000. Morphological variation and female reproductive success in two sympatric Trillium species:evidence for phenotypic selection in Trillium erectum and Trillium grandiflorum(Liliaceae). American Journal of Botany, 87(2): 205-214. |
James E A, Brown A J. 2000. Morphological and genetic variation in the endangered Victorian endmic grass Agrostis adamsonii Vickery (Poaceae). Australian Journal of Botany, 48: 383-395. DOI:10.1071/BT98085 |
Jenczewski E, Prosperi J M, Ronfort J. 1999. Evidence for gene flow between wild and cultivated Medicago sativa(Leguminosae) based on allozyme markers and quantitative traits. American Journal of Botany, 86: 677-687. DOI:10.2307/2656577 |
Jonas C S, Geber M A. 1999. Variation among populations of Clarkia unguiculata(Onagraceae) along altitudinal and latitudinal gradients. American Journal of Botany, 86: 333-343. DOI:10.2307/2656755 |
Olfelt J J, Furnier G R, Luby J J. 2001. What data determine whether a plant taxon is distinct enough to merit legal protection? A case study of Sedum integrifolium(Crassulaceae). American Journal of Botany, 88(3): 401-410. DOI:10.2307/2657104 |
Pecetti L, Piano E, Valentini P, et al. 1999. Phenotypic variation and germplasm discrimination in Lucerne (Medicago sativa) complex as evidenced by multivariate analysis. Journal of Genetics and Breeding, 53: 37-45. |
Susko D J, Lovett-Doust L. 2000. Patterns of seed mass variation and their effects on seedling traits in Alliaria petiolata(Brassicaceae). American Journal of Botany, 87(1): 56-66. |
Volis S, Mendlinger S, Whittaker L O, et al. 1998. Phenotypic variation and stress resistance in core and peripheral populations of Hordeum spontaneum. Biodiversity and Conservation, 7: 799-813. DOI:10.1023/A:1008844504010 |
Xie C Y, Ying C C. 1995. Genetic architecture and adaptive landscape of interior lodgepole pine (Pinus contorta ssp. Latifolia) in Canada. Canadian Journal of Forest Research, 25: 2010-2021. DOI:10.1139/x95-217 |
Zeng J, Zheng H S, Weng Q J. 1999. Betula alnoides——a valuable ree for tropical and warm-tropical areas. Forest, Farm and Community Tree Research Reports, 4: 60-63. |
 2005, Vol. 41
2005, Vol. 41