文章信息
- 梁军, 贾秀贞, Hai Nguyen, 王媛, 张星耀.
- Liang Jun, Jia Xiuzhen, Hai Nguyen, Wang Yuan, Zhang Xingyao.
- 2种牛肝菌的生理学特性及抗盐碱性
- The Physiological Characteristics and Salinity and Alkalinity Resistance of Two Ectomycorrhizal Fungi
- 林业科学, 2004, 40(6): 115-120.
- Scientia Silvae Sinicae, 2004, 40(6): 115-120.
-
文章历史
- 收稿日期:2004-04-28
-
作者相关文章
2. 加拿大艾伯塔大学可更新资源学院 埃德蒙顿,加拿大 T6G2E1
2. Department of Renewable Resources, University of Alberta Edmonton, Canada T6G2E1
大量的试验研究已证明, 外生菌根菌与陆地植物的共生对干旱、盐碱化等逆境中植物的成活和生长有积极的作用(Cantrell et al., 2001; Muhsin et al., 2002)。菌根菌在森林生物化学循环中是主要的碳汇和氮汇成员(Pfeffer et al., 2001),起着平衡和重新分配土壤中物质流、能源流的作用(Nehls et al., 2001),可有效改善土壤肥力状况(Setala et al., 1999),参与维系物种多样性,进而保持森林生态系统的稳定和发展。森林生态系统中外生菌根的主要作用表现在可以代替根毛扩大寄主植物根系的吸收面积,促进寄主植物从土壤中吸收水分和养分,增加寄主的高、径生长,提高生物产量;可以产生多种植物生长激素和生长调节物质,促进林木生长发育(Slankis, 1973);调节植物之间的竞争关系,促进营养循环和贮存,增强林木对逆境的适应能力,保持森林生态系统的稳定;分泌抗生素,诱导林木提高抗性相关酶的活性,产生抗性物质,抑制病原菌的侵入,提高林木抗逆性和抗病性(雷增普等,1989)。我国广大的西部地区,气候和立地条件往往较为恶劣,外生菌根菌可作为一种潜在的生物肥料,部分替代或补充化学肥料的使用,可在造林中有效提高成活率和保存率,实现林木速生丰产。菌根技术已被列为植物病害生态控制和生物防治手段之一(Zhang et al., 2002)。
本研究所选用的2种牛肝菌对土传病菌有良好的拮抗作用(栾庆书,1982;李玉等,2000),能显著提高植物的抗旱能力(吕全等,1999)及抗病能力(梁军等,2003),在生产中有广阔的应用前景。而外生菌根菌的有益作用要想在生产实践中大规模体现,需要将菌根真菌扩大培养,制成各种形式的菌剂,以便在生产过程中使用。针对这2种菌的生理学特性还没有一个系统完整的研究,特别是2种菌抗盐碱性的研究仍属空白,因此本研究旨在通过对2种菌的生长条件筛选及抗盐碱性的初步研究,为2种菌在生产上的应用特别是在西部干旱及盐碱地区的开发利用提供科学依据。
1 材料与方法 1.1 供试菌种美味牛肝菌(Boletus edulis),褐疣柄牛肝菌[Leccinum scabrum(Bull.Ex Fr.)]。供试菌种均由西北农林科技大学提供。
1.2 试验方法 1.2.1 培养基对菌丝生长的影响选用4种培养基,分别为PDA(葡萄糖20 g,马铃薯20 g,琼脂18 g,蒸馏水1 000 mL),MMN(葡萄糖10 g,(NH4)2HPO4 0.5 g,MgSO4·7H2O 0.15 g,CaCl2·2H2O 0.055 g,NaCl 0.025 g,FeCl3·6H2O 0.02 g,麦芽浸膏3 g,蛋白胨15 g,琼脂8 g,维生素B1 1×10-4 g,生物素2.5×10-5 g,蒸馏水1 000 mL),FM(葡萄糖5 g,MgSO4·7H2O 0.1 g,CaCl2·2H2O 0.026 g,NaCl 0.02 g,FeCl3·6H2O 0.001 g,琼脂18 g,维生素B1 1×10-4 g,维生素B2 1×10-4 g,尼克酰胺1×10-4 g,生物素2.5×10-5 g,酒石酸铵1 g,MnSO4·4H2O 0.001 g,肌醇0.01 g,对氨基苯甲酸1×10-4 g,泛酸钙1×10-4 g,ZnSO4·7H2O 0.001 g,KH2PO4 0.2 g,蒸馏水1 000 mL),MRD(葡萄糖20 g,MgSO4·7H2O 0.5 g,琼脂20 g,维生素B1 1×10-4 g,酒石酸铵0.5 g,ZnSO4(2%) 0.5 mL,KH2PO4 0.2 g,蒸馏水1 000 mL)。各培养基均经高压蒸汽灭菌20 min后倒入9 cm培养皿制成平板备用。用5 mm灭菌打孔器在事先培养好的母菌落边缘取直径5 mm的菌丝圆片[大小0.25 cm2,菌丝干质量4 mg·(100 mL)-1],接种于平板中央,每处理3个重复,置于25 ℃恒温箱内培养10 d。从接种第2天起,每天在2个固定的垂直方向测量菌落生长直径,并记录。
测定指标:日直径扩展速度(cm·d-1,第2天菌落直径减第1天菌落直径)。本研究日直径扩展速度均取各重复及各日的平均值。
1.2.2 温度对菌丝生长的影响温度梯度设置为5、10、15、20、25、30、35、40 ℃,PDA培养基培养,每温度设3个重复,测定并计算菌落平均的日直径扩展速度。
1.2.3 pH值对菌丝生长的影响pH值梯度设置为3.0、4.0、5.0、6.0、7.0、8.0、9.0、10.0,每梯度设3个重复。采用MMN液体培养。培养容器为250 mL三角瓶,装液量为100 mL,用缓冲液初步调节p H值,再借助pHS-25型酸度计,用1 mol·L-1 HCl或1 mol·L-1 NaOH将培养基的pH值准确调至所需值。接种后置于旋转式摇床,27 ℃下振荡培养,转速为150 r·min -1,每瓶接种母菌落菌丝圆片3片。培养10 d后将菌丝体从培养液中过滤出来,并用蒸镏水清洗附着的培养基,放在已预先干燥好的滤纸上,置于105 ℃干燥箱内烘至恒重,测定菌丝体干质量。
1.2.4 C源和N源对菌丝生长的影响供试C源为葡萄糖、麦芽糖、蔗糖、乳糖、淀粉、肌醇、山梨醇、甘露醇。供试N源为(NH4)2HPO4、NH4Cl、(NH4)2SO4、NH4NO3、KNO3、蛋白胨、牛肉浸膏、酵母浸膏。培养基为MMN液体培养基(C源10 g·L-1,N源15 g·L-1),振荡培养10 d后测定菌丝体干质量。
1.2.5 菌种的抗盐碱性NaCl盐处理,设置梯度为0、200、400、800 mmol·L-1;pH值设置为5(CK)、7、8等3个梯度。用MMN液体振荡培养方法,采用完全随机区组设计,每菌种12个处理,每处理3个重复。各接种菌丝圆片1片,培养结束后测定菌丝体干质量。
1.3 指标测定及分析方法平板培养的菌落,测定并计算出日直径扩展速度;液体培养的菌种,测定菌丝体干质量,并计算菌丝体增殖倍数。
增殖倍数为培养后菌丝干质量/接种菌丝干质量,各数据均采用几个重复的平均值。用SPSS统计软件进行方差分析和多重比较。
2 结果与分析 2.1 2菌种的生理学特性 2.1.1 培养基对菌种生长的影响经过方差分析(表 1)可以看出,美味牛肝菌在MMN培养基上生长量最大,日直径扩展速度达到1.03 cm,且菌丝稠密,其次为PDA和MRD培养基,而在FM培养基上生长最差;褐疣柄牛肝菌在MMN、PDA和MRD培养基上的日直径扩展速度之间差异不显著,而与FM相比差异显著。
|
|
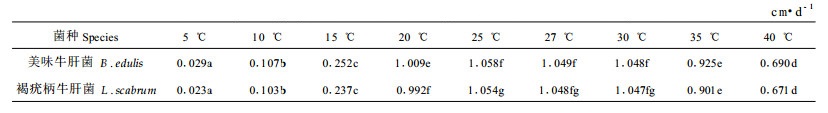
经方差分析(表 1)可知,温度对2菌种生长的影响差异显著。再做进一步的多重比较(表 2)可以发现,美味牛肝菌和褐疣柄牛肝菌在25、27 ℃和30 ℃这3个温度下生长速度差异不显著,说明它们的最适生长温度范围均为25~30 ℃。杨新美(1988)研究表明,美味牛肝菌菌丝体可在20~35 ℃条件下生长,而本研究得出美味牛肝菌和褐疣柄牛肝菌在40 ℃下仍能生长良好,日直径扩展速度可达到0.671 cm·d-1以上。这体现出了同一菌种不同菌株间生态型差异。
|
|
从表 3可知,美味牛肝菌和褐疣柄牛肝菌在pH值4~9范围内均可生长,但在pH值5~6上生长最佳,每100 mL培养液中2菌种菌丝体干质量分别为1 054.8~1 057.0 mg·(100 mL)-1和1 035.1~1 111.8 mg·(100 mL)-1。美味牛肝菌和褐疣柄牛肝菌在中性和微碱性(pH值为8)培养基中仍可生长,菌丝增殖倍数在167.68以上,尤其褐疣柄牛肝菌在pH值为8时,菌丝干质量可达919.3 mg·(100 mL)-1。但在pH值9条件下,2菌种生长较为缓慢,而在pH值为10条件下,美味牛肝菌和褐疣柄牛肝菌几乎不生长。经回归分析发现,2菌种菌丝体干质量(y)与pH值(x)呈显著的抛物线相关关系:
|
|
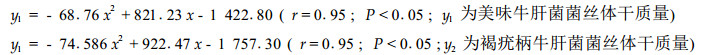
|
培养基pH值在3~4时,经灭菌后pH值略有提高,而pH值6以上的培养基灭菌后则pH值略有下降,并且pH值7~10的培养液经灭菌后有少量沉淀产生。另外,在菌丝体增殖过程中,由于新陈代谢所产生的有机酸(醋酸、草酸等)的积累,使得培养液pH值降低,并导致沉淀消失。本试验中培养后的培养液pH值(y)与初始pH值(x)呈显著正相关:
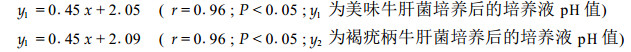
|
C源是菌丝体最重要的营养来源,它不仅是合成碳水化合物和氨基酸的原料,而且也是重要的能量来源。在MMN培养液中分别以葡萄糖、麦芽糖、蔗糖、乳糖、淀粉、肌醇、山梨醇及甘露醇作为C源,结果见表 4所示,美味牛肝菌对葡萄糖和淀粉利用最佳,增殖倍数分别为156.58和152.93,其次为蔗糖、乳糖与肌醇,而对甘露醇、山梨醇与麦芽糖利用较差;褐疣柄牛肝菌除了能较好地利用葡萄糖与淀粉外,对其他C源的利用均较差。
|
|
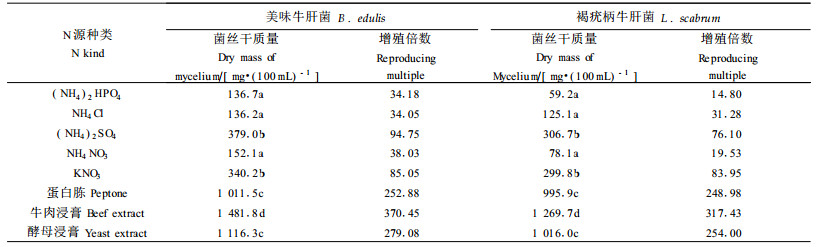
N源是菌丝体合成蛋白质和核酸的重要营养来源。从表 5可看出,美味牛肝菌和褐疣柄牛肝菌均对有机N利用率高,其中以牛肉浸膏为最佳,100 mL培养液中菌丝体干质量分别达1 481.8 mg和1 269.7 mg,分别增殖370.45和317.43倍,其次为酵母浸膏和蛋白胨。在无机N源中,2菌种均对(NH4)2SO4和KNO3利用较好,100 mL培养液中菌丝体干质量分别达379.0 mg和306.7 mg与340.2 mg和299.8 mg;而对(NH4)2HPO4、NH4Cl和NH4NO3利用较差,其中褐疣柄牛肝菌利用(NH4)2HPO4时,增殖倍数仅为14.8。
|
|
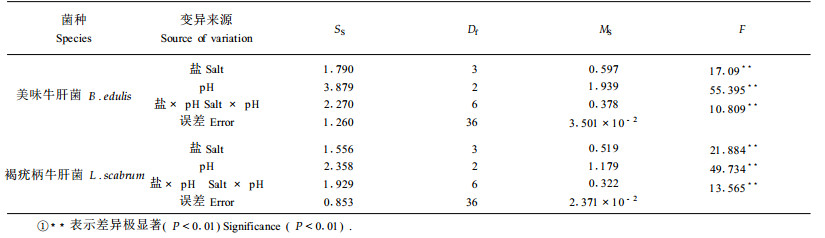
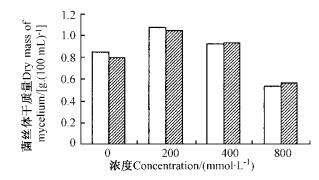
方差分析(表 6)显示,盐、pH值及两因素交互作用对2菌种生长均有显著的影响。单因素方差分析表明,美味牛肝菌和褐疣柄牛肝菌均在盐浓度为200 mmol·L-1时生长最好,与对照(盐浓度为0)差异显著(图 1),而高浓度(800 mmol·L-1)的盐处理则抑制2菌种的生长;pH因子单因素方差分析表明,pH对菌丝体、干质量影响显著,2菌种在不同梯度的pH值下的生长趋势相似,菌丝体干质量均随pH值的升高而降低(图 2)。
|
|
|
图 1 盐浓度对菌种生长的影响 Fig. 1 The effect of salt concentration on the species growth □美味牛肝菌B.edulis; ■褐疣柄牛肝菌L.scabrum. |

|
图 2 pH对菌种生长的影响 Fig. 2 The effect of media pH on the species growth □美味牛肝菌B.edulis; ■褐疣柄牛肝菌L.scabrum. |
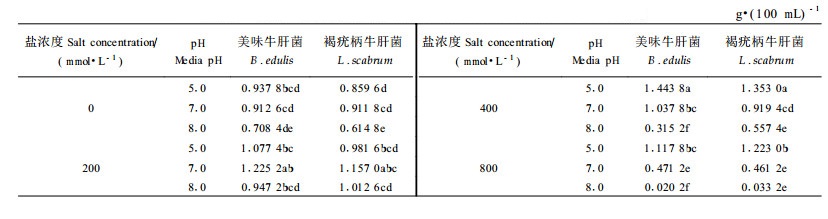
从表 7可以看出,当盐浓度为200 mmol·L-1时,2菌种在各种pH值下生长量没有显著差异,美味牛肝菌和褐疣柄牛肝菌均在pH 7.0下生长量最大,分别为1.225 2和1.157 0 g·(100 mL)-1,但与pH 5.0和8.0下的生长量相比差异不显著;当盐浓度达到400 mmol·L-1时,美味牛肝菌和褐疣柄牛肝菌均在pH 5.0下达到最大的生长量,但随着pH升高生长量下降也达到显著;在盐浓度为800 mmol·L-1时,2菌种在不同的pH值下的生长量下降幅度更大,菌丝体干质量极差分别达到1.097 6和1.189 8 g·(100 mL)-1,有非常明显的盐和pH值的双胁迫效应。
|
|
最适合美味牛肝菌生长的培养基为MMN培养基,其次为PDA和MRD培养基;最适合褐疣柄牛肝菌生长的培养基为PDA、MMN和MRD培养基;2菌种均不适合在FM培养基上生长。
最利于美味牛肝菌生长的C源为葡萄糖和淀粉,其次为蔗糖、乳糖和肌醇;最利于褐疣柄牛肝菌生长的C源为葡萄糖,淀粉次之,而对其他C源利用较差。最利于美味牛肝菌和褐疣柄牛肝菌生长的有机N源是牛肉浸膏,其次为蛋白胨和酵母浸膏;在无机N源中,2菌种均对(NH4)2SO4和KNO3利用较好,而对(NH4)2HPO4、NH4Cl和NH4NO3利用较差,其中褐疣柄牛肝菌应用(NH4)2HPO4时,增殖倍数仅为14.8倍。
外生菌根菌的耐盐碱性往往影响其在盐碱地区的定殖。经过盐和pH值的单因素分析可知,2菌种对中等程度的盐浓度有一定适应性,生长量比对照有显著增加,有一定的抗盐能力,在培养这2种外生菌根菌时,可以适当增加盐浓度以促进菌丝生长。2菌种对pH值则较为敏感,随着pH值的升高,生长量显著下降,均比对照有显著降低。本研究中供试的2菌种可在中等程度的盐浓度下良好生长,具有在盐碱地上定殖生长的潜力,但在盐与pH值交互作用下,菌丝体干质量下降达显著水平,说明盐浓度与pH值的交互作用导致菌种的耐盐、耐pH值能力下降,2菌种表现出遭受双胁迫的累积效应。
雷增普, 金均然, 王昌温. 1989. 外生菌根菌对植物根部病害病原菌拮抗作用的研究. 林业科学, 25(6): 502-507. DOI:10.3321/j.issn:1001-7488.1989.06.004 |
李玉, 王淑清, 鞠文鹏. 2000. 菌根真菌对松苗根部病害的防治作用. 辽宁林业科技, (4): 21-22. |
梁军, 张颖, 贾秀贞, 等. 2003. 外生菌根菌对杨树生长及抗逆性指标的效应. 南京林业大学学报, 27(4): 39-43. |
吕全, 雷增普. 1999. 外生菌根提高板栗苗木抗旱性能及其机理的研究. 林业科学研究, 3(13): 249-256. |
栾庆书. 1982. 几种外生菌根菌对土传病原菌的拮抗作用. 辽宁林业科技, 6(6): 45-50. |
Cantrell I C, Linderman R G. 2001. Preinoculation of lettuce and onion with VA mycorrhizal fungi reduces deleterious effects of soil salinity. Plant Soil, 233(2): 269-281. DOI:10.1023/A:1010564013601 |
Muhsin T M, Zwiazek J J. 2002. Ectomycorrhizas increase apoplastic water transport and root hydraulic conductivity in Ulmus americana seedlings. New Phytologist, 153(1): 153-158. DOI:10.1046/j.0028-646X.2001.00297.x |
Nehls U, Mikolajewski S, Magel E, et al. 2001. Carbohydrate metabolism in ectomycorrhizas: gene expression, monosacchairide transport and metabolic control. New Phytologist, 150: 533-541. DOI:10.1046/j.1469-8137.2001.00141.x |
Pfeffer P E, Bago B, Shachar-Hill Y. 2001. Exploring mycorrhizal function with NMR spectroscopy. New Phytologist, 150: 545-553. |
Setala H, Kulmala P, Mikola J, et al. 1999. Influence of ectomycorrhiza on the structure of detrital food webs in pine rhizosphere. Oikos, 87: 113-122. DOI:10.2307/3547002 |
Slankis V. Hormonal relationships in mycorrhizal development. In: Marks G C and Kozlowski T T eds. Ectomycorrhiza. New York: Academic Press, 1973: 231-298
|
Zhang Xingyao, Liang Jun, Lü Quan, et al. 2002. Management strategies and research orientations of forest diseases and pests in China. Chinese Forestry Science and Technology, (2): 60-65. |
 2004, Vol. 40
2004, Vol. 40