文章信息
- 薛永常, 李金花, 卢孟柱, 张绮纹.
- Xue Yongchang, Li Jinhua, Lu Mengzhu, Zhang Qiwen.
- 107杨次生木质部PAL基因的RT-PCR扩增及其鉴定
- Cloning and Identification of PAL Gene Amplified by RT-PCR from Populus × euramericana cv. "74/76" Second Xylem mRNA
- 林业科学, 2004, 40(4): 193-197.
- Scientia Silvae Sinicae, 2004, 40(4): 193-197.
-
文章历史
- 收稿日期:2002-11-06
-
作者相关文章
2. 中国林业科学研究院林业研究所 北京 100091
2. Research Institute of Forestry,CAF Beijing 100091
木质素是一种由肉桂醇等单体聚合而成的酚类多聚体,是植物体中一种主要的天然产物,广泛存在于维管植物中。木本植物中木质素含量较高,一般约占干重的15%~36%(Douglas, 1996)。木质素与纤维素、几丁质一起成为世界上最丰富的天然多聚物之一,是仅次于纤维素而居第二的有机组分。木材中木质素的含量与木材利用关系密切。培育木质素含量低的林木品种是提高纸浆材纸浆得率的一个重要手段。木质素是在一系列酶类催化下聚合而成的,通过对这些酶的调节可以控制木质素单体的合成速率,从而影响木质素的组成和含量。在此方面已经做了大量的工作,并且得到了木质素含量或组成发生变化的转基因植株(Atanassova et al., 1995; Campbell et al., 1996; Douglas, 1996; Grima-Pettenati et al., 1999; Boerjan et al., 2003)。PAL(苯丙氨酸解氨酶)作为木质素生物合成途径中的第一个限速酶,其表达及其丰度直接影响木质素生物合成的整个过程。杨树PAL活性主要在正在发育的木质部、嫩茎和嫩叶中最高(Shinji et al., 1997)。而在刺槐(Robinia pseudoacacia)树干中,显著的PAL活性表现在边材的较嫩部分(与木质化有关)和边材-心材的分界处(与类黄酮生物合成有关)(Hu et al., 1999)。当PAL活性下降时,植物体中的木质素含量下降2倍(Bate et al., 1994; Sewalt et al., 1997),木质素单体发生变化,G单体含量降低。PAL的超量表达后木质素的含量明显增加了(Osakabe et al., 1995)。本文通过对欧美杨107杨(Populus × euramericana cv. “74/76”)次生木质部中mRNA进行RT-PCR扩增,期望得到在木质部特异表达的PAL基因片段,通过载体构建转化其它树种,得到木质素含量或其组成发生改变的转基因植株。
1 材料与方法 1.1 材料和试剂植物材料为正在分化的2 a生107杨茎的次生木质部。试剂中Quickprop Mirco mRNA Purification kit为Amersham Pharmacia Biotech.公司产品,SuperscriptTM One-Step RT-PCR System为GIBCO-BRL公司产品,pGEM-T Easy载体(pGEM-T Easy Vector)、pGEM-7Zf(+)、CIAP、琼脂糖、T4 DNA连接酶、dNTP、1kb DNA Ladd er为Promega公司产品。Taq DNA聚合酶为北京鼎国生物技术发展中心产品,使用的重蒸水为经过Milli-Q超纯水器过滤及除菌并经高温高压灭菌后的水。
1.2 研究方法与步骤(1) 材料的处理:参考Bugos等(1995)法。取正在分化的2 a生107杨茎部,剥去树皮部分,只剩下里面的木质部和部分形成层部分,用消毒过的医用解剖刀迅速刮取次生木质部表面,厚度约1 mm左右。液氮研磨成粉末后,提取mRNA。
(2) mRNA提取:按Quickprop Micro mRNA Purification kit试剂盒提供的方法提取mRNA。
(3) RT-PCR扩增:按SuperScriptTM One-Step RT-PCR试剂盒提供的条件对提取的mRNA进行RT-PCR扩增,根据实际情况略有改动。扩增引物是根据EMBL(欧洲分子生物学实验室)中Osakabe等(1995)发表的Populus kitakamiensis叶片PAL的cDNA序列(D30656)设计的,其序列为:正向引物: 5′-TTGCAGAAACCAAAGCAAGA3′;反向引物: 5′-CTCCTCCAAATGCCTCAAGT 3′。在Perkin-Elmer GeneAmp PCR System 9600上进行RT-PCR扩增。扩增体系为50 μL,其中2×反应混合物25 μL,模板mRNA (约10 ng·μL-1) 2 μL,正向引物及反向引物(10 μmol·L-1)各1 μL,水20 μL,RT/Taq酶混合物1 μL。扩增条件:cDNA合成为50℃ 30 min。预变性为94℃ 3 min。36个循环为:变性,94℃ 30 s;退火,57℃ 1 min;延伸,72℃ 1 min。循环完毕后在72℃延伸10 min。利用Supelco Inc.公司的GenElut eTM Minus EtBr Spin Columns试剂盒条件纯化回收1%琼脂糖电泳后的目的片段。
(4) 目的片段与T-载体(pGEM-T Easy Vector)的直接连接:按试剂盒条件进行,在室温(25℃)连接3 h后,用于转化大肠杆菌JM109。
(5) 重组质粒的鉴定:采用限制性内切酶酶切、特异性引物扩增及测序。
(6) 中间载体的构建:将pGEM-7Zf(+)载体和上面获得的经鉴定正确的重组质粒分别用E coRⅠ进行单酶切。单酶切后的pGEM-7Zf(+)载体经CIAP(小牛碱式磷酸酶)脱磷酸化,然后与上述重组质粒的EcoRⅠ酶切后的目的片段进行连接,转化大肠杆菌JM109。所得重组质粒经测序鉴定插入片段的方向。
(7) PAL表达载体的构建:分别用XbaⅠ和BamHⅠ双酶切(6)中得到的已经鉴定方向的重组质粒和pBⅠ 121质粒,回收重组质粒酶切的目的DNA片段和中间载体pBⅠ 121的D NA大片段,进行连接,构建了正义PAL植物表达载体。同理,分别用Xba Ⅰ和BamH Ⅰ双酶切(6)中得到的已经鉴定方向的重组质粒和pBin 438质粒,回收目的DNA片段和中间载体pBin 438的DNA大片段,进行连接,从而构建了PAL反义植物表达载体。用于转化根瘤农杆菌(Agrobacterium tumefeciens)LBA4404。
2 结果与分析 2.1 107杨次生木质部中mRNA含量及性质的鉴定制备高纯度的mRNA是RT-PCR成功的必要前提。对步骤(2)提取的mRNA经稀释后分别在2 60 nm和280 nm处测定其吸收值。其OD260/OD280比值大于1.6,表明该mRNA纯度符合试验要求。经计算mRNA的得率为20.8 μg·g-1鲜重。
2.2 目的基因片断的克隆及其鉴定按Bugos等(1995)法提取的mRNA经RT-PCR扩增、1%琼脂糖电泳后分析可知,其扩增的DNA片段约为600 bp左右,和期望的大小基本相当。选取在pGEM-T Easy载体上的2个内切酶PstⅠ和NcoⅠ对重组质粒进行双酶切,得到一个约600 bp的片段,且在测序结果中找到了所采用的正向引物序列与反向引物序列,插入片段为565bp,因此可以断定插入载体的DNA片段即为所扩增的DNA片段,从而证明了重组质粒的正确性。
利用Clustalx 1.8软件将RT-PCR扩增的PAL片段序列与Osakabe等(1995)在EMBL核酸序列库上发表的P. kitakamiensis叶片PAL的cDNA序列(D30656)进行比较,其结果如图 1。从图 1可以看出,经RT-PCR所扩增的DNA片段与P. kitakamiensis的PAL的cDNA序列的前400个碱基几乎完全相同,其相似度超过95%。基本可以断定此扩增的DNA片段即为PAL基因片段。从而证明了重组质粒中插入片段的正确性。此重组质粒定名为pGEM-T-PAL质粒。

|
图 1 扩增的DNA片段与P. kitakamiensis PAL cDNA序列的比较图 Fig. 1 Alignment of DNA sequence amplified from P. × euramericana cv."74/76" second xylem mRNA with the PAL cDNA sequence from P. kitakamiensis 相同碱基用*表示。pal为107杨扩增产物PAL片段序列,PAL1为P. kitakamiensis的PAL cDNA序列。Idential residues are marked by asterisks blow the alignment. pal is DNA sequence amplified from P. × euramericana cv.“74/ 76"; PAL1 is the original PAL cDNA sequence from P. kitakamiensis. |
在方法(6)中构建的重组质粒经限制性内切酶酶切、特异引物扩增及测序证明插入到pGEM-7Zf(+)载体的DNA片段即为所扩增的片段,测序证明该片段是以正向插入的,此中间载体定名为pGEM-7Zf(+)-PAL。
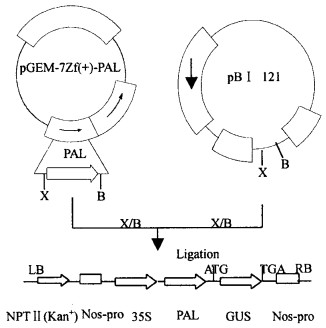
2.4 表达载体构建在选择双元载体时就应该考虑载体上的多克隆位点与中间载体相应酶切位点间的相互关系问题,以便最终决定中间载体的酶切片段在双元载体的插入方向。本文所选择的双元载体pBⅠ121和pBin 438都有XbaⅠ和BamHⅠ酶切位点,但二者的方向相反,这就为构建P AL的正义和反义表达载体提供了方便。构建结果示意图如图 2、3。通过对重组质粒的特异引物的PCR扩增,能够扩增出和目的片段一样大小的扩增片段,从而证明该目的片段的确插入了该载体中。
|
图 2 PAL的正向表达载体pBⅠ121-PAL的构建 Fig. 2 Construction of sense expressional vector pBⅠ121-PAL of PAL Gene |

|
图 3 PAL反义表达载体pBin438-PAL的构建 Fig. 3 Construction of anti-sense expressional vector pBin438-PAL of PAL Gene |
pBin438为中国科学院微生物研究所构建的一个双元载体,它含有双倍增强子的CaMV35S启动子及TM“Ω”片段翻译增强子,它能介导外源基因在杨树中的高效表达(李太元等,1994;陈颖等,1995)。本文将目的DNA片段克隆到该双元载体,去转化农杆菌。通过对重组质粒的特异引物PCR扩增,能够得到和目的片段一样大小的扩增片段,从而证明该目的片段的确插入到了该载体中。
3 讨论木质素是由不同的木质素单体聚合而成的。高等植物中主要有2种类型:(a)裸子植物木质素主要包括邻甲氧基苯基亚基(G单体),及由松柏醇及少数由p-肉桂醇聚合而成的p-羟苯基亚基(H单体);(b)被子植物木质素既包括由芥子醇聚合成的芥子基亚基(S单体),还有G单体及少量的H单体。在双子叶植物中,G单体和S单体占主要。木质素含量是造纸业中的主要限制因子,G/S单体的比例对于造纸中木质素的去除难易起着决定性作用。在具相似木质素含量的裸子植物和被子植物中,被子植物中的木质素较易去除(Chiang et al., 1988),且针叶树纸浆的残余木质素含量要比阔叶树纸浆高,表明木质素分子结构而不是其含量是决定其能否快速去除的主要因子。而被子植物中G亚基的降低和S亚基的比例增加,木质素在造纸中更易去除(Chiang et al., 1988; Piquemal et al., 1998)。因为PAL活性下降导致木质素单体中G单体含量降低,因此S/G比率上升(Sewalt et al., 1997),对于造纸的木材中木质素的去除有利。PAL可能参与了G单体或S单体特异途径的代谢调节从而影响了S/G的比率(Bate et al., 1994)。因此木质素单体组成改变已经成为基因工程提高木浆得率的主要手段。木质素合成酶基因的表达具有一定的时空性,Hu等(1998)在美洲山杨(P.tremuloides)发现2种在区域化和生理功能上不同的4CL(4-肉桂酸CoA连接酶)基因——Pt4CL1和Pt4CL2,二者分别在正在分化的木质部组织及表皮细胞中表达。另外他们发现在Pt4CL1表达受抑制的杨树中虽然木质素最高降低了45%,但其纤维素含量增加了15%,在转基因品系中在细胞水平和整株水平上的结构整体性没有变化(Hu et al.,1999)。木质素和纤维素间的消长对于提高木浆得率也起着主要的作用。本文从107杨次生木质部mRNA所扩增的DNA片段与P. kitakamiensis的叶片PA L的cDNA序列的前400个碱基几乎完全相同,但整个序列仍有很大差别,说明PAL基因在叶片、次生木质部不同部位表达也具有时空性,可能是同一个基因的不同区域表达。
因此,在基因工程改造林木木质素方面,应从两方面入手:一方面是调节控制阔叶树种木质素单体的比例,F5H(阿魏酸5-脱氢酶)在G/S单体比例中起着重要的作用,缺乏F5H的 fah1突变体只累积G-木质素(Humphreys et al.,2002;薛永常等,2003);在降低木质素含量或不改变其含量的同时,通过增加F5H的表达,使木质素G单体更多地向S单体转化,有利于在造纸中木质素的去除。另一方面从整体上降低木质素含量,如对4CL、CCR(肉桂酰CoA还原酶)、CAD(肉桂醇脱氢酶)的降低调节,在调低木质素含量的同时,增加纤维素的含量,以满足我国造纸工业的需要。
随着木质素合成途径的进一步修正和完善(Humphreys et al.,2002;薛永常等,2003),对木质素合成酶调节有了进一步的认识,木质素生物合成酶基因调节是许多酶相互作用共同调节的结果。这对于今后目的基因的选定、载体的构建有重要的指导意义。
陈颖, 韩一凡, 田颖川, 等. 1995. 苏云金杆菌杀虫晶体蛋白基因转化美洲黑杨的研究. 林业科学, 31(2): 97-103. |
李太元, 田颖川, 秦晓峰, 等. 1994. 高效抗虫转基因烟草的研究. 中国科学(B辑), 24(3): 276-282. |
薛永常, 李金花, 卢孟柱, 等. 2003. 木质素单体生物合成途径及其修订. 林业科学, 39(6): 146-153. DOI:10.3321/j.issn:1001-7488.2003.06.025 |
Atanassova R, Favet N, Martz F, et al. 1995. Altered lignin composition in transgenic tobacco expression O-methyltransferase sequences in sense and antisense orientation. Plant J, 8: 465-477. DOI:10.1046/j.1365-313X.1995.8040465.x |
Bate N J, Orr J, Ni W, et al. 1994. Quantitative relationship between phenylalanine ammonia-lyase level and phenylpropanoid accumulation in transgenic tobacco identifies a rate-determining step in natural product synthesis. Proc Natl Acad Sci USA, 91: 7608-7612. DOI:10.1073/pnas.91.16.7608 |
Boerjan W, Ralph J, Baucher M. 2003. Lignin biosynthesis. Ann Rev Plant Biol, 54: 519-546. DOI:10.1146/annurev.arplant.54.031902.134938 |
Bugos R C, Chiang V L, Campbell E R, et al. 1995. RNA isolation from plant tissues recalcitrant to extraction in guanidine. Bio Techniques, 19(5): 734-737. |
Campbell M M, Sederoff R R. 1996. Variation in lignin content and composition. Plant Physiology, 110: 3-13. DOI:10.1104/pp.110.1.3 |
Chiang V L, Funaoka M. 1990. The difference between guaiacyl and guaiacyl-syringyl lignins in their reponses to kraft delignification. Holzforschung, 44: 309-313. DOI:10.1515/hfsg.1990.44.4.309 |
Chiang V L, Puumala R J, Takeuchi H. 1988. Comparison of softwood and hardwood kraft pulping. Tappi, 71: 173-176. |
Douglas C J. 1996. Phenylpropaniod metabolism and lignin biosynthesis: from weeds to trees. Trends in Plant Sci, 1: 171-178. DOI:10.1016/1360-1385(96)10019-4 |
Grima-Pettenati J, Goffner D. 1999. Lignin genetic engineering revisited. Plant Science, 145: 51-65. DOI:10.1016/S0168-9452(99)00051-5 |
Hu W J, Kawaoka A, Tsai C J, et al. 1998. Compartmentalized expression of two structurally and functionally distinct 4-coumarate:CoA ligase genes in aspen (Populus tremuloides). Proc Natl Acad Sci USA, 95: 5407-5412. DOI:10.1073/pnas.95.9.5407 |
Hu W J, Harding S A, Lung J, et al. 1999. Repression of lignin biosynthesis promotes cellulose accumulation and growth in transgenic trees. Nature Biotechnology, 17: 808-812. DOI:10.1038/11758 |
Humphreys J M, Chapple C. 2002. Rewriting the lignin roadmap. Current Opinion in Plant Biology, 5: 224-229. DOI:10.1016/S1369-5266(02)00257-1 |
Magel E, Hubner B. 1997. Distribution of phenylalanine ammonia-lyase and synthase within trunks of Robinia pseudoacacia L. Bot Acta, 110: 314-322. DOI:10.1111/j.1438-8677.1997.tb00646.x |
Osakabe Y, Ohtsubo Y, Kawai S, et al. 1995. Structure and tissue-specific expression of genes for phenylalanine ammonia-lyase from a hybrid aspen, Populus kitakamiensis. Plant Science, 105(2): 217-226. DOI:10.1016/0168-9452(94)04042-7 |
Piquemal J, Lapierre C, Myton K. 1998. Down-regulation of Cinnamoyl-CoA Reductase induces significant changes of lignin profiles in transgenic tobacco plants. The Plant Journal, 13(1): 71-83. |
Sewalt V J H, Ni W, Blount J W, et al. 1997. Reduced lignin content and altered lignin composition in transgenic tobacco down-regulated in expression of L-phenylalanine ammonia-lyase or cinnamate 4-hydroxylase. Plant Physiol, 115: 41-50. DOI:10.1104/pp.115.1.41 |
Shinji K, Koji S, Yoshiyuki I, et al. 1997. Temporal and spatial pattern of expression of the pea phenylalanine ammonia-lyase gene promoter in transgenic tobacco. Plant Cell Physiol, 38(7): 792-803. DOI:10.1093/oxfordjournals.pcp.a029237 |
Subramniam R, Reinold S, Molitor E, et al. 1993. Structure, inheritance, and expression of hybrid poplar (Populus trichocarpa × Populus deltoides) phenylalanine ammonia-lyase genes. Plant Physiol, 102: 71-83. DOI:10.1104/pp.102.1.71 |
 2004, Vol. 40
2004, Vol. 40
